一种抗幽门螺旋杆菌活性的聚酮化合物及其制备方法和应用与流程
本发明属于抗幽门螺旋杆菌活性的聚酮化合物技术领域。
背景技术:
幽门螺旋杆菌(helicobacterpylori)是一种能长期定植于胃粘膜的微需氧、螺旋状的革兰氏阴性细菌,其感染率已达到全球人口的50%以上,中国也是一个感染率较高的国家,据统计感染率为40-90%。幽门螺旋杆菌是慢性胃炎,链球菌疾病,胃癌和粘膜相关淋巴组织淋巴瘤的发病机制中重要致病因子。世界卫生组织/国际癌症研究机构已将幽门螺旋杆菌列为人类ⅰ类致癌原。因此研发高效、低毒的幽门螺旋杆菌药物迫在眉睫。
技术实现要素:
本发明的第一目的是提供一种抗幽门螺旋杆菌活性的化合物,其结构式如式ⅰ所示:
本发明的第二目的是提供一株木贼镰刀菌(fusariumequiseti)菌株shsl21,其已于2019年9月19日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称为cgmcc,地址为:北京市朝阳区北辰西路1号院3号),保藏中心登记入册编号为cgmccno.18550。
本发明的第三目的是提供一种化合物的制备方法,包括如下步骤:
活化菌株shsl21;
固体发酵菌株shsl21;
用乙酸乙酯浸提固体发酵物得粗提物;
用减压硅胶柱层析得到洗脱液;
用反向硅胶色谱分离得反向洗脱液;
用凝胶色谱分离得凝胶洗脱液;
用反相hplc分离得hplc洗脱液。
本发明提供的菌株和化合物,具有较好的抗幽门螺旋杆菌(h.pyloribhks159)活性,适宜于抗幽门螺旋杆菌先导化合物研究或制备抗幽门螺旋杆菌药物。
附图说明
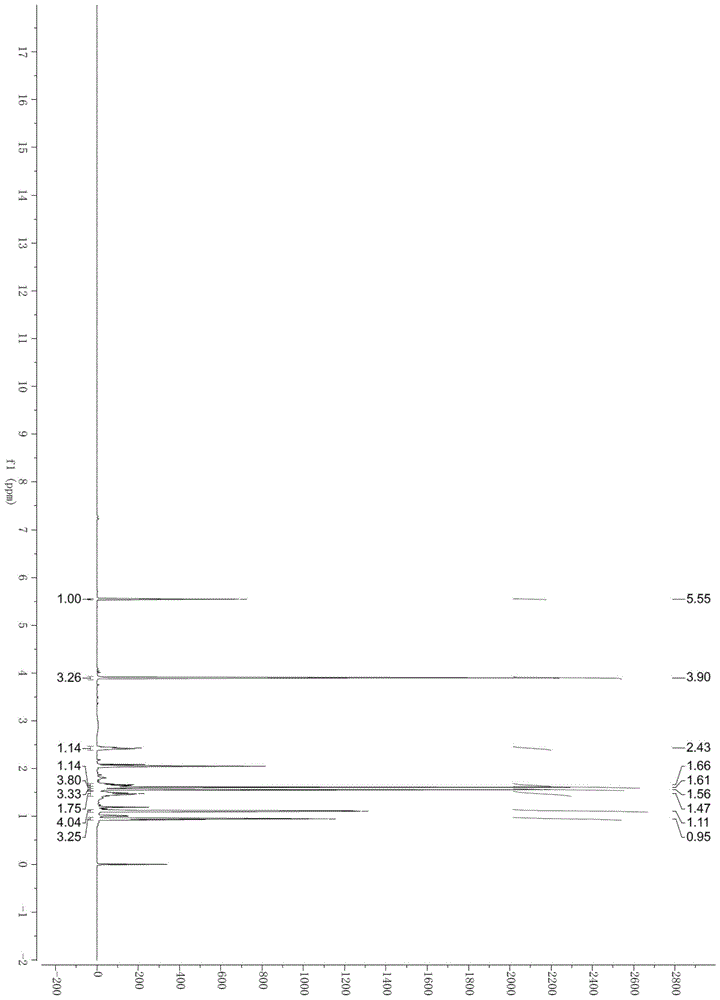
图1为化合物的1h核磁共振图谱。
图2为化合物的13c核磁共振图谱。
具体实施方式
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置3次重复实验,结果取平均值。
实施例1
菌株shsl21的分离和鉴定
一、菌株shsl21的采集与分离
2015年从广西防城港市北仑河口桐花树的花上分离到一株菌,命名为菌株shsl21。
菌株shsl21为一种红树林内生真菌。
二、菌株shsl21的鉴定
1、分子鉴定
菌株shsl21的18sribosomalrna部分序列见序列表的序列1,如genbankaccessionno.mn443741的序列相似性最高,相似性为99%。
根据以上鉴定结果,菌株shsl21属于木贼镰刀菌(fusariumequiseti)。
三、菌株shsl21的保藏
菌株shsl21,属于木贼镰刀菌(fusariumequiseti),已于2019年9月19日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称cgmcc,地址为:北京市朝阳区北辰西路1号院3号),保藏号为cgmccno.18550。
实施例2
化合物的制备
pda培养基:将马铃薯200g、葡萄糖20g、琼脂15g和水1000ml混匀,121℃高压蒸汽灭菌30min。
种子培养基:将葡萄糖4.0g、麦芽汁10.0g、酵母提取物4.0g和水1000ml混匀,将ph调节到6.5,每个250ml三角瓶中加入50ml并121℃灭菌30min。
大米培养基:将80g大米和120ml水加入500ml三角瓶中,浸泡过夜,121℃高压蒸汽灭菌30min。
1菌株shsl21的固体发酵
1.1菌株shsl21的活化
将菌株shsl21在pda平板上培养5d,待菌落长满平板后,将5个1cm2大小的菌块连同培养基接种到含有50ml种子培养基的250ml三角瓶中,在摇床上培养(25℃、200rpm)7d后作为种子培养液。
1.2菌株shsl21的固体发酵
将5ml种子培养液接种于装有大米培养基的三角瓶中,25℃无菌培养30d。
2化合物的提取
2.1在步骤1.2得到的三角瓶(含固体发酵物)中加入1.0l乙酸乙酯,室温浸提24h,收集第一次上清液。
2.2在步骤2.1的三角瓶中再次加入1.0l乙酸乙酯,室温浸提24h,收集第二次上清液。
2.3在步骤2.2的三角瓶中再次加入1.0l乙酸乙酯,室温浸提24h,收集第三次上清液。
2.4在步骤2.3的三角瓶中再次加入1.0l乙酸乙酯,室温浸提24h,收集第四次上清液。
2.5将步骤2.1的第一次上清液、步骤2.2的第二次上清液、步骤2.3的第三次上清液和步骤2.4的第四次上清液合并,减压蒸馏至干燥,得到14.0g粗提物。
3、化合物的分离纯化
3.1减压硅胶柱层析得到洗脱液
将步骤2.5得到的粗提物进行减压硅胶柱层析。
柱子型号为:8×30cm;
填充物为:薄层层析硅胶h和柱层层析硅胶(精制型);
洗脱过程为:
(1)依次用1000ml洗脱液a(由6体积份石油醚和4体积份乙酸乙酯组成)进行洗脱;
(2)1000ml洗脱液b(由5体积份石油醚和5体积份乙酸乙酯组成)进行洗脱;
(3)1000ml洗脱液c(由4体积份石油醚和6体积份乙酸乙酯组成)进行洗脱;
(4)1000ml洗脱液d(由3体积份石油醚和7体积份乙酸乙酯组成)进行洗脱;
(5)1000ml洗脱液e(由2体积份石油醚和8体积份乙酸乙酯组成)进行洗脱;
流速为50ml/min,收集洗脱液a-e的过柱后洗脱液。
3.2将层析洗脱液进行反向硅胶色谱分离得反向洗脱液
所述反向硅胶色谱分离的参数具体如下:
柱子型号为:3×60cm;
填充物为:c18;
流动相为500ml洗脱液(由6体积份甲醇和4体积份水组成),流速为0.5ml/min;
收集过柱后反向洗脱液。
3.3将反向洗脱液进行凝胶色谱分离得凝胶洗脱液
所述凝胶色谱分离的参数具体如下:
柱子型号为:3×60cm;
填充物为:sephadexlh-20;
流动相为百分含量为100%甲醇有机溶剂,流速为0.5ml/min;
收集保留体积为80-100ml的过柱后得凝胶洗脱液。
3.4将凝胶洗脱液进行反相hplc分离得hplc洗脱液
所述反相hplc分离的参数具体如下:
柱子型号为:kramosilc18柱(10μm;10×250mm);
洗脱过程为:用体积百分含量为57-59%的甲醇水溶液洗脱30min,流速为2ml/min。
收集保留时间为20.6-21.0min(峰值的保留时间tr为20.8min)的过柱后洗脱液。
3.5将步骤3.4收集的hplc洗脱液减压蒸馏至干燥,得到5.5mg产物。
4化合物的确认
将步骤3.5的产物进行有机质谱和核磁共振谱分析。
产物的表征数据如下:
黄色针状;
分子式:c14h20o6;分子量:284;
1h核磁共振图谱见图1,13c核磁共振图谱见图2;
依据以上表征数据上述化合物的理化数据和图谱,步骤3.5的产物为式(i)所示的化合物。
实施例3
式(i)所示化合物对抗幽门螺旋杆菌(h.pyloribhks159)的抑制作用
采用微量稀释法检测式(i)所示化合物对抗幽门螺旋杆菌(h.pyloribhks159)的最低抑菌浓度(mic,100μl体系)。
将甲硝唑(aladdin公司)作为化合物的阳性对照,进行平行实验。
本实施例所用细菌为:抗幽门螺旋杆菌(h.pyloribhks159)。
实验具体步骤如下:
1.制备mic板
第1孔先加脑心浸出液培养基(bhi)(具体成分包括:蛋白胨、脱水小牛脑浸粉、脱水牛心浸粉、氯化钠、葡萄糖、磷酸氢二钠,ph=7.4)173.6μl,再加6.4μl待测化合物,倍比稀释至第7孔;第8孔不加,保留90μl培养基,作为加菌不加待测化合物对照。
2.制备菌液
取固体平板上对数期生长的抗幽门螺旋杆菌(h.pyloribhks159),用bhi培养基制作成菌悬液,调整浓度od600为0.3(1×108cfu/ml),稀释10倍,为1×107cfu/ml,备用。
3.接种菌液
取10μl加至第1-8孔(每孔菌液浓度约为1.0×106cfu/ml)。培养72h判断结果。第1孔至第7孔化合物浓度分别为64、32、16、8、4、2、1μg/ml。
4.结果判断
以在小孔内完全抑制细菌生长的最低式(i)所示化合物浓度为mic。
当阳性对照孔第8孔(即不含抗生素)内细菌明显生长试验才有意义。
当在微量稀释法出现单一的跳孔时,应记录抑制细菌生长的最高式(i)所示化合物浓度。如出现多处跳孔,则不应报告结果,需重复试验。
式(i)所示化合物对抗幽门螺旋杆菌(h.pyloribhks159)的抑菌作用需重复3次试验。
式(i)所示化合物对抗幽门螺旋杆菌(h.pyloribhks159)的mic值为8μg/ml。
甲硝唑对抗幽门螺旋杆菌(h.pyloribhks159)的mic值为大于16μg/ml。
序列表
<110>中国科学院微生物研究所
<120>一种抗幽门螺旋杆菌活性的聚酮化合物及其制备方法和应用
<160>1
<170>siposequencelisting1.0
<210>1
<211>481
<212>dna
<213>镰刀菌(fusariumequiseti)
<400>1
acggcgtggccgcgacgatcaccagtaacgaggtgtatgattactacgctatggaagctc60
gacgtgaccgccaatcgatttggggaacgcgggttaccgcgagtcccaacaccaagctga120
gcttgagggttgaaatgacgctcgaacaggcatgcccgccagaatactggcgggcgcaat180
gtgcgttcaaagattcgatgattcactgaattctgcaattcacattacttatcgcatttt240
gctgcgttcttcatcgatgccagaaccaagagatccgttgttgaaagttttgatttattt300
gtttgttttactcagaagttccactaaaaacagagtttaggggtcctcgggcgggccgtc360
ccgttttacggggcgcgggctgatccgccgaggcaacgtataggtatgttcacaggggtt420
tgggagttgtaaactcggtaatgatccctccgctggttcaccaacggagaccttgttacg480
a481
- 还没有人留言评论。精彩留言会获得点赞!