一种检测血液中HBVpgRNA的试剂盒的制作方法
本发明属于分子生物学技术领域,具体涉及一种检测血液中hbvpgrna的试剂盒。
背景技术:
乙型肝炎病毒(hbv)感染是引起肝脏疾病,如肝硬化和原发性肝癌,最常见的病因之一。全球超过20亿人感染了乙肝病毒,约有2.4亿慢性乙型肝炎患者,我国约有9300万慢性乙肝病毒携带者,其中发展为慢性乙型肝炎的患者约2000~3000万人。
乙型肝炎病毒属于嗜肝性dna病毒,病毒侵入人体后,通过pres1区域与肝细胞膜上钠离子-牛磺胆酸共转运蛋白受体结合,脱去包膜后进入肝细胞质,释放松环dna(rcdna)进入肝细胞核,在肝细胞核中rcdna转变成共价闭合环状dna(cccdna),再以cccdna为模板转录出4种mrna,其中长度3.5kb的前基因组rna(pgrna)包含hbvdna上的所有遗传信息,并且pgrna能够在胞质中逆转录形成rcdna和病毒蛋白,最后装配成完整的hbv,释放至肝细胞外,而一部分rcdna进入细胞核中,再转变成cccdna,形成乙肝病毒持续复制的过程。
cccdna能以游离的形态长期稳定存在于肝细胞核中,所以cccdna的水平与乙肝复发有极大的相关性,而cccdna的检测需要对患者肝脏进行穿刺取样,侵入性检查会对患者造成一定伤害。有研究表明慢性乙肝患者血清中存在pgrna,pgrna来源于非整合的完整的hbv基因组,以衣壳化hbvpgrna病毒颗粒形式进入血液中,pgrna能够反映肝脏内cccdna的转录活动状态,在hbeag阳性hbv感染者中,血清pgrna与肝内cccdna的水平呈正相关,所以pgrna可以作为hbv病毒复制和预后的敏感性血清标志物,hbvpgrna持续阴性和低hbsag水平可以判定为慢性乙型肝炎的“准临床治愈”,在指导乙肝治疗安全停药方面具有重要意义。但目前市场上用于检测pgrna的技术和试剂盒较少,且pgrna的检测易受到来自dna的干扰,已有产品的灵敏度不能满足实际需求。虽然申请号为201611099305.8的中国发明专利,公开了一种组合物、其应用以及含有该组合物的试剂盒,其能够对血液中的hbvpgrna定量检测,且灵敏度可低至5个拷贝,但是其检测是基于数字pcr技术,而基于荧光定量pcr检测技术的试剂盒还无法达到上述灵敏度。
技术实现要素:
为了克服上述现有技术的缺陷,本发明所要解决的技术问题是:提供一种利用荧光定量pcr检测技术的高灵敏度hbvpgrna检测试剂盒。
为了解决上述技术问题,本发明采用的技术方案为:一种检测血液中hbvpgrna的试剂盒,包括扩增试剂,所述扩增试剂包括pcr反应液ⅰ,所述pcr反应液ⅰ包括seqidno:1、seqidno:2和seqidno:3所示的引物以及seqidno:4和seqidno:5所示的探针(见表1)。
表1
本发明的有益效果在于:本发明提供的试剂盒,利用rna单链需逆转录的特点,在逆转录引物的5’端增加一段特异的非hbv的序列,同时将合成该段序列的寡核苷酸作为cdna扩增的引物,达到特异性扩增pgrna的目的,使得检测过程中不受dna干扰,有效提高了试剂盒检测时的灵敏度,对乙肝病毒pgrna的检测下限(最低检出限)可达10copies/ml。
附图说明
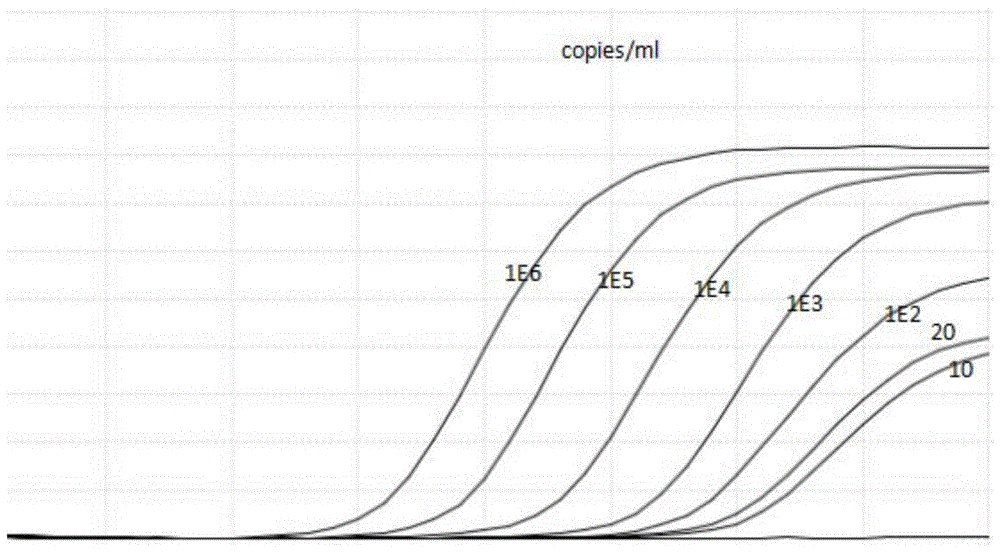
图1所示为本发明具体实施方式的检测血液中hbvpgrna的试剂盒的灵敏度检测结果图;
图2所示为本发明具体实施方式的检测血液中hbvpgrna的试剂盒的特异性检测结果图。
具体实施方式
为详细说明本发明的技术内容、所实现目的及效果,以下结合实施方式并配合附图予以说明。
本发明最关键的构思在于:在逆转录引物的5’端增加一段特异的非hbv的序列,同时将合成该段序列的寡核苷酸作为cdna扩增的引物。
请参照图1至图2所示,本发明的一种检测血液中hbvpgrna的试剂盒,包括扩增试剂,所述扩增试剂包括pcr反应液ⅰ,所述pcr反应液ⅰ包括seqidno:1、seqidno:2和seqidno:3所示的引物以及seqidno:4和seqidno:5所示的探针。
从上述描述可知,本发明的有益效果在于:本发明提供的试剂盒,利用rna单链需逆转录的特点,在逆转录引物的5’端增加一段特异的非hbv的序列,同时将合成该段序列的寡核苷酸作为cdna扩增的引物,达到特异性扩增pgrna的目的,使得检测过程中不受dna干扰,有效提高了试剂盒检测时的灵敏度,对乙肝病毒pgrna的检测下限(最低检出限)可达10copies/ml。
进一步的,所述pcr反应液ⅰ还包括pcr缓冲液、datp、dutp、dgtp和dctp。
进一步的,所述扩增试剂还包括内标,所述内标为克隆质粒。
进一步的,所述括扩增试剂还包括pcr反应液ⅱ,所述pcr反应液ⅱ包括taq酶、udg酶、mmlv逆转录酶和rnase抑制剂。
进一步的,所述括扩增试剂还包括阳性质控品、阴性质控品和定量参考品,所述阳性质控品为hbv阳性血清样本,所述阴性质控品为hbv阴性血清样本,所述定量参考品为定值的hbv阳性血清样本。
进一步的,上述的试剂盒还包括pgrna提取试剂,所述pgrna提取试剂包括裂解液、抑制物去除液、洗涤液a、洗涤液b、洗脱液和dna消化反应液。
从上述描述可知,通过设置pgrna提取试剂,便于利用同一试剂盒快速进行血液中hbvpgrna的检测。
进一步的,所述裂解液为硫氰酸胍,所述抑制物去除液为蛋白酶k,所述洗涤液a由硫氰酸胍和无水乙醇组成,所述洗涤液b由氯化钠和无水乙醇组成,所述洗脱液为灭菌纯化水,所述dna消化反应液为dnaseⅰ。
实施例1:
一种检测血液中hbvpgrna的试剂盒,包括表2所示组分,其中引物和探针的序列如seqidno:1-seqidno:5所示;
表2
其中,pcr反应液1中datp、dutp、dgtp、dctp为0.5-2mm、mg2+为2-4mm、引物为200-500nm、探针为100-300nm。
所述内标中克隆质粒的基因序列为:taggaggctgtaggcataaagttcgtagtggtgtcacacgtctgtctcgcacgctagctcctcaggtgtcgtagtgtggacacatacgggctaaacag。
所述定量参考品1、定量参考品2、定量参考品3、定量参考品4分别为1×104copies/ml、1×105copies/ml、1×106copies/ml、1×107copies/ml的阳性血清样本。
所述阳性质控品1和阳性质控品2分别为1×103-5×104copies/ml和1×106-5×107copies/ml的阳性血清样本。
实施例2:
利用实施例1的试剂盒,检测血液中hbvpgrna,具体步骤如下:
1、病毒核酸提取
1)配制相关试剂。
2)取2.0ml离心管n个并编号(n=样本例数+阳性质控品×2+阴性质控品×1+定量参考品×4),分别加入10μl抑制物去除液,400μl样本,再加入600μl裂解液+内标质粒混合液(裂解液:内标质粒=600:1,现配现用),震荡混匀,瞬时离心,置70℃金属浴10min后,瞬时离心,冷却至室温;
3)分别加入500μl乙醇,颠倒混匀,瞬时离心,再加入10μl磁珠悬液,颠倒混匀,室温静置10min,每隔1-2min再次颠倒混匀,保持磁珠混匀状态;
4)将离心管置于磁力架上,待磁珠完全吸附至管壁后,吸弃废液;取下离心管,分别加入1ml洗涤液a,颠倒数次使磁珠均匀分散;
6)将离心管再次置于磁力架上,待磁珠完全吸附至管壁后,吸弃废液;取下离心管,分别加入1ml洗涤液b,颠倒数次使磁珠均匀分散;
7)将离心管置于磁力架上,待磁珠完全吸附至管壁后,尽量将废液吸弃干净,然后再重复依次步骤6)和7);
8)离心管开盖置于50℃金属浴30s~2min,待磁珠表面无水迹,加入20μl洗脱液,轻弹管壁使磁珠分散,再次置于50℃金属浴5min,期间若磁珠沉降至管底,再次轻弹管壁混匀;
9)将离心管置于磁力架上,待磁珠完全吸附至管壁后,取上清即为hbv核酸。
2、pcr反应体系配制及加样
取pcr反应液1和pcr反应液2,根据样本例数按如下体系配制pcr反应体系:
pcr反应液ⅰ7.5μl×n;pcr反应液ⅱ1.5μl×n;
充分混匀后每管10μl分装至pcr管中,每管加入15μlhbv核酸样本,最终体系为25μl/管,混匀,瞬时离心。
3、pcr扩增检测
将上述pcr反应管放入荧光pcr仪中,程序设置如表3所示。
表3
其中,荧光信号收集在阶段3:60℃40sec(*标记),收集的荧光信号为探针标记的荧光(fam/vic)。
4、结果分析
根据仪器自动分析后的图像适当调节基线的start值和stop值以及阈值(使阴性质控品的曲线平直或低于阈值线),软件自动定量。
5、质量控制
1)内标:vic通道的33<ct值≤35,扩增曲线呈s形;
2)阴性质控品:fam通道无ct值;
3)阳性质控品1:定量值介于1×103-5×104copies/ml;
4)阳性质控品2:定量值介于1×106-5×107copies/ml;
5)定量参考品:均为阳性,线性相关系数介于0.98-1;
以上参数须全部满足,否则应重新测试。
实施例3:
对实施例1的试剂盒进行灵敏度和特异性的检测。
1)灵敏度检测
用阴性血清将hbv定量国家标准品梯度稀释至1e5、1e4、1e3、1e2、50、20、10copies/ml及以下,使用本试剂盒对hbvpgrna进行定量检测,检测结果见图1所示。
可以看出,本试剂盒的最低检出限可达到10copies/ml,且经重复实验,结果显示浓度为10copies/ml的病毒样本检出率为95%。
2)特异性检测
取临床hbv阴性标本用本试剂盒进行检测,阴性标本中包括甲型肝炎病毒、丙型肝炎病毒、1型/2型单纯疱疹病毒、带状疱疹病毒、细胞巨化病毒、黄热病病毒等常见病原体核酸样本,检测结果均显示为阴性,符合率100%。检测结果如图2所示。
可以看出,本试剂盒具有良好的特异性。
综上所述,本发明提供的试剂盒,利用rna单链需逆转录的特点,在逆转录引物的5’端增加一段特异的非hbv的序列,同时将合成该段序列的寡核苷酸作为cdna扩增的引物,达到特异性扩增pgrna的目的,使得检测过程中不受dna干扰,有效提高了试剂盒检测时的灵敏度,对乙肝病毒pgrna的检测下限(最低检出限)可达10copies/ml。
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等同变换,或直接或间接运用在相关的技术领域,均同理包括在本发明的专利保护范围内。
序列表
<110>阿吉安(福州)基因医学检验实验室有限公司
<120>一种检测血液中hbvpgrna的试剂盒
<160>5
<170>siposequencelisting1.0
<210>1
<211>19
<212>dna
<213>人工序列
<400>1
taggaggctgtaggcataa19
<210>2
<211>14
<212>dna
<213>人工序列
<400>2
aagccacccaaggc14
<210>3
<211>21
<212>dna
<213>人工序列
<400>3
ctgtttagcccgtatgtgtcc21
<210>4
<211>22
<212>dna
<213>人工序列
<400>4
ctttttcacctctgcctaatca22
<210>5
<211>23
<212>dna
<213>人工序列
<400>5
ctgtctcgcacgctagctcctca23
- 还没有人留言评论。精彩留言会获得点赞!