用于跟踪和操纵细胞RNA的融合蛋白和融合核糖核酸的制作方法
相关申请的交叉引用本申请要求2018年4月20日提交的美国临时申请序列号62/660,849和2018年5月2日提交的美国临时申请序列号62/665,860的优先权,这两个申请通过引用全文纳入本文。政府支持声明本发明是在政府支持下由国家卫生研究院(nationalinstitutesofhealth)授予的基金号ns103172资助完成。美国政府享有本发明的一定权利。
背景技术:
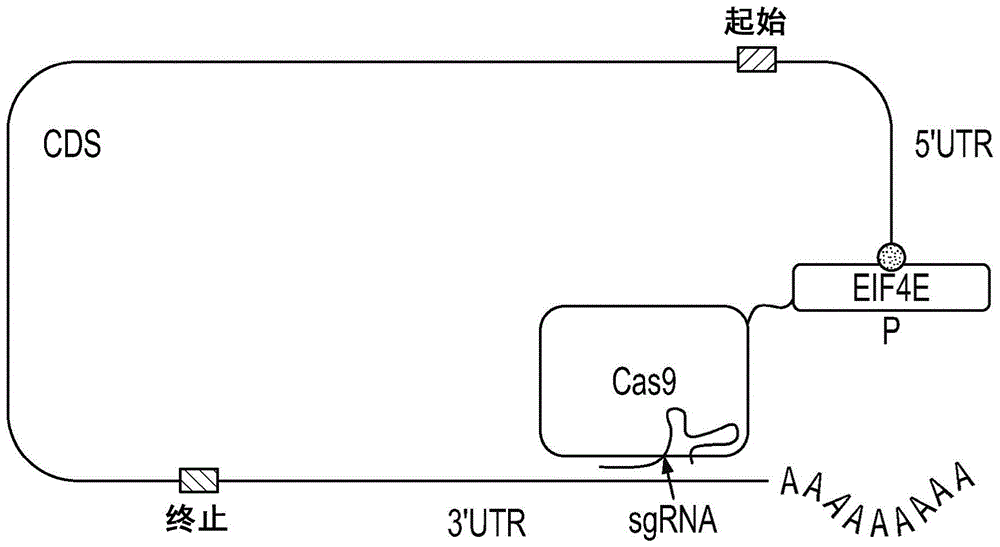
:当前没有统一的系统可以既上调又下调特定信使rna(mrna)靶标的翻译。实现靶向下调的已知方法包括反义寡核苷酸(aso)和短干扰rna(sirna)。但是,这两种技术的作用都是使信使rna靶标不稳定并下调翻译,而不是上调翻译。几乎没有增加mrna翻译的已知方法,并且这些方法还没有充分表征。因此,需要提供用于招募反式的翻译起始前复合物并由此在细胞和基因治疗技术中控制翻译的组合物和方法。技术实现要素:本公开涉及使用crispr-cas蛋白融合物控制细胞中mrna翻译的组合物,系统,方法和试剂盒。这些组合物,方法,系统和试剂盒利用了crispr-cas系统的rna靶向能力,该系统使用向导rna来提供一个简单且可快速编程的系统,用于识别细胞中的rna分子。这些组合物,方法,系统和试剂盒进一步利用crispr-cas系统结合靶信使rna的能力,通过将募集翻译起始前复合物的核糖核酸序列融合到单链向导rna上从而融合到结合的信使rna来启动反式翻译。crispr-cas系统还对信使rna的稳定性产生中性影响,这使得蛋白质表达的任何测量变化都成为融合蛋白质效应物的变量。当与用于控制mrna表达的其他组合物,方法,系统和试剂盒相比时,本文所述的组合物,系统,方法和试剂盒提供了高实用性和多功能性。一方面,组合物包含一种或多种编码以下物质的多核苷酸:(i)向导核苷酸序列-可编程rna结合蛋白;和(ii)翻译修饰蛋白。在一些实施方式中,所述向导核苷酸序列可编程rna结合蛋白包含以下的至少一种:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,casm及其各自的生物等同物。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白包含以下的至少一种:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白是核酸酶失活的。在一些实施方式中,翻译修饰蛋白是以下的至少一种:真核翻译起始因子4e(eif4e)(seqidno:52-59),真核翻译起始因子4e结合蛋白(eif4e-bp1)(seqidno:61-62),泛素相关蛋白2-样(ubap2l)(seqidno:64-71)及其各自的生物等同物。在一些实施方式中,翻译修饰蛋白由具有以下序列的多核苷酸编码,该序列包含以下的至少一种的全部或部分:seqidno:52-55,seqidno:61,seqidno:64-67,seqidno:94-193,seqidno:285及其各自的生物等同物。在一些实施方式中,其中所述翻译修饰蛋白具有氨基酸序列,该氨基酸序列包含以下的至少一种的全部或部分:seqidno:56-59,seqidno:62,seqidno:68-71及其各自的生物等同物。在一些实施方式中,所述组合物还包含接头。在一些实施方式中,接头是肽接头。在一些实施方式中,肽接头包含三肽ggs的一个或多个重复。在一些实施方式中,接头是非肽接头。在一些实施方式中,非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白与向导rna(grna),crisprna(crrna)或反式激活crrna(tracrrna)结合。在一些实施方式中,翻译修饰蛋白的一个或多个激酶磷酸化结构域被突变。在一些实施方式中,组合物还包含载体。在一些实施方式中,载体是腺病毒载体,腺相关病毒载体或慢病毒载体。在一些实施方式中,载体还包含表达控制元件。在一些实施方式中,载体还包含可选择标志物。在一些实施方式中,载体还包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸。在一些实施方式中,grna或crrna包含与靶rna2补的核苷酸序列。在一个方面,一种融合蛋白,其包含:(i)向导核苷酸序列-可编程rna结合蛋白;和(ii)翻译修饰蛋白。在一些实施方式中,一种用于转录后基因调控的系统,该系统包括:(i)融合蛋白;和(ii)grna;或(iii)crrna和tracrrna;其中grna或crrna包含与靶mrna互补的序列。在一些实施方式中,一种用于转录后调节基因表达的方法,所述方法包括使靶mrna与融合蛋白接触,其中所述向导核苷酸序列-可编程rna结合蛋白能结合与靶rna的区域杂交的grna或crrna。在一个方面,一种融合rna,其包含:(i)向导核苷酸序列-可编程rna;和(ii)一个或多个内部核糖体进入位点(ires)。在一些实施方式中,所述向导核苷酸序列-可编程rna是向导rna(grna)或crisprrna(crrna)。在一些实施方式中,所述向导核苷酸序列-可编程rna衍生自来自化脓性链球菌,金黄色葡萄球菌,新凶手弗朗西丝氏菌,脑膜炎奈瑟氏球菌,嗜热链球菌或侧孢短芽孢杆菌的向导rna支架。在一些实施方式中,ires是以下的至少一种:脊髓灰质炎ires,鼻病毒ires,脑心肌炎病毒ires(emcv-ires),小核糖核酸病毒ires,口蹄疫病毒ires(fmdv-ires),口咽病毒ires,卡波西氏肉瘤相关疱疹病毒ires(kshv-ires),甲型肝炎ires,丙型肝炎ires,经典猪瘟病毒ires,瘟病毒ires,牛病毒性腹泻病毒ires,弗云德(friend)鼠白血病ires,莫洛尼鼠白血病ires(mmlv-ires),劳斯肉瘤病毒ires,人类免疫缺陷病毒ires(hiv-ires),小珀椿象肠病毒ires,双顺反子病毒(cripavirus)ires,蟋蟀麻痹病毒ires,锥蝽病毒ires,禾谷缢管蚜病毒ires,马立克氏病病毒ires,成纤维细胞生长因子(fgf-1ires和fgf-2ires),血小板衍生生长因子b(pdgf/c-sisires),血管内皮生长因子(vegfires)和胰岛素样生长因子2(igf-iiires)。在一些实施方式中,一种用于转录后调节基因表达的方法,该方法包括使靶mrna与融合rna和向导核苷酸序列-可编程rna结合蛋白接触。除非另外定义,本文中使用的所有技术和科学术语为本发明所属领域普通技术人员通常所理解的含义。本文描述了本发明中所用的方法和材料;也可以使用本领域已知的其它合适的方法和材料。所述材料、方法和实施例都仅是说明性的,不构成限制。本文中述及的所有出版物、专利申请、专利、序列、数据库条目和其它参考文献都通过引用其全文纳入本文。若有抵触,以本包括定义在内的本申请说明书为准。通过引用纳入本说明书中提到的所有发表物、专利和专利申请通过引用纳入本文,就好像将各篇单独的发表物、专利或专利申请专门和单独地通过引用纳入本文那样。对于通过引用纳入的出版物和专利或专利申请与本说明书中所含公开内容相矛盾的内容,均意于以本说明书为准和/或本说明书优先于任何相矛盾的材料。附图简要说明所附权利要求书中具体说明了本公开的新特征。通过参考下面的详细描述,可以获得对特征和优点的更好的理解,下面的详细描述阐述了示例性实施方式和附图(本文中的“图”),其中:图1描绘了与修饰的eif4e蛋白融合的核酸酶失活(dead)的cas9(dcas9)。示意图显示dcas9-eif4e靶向代表性靶转录物mrna的3′utr。修饰的eif4e有助于转录物环化以及eif4g和核糖体起始前复合物的招募。图2描绘了与修饰的eif4e-bp1融合的dcas9。示意图显示dcas9-eif4e-bp1靶向代表性靶转录物的3′utr。修饰的eif4e-bp1有助于转录物mrna环化,并防止eif4e-bp1从eif4e脱离。组成性结合阻止eif4g和核糖体起始前复合物的招募。图3a-3c描绘了(图3a)效应物和(图3b)报告物构建体的dna构建体的示意图,用于表征研究。cas9-eif4e的表达水平与效应物上共表达的cfp荧光团相关。yfp和rfp由报告物上的不同启动子共同表达。但是,只有yfp信使rna带有与单向导rna(sgrna)的间隔区互补的靶位点(luc靶位点)。(图3c)结果:(i)热图显示相对于报告物(x轴)和效应物(y轴)dna构建体水平的yfp/rfp比如何倍数变化。用于热图的数据点表示落入定义箱(bin)中的单细胞的平均荧光。(ii)与(i)中提供的数据相同,但yfp/rfp比绘制为第三变量(z轴)。(iii)用于生成热图的数据点的残差。图4a-4c描绘了(图4a)效应物和(图4b)报告物构建体的dna构建体的示意图,用于表征研究。cas9-eif4e-bp1的表达水平与效应物上共表达的cfp荧光团相关。yfp和rfp由报告物上的不同启动子共同表达。但是,只有yfp信使rna带有与单向导rna(sgrna)的间隔区互补的靶位点(luc靶位点)。(图4c)结果:(i)热图显示相对于报告物(x轴)和效应物(y轴)dna构建体水平的yfp/rfp比如何倍数变化。用于热图的数据点表示落入定义箱中的单细胞的平均荧光。(ii)与(i)中提供的数据相同,但yfp/rfp比绘制为第三变量(z轴)。(iii)用于生成热图的数据点的残差。图5描绘了用于调节靶mrna翻译的示例性系统的示意图。ires可用于在靶信使rna上成核(nucleate)翻译起始因子。当它们与靶向向导3′融合时,crispr/cas蛋白将ires元件共定位到靶信使rna。i型和ii型ires元件采用扫描机制来找到合适的起始密码子(aug=绿色矩形)。ires的结构特征稳定化起始密码子(aug)上的起始前复合物,从而启动了反式翻译。图6a-6c显示了示例性效应物和报告物系统的设计,以测试dcas9和dcas13b的反式ires活性。用于表征(图6a)dcas9和(图6b)dcas13b调控的dna构建体示意图。显示了每个crispr/cas系统的示例性(i)效应物和(ii)报告物构建体。dcas表达水平与效应物上共表达的cfp荧光团相关。yfp和rfp由报告物上的不同启动子共同表达。然而,只靶向yfp信使rna用于转录后调控。结果,可以将转录后调控测量为yfp表达相对于rfp表达的变化。(图6c)翻译可能更倾向于在三个潜在阅读框(+0,+1,+2)中的任何一个上存在的特定起始密码子(绿色框)。从+0阅读框表达:可以使用elisa或质谱对flag肽的表达进行概况分析。从+1阅读框表达:c末端ha标签标记所有翻译的蛋白同种型,且可使用western印迹进行概况分析。从+2阅读框表达:对于此框的表达的监测无特定方法。以下是crispr引导物靶向的位置(dcas9宽度为20nt,dcas13b宽度为30nt)。图7a-7b显示了使用emcvires的cas9介导的反式翻译起始,以增强蛋白质产量。(图7a)dcas9靶向的间隔区的位置,其用于对30.5kda蛋白产物表达的变化进行概况分析。(图7b)使用通过western印迹的光密度测定计算,相对于使用非靶向(nt)sgrna-ires的观察结果,绘制了每个间隔区靶向dcas9后ha标签信号相对cherry信号的变化。图8描述了转基因表达报告物构建体。rcas9由四环素反应元件(tre)报告物表达。组成型启动子驱动多顺反子转录物,该转录物包含由p2a自裂解肽隔开的嘌呤霉素n-乙酰基转移酶(puro)和反向四环素(tet)控制的反式激活子(rtta),以及与核定位信号(nls)融合的cfp,之前是内部核糖体进入位点(ires)。第二构建体在同一质粒背景中驱动融合到ubap2l的rcas9。将rcas9和rcas9-ubap2l构建体以随机拷贝数整合到基因组中以建立稳定表达的品系。第三报告物构建体包含靶向yfp报告物中指示位点的u6启动子驱动的单向导(sg)rna,yfp报告物包含与由tet诱导型启动子驱动的组蛋白h2b融合的yfp,和由ef1α启动子驱动的nls融合rfp。图9描绘了在每个靶向位点上瞬时转染入表达rcas9-ubap2l的细胞中的报告物的定量基于荧光激活细胞分选(facs)的报告物测定,将其标准化至表达rcas9的细胞。误差线表示每个位点与n=2,000rcas9-ubap2l和n=2,000rcas9表达细胞的标准差(sd)。具体实施方式下文将更完整地描述本公开的实施方式。但是,本公开的各方面可以以许多不同的形式来实施,并且不应被解读成限制于本文阐述的实施方式。当然,提供这些实施方式使得本公开透彻而完整,并且能够向本领域技术人员完整地展示本发明的范围。本文描述中所用的术语仅出于描述特定实施方式的目的,而不是限制性的。除非另外定义,本文中所使用的所有术语(包括技术和科学术语)的含意与本发明所属领域普通技术人员通常所理解的相同。还将进一步理解的是,术语,诸如在常用词典中定义的术语,应被解释为具有与其在本申请和相关领域上下文中的含义一致的含义,并且不应当以理想化或过度正式的意义解释,除非本文明确定义。虽然下文没有明确定义,但是应当根据其通常含义理解这类术语。需要具体说明的是,除非另有说明,否则本文描述的本发明的各种特征可以以任意组合方式使用。此外,本公开还考虑了在一些实施方式中,可以排除或省略本文所示的任何特征或特征的组合。举例说明,如果说明书指出复合体包含组分a、b或c,其具体旨在说明a、b或c中任意一种或其组合可以被省略并且单独或以任意组合方式排除。除非以其他方式明确地指出,所有特定的实施方式、特征和术语旨在包括所述实施方式、特征或术语及其生物学等同物。所有指定数值,例如ph、温度、时间、浓度和分子量,包括范围,都涵盖(+)或(-)1.0或0.1(如适用)幅度变动的近似值,或者+/-15%,或者10%,或者5%或者2%的变化。应理解,尽管并非均为明示,所有指定数值之前都有“约”。还应理解,尽管并非均为明示,本文述及的试剂仅仅是示例性的,其等同物是本领域所知的。定义如在本发明和所附权利要求的描述中所使用的,单数形式的“一个”,“一种”和“该”也包括复数形式,除非文本中有另外的明确表示。本文所用术语“约”在指示诸如量或浓度等可测量值时,表示涵盖了该特定量的20%、10%、5%、1%、0.5%或甚至0.1%的变化。该术语或“可接受的”、“有效的”或“足够的”在用于描述本文所公开的任何组分、范围、剂型等的选择时旨在表示所述组分、范围、剂型适合所公开的目的。本文所用术语“腺相关病毒”或“aav”指这样类型的病毒的成员,所述病毒与该名称相关并属于依赖细小病毒(dependoparvovirus)属,细小病毒科。已知该病毒的多种血清型适于基因递送;所有已知的血清型可以感染来自各种组织类型的细胞。现有技术公开了至少11或12种(依次编号)。能够用于本公开方法的非限制性示例性血清型包括11或12种血清型中的任一种,例如,aav2、aav5和aav8,或变体血清型,例如,aav-dj。aav结构颗粒包含vp1,vp2和vp3形成的60个蛋白质分子。每个颗粒包含约5个vp1蛋白,5个vp2蛋白和50个vp3蛋白,排列成二十面体结构。本文所用,试剂(例如,融合rna,病毒颗粒,载体,多核苷酸,细胞,细胞群,组合物或药物组合物)的“给药”包括向对象引入或递送试剂以实现其预定功能的任何途径。给药可以通过任何合适的途径进行,包括口服,鼻内,眼内,眼科,肠胃外(静脉内,肌内,腹膜内或皮下)或局部进行。给药包括自我给药和他人给药。此外,如本文所述,“和/或”表示涵盖了任何以及所有可能的一种或多种相关所列项目的组合,以及当在可选情况下解释时缺少组合(“或”)。术语“向导核苷酸序列可编程rna”是指与crispr相关的rna,其包含与靶核酸互补和/或同源的序列。向导核苷酸序列可编程rna的非限制性实例包括单向导rna(sgrna)和crrna,及其生物学等同物。在一些实施方式中,向导核苷酸序列可编程rna是合成的。在一些实施方式中,“支架”rna是指向导核苷酸序列可编程rna,其中与融合rna中的靶核酸互补和/或同源的序列可以被修饰。本公开的向导rna(grna)可以包含间隔区序列和支架序列。在一些实施方式中,向导rna是包含连续间隔区序列和支架序列的单向导rna(sgrna)。在整个公开中,术语向导rna(grna)和单向导rna(sgrna)可互换使用。在一些实施方式中,间隔区序列和支架序列不连续。在一些实施方式中,支架序列包含“直接重复”(dr)序列。dr序列是指crispr基因座中的重复序列(天然存在于细菌基因组或质粒中),其间散有间隔区序列。众所周知,如果相关的crispr基因座的序列是已知的,人们将能够推断出相应cas蛋白的dr序列。在一些实施方式中,编码本发明的向导rna或单向导rna的序列包含由接头序列隔开的间隔区序列和支架序列或由其组成。在一些实施方式中,接头序列可包含1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50个核苷酸或任何两者之间数量的核苷酸或由其组成。在一些实施方式中,接头序列可包含至少1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50个核苷酸或任何两者之间数量的核苷酸。本公开的向导rna(grna)可以包含非天然存在的核苷酸。在一些实施方式中,本发明的向导rna或编码该向导rna的序列包含修饰的或合成的rna核苷酸或由其组成。示例性的修饰的rna核苷酸包括但不限于假尿苷(ψ),二氢尿苷(d),肌苷(i)和7-甲基鸟苷(m7g),次黄嘌呤,黄嘌呤,黄嘌呤核苷,7-甲基鸟嘌呤,5,6-二氢尿嘧啶,5-甲基胞嘧啶,5-甲基胞嘧啶,5-羟甲基胞嘧啶,异鸟嘌呤和异胞嘧啶。本公开的向导rna(grna)可以结合靶序列内的修饰的rna。在靶序列内,本公开的向导rna(grna)可以结合修饰的rna。表观遗传或转录后修饰的rna包括但不限于2′-o-甲基化(2′-ome)(2′-o-甲基化发生在核糖部分的游离2′-oh的氧上),n6-甲基腺苷(m6a)和5-甲基胞嘧啶(m5c)。在本发明的组合物的一些实施方式中,本发明的向导rna包含编码非编码c/d盒小核仁rna(snorna)序列的至少一个序列。在一些实施方式中,snorna序列包含与靶rna互补的至少一个序列,其中rna分子的靶序列包含至少一个2′-ome。在一些实施方式中,snorna序列包含与靶rna互补的至少一个序列,其中与靶rna互补的至少一个序列包含c盒基序(rugauga)和d盒基序(cuga)。本公开的间隔区序列与rna分子的靶序列结合。本公开的间隔区序列可包含crisprrna(crrna)。本公开的间隔区序列包含与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列或由其组成。与rna分子的靶序列结合后,间隔区序列可将支架序列和融合蛋白中的一个或多个引导至rna分子。在一些实施方式中,与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列与靶序列具有至少50%,55%,60%,65%,70%,75%,80%,85%,90%,95%,96、97%,98%,99%或期间任何百分比的相同性。在一些实施方式中,与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列与靶序列具有100%的相同性。本公开的支架序列结合本公开的rna结合蛋白。本公开的支架序列可以包含反式作用rna(tracrrna)。本公开的支架序列包含与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列或由其组成。在与rna分子的靶序列结合后,支架序列可将融合蛋白引导至rna分子。在一些实施方式中,与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列与靶序列具有至少50%,55%,60%,65%,70%,75%,80%,85%,90%,95%,96、97%,98%,99%或其间任何百分比的相同性。在一些实施方式中,与rna分子的靶序列具有足够互补性以选择性地结合至靶序列的序列与靶序列具有100%的相同性。替代地或另外,在一些实施方式中,本公开的支架序列包含与本公开的融合蛋白的第一rna结合蛋白或第二rna结合蛋白结合的序列或由其组成。在一些实施方式中,本公开的支架序列包括二级结构或三级结构。示例性的二级结构包括但不限于螺旋,茎环,凸起,四环和假结。示例性的三级结构包括但不限于a形螺旋,b形螺旋和z形螺旋。示例性的三级结构包括但不限于扭曲的或螺旋状的茎环。示例性的三级结构包括但不限于扭曲的或螺旋状的假结。在一些实施方式中,本公开的支架序列包括至少一个二级结构或至少一个三级结构。在一些实施方式中,本公开的支架序列包含一个或多个二级结构或一个或多个三级结构。在本公开的组合物的一些实施方式中,向导rna或其部分选择性地结合至本公开的rna分子中的四环基序(tetraloopmotif)。在一些实施方式中,rna分子的靶序列包含四环基序。在一些实施方式中,四环基序是包含gaaa,guga,gcaa或gaga的一个或多个序列或由其组成的“grna”基序。在本公开的组合物的一些实施方式中,与rna分子的靶序列结合的向导rna或其部分与rna分子的靶序列杂交。在一些实施方式中,与第一rna结合蛋白或第二rna结合蛋白结合的向导rna或其部分与第一rna结合蛋白或第二rna结合蛋白共价结合。在一些实施方式中,与第一rna结合蛋白或第二rna结合蛋白结合的向导rna或其部分与第一rna结合蛋白或第二rna结合蛋白非共价结合。在本公开的组合物的一些实施方式中,向导rna或其部分包含10-100个核苷酸或由其组成,包括端点。在一些实施方式中,本公开的间隔区序列包含10-30个核苷酸或由其组成,包括端点。在一些实施方式中,本公开的间隔区序列包含15、16、17、18、19、20、21、22、23、24、25、26、27、28、29或30个核苷酸或由其组成。在一些实施方式中,本公开的间隔区序列包含20个核苷酸或由20个核苷酸组成。在一些实施方式中,本公开的间隔区序列包含21个核苷酸或由21个核苷酸组成。在一些实施方式中,本公开的支架序列包含10-100个核苷酸或由其组成,包括端点。在一些实施方式中,本公开的支架序列包含30、35、40、45、50、55、60、65、70、76、80、87、90、95、100或其之间任何数目的核苷酸或由其组成。在一些实施方式中,本公开的支架序列包含85-95个核苷酸或由其组成,包括端点。在一些实施方式中,本公开的支架序列包含85个核苷酸或由其组成。在一些实施方式中,本公开的支架序列包含90个核苷酸或由其组成。在一些实施方式中,本公开的支架序列包含93个核苷酸或由其组成。在本公开的组合物的一些实施方式中,向导rna或其部分不包含核定位序列(nls)。在本公开的组合物的一些实施方式中,向导rna或其部分不包含与原间隔区相邻基序(pam)互补的序列。在一些实施方式中,本公开的治疗或药物组合物不包含含pam的寡核苷酸(pammeroligonucleotide)。在其他实施方式中,任选地,非治疗或非药物组合物可以包含含pam的寡核苷酸。在本公开的组合物的一些实施方式中,向导rna或其部分包含与原间隔区侧翼序列(pfs)互补的序列。在一些实施方式中,包括其中向导rna或其部分包含与pfs互补的序列的那些,rna结合蛋白可以包含分离或衍生自cas蛋白的序列,例如但不限于cas9,cas13b或cas13d蛋白。在一些实施方式中,包括其中向导rna或其部分包含与pfs互补的序列的那些,rna结合蛋白可包含编码cas蛋白的序列,例如但不限于cas9,cas13b或cas13d蛋白,或其rna结合部分。在一些实施方式中,向导rna或其部分不包含与pfs互补的序列。在一些实施方式中,编码本公开的向导rna的序列还包含编码启动子以驱动向导rna表达的序列。在一些实施方式中,包含编码本公开的向导rna的序列的载体还包含编码启动子以驱动向导rna表达的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码组成型启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码诱导型启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码杂合或重组启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码能够在哺乳动物细胞中表达向导rna的启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码能够在人细胞中表达向导rna的启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码能够表达向导rna并将向导rna限制在细胞核内的启动子的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码人rna聚合酶启动子的序列或从编码人rna聚合酶启动子的序列分离或衍生的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码u6启动子的序列或从编码u6启动子的序列分离或衍生的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码人trna启动子的序列或从编码人trna启动子的序列分离或衍生的序列。在一些实施方式中,编码启动子以驱动向导rna表达的序列包括编码人缬氨酸trna启动子的序列或从编码人缬氨酸trna启动子的序列分离或衍生的序列。在本公开的组合物的一些实施方式中,编码启动子以驱动向导rna表达的序列进一步包含调节元件。在一些实施方式中,包含编码启动子以驱动向导rna表达的序列的载体还包含调节元件。在一些实施方式中,调节元件增强了向导rna的表达。示例性调节元件包括但不限于增强子元件,内含子,外显子或其组合。在本公开的组合物的一些实施方式中,本公开的载体包含以下的一个或多个:编码向导rna的序列,编码驱动向导rna表达的启动子的序列和编码调节元件的序列。在本发明的组合物的一些实施方式中,载体还包含编码本公开的融合蛋白的序列。术语“向导核苷酸序列可编程rna结合蛋白”是指与crispr相关的,rna向导的核酸内切酶,例如但不限于ii型crisprcas蛋白,例如化脓性链球菌cas9(spcas9)及其直系同源物和生物学等同物。本公开的示例性cas9蛋白可以分离或衍生自任何物种,包括但不限于细菌或古细菌。本公开的示例性cas9蛋白可以分离或衍生自任何物种,包括但不限于化脓性链球菌(streptococcuspyogenes),地中海嗜盐杆菌(haloferaxmediteranii),结核分枝杆菌(mycobacteriumtuberculosis),土拉热弗朗西丝氏菌新凶手亚种(francisellatularensissubsp.novicida),多杀巴斯德氏菌(pasteurellamultocida),脑膜炎奈瑟氏球菌(neisseriameningitidis),空肠弯曲菌(campylobacterjejune),嗜热链球菌(streptococcusthermophilus),红嘴鸥弯曲杆菌cf89-12(campylobacterlaricf89-12),鸡毒枝原体f株(mycoplasmagallisepticumstr.f),硝酸盐还原海杆状菌dsm16511株(nitratifractorsalsuginisstr.dsm16511),食清洁剂细小棒菌(parvibaculumlavamentivorans),肠道罗斯拜瑞氏菌(roseburiaintestinalis),灰质奈瑟氏球菌(neisseriacinerea),重氮糖杆菌杆菌(gluconacetobacterdiazotrophicus),固氮螺菌b510(azospirillumb510),螺旋体球菌伙伴株(sphaerochaetaglobusstr.buddy),柱状黄杆菌(flavobacteriumcolumnare),塔氏杆菌(fluviicolataifensis),共生拟杆菌(bacteroidescoprophilus),流动支原体(mycoplasmamobile),香肠乳杆菌(lactobacillusfarciminis),巴斯德链球菌(streptococcuspasteurianus),约氏乳杆菌(lactobacillusjohnsonii),伪中间型葡萄球菌(staphylococcuspseudintermedius),产线龈沟菌(filifactoralocis),牙密螺旋体(treponemadenticola),嗜肺军团杆菌巴黎株(legionellapneumophilastr.paris),华德萨特菌(sadellawadsworthensis),白喉棒状杆菌(corynebacterdiphtherias),金黄色链球菌(streptococcusaureus)和新凶手弗朗西丝氏菌(francisellanovicida)。cas9的生物学等同物包括但不限于v型系统(例如cpf1蛋白)和vi型crispr系统(例如cas13a,c2c2,cas13b,casrx,cas13d和casm),它们靶向rna而不是dna。向导核苷酸序列可编程rna结合蛋白可以指引起rna断裂或切口的核酸内切酶以及其他变异,例如核酸酶失活的cas蛋白,例如失活cas9或dcas9,其缺乏核酸内切酶活性。向导核苷酸序列可编程rna结合蛋白也可以指“分裂”蛋白,其中该蛋白质被分为两半(例如,c-cas9和n-cas9)并与两个内含蛋白部分融合。参见,例如,美国专利号9,074,199b1;zetsche等,(2015)natbiotechnol.33(2):139-42;wright等,(2015)pnas112(10)2984-89。在特定的实施方式中,对向导核苷酸序列可编程rna结合蛋白进行修饰以消除核酸内切酶活性(“核酸酶失活”)。例如,可以通过点突变(例如,spcas9中的d10a和h840a)使ruvc和hnh核酸酶结构域失活,导致不能切割靶dna的核酸酶失活的cas9(dcas9)分子。该dcas9分子保留了基于grna靶向序列与靶rna结合的能力。表1提供了直系同源物和生物等同物cas9的其他非限制性实例。表1核酸酶失活的化脓性链球菌cas9蛋白可以在位置10处用丙氨酸(a)替换天冬氨酸(d),在位置840处用丙氨酸(a)替换组氨酸(h)。本公开的示例性的核酸酶失活的化脓性链球菌cas9蛋白可以包含以下氨基酸序列或由其组成(d10a和h840a以粗体和下划线表示):本公开的示例性野生型土拉热弗朗西丝氏菌新凶手亚种cpf1(fncpf1)蛋白可包含以下氨基酸序列或由其组成:本公开的示例性野生型毛螺旋科菌nd2006cpf1(lbcpf1)蛋白可包含以下氨基酸序列或由其组成:本公开的示例性野生型氨基酸球菌bv3l6cpf1(ascpf1)蛋白可包含以下氨基酸序列或由其组成:在本公开的组合物的一些实施方式中,编码rna结合蛋白的序列包括从crisprcas蛋白或其rna结合部分分离或衍生的序列。在一些实施方式中,crisprcas蛋白包含vi型crisprcas蛋白。在一些实施方式中,vi型crisprcas蛋白包含cas13蛋白。本公开的示例性cas13蛋白可以分离或衍生自任何物种,包括但不限于细菌或古细菌。本公开的示例性cas13蛋白可以分离或衍生自任何物种,包括但不限于瓦氏淡杆菌(leptotrichiawadei),斯氏李斯特菌血清型1/2b(atcc35967/dsm20751/cip100100/slcc3954株),链霉菌细菌(lachnospiraceaebacterium),嗜氨基梭状杆菌dsm10710(clostridiumaminophilumdsm10710),鸡食杆菌dsm4847(carnobacteriumgallinarum),丙酸杆状杆菌wb4(paludibacterpropionicigeneswb4),魏氏李斯特菌fslr9-0317(listeriaweihenstephanensisfslr9-0317),魏氏李斯特菌fslr9-0317(listeriaweihenstephanensisfslr9-0317),菌fslm6-0635(纽约李斯特菌(listerianewyorkensis)),瓦氏纤毛菌f0279(leptotrichiawadeif0279),荚膜红球菌sb1003(rhodobactercapsulatussb1003),荚膜红球菌r121(rhodobactercapsulatusr121),荚膜红球菌de442(rhodobactercapsulatusde442)和溃疡棒状杆菌(corynebacteriumulcerans)。本公开的示例性cas13蛋白可以是dna核酸酶失活的。本公开的示例性cas13蛋白包括但不限于cas13a,cas13b,cas13c,cas13d及其直系同源物。本公开的示例性cas13b蛋白包括但不限于在本文中分别称为csx27和csx28的亚型1和2。示例性cas13a蛋白包括但不限于:本公开的示例性野生型cas13a蛋白可包含以下氨基酸序列或由其组成:示例性cas13b蛋白包括但不限于:本公开的示例性野生型动物溃疡伯杰氏菌atcc43767cas13b(bzcas13b)蛋白可包含以下氨基酸序列或由其组成:本公开的示例性野生型cas13d蛋白可包含以下氨基酸序列或由其组成:本文所用术语“细胞”可以指原核细胞或真核细胞,任选地获自对象获自可商购的来源。如本文所用,术语“crispr”是指成簇的规则间隔的短回文重复序列(crispr)。crispr还可以指依赖于crispr途径的序列特异性基因操作的技术或系统。可以对crispr重组表达系统进行编程,以使用crispr核酸内切酶和向导rna或crrna和tracrrna的组合来切割靶多核苷酸。crispr系统可用于在靶多核苷酸(例如dna或rna)中引起双链或单链断裂。crispr系统也可用于募集蛋白质或标记靶多核苷酸。在某些方面,crispr介导的基因编辑利用非同源末端连接(nhej)或同源重组的途径进行编辑。crispr技术的这些应用在本领域中是已知且广泛应用的。参见例如,美国专利号8,697,359和hsu等,(2014)cell156(6):1262-1278。如本文所用,术语“包括/包含”意在表示所述组合物和方法包括所提及的要素,但并不排除其它要素。本文所用“基本上由......组成”(以及语法上的变形)将理解成涵盖所述物质或步骤以及所述实施方式“本质上不影响基本和新特征的那些”。因此,本文所用术语“基本上由......组成”不应当理解为等于“包括/包含”。“由......组成”表示排除多于用于给予本公开组合物的微量元素的其它成分和基本方法步骤。通过各个这些转换术语定义的方面在本发明范围内。在术语“编码”应用于核酸序列时指代据信将“编码”多肽,mrna或效应rna的多核苷酸,如果在其天然状态或者当通过本领域技术人员已知的方法操纵时,可以经转录和/或翻译以产生效应rna、mrna、或多肽的mrna和/或其片段。反义链与这类核酸互补,并且可以由此推导出编码序列。本文所用术语“表达”或“基因表达”指多核苷酸转录成mrna的过程和/或转录的mrna随后被翻译成肽、多肽或蛋白质的过程。如果多核苷酸源自基因组dna,则表达可包括真核细胞中mrna的剪接。基因的表达水平可以通过测量细胞或组织样品内mrna或蛋白质的量予以确定;此外,可以确定多个基因的表达水平以建立特定样品的表达概况。本文所用术语“功能性”可以用于修饰任何分子、生物或细胞材料,从而意指其实现特定、具体作用。本文所用术语“grna靶序列”指代用于靶向特定基因从而采用crispr技术进行校正的向导rna序列。本领域已经熟知针对靶特异性设计grna和供体治疗性多核苷酸的技术。例如,doench,j.等,naturebiotechnology2014;32(12):1262-7,mohr,s.等,(2016)febsjournal283:3232-38,和graham,d.等,genomebiol.2015;16:260。grna包含或可选地基本由以下组成,或者进一步由以下组成:包含crisprrna(crrna)和反式激活cripsprrna(tracrrna)的融合多核苷酸;或包含crisprrna(crrna)和反式激活cripsprrna(tracrrna)的多核苷酸。在一些方面,grna是合成的(kelley,m.等,(2016)jofbiotechnology233(2016)74-83)。在本公开的组合物的一些实施方式中,rna分子的靶序列包含对应于一个和/或多个rna结合蛋白和/或其融合蛋白的序列基序。在本公开的组合物和方法的一些实施方式中,序列基序是疾病或病症的标志。本公开的序列基序可以分离或衍生自基因组序列中存在的外源或外来序列的序列,因此被翻译成本公开的mrna分子或在本公开的rna序列中存在的外源或外来序列的序列。本公开的序列基序可以包含引起疾病或病症的内源序列中的突变或由其组成。突变可以包含序列取代,倒置,缺失,插入,转座或其任何组合或由其组成。本公开的序列基序可以包含重复序列或由重复序列组成。在一些实施方式中,重复的序列可以与微卫星不稳定性(msi)相关。一个或多个基因座处的msi是由本公开的细胞的dna错配修复机制受损引起的。dna的高变序列可以被转录成本公开的mrna,其包含靶序列,该靶序列包含或由高变序列组成。本公开的序列基序可以包含生物标志物或由生物标志物组成。该生物标志物可以指示发生疾病或病症的风险。生物标志物可以指示健康的基因(发生疾病或病症的风险低或没有确定的风险。生物标志物可以指示已编辑的基因。示例性生物标志物包括但不限于单核苷酸多态性(snp),序列变异或突变,表观遗传标志物,剪接受体位点,外源序列,异源序列及其任何组合。本公开的序列基序可以包含二级,三级或四级结构或由其组成。二级,三级或四级结构可以是内源的或天然存在的。二级,三级或四级结构可以是诱导的或非天然存在的。二级,三级或四级结构可以由内源,外源或异源序列编码。在本公开的组合物和方法的一些实施方式中,rna分子的靶序列包含2至100个核苷酸或核酸碱基或由其组成,包括端点。在一些实施方式中,rna分子的靶序列包含2-50个核苷酸或核酸碱基或由其组成,包括端点。在一些实施方式中,rna分子的靶序列包含2-20个核苷酸或核酸碱基或由其组成,包括端点。在本发明的组合物和方法的一些实施方式中,rna分子的靶序列是连续的。在一些实施方式中,rna分子的靶序列是不连续的。例如,rna分子的靶序列可以包含一个或多个不连续的核苷酸或核酸碱基或由其组成,所述一个或多个核苷酸或核酸碱基是不连续的,因为一个或多个间歇性(intermittent)核苷酸位于靶序列的核苷酸之间。在本发明的组合物和方法的一些实施方式中,rna分子的靶序列是天然存在的。在一些实施方式中,rna分子的靶序列是非天然存在的。示例性的非天然存在的靶序列可以包含序列变异或突变,嵌合序列,外源序列,异源序列,嵌合序列,重组序列,包含修饰的或合成的核苷酸的序列或它们的任意组合或由其组成。在本发明的组合物和方法的一些实施方式中,rna分子的靶序列结合本公开的向导rna。在本发明的组合物和方法的一些实施方式中,rna分子的靶序列与本公开的第一rna结合蛋白结合。在本发明的组合物和方法的一些实施方式中,rna分子的靶序列与本公开的第二rna结合蛋白结合。在本发明的组合物和方法的一些实施方式中,本公开的rna分子包含靶序列。在一些实施方式中,本公开的rna分子包含至少一个靶序列。在一些实施方式中,本公开的rna分子包含一个或多个靶序列。在一些实施方式中,本公开的rna分子包含两个或更多个靶序列。在本发明的组合物和方法的一些实施方式中,本公开的rna分子是天然存在的rna分子。在一些实施方式中,本公开的rna分子是非天然存在的分子。示例性的非天然存在的rna分子可以包含序列变异或突变,嵌合序列,外源序列,异源序列,嵌合序列,重组序列,包含修饰的或合成的核苷酸的序列或它们的任意组合或由其组成。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含从病毒分离或衍生的序列或由其组成。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含从原核生物分离或衍生的序列或由其组成。在一些实施方式中,本公开的rna分子包含从古细菌的物种或菌株或细菌的物种或菌株分离或衍生的序列或由其组成。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含从真核生物分离或衍生的序列或由其组成。在一些实施方式中,本公开的rna分子包含从以下类别的物种分离或衍生的序列或由其组成:原生动物,寄生虫,原生生物,藻类,真菌,酵母,变形虫,蠕虫,微生物,无脊椎动物,脊椎动物,昆虫,啮齿动物,小鼠,大鼠,哺乳动物或灵长类动物。在一些实施方式中,本公开的rna分子包含从人分离或衍生的序列或由其组成。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含从生物体或病毒的基因组的编码序列衍生的序列或由其组成。在一些实施方式中,本公开的rna分子包含一级rna转录物,前体信使rna(pre-mrna)或信使rna(mrna)或由其组成。在一些实施方式中,本公开的rna分子包含未加工的基因产物(例如,转录物)或由其组成。在一些实施方式中,本公开的rna分子包含已经过转录后加工的基因产物或由其组成(例如,包含5’帽和3′聚腺苷酸化信号的转录物)。在一些实施方式中,本公开的rna分子包含已经替代式剪接的基因产物(例如剪接变体)或由其组成。在一些实施方式中,本公开的rna分子包含已经去除非编码和/或内含子序列的基因产物(例如信使rna(mrna))或由其组成。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含从非编码序列(例如,非编码rna(ncrna))衍生的序列或由其组成。在一些实施方式中,本公开的rna分子包含核糖体rna或由核糖体rna组成。在一些实施方式中,本公开的rna分子包含小ncrna或由小ncrna组成。本公开的示例性小rna分子包括但不限于,微小rna(mirna),小干扰(sirna),与piwi蛋白相互作用rna(pirna),小核仁rna(snorna),小核rna(snrna),细胞外或外体rna(exrna)和小cajal体特异性rna(scarna)。在一些实施方式中,本公开的rna分子包含长ncrna或由长ncrna组成。本公开的示例性长rna分子包括但不限于x非活性特异性转录物(xist)和hox转录物反义rna(hotair)。在本公开的组合物和方法的一些实施方式中,本公开的rna分子在细胞内空间中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在胞质空间中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在细胞核中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在细胞的囊泡,膜结合区室或细胞器中与本公开的组合物接触。在本公开的组合物和方法的一些实施方式中,本公开的rna分子在细胞外空间中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在外泌体中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在脂质体,聚合物小体,胶束或纳米颗粒中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在细胞外基质中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在液滴中与本公开的组合物接触。在一些实施方式中,本公开的rna分子在微流体液滴中与本公开的组合物接触。在本公开的组合物和方法的一些实施方式中,本公开的rna分子包含单链序列或由单链序列组成。在一些实施方式中,本公开的rna分子包含双链序列或由双链序列组成。在一些实施方式中,该双链序列包含两个rna分子。在一些实施方式中,该双链序列包含一个rna分子和一个dna分子。在一些实施方式中,包括其中双链序列包含一个rna分子和一个dna分子的那些实施方式,本公开的组合物选择性地结合并且任选地选择性地切割rna分子。术语“内含肽”是指一类蛋白质,其能够切除自身并通过蛋白质剪接连接蛋白质的其余部分。“分裂内含肽”来自两个基因。“分裂-内含肽”的非限制性实例是最初衍生自点状念珠藻(n.punctiforme)的c-内含肽和n-内含肽序列。本文所用术语“分离的”指分子或生物制品或细胞材料基本上不含其他材料。本文使用的术语“核酸序列”和“多核苷酸”可互换使用,是指任何长度的核苷酸的聚合形式,即核糖核苷酸或脱氧核糖核苷酸。因此,该术语包括但不限于单链、双链或多链dna或rna,基因组dna,cdna,dna-rna杂合体或包含嘌呤和嘧啶碱基或其它天然化学修饰、生化修饰的、非天然的或衍生的核苷酸碱基的聚合物。术语“直系同源物”用于指另一种基因或蛋白质,并且意指所述基因或蛋白质的同源物,所述同源物是从相同的祖先来源进化而来的。直系同源物可以保留或不保留与其直系同源的基因或蛋白质相同的功能。cas9直系同源物的非限制性实例包括金黄色葡萄球菌cas9(“spcas9”),嗜热链球菌cas9,嗜肺乳杆菌cas9,内生乳杆菌cas9,脑膜炎奈瑟氏菌cas9,长双歧杆菌cas9,嗜粘蛋白阿克曼氏菌cas9和羊毛臭气杆菌(o.laneus)cas9。本文所用术语“表达控制元件”指调节编码序列如基因的表达的任何序列。示例性表达控制元件包括但不限于启动子,增强子,微小rna,转录后调控元件,聚腺苷酸化信号序列和内含子。表达控制元件可以是,例如,组成型,诱导型,抑制型或组织特异性的。“启动子”是控制序列,其是多核苷酸序列的一个区域,在该区域中控制转录的启动和速率。其可含有调控蛋白和分子(如rna聚合物和其他转录因子)可结合的遗传元件。在一些实施方式中,启动子的表达控制是组织特异性的。非限制性示例性启动子包括cmv,cba,cag,cbh,ef-1a,pgk,ubc,gusb,ucoe,haat,tbg,结蛋白,mck,c5-12,nse,突触蛋白,pdgf,mecp2,camkii,mglur2,nfl,nfh,nβ2,ppe,enk,eaat2,gfap,mbp和u6启动子。“增强子”是dna的一个区域,可以通过激活蛋白质来结合以增加转录的可能性或频率。非限制性示例性增强子和转录后调控元件包括cmv增强子和wpre。术语“ires”是指病毒,原核或真核来源的内部核糖体进入位点或其部分。在一些实施方式中,ires是允许以不依赖于帽的方式进行翻译起始的rna元件。在gritsenkoa.等,(2017)ploscomputbiol13(9):e1005734中描述了ires元件的共同结构特征,以引用方式并入本文。本文公开的融合rna的“ires样序列”是指合成来源的序列,其以ires或其部分的方式起作用以控制靶核酸在细胞中的翻译。在一些实施方式中,ires是本文公开的ires或ires样序列中的一个或多个。在一些实施方式中,ires与本文公开的一个或多个ires或ires样序列的序列具有至少65%,至少70%,至少75%,至少78%,至少80%,至少83%,至少85%,至少88%,至少为90%,至少92%,至少95%,至少96%,至少97%,至少98%,至少99%或100%序列相同性。术语“自切割肽”或“编码自切割肽的序列”是指在载体构建体中用于纳入促进核糖体跳跃的位点并由此从单个启动子产生两个多肽的连接序列,这类自切割肽包括但不限于t2a和p2a肽或编码自切割肽的序列。术语“蛋白质”、“肽”和“多肽”可以互换使用并以其最广泛的含义使用,是指两个或更多个亚基的氨基酸、氨基酸类似物或肽模拟物的化合物。亚基可以通过肽键连接。在另一方面中,亚基可以通过其他键连接,例如,酯、醚等。蛋白质或肽必须包含至少两个氨基酸,并且对构成蛋白质或肽序列的最大氨基酸数没有限制。本文所用术语“氨基酸”指天然和/或非天然或合成的氨基酸,包括甘氨酸,以及d和l光学异构体,氨基酸类似物和肽模拟物。术语“含pam的寡核苷酸”是指包含能够与向导核苷酸序列可编程rna结合蛋白相互作用的pam序列的寡核苷酸。o’connell等,nature516,pages263-266(2014)描述了含pam的寡核苷酸的非限制性实例,在此通过引用纳入本文。pam序列是指包含约2至约10个核苷酸的原间隔区相邻基序。pam序列对与之相互作用的向导核苷酸序列可编程rna结合蛋白具有特异性,并且是本领域已知的。例如,化脓性链球菌pam具有序列5’-ngg-3’,其中“n”是任何核苷碱基,后接两个鸟嘌呤(“g”)核苷碱基。新凶手弗朗西丝氏菌的cas9识别标准pam序列5′-ngg-3′,但经过工程改造以识别pam5′-yg-3′(其中“y”是嘧啶),因此增加了可能的cas9靶标范围。新凶手弗朗西丝氏菌的cpf1核酸酶识别pam5′-tttn-3′或5′-ytn-3′。本文所用术语“重组表达系统”指用于表达通过重组形成的某些遗传物质的遗传构建体。如本文所用,术语“rna结合蛋白”或“rbp”包括rna结合蛋白,多肽或其结构域,包括但不限于rna结合蛋白或多肽或结构域的一个或多个rna结合部分。在一些实施方式中,本公开的rna结合蛋白是本文公开的向导核苷酸序列可编程rna结合蛋白。在其他实施方式中,本公开的rna结合蛋白是pumilio和fbf(puf)蛋白或其rna结合部分。在一些实施方式中,rna结合蛋白包含基于pumilio的装配体(assembly)(pumby)蛋白或其rna结合部分。在一些实施方式中,rna结合蛋白包含一个或多个五肽重复(ppr)基序或其rna结合部分。在一些实施方式中,rna结合蛋白不需要针对rna结合活性的多聚化。在一些实施方式中,rna结合蛋白不是多聚体复合物的单体。在一些实施方式中,多聚体蛋白复合物不包含rna结合蛋白。在一些实施方式中,rna结合蛋白选择性地结合至rna分子内的靶序列。在一些实施方式中,rna结合蛋白不包含对rna分子内第二序列的亲和力。在一些实施方式中,rna结合蛋白对rna分子内的第二序列不具有高亲和力或不与其选择性结合。在一些实施方式中,rna结合蛋白包含2至1300个氨基酸,包括端点。在一些实施方式中,编码rna结合蛋白的序列还包含编码核定位信号(nls)的序列。在一些实施方式中,编码核定位信号(nls)的序列位于编码rna结合蛋白的序列的3’。在一些实施方式中,rna结合蛋白在该蛋白的c末端包含nls。在一些实施方式中,编码rna结合蛋白的序列还包含编码第一nls的第一序列和编码第二nls的第二序列。在一些实施方式中,编码第一nls或第二nls的序列位于编码rna结合蛋白的序列的3’。在一些实施方式中,rna结合蛋白在该蛋白的c末端包含第一nls或第二nls。在一些实施方式中,rna结合蛋白还包含nes(核输出信号)或其他肽标签或分泌信号。在一些实施方式中,本文公开的融合蛋白包含该rna结合蛋白作为第一rna结合蛋白以及包含核酸酶结构域或由核酸酶结构域组成的第二rna结合蛋白。如本文所用,术语“对象”旨在表示任何真核生物,例如植物或动物。在一些实施方式中,对象可以是哺乳动物;在进一步的实施方式中,对象可以是牛,马,猫,鼠,猪,犬,人或大鼠。本文所用“治疗”或“处理”对象中的疾病指(1)防止症状或疾病在易患或尚未表现出疾病症状的对象中发生;(2)抑制疾病或阻止其发展;或者(3)改善或导致疾病或疾病症状的消退。如本领域中所理解的,“治疗”是一种用于获得有益或所需结果(包括临床结果)的方法。出于本公开技术的目的,有益或所需结果可以包括下述一种或多种但不限于:缓和或改善一种或多种症状,减轻病症(包括疾病)的程度,使病症(包括疾病)的状态稳定(即,不恶化),延缓或减慢病症(包括疾病),进展,改善或缓和病症(包括疾病),状态和缓解(无论是部分还是全部),无论是可检测的还是不可检测的。本文所用术语“载体”意指重组载体,其保留了感染和转导非分裂和/或缓慢分裂细胞并整合到靶细胞基因组中的能力。载体可以是病毒载体、细菌噬菌体、细菌人工染色体或酵母人工染色体。载体可以是dna或rna载体。载体可以是自复制的染色体外载体。载体可以是dna质粒。载体可以源自或基于野生型病毒。本公开的方面涉及腺相关病毒载体,腺病毒载体和慢病毒载体。术语“翻译修饰蛋白”是指能够修饰翻译的蛋白。在一些实施方式中,翻译修饰蛋白抑制翻译。在一些实施方式中,翻译修饰蛋白增强翻译。在一些实施方式中,与对照相比,翻译修饰蛋白抑制1%,2%,5%,10%,15%,20%,25%,35%,50%,75%,80%,85%,90%,95%,97%,98%,99%或100%的翻译。在一些实施方式中,与对照相比,翻译修饰蛋白增强1%,2%,5%,10%,15%,20%,25%,35%,50%,75%,80%,85%,90%,95%,97%,98%,99%或100%的翻译。如在本文的一些实施方式中所使用的,“激酶磷酸化结构域”是指分子内的区域,通常但不总是氨基酸,该区域易于被激酶通过化学方式添加一个或多个磷酸基团。已知激酶调节许多细胞和信号转导途径。有时,激酶的磷酸化结构域发生突变,其中突变影响分子的功能。如本文的一些实施方式中所使用的,“选择标志物”是指载体的组分。在一些实施方式中,选择标志物是一种类型的用于指示转染成功的报告基因。有正选择标志物,其中该标志物为宿主生物提供了优势。也有消除或阻碍宿主生物生长的负选择标志物。也有正负选择标志物,这些标记可以根据情况促进或抑制生长。标志物的非限制性实例或类型是抗药性标志物和营养缺陷型标志物。如本文的一些实施方式中所用,“转录后”是指基因转录后发生的事件。在一些实施方式中,转录后修饰是当rna一级转录物从基因转录后发生化学改变以产生功能性rna分子时的修饰。转录后修饰的非限制性实例包括在rna分子的5’末端添加一个帽,在rna分子的3’末端添加一个聚腺苷酸尾,以及剪接。转录后修饰的其他非限制性实例包括2′-o-甲基化(2′-ome)(2′-o-甲基化发生在核糖部分的游离2′-oh的氧上),n6-甲基腺苷(m6a)和5-甲基胞嘧啶(m5c)。在一些实施方式中,基因表达可以通过实施本文所述的组合物和方法而在转录后增加或上调。在一些实施方式中,基因表达可以通过实施本文所述的组合物和方法而在转录后降低或下调。如本文所用,术语“2-组分rna靶向系统”是编码2-组分rna靶向系统的核酸分子,其包含(a)编码rna靶向的crispr/cas蛋白或翻译修饰蛋白融合体的核酸序列;和(b)单向导rna(sgrna)序列,其包含:在其5′端,与靶rna序列杂交或结合的rna序列(或间隔区序列);和在其3′端,能够与crispr/cas蛋白结合或缔合的rna序列(或支架序列);并且其中2-组分rna靶向系统在不存在含pam的寡核苷酸的情况下识别并改变细胞中的靶rna。在一些实施方式中,2-组分系统的序列在单个载体中。在一些实施方式中,2-组分系统的间隔区序列是选自cug,ccug,cag和ggggcc的重复序列。可以推断出,在没有明确叙述的情况下,除非另有意图,否则当本公开涉及多肽,蛋白质,多核苷酸或抗体时,其等同物或生物学等同物应在本公开的范围内。如本文所用,术语“其生物等同物”旨在当指代参考蛋白,抗体,多肽或核酸时与“其等同物”同义,意指具有最小同源性而仍保持所需结构或功能的那些。除非本文具体叙述,否则预期本文提及的任何多核苷酸,多肽或蛋白质也包括其等同物。例如,等同物意指至少约70%的同源性或相同性,或至少80%的同源性或相同性,或者,或至少约85%,或至少约90%,或至少约95%,或者,具有98%的同源性或相同性,并且与参考蛋白,多肽或核酸表现出基本相等的生物学活性。或者,当提及多核苷酸时,其等同物是在严格条件下与参考多核苷酸或其互补序列杂交的多核苷酸。本文提供了用于下文所述的基因和蛋白质转移和表达技术的多肽和/或多核苷酸序列。应当理解,尽管并非总是明确指出,本文提供的序列可用于提供表达产物以及产生具有相同生物学特性的蛋白质的基本相同的序列。这些“生物等同”或“生物活性”或“等同”多肽由本文所述的等同多核苷酸编码。至少当使用在默认条件下运行的序列相同性方法进行比较时,它们可以与参考多肽具有至少60%,或可选地至少65%,或可选地至少70%,或可选地至少75%,或可选地至少80%,或可选地至少85%,或可选地至少90%,或可选地至少95%或可选地至少98%相同的一级氨基酸序列。提供了特定的多肽序列作为特定实施方式的实例。用具有相似电荷的替代氨基酸对氨基酸进行序列修饰。另外,等同多核苷酸是在严格条件下与参考多核苷酸或其互补序列杂交的多核苷酸,或者对于多肽,由在严格条件下与参考编码多核苷酸杂交的多核苷酸或其互补链编码的多肽。或者,等同多肽或蛋白质是从等同多核苷酸表达的多肽或蛋白质。本文公开的核酸序列(例如,多核苷酸序列)可以是密码子优化的,这是本领域众所周知的技术。在本文公开的一些实施方式中,示例性cas序列,例如seqidno:46(cas13d),被密码子优化以在人细胞中表达。密码子优化是指不同细胞对特定密码子的使用不同的情形。该密码子偏倚对应于特定trna在细胞类型中的相对丰度的偏倚。通过改变序列中的密码子以与相应trna的相对丰度匹配,可能增加表达。通过故意选择已知相应trna在特定细胞类型中罕见的密码子,也可能降低表达。对于哺乳动物细胞以及多种其他生物,密码子使用表是本领域已知的。基于遗传密码,可以产生编码例如cas蛋白的核酸序列。在一些实施方式中,这样的序列被优化用于在宿主或靶细胞,例如用于表达cas蛋白的宿主细胞或其中实践所公开的方法的细胞(例如在哺乳动物细胞,例如人细胞中)中表达。特定物种的密码子偏好和密码子使用表可用于工程改造编码cas蛋白的分离的核酸分子(例如编码与其对应的野生型蛋白质具有至少80%,至少85%,至少90%,至少92%,至少95%,至少96%,至少97%,至少98%,至少99%或100%的序列相同性的蛋白质的核酸分子),其利用该特定物种的密码子使用偏好。例如,本文公开的cas蛋白可以被设计成具有优先被感兴趣的特定生物使用的密码子。在一实例中,优化cas核酸序列以在人细胞中表达,例如与其相应的野生型或起始核酸序列具有至少70%,至少80%,至少85%,至少90%,至少92%,至少95%,至少98%或至少99%的序列相同性的cas核酸序列。在一些实施方式中,编码至少一种cas蛋白(可以是载体的一部分)的分离的核酸分子包括经密码子优化以在真核细胞中表达的至少一种cas蛋白编码序列,或经密码子优化以在人细胞中表达的至少一种cas蛋白编码序列。在一个实施方式中,这种密码子优化的cas编码序列与其相应的野生型或起源序列具有至少80%,至少85%,至少90%,至少92%,至少95%,至少96%,至少97%,至少98%,至少99%或100%的序列相同性。在另一个实施方式中,真核细胞密码子优化的核酸序列编码与其相应的野生型或起源蛋白具有至少85%,至少90%,至少92%,至少95%,至少96%,至少97%,至少98%,至少99%或100%序列相同性的cas蛋白。在另一个实施方式中,可以常规地产生含有功能上等同的核酸的多种克隆,例如序列不同但编码相同cas蛋白序列的核酸。编码序列中的沉默突变是由遗传密码的简并性(即冗余)产生的,由此超过一种密码子可以编码相同的氨基酸残基。因此,例如,亮氨酸可以由ctt,ctc,cta,ctg,tta或ttg编码;丝氨酸可以由tct,tcc,tca,tcg,agt或agc编码;天冬酰胺可以由aat或aac编码;天冬氨酸可以由gat或gac编码;半胱氨酸可以由tgt或tgc编码;丙氨酸可以由gct,gcc,gca或gcg编码;谷氨酰胺可以由caa或cag编码;酪氨酸可以通过tat或tac编码;并且异亮氨酸可以由att,atc或ata编码。显示标准遗传密码的表可以在各种来源中找到(参见,例如,stryer,1988,《生物化学》(biochemistry),第三版,w.h.5费曼公司(w.h.5freemanandco.),纽约州)。“杂交”表示这样的反应,所述反应中一个或多个多核苷酸反应以形成经由核苷酸残基的碱基之间的氢键稳定的复合物。氢键可以沃森-克里克碱基配对、霍格斯坦结合(hoogsteinbinding)或任何其他序列特异性方式出现。复合物可以包含形成双链结构的两条链,形成多链复合物的三条或更多条链,单一自杂交链,或它们的任意组合。杂交反应可以成为更多过程中的一个步骤,如pcr反应的起始,或者通过核酶对多核苷酸进行酶促切割。严格杂交条件的示例包括:孵育温度为约25℃-约37℃;杂交缓冲液浓度为约6×ssc-约10×ssc;甲酰胺浓度为约0%-约25%;和洗涤溶液为约4×ssc-约8×ssc。中度杂交条件的示例包括:孵育温度为约40℃-约50℃;杂交缓冲液浓度为约9×ssc-约2×ssc;甲酰胺浓度为约30%-约50%;和洗涤溶液为约5×ssc-约2×ssc。高度严格杂交条件的示例包括:孵育温度为约55℃-约68℃;缓冲液浓度为约1×ssc-约0.1×ssc;甲酰胺浓度为约55%-约75%;和洗涤溶液为约1×ssc、0.1×ssc或去离子水。通常,杂交孵育时间为5分钟-24小时,包括1、2或更多个洗涤步骤,并且洗涤孵育时间为约1、2或15分钟。ssc是0.15mnacl和15mm柠檬酸盐缓冲液。应当理解的是,可以采用使用其他缓冲液系统的ssc等同物。“同源性”或“相同性”或“相似性”指两个肽之间或两个核酸分子之间的序列相似性。同源性可以通过比较各序列中出于比较的目的可以对齐的位置确定。当经比较的序列中的位置被相同的碱基或氨基酸占据,那么分子在该位置具有同源性。序列之间的同源性程度是序列所共享的匹配或同源位置数量的函数。“不相关”或“非同源性”序列与本发明的任一序列共享小于40%的相同性,或者任选地,小于25%的相同性。融合rna在一些方面,本文提供了包含以下,由以下组成或基本上由以下组成的融合rna:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires)或其部分。在一些实施方式中,融合rna包含向导rna和一个或多个ires样序列,其发挥如本文公开的ires的作用以控制靶核酸的翻译。在一些实施方式中,所述向导核苷酸序列可编程rna是向导rna(grna,如单grna(sgrna))或crisprrna(crrna)。在融合rna的一些实施方式中,向导核苷酸序列可编程rna衍生自来自化脓性链球菌,金黄色葡萄球菌,新凶手弗朗西丝氏菌,脑膜炎奈瑟氏球菌,嗜热链球菌或侧孢短芽孢杆菌的向导rna支架。在一些实施方式中,向导核苷酸序列可编程rna支架源自与所述向导核苷酸序列可编程rna结合蛋白相同的细菌物种。在融合rna的一些实施方式中,向导核苷酸序列可编程rna包含与靶核酸互补的核苷酸序列。在一些实施方式中,靶核酸是rna,信使rna(mrna),转移rna(trna)或核糖体rna(rrna)。在特定的实施方式中,靶核酸是mrna。在一些实施方式中,与靶核酸互补和/或同源的序列的长度是约8至约100,约10至约50,约15至约40,约15至约30,或约20至约30个核苷酸。在一些实施方式中,与靶核酸互补和/或同源的序列的长度为约20个核苷酸。在一些实施方式中,该序列与靶核酸约50%,约60%,约70%,约75%,约80%,约85%,约90%,约95%,约97%,约98%,约99%,或约100%同源。在特定的实施方式中,该序列与靶核酸约90-100%同源。在一些实施方式中,与融合rna中的靶核酸互补和/或同源的序列是间隔区序列。在融合rna的一些实施方式中,ires是i型或ii型ires。在一些实施方式中,ires是病毒ires或真核ires。在一些实施方式中,ires选自:脊髓灰质炎ires,鼻病毒ires,脑心肌炎病毒ires(emcv-ires),小核糖核酸病毒ires,口蹄疫病毒ires(fmdv-ires),口咽病毒ires,卡波西氏肉瘤相关疱疹病毒ires(kshv-ires),甲型肝炎ires,丙型肝炎ires,经典猪瘟病毒ires,瘟病毒ires,牛病毒性腹泻病毒ires,弗云德鼠白血病ires,莫洛尼鼠白血病ires(mmlv-ires),劳斯肉瘤病毒ires,人类免疫缺陷病毒ires(hiv-ires),小珀椿象肠病毒ires,双顺反子病毒(cripavirus)ires,蟋蟀麻痹病毒ires,锥蝽病毒ires,禾谷缢管蚜病毒ires,马立克氏病病毒ires,成纤维细胞生长因子(fgf-1ires和fgf-2ires),血小板衍生生长因子b(pdgf/c-sisires),血管内皮生长因子(vegfires)和胰岛素样生长因子2(igf-iiires)。在一些实施方式中,ires或ires样序列是ires或ires样序列的一部分。在融合rna的一些实施方式中,融合rna进一步包含位于向导核苷酸序列可编程rna和ires之间的接头序列。在一些实施方式中,融合rna包含结构5’-[向导核苷酸序列可编程rna]-[接头序列]-[ires]-3’。在一些实施方式中,融合rna包含结构5’-[ires]-[接头序列]-[向导核苷酸序列可编程rna]-3’。在一些实施方式中,接头序列的长度为约1至约3,约1至约5,约1至约10,约5至约20,约10至约50或约50至约200个核碱基。在一些实施方式中,接头序列rna与靶核酸不互补。融合蛋白在一些方面,本文提供了包含编码以下组分的一种或多种多核苷酸的组合物:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)翻译修饰蛋白或其生物学等同物。在一些方面,本文提供了融合蛋白,其包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)翻译修饰蛋白或其生物学等同物。在一些实施方式中,翻译修饰蛋白是以下的至少一种:真核翻译起始因子4e(eif4e)(seqidno:52-59),真核翻译起始因子4e结合蛋白(eif4e-bp1)(seqidno:61-22),泛素相关蛋白2-样(ubap2l)(seqidno:64-71)及其各自的生物学等同物。在一些实施方式中,翻译修饰蛋白由表2中的至少一种多核苷酸编码。表2在一些实施方式中,翻译修饰蛋白是以下的至少一种:真核翻译起始因子4g(eif4g),真核翻译起始因子4a(eif4a),真核翻译起始因子4b(eif4b),真核翻译起始因子4h(eif4h),真核翻译起始因子3(eif3),聚腺苷酸结合蛋白1(pabp1)及其各自的生物学等同物。eif4g和eif3是真核翻译起始因子,其通过靶向5’utr来参与稳定预起始复合物。pabp1是一种真核聚腺苷酸结合蛋白,其增强信使rna的环化并促进核糖体回收。eif4a,eif4b和eif4h是真核解旋酶,其解开5’utr二级结构并帮助预起始复合物找到靶起始密码子。在一些方面,本文提供了融合蛋白,其包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)真核翻译起始因子4e(eif4e)蛋白或其生物学等同物。eif4e是真核翻译起始因子,其参与将核糖体导向mrna的帽结构。在一些实施方式中,它是24-kd多肽,其以游离形式和eif4f预起始复合物的一部分存在。许多细胞mrna需要eif4e才能翻译成蛋白质。在一些实施方式中,eif4e多肽是真核翻译设备的限速组分,并且参与真核蛋白质合成的mrna-核糖体结合步骤。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:cas9,修饰的cas9,cpf1,cas13a,cas13b,casm,casrx/cas13d及其各自的生物学等同物。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)crispr1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)crispr3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白经修饰成核酸酶失活的。在一些实施方式中,casrx/cas13d蛋白是vi-d型crispr-cas系统的效应物。在一些实施方式中,casrx/case13d蛋白是可切割或结合rna的rna引导的rna内切核酸酶。在一些实施方式中,casrx/cas13d蛋白可以包括一个或多个高级真核生物和原核生物核苷酸结合(hepn)结构域。在一些实施方式中,casrx/case13d蛋白可包括野生型或突变的hepn结构域。在一些实施方式中,casrx/case13d蛋白包括不能切割rna但是可以加工向导rna的突变的hepn结构域。在一些实施方式中,casrx/cas13d蛋白不需要原间隔区侧翼序列。还参见wo公开号wo2019/040664和us2019/0062724(其通过引用全文并入本文)中casrx/cas13d蛋白的其他实例和序列,但不限于,特参考seqidno:54,57,61,67,69,71,72,73,74,75,76,77,78,85,86,87,88,113,147,153,154,155,158,160,162,164,170,179,183,185,187,189,190,202,204、206,208,209,210和212。yan等,(2018)molcell.70(2):327-339(doi:10.1016/j.molcel.2018.02.2018)和konermann等,(2018)cell173(3):665-676(doi:10.1016/i.cell/2018.02.033)已经描述了casrx/cas13d蛋白,二者均通过引用全文并入本文。还参见wo公开号wo2018/183703(casm)和wo2019/006471(cas13d),其通过引用全文并入本文。本公开的融合蛋白的一些实施方式中,可以使用rna结合蛋白或其作为puf(pumilio和fbf同源性家族)的rna结合部分来代替向导核苷酸序列可编程rna结合蛋白。参与介导mrna稳定性和翻译的puf蛋白(以果蝇和秀丽隐杆线虫fem-3结合因子命名)的独特rna识别模式是本领域众所周知的。人pumiliol的puf结构域也是本领域已知的,其与同源rna序列紧密结合,并且其特异性可以被修饰。它包含八个puf重复序列,其识别八个连续的rna碱基,每个重复序列可识别一个碱基。由于每个重复序列中的两个氨基酸侧链识别相应碱基的沃森-克里克边缘并确定该重复序列的特异性,因此可将puf结构域设计为特异性结合大多数8-ntrna。wang等,natmethods.2009;6(11):825-830。还参见wo2012/068627,其通过引用全文并入本文。本公开的融合蛋白的一些实施方式中,可以使用rna结合蛋白或其作为puf(基于pumilio的装配体)蛋白的rna结合部分代替向导核苷酸序列可编程rna结合蛋白。rna结合蛋白pumhd(pumilio同源结构域,puf家族的成员)已被广泛用于以天然和修饰形式靶向rna,已被工程改造以产生一组四个典型的蛋白质模块,每个模块均靶向一个rna碱基。这些模块(即,针对基于pumilio的装配体的pumby)可以连接在具有不同组成和长度的链中,以结合所需的靶rna。这种pumby-rna相互作用的特异性很高,无法检测到pumby链与和靶序列具有三个或更多个错配的rna序列的结合。katarzyna等,pnas,2016;113(19):e2579-e2588。还参见us2016/0238593,其通过引用全文并入本文。在本公开的融合蛋白的一些实施方式中,可以使用rna结合蛋白或其作为ppr蛋白的rna结合部分代替本文公开的向导核苷酸序列可编程rna结合蛋白。ppr蛋白(来自植物的具有五肽重复序列(ppr)基序的蛋白)是核编码的,仅在rna水平的细胞器(叶绿体和线粒体)上受控制,可切割,翻译,剪接,rna编辑,专门作用于rna稳定性的基因。ppr蛋白通常是35个氨基酸的基序,并具有其中ppr基序是约10个连续氨基酸的结构。ppr基序的组合可用于与rna的序列选择性结合。ppr蛋白通常由约10个重复结构域的ppr基序组成。ppr结构域或rna结合结构域可以被配置为催化失活的。通过引用全文并入本文的wo2013/058404。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白与融合rna结合。在一些实施方式中,编码rna结合蛋白的核酸序列和融合rna序列包含在单个载体内。在一些实施方式中,编码rna结合蛋白的核酸序列和融合rna序列包含在两个载体内。在一些实施方式中,融合蛋白进一步包含接头,由接头组成或基本上由接头组成。在一些实施方式中,接头是肽接头。在一些实施方式中,肽接头包含三肽ggs的一个或多个重复。在其他实施方式中,接头是非肽接头。在一些实施方式中,非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。在一些实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[eif4e]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。在其他实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[eif4e]-cooh。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白与向导rna(grna)如单grna(sgrna),crisprna(crrna)和/或反式激活crrna(tracrrna)结合。在一些实施方式中,编码向导核苷酸序列可编程rna结合蛋白和grna的序列是2组分系统。在一些实施方式中,2组分系统包含在单个载体内。在一些实施方式中,eif4e蛋白由具有包含以下,由以下组成,或基本上由以下组成的序列的多核苷酸编码:选自seqidno:52,seqidno:53,seqidno:54,seqidno:55,及其各自的生物学等同物的序列的全部或部分。在一些实施方式中,eif4e是人eif4e的直系同源物。例如,在一些实施方式中,eif4e是植物直系同源物,例如在german-retana,s.等,j.virol.(2008)卷82第15期7601-7612中描述的蛋白质(通过引用并入本文)。在一些实施方式中,eif4e蛋白具有包含以下,由以下组成,或基本上由以下组成的氨基酸序列:选自seqidno:56,seqidno:57,seqidno:58,seqidno:59,及其各自的生物学等同物的序列的全部或部分。在一些实施方式中,eif4e蛋白的一个或多个激酶磷酸化结构域被突变。在一些实施方式中,eif4e蛋白的全部激酶磷酸化结构域被突变。在一些实施方式中,突变用带负电荷的氨基酸例如天冬氨酸或谷氨酸替换磷酸化结构域的氨基酸。在其他实施方式中,突变用不带电荷的残基例如丙氨酸或甘氨酸替换磷酸化结构域的氨基酸。在一些实施方式中,eif4e包含一个或多个模拟磷酸化突变和/或减少eif4e与eif4g相互作用的突变。在一些实施方式中,eif4e蛋白包含一种或多种选自下组的突变:s209d,h37r,v69a和w73f。在一些实施方式中,突变的eif4e是组成性活性的。突变类型s209d模拟磷酸化h37r减少eif4g相互作用v69a减少eif4g相互作用w73f减少eif4g相互作用在一些实施方式中,融合蛋白是由包含以下核酸序列的核酸编码的dcas9-eif4e融合蛋白:在其他方面,本文提供了融合蛋白,其包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)真核翻译起始因子4e结合蛋白1(eif4e-bp1)蛋白。eif4e-bp1是翻译阻遏蛋白家族的一部分。在一些实施方式中,eif4e-bp1直接与内源或外源eif4e相互作用。不受理论的束缚,据信eif4e-bp1蛋白与eif4e的相互作用抑制了复合物组装并抑制了翻译。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d及其各自的生物学等同物。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)crispr1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)crispr3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白是核酸酶失活的。在一些实施方式中,融合蛋白进一步包含接头,由接头组成或基本上由接头组成。在一些实施方式中,接头是肽接头。在一些实施方式中,肽接头包含三肽ggs的一个或多个重复。在其他实施方式中,接头是非肽接头。在一些实施方式中,非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。在一些实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[eif4e-bp1]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。在其他实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[eif4e-bp1]-cooh。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白与向导rna(grna),crisprna(crrna)和/或反式激活crrna(tracrrna)结合。在一些实施方式中,eif4e-bp1蛋白由具有包含全部或部分seqidno:61或其生物等同物的序列的多核苷酸编码。在一些实施方式中,eif4e-bp1蛋白具有包含全部或部分seqidno:62或其生物等同物的氨基酸序列。野生型eif4e-bp1可以响应多种不同信号(包括紫外线辐射和胰岛素信号传导)而被磷酸化,从而使其与eif4e分离并激活帽依赖性mrna翻译。在一些实施方式中,eif4e-bp1蛋白的一个或多个激酶磷酸化结构域被突变。在一些实施方式中,eif4e-bp1蛋白的全部激酶磷酸化结构域被突变。在一些实施方式中,突变用带负电荷的氨基酸例如天冬氨酸或谷氨酸替换磷酸化结构域的氨基酸。在其他实施方式中,突变用不带电荷的残基例如丙氨酸或甘氨酸替换磷酸化结构域的氨基酸。在一些实施方式中,eif4e-bp1包含一个或多个模拟磷酸化突变和/或减少eif4e-bp1与mtor激酶相互作用的突变。在一些实施方式中,eif4e-bp1蛋白包含一个或多个选自以下的突变:突变的femdi基序,突变的raip基序,残基25处的突变的胱天蛋白酶位点,mt37a,t46a,s65a和t70a。在一些实施方式中,突变的eif4e-bp1是组成性活性的。在一些实施方式中,融合蛋白是由包含以下核酸序列的核酸编码的dcas9-eif4e-bp1融合蛋白:在其他方面,本文提供了融合蛋白,其包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)泛素相关蛋白2-样(ubap2l)蛋白。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d及其各自的生物学等同物。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白是选自以下的蛋白质的全部或部分:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)crispr1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)crispr3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白是核酸酶失活的。在一些实施方式中,融合蛋白进一步包含接头,由接头组成或基本上由接头组成。在一些实施方式中,接头是肽接头。在一些实施方式中,肽接头包含三肽ggs的一个或多个重复。在其他实施方式中,接头是非肽接头。在一些实施方式中,非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。在一些实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[ubap2l]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。在其他实施方式中,融合蛋白包含以下结构,由以下结构组成或基本上由以下结构组成:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[ubap2l]-cooh。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白与向导rna(grna),crisprna(crrna)和/或反式激活crrna(tracrrna)结合。在一些实施方式中,ubap2l蛋白由多核苷酸编码,该多核苷酸具有包含选自seqidno:64,seqidno:65,seqidno:66,seqidno:67的序列以及生物学等同物的全部或部分的序列。在一些实施方式中,ubap2l蛋白具有包含以下,由以下组成,或基本上由以下组成的氨基酸序列:选自seqidno:68,seqidno:69,seqidno:70,seqidno:71,及其各自的生物学等同物的序列的全部或部分。在一些实施方式中,融合蛋白是由包含以下核酸序列的核酸编码的dcas9-ubap2l融合蛋白:多核苷酸和载体在一些方面,本文提供了编码融合蛋白的多核苷酸,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e蛋白。在其他方面,本文提供了编码融合蛋白的多核苷酸,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e-bp1蛋白。在一些实施方式中,多核苷酸还包含编码接头肽的核酸序列。在一些方面,本文提供了载体,该载体包含编码融合蛋白的多核苷酸或由其组成或基本上由其组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e蛋白。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白和eif4e蛋白在单个载体中被编码。在其他方面,本文提供了载体,该载体包含编码融合蛋白的多核苷酸或由其组成或基本上由其组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e-bp1蛋白。在一些实施方式中,多核苷酸还包含编码接头肽的核酸序列。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白和eif4-bp1蛋白在单个载体中被编码。在一些方面,本文提供了编码包含以下,由以下组成或基本上由以下组成的融合rna的多核苷酸:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires)。在一些实施方式中,多核苷酸还包含编码间隔区rna的核酸序列。在一些方面,本文提供了载体,其包含编码融合rna的多核苷酸,由其组成或基本上由其组成,所述多核苷酸包含,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires),任选地,其中所述载体是腺病毒载体,腺相关病毒载体或慢病毒载体。在一些实施方式中,载体还包含表达控制元件。在一些实施方式中,载体还包含可选择标志物。在一些实施方式中,载体还包含编码tracrrna和/或含pam的寡核苷酸的多核苷酸。在一些实施方式中,向导核苷酸序列可编程rna和一个或多个内部核糖体结合位点(ires)在单个载体中编码。在一些实施方式中,所述载体是病毒载体。在一些实施方式中,载体是腺病毒载体,腺相关病毒(aav)载体或慢病毒载体。在一些实施方式中,载体是逆转录病毒载体,腺病毒/逆转录病毒嵌合体载体,单纯疱疹病毒i或ii载体,细小病毒载体,网状内皮组织增殖病毒载体,脊髓灰质炎病毒载体,乳头瘤病毒载体,牛痘病毒载体或结合了两个或更多个病毒载体有利方面的任何杂合或嵌合载体。在一些实施方式中,载体还包含可操作地连接至多核苷酸的一种或多种表达控制元件。在一些实施方式中,载体还包含一种或多种选择标志物。在一些实施方式中,aav载体具有低毒性。在一些实施方式中,aav载体不纳入宿主基因组中,从而引起插入诱变的可能性低。在一些实施方式中,aav载体可以编码从4.5kb至4.75kb的一定范围的总多核苷酸。在一些实施方式中,可用于本文所述的任何组合物,系统,方法和试剂盒中的示例性aav载体可包括aav1载体,修饰的aav1载体,aav2载体,修饰的aav2载体,aav3载体,修饰的aav3载体,aav4载体,修饰的aav4载体,aav5载体,修饰的aav5载体,aav6载体,修饰的aav6载体,aav7载体,修饰的aav7载体,aav8载体,aav9载体,aav.rh10载体,修饰的aav.rh10载体,aav.rh32/33载体,修饰的aav.rh32/33载体,aav.rh43载体,修饰的aav.rh43载体,aav.rh64r1载体和修饰的aav.rh64r1载体及其任何组合或等同物。在一些实施方式中,慢病毒载体是具有整合酶能力的慢病毒载体(iclv)。在一些实施方式中,慢病毒载体可以指转基因质粒载体以及转基因质粒载体与相关质粒(例如,包装质粒,表达rev的质粒,包膜质粒)结合,以及能够通过病毒或类病毒进入机制将外源核酸引入细胞的基于慢病毒的颗粒。慢病毒载体是本领域众所周知的(参见例如,tronod.(2002)lentiviralvectors,newyork:spring-verlagberlinheidelberg和durand等,(2011)viruses3(2):132-159doi:10.3390/v3020132)。在一些实施方式中,可用于本文所述的任何组合物,系统,方法和试剂盒中的示例性慢病毒载体可包括人免疫缺陷病毒(hiv)1载体,修饰的人免疫缺陷病毒(hiv)1载体,人免疫缺陷病毒(hiv)2载体,修饰的人免疫缺陷病毒(hiv)2载体,乌白眉猴免疫缺陷病毒(sivsm)载体,修饰的乌白眉猴免疫缺陷病毒(sivsm)载体,非洲绿猴猿免疫缺陷病毒(sivagm)载体,修饰的非洲绿猴猿猴免疫缺陷病毒(sivagm)载体,马传染性贫血病毒(eiav)载体,修饰的马传染性贫血病毒(eiav)载体,猫免疫缺陷病毒(fiy)载体,修饰的猫科动物免疫缺陷病毒(fiy)载体,维斯纳/马迪病毒(vnv/vmv)载体,修饰的维斯纳/马迪病毒(vnv/vmv)载体,山羊关节炎-脑炎病毒(caev)载体,修饰的山羊关节炎-脑炎病毒(caev)载体,牛免疫缺陷病毒(biv)或修饰的牛免疫缺陷病毒(biv)。在一些实施方式中,载体还包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸,或由其组成,或基本上由其组成。在一些实施方式中,grna或crrna包含与靶rna互补的核苷酸序列。在一些实施方式中,在单个载体中编码所述向导核苷酸序列可编程rna结合蛋白和eif4e蛋白,所述单个载体进一步包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸,或由其组成,或基本上由其组成。在一些实施方式中,在单个载体中编码所述向导核苷酸序列可编程rna结合蛋白和eif4e-bp1蛋白,所述单个载体进一步包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸,或由其组成,或基本上由其组成。在一些实施方式中,载体还包含编码(i)tracrrna和/或(ii)含pam的寡核苷酸的多核苷酸,或由其组成,或基本上由其组成。在一些实施方式中,融合rna包含与靶rna互补的核苷酸序列。在一些实施方式中,向导核苷酸序列可编程rna和一个或多个内部核糖体结合位点(ires)在单个载体中编码,所述单个载体进一步包含编码(i)tracrrna和/或(ii)含pam的寡核苷酸的多核苷酸,或由其组成,或基本上由其组成。在本公开的组合物和方法的一些实施方式中,载体包含本公开的向导rna。在一些实施方式中,载体包含至少一个本公开的向导rna。在一些实施方式中,载体包含一个或多个本公开的向导rna。在一些实施方式中,载体包含两个或更多个本公开的向导rna。在一些实施方式中,载体还包含本发明的融合蛋白。在一些实施方式中,融合蛋白包含第一rna结合蛋白和第二rna结合蛋白。在本公开的组合物和方法的一些实施方式中,第一载体包含本公开的向导rna,并且第二载体包含本公开的融合蛋白。在一些实施方式中,第一载体包含至少一个本公开的向导rna。在一些实施方式中,第一载体包含一个或多个本公开的向导rna。在一些实施方式中,第一载体包含两个或更多个本公开的向导rna。在一些实施方式中,融合蛋白包含第一rna结合蛋白和第二rna结合蛋白。在一些实施方式中,第一载体和第二载体是相同的。在一些实施方式中,第一载体和第二载体是不同的。在本公开的组合物和方法的一些实施方式中,本公开的载体是病毒载体。在一些实施方式中,病毒载体包含分离或衍生自逆转录病毒的序列。在一些实施方式中,病毒载体包含分离或衍生自慢病毒的序列。在一些实施方式中,病毒载体包含分离或衍生自腺病毒的序列。在一些实施方式中,病毒载体包含分离或衍生自腺相关病毒(aav)的序列。在一些实施方式中,病毒载体无复制能力。在一些实施方式中,病毒载体是分离的或重组的。在一些实施方式中,病毒载体是自我互补的。在本公开的组合物和方法的一些实施方式中,病毒载体包含分离或衍生自腺相关病毒(aav)的序列。在一些实施方式中,病毒载体包含分离或衍生自血清型aav1,aav2,aav3,aav4,aav5,aav6,aav7,aav8,aav9,aav10,aav11或aav12的aav的反式末端重复序列或衣壳序列,或者载体和/或组分衍生自合成的aav血清型,例如但不限于anc80aav(aav1、2、6、8和9的祖先)。在一些实施方式中,病毒载体无复制能力。在一些实施方式中,病毒载体是分离的或重组的(raav)。在一些实施方式中,病毒载体是自我互补的(scaav)。在本公开的组合物和方法的一些实施方式中,本公开的载体是非病毒载体。在一些实施方式中,载体包含纳米颗粒,胶束,脂质体或脂质复合物,聚合物体,多聚复合物或树枝状聚合物,或由其组成。细胞在其他方面,本文提供的细胞包含一种或多种载体,或由一种或多种载体组成,或基本上由一种或多种载体组成,所述载体包含编码融合蛋白的多核苷酸,由其组成或基本上由其组成,所述融合蛋白包含(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e蛋白,由其组成或基本上由其组成。在其他方面,本文提供的细胞包含载体,或由载体组成,或基本上由载体组成,所述载体包含编码融合蛋白的多核苷酸,由其组成或基本上由其组成,所述融合蛋白包含(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e-bp1蛋白,由其组成或基本上由其组成。在一些实施方式中,多核苷酸还包含编码接头肽的核酸序列。在一些方面,本文提供了细胞,该细胞包含融合蛋白或由其组成或基本上由其组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e蛋白。在其他方面,本文提供了细胞,该细胞包含融合蛋白或由其组成或基本上由其组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e-bp1蛋白。在一些方面,本文提供了包含以下,由以下组成,或基本上由以下组成的细胞:融合rna,编码融合rna的多核苷酸,包含该多核苷酸的载体,或包含该融合rna,多核苷酸或载体的病毒颗粒;其中融合rna包含:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires),由其组成或基本上由其组成。在一些实施方式中,所述向导核苷酸序列-可编程rna是向导rna(grna)或crisprrna(crrna)。在一些实施方式中,细胞是真核细胞。在一些实施方式中,细胞是原核细胞。在一些实施方式中,细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猴或人细胞。在一些方面,本文提供了包含以下,由以下组成,或基本上由以下组成的细胞群:融合rna,编码融合rna的多核苷酸,包含该多核苷酸的载体,或包含该融合rna,多核苷酸或载体的病毒颗粒;其中融合rna包含:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires),由其组成或基本上由其组成。在一些实施方式中,所述向导核苷酸序列-可编程rna是向导rna(grna)或crisprrna(crrna)。在一些实施方式中,细胞是真核细胞。在一些实施方式中,细胞是原核细胞。在一些实施方式中,细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猴或人细胞。在一些实施方式中,细胞是真核细胞。在其他实施方式中,细胞是原核细胞。在一些实施方式中,所述细胞是哺乳动物细胞。在一些实施方式中,细胞是牛,鼠,猫,马,猪,犬,猿或人细胞。在特定的实施方式中,细胞是人细胞。在一些实施方式中,细胞从对象分离。在一些实施方式中,本公开的细胞是体细胞。在一些实施方式中,本公开的细胞是生殖细胞。在一些实施方式中,本公开的生殖细胞不是人细胞。在本公开的组合物和方法的一些实施方式中,本公开的细胞是干细胞。在一些实施方式中,本公开的细胞是胚胎干细胞。在一些实施方式中,本公开的胚胎干细胞不是人细胞。在一些实施方式中,本公开的细胞是多能干细胞或多潜能干细胞。在一些实施方式中,本公开的细胞是成体干细胞。在一些实施方式中,本公开的细胞是诱导性多潜能干细胞(ipsc)。在一些实施方式中,本公开的细胞是造血干细胞(hsc)。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是免疫细胞。在一些实施方式中,本公开的免疫细胞是淋巴细胞。在一些实施方式中,本公开的免疫细胞是t淋巴细胞(在本文中也称为t细胞)。本公开的示例性t细胞包括但不限于幼稚t细胞,效应t细胞,辅助t细胞,记忆t细胞,调节性t细胞(treg)和γδt细胞。在一些实施方式中,本公开的免疫细胞是b淋巴细胞。在一些实施方式中,本公开的免疫细胞是自然杀伤细胞。在一些实施方式中,本公开的免疫细胞是抗原呈递细胞。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是肌肉细胞。在一些实施方式中,本公开的肌肉细胞是成肌细胞或肌细胞。在一些实施方式中,本公开的肌肉细胞是心肌细胞,骨骼肌细胞或平滑肌细胞。在一些实施方式中,本公开的肌肉细胞是横纹细胞。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是上皮细胞。在一些实施方式中,本公开的上皮细胞形成鳞状细胞上皮,立方形细胞上皮,柱状细胞上皮,分层的细胞上皮,假复层的柱状细胞上皮或移行细胞上皮。在一些实施方式中,本公开的上皮细胞形成腺体,包括但不限于松果体腺,胸腺,垂体腺,甲状腺,肾上腺,载脂腺,全肾上腺,甲氧肾上腺素腺,浆液腺,粘液腺和皮脂腺。在一些实施方式中,本公开的上皮细胞接触器官的外表面,所述器官包括但不限于肺,脾,胃,胰腺,膀胱,肠,肾,胆囊,肝,喉或咽。在一些实施方式中,本公开的上皮细胞接触血管或静脉的外表面。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是神经元细胞。在一些实施方式中,本公开的神经元细胞是中枢神经系统的神经元。在一些实施方式中,本公开的神经元细胞是脑或脊髓的神经元。在一些实施方式中,本公开的神经元细胞是视网膜的神经元。在一些实施方式中,本公开的神经元细胞是颅神经或视神经的神经元。在一些实施方式中,本公开的神经元细胞是周围神经系统的神经元。在一些实施方式中,本公开的神经元细胞是神经胶质细胞或胶质细胞。在一些实施方式中,本发明的胶质细胞是中枢神经系统的胶质细胞,包括但不限于少突胶质细胞,星形胶质细胞,室管膜细胞和小胶质细胞。在一些实施方式中,本公开的胶质是周围神经系统的胶质细胞,包括但不限于雪旺氏细胞和卫星细胞。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是原代细胞。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是培养的细胞。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是体内,体外,离体或原位的。在本公开的组合物和方法的一些实施方式中,本公开的体细胞是自体的或同种异体的。rna靶向的crispr系统在一些方面,本文提供了用于转录后基因调控的系统,该系统包含以下,由以下组成或基本上由以下组成:(i)融合蛋白,其包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e蛋白;以及(ii)grna或(iii)crrna和tracrrna,其中所述grna或crrna包含与靶mrna互补的序列。在一些实施方式中,互补序列是间隔区序列。在其他方面,本文提供了用于转录后基因调控的系统,该系统包含以下,由以下组成或基本上由以下组成:(i)融合蛋白,其包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e-bp1蛋白;以及(ii)grna或(iii)crrna和tracrrna,其中所述grna或crrna包含与靶mrna互补的序列。在一些实施方式中,互补序列是间隔区序列。在一些实施方式中,本文公开的融合蛋白与本文公开的融合rna一起使用。在一些方面,本文提供了用于上调或增加靶mrna翻译的系统,该系统包含以下,由以下组成或基本上由以下组成:(i)融合蛋白,其包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e蛋白;以及(ii)grna或(iii)crrna和tracrrna,其中所述grna或crrna包含与靶mrna互补的序列。在一些实施方式中,互补序列是间隔区序列。在一些方面,本文提供了用于转录后基因调控的系统,该系统包含以下,由以下组成或基本上由以下组成:(a)包含以下,由以下组成或基本上由以下组成的融合rna:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires);和(b)向导核苷酸序列可编程rna结合蛋白,其中所述融合rna包含与靶mrna互补的序列。在一些实施方式中,该系统还包括含pam的寡核苷酸。在一些实施方式中,靶mrna不包含pam序列或其互补物。在一些方面,本文提供了用于增加靶mrna翻译的系统,该系统包含以下,由以下组成或基本上由以下组成:(a)包含以下,由以下组成或基本上由以下组成的融合rna:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires);和(b)向导核苷酸序列可编程rna结合蛋白,其中所述融合rna包含与靶mrna互补的序列。在一些实施方式中,该系统还包括含pam的寡核苷酸。在一些实施方式中,靶mrna不包含pam序列或其互补物。在系统的一些实施方式中,向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cpf1,cas13a,cas13b,casrx/cas13d,casm及其各自的生物学等同物。在一些实施方式中,向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。在一些实施方式中,向导核苷酸序列-可编程rna结合蛋白是核酸酶失活的。在一些实施方式中,casrx/cas13d蛋白是vi-d型crispr-cas系统的效应物。在一些实施方式中,casrx/case13d蛋白是可切割或结合rna的rna引导的rna内切核酸酶。在一些实施方式中,casrx/cas13d蛋白可以包括一个或多个高级真核生物和原核生物核苷酸结合(hepn)结构域。在一些实施方式中,casrx/case13d蛋白可包括野生型或突变的hepn结构域。在一些实施方式中,casrx/case13d蛋白包括不能切割rna但是可以加工向导rna的突变的hepn结构域。在一些实施方式中,casrx/cas13d蛋白不需要原间隔区侧翼序列。还参见wo公开号wo2019/040664和us2019/0062724(其通过引用全文并入本文)中casrx/cas13d蛋白的其他实例和序列,但不限于,特参考seqidno:54,57,61,67,69,71,72,73,74,75,76,77,78,85,86,87,88,113,147,153,154,155,158,160,162,164,170,179,183,185,187,189,190,202,204、206,208,209,210和212。yan等,(2018)molcell.70(2):327-339(doi:10.1016/j.molcel.2018.02.2018)和konermann等,(2018)cell173(3):665-676(doi:10.1016/i.cell/2018.02.033)已经描述了casrx/cas13d蛋白,二者均通过引用全文并入本文。还参见wo公开号wo2018/183703(casm)和wo2019/006471(cas13d),其通过引用全文并入本文。在一些实施方式中,增加或上调翻译是指与对照相比,从靶mrna翻译的肽的量增加。在一些实施方式中,对照包含在不存在融合蛋白的情况下从靶mrna翻译的肽的水平。在一些实施方式中,对照包含在添加融合蛋白之前从靶mrna翻译的肽的水平。在一些实施方式中,翻译相对于对照增加约1.1倍,约1.2倍,约1.3倍,约1.4倍,约1.5倍,约1.6倍,约1.7倍,约1.8倍,约1.9倍,约2倍,约2.5倍,约3倍,约4倍,约5倍,约6倍,约7倍,约8倍,约9倍,约10倍,约20倍,约50倍,约100倍,约1000倍或约10,000倍。在其他方面,本文提供了用于降低或下调靶mrna翻译的系统,该系统包含以下,由以下组成或基本上由以下组成:(i)融合蛋白,其包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e-bp1蛋白;以及(ii)grna或(iii)crrna和tracrrna,其中所述grna或crrna包含与靶mrna互补的序列。在一些实施方式中,互补序列是间隔区序列。在一些实施方式中,降低或下调翻译是指与对照相比,从靶mrna翻译的肽的量减少。在一些实施方式中,对照包含在不存在融合蛋白的情况下从靶mrna翻译的肽的水平。在一些实施方式中,对照包含在添加融合蛋白之前从靶mrna翻译的肽的水平。在一些实施方式中,翻译相对于对照降低约1.1倍,约1.2倍,约1.3倍,约1.4倍,约1.5倍,约1.6倍,约1.7倍,约1.8倍,约1.9倍,约2倍,约2.5倍,约3倍,约4倍,约5倍,约6倍,约7倍,约8倍,约9倍,约10倍,约20倍,约50倍,约100倍,约1000倍或约10,000倍。可以通过本领域已知的任何方法确定翻译的肽的量。合适的检测方法的非限制性实例包括western印迹,elisa,质谱,免疫组织化学,免疫荧光和使用报告基因例如荧光报告基因。在本文描述的系统的一些实施方式中,靶mrna包含pam序列。在其他实施方式中,靶mrna不包含pam序列。在一些实施方式中,该系统包含含pam的寡核苷酸。在其他实施方式中,该系统不包含含pam的寡核苷酸。方法在一些方面,本文提供了用于转录后增加或上调基因表达的方法,该方法包括使靶mrna与融合蛋白接触,由其组成或基本上由其组成,所述融合蛋白包括以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e蛋白,其中所述向导核苷酸序列可编程rna结合蛋白结合与靶rna的区域杂交的grna或crrna。在一些实施方式中,增加或上调基因表达是指与对照相比,从靶mrna翻译的肽的量增加。在一些实施方式中,对照包含在不存在融合蛋白的情况下从靶mrna翻译的肽的水平。在一些实施方式中,对照包含在添加融合蛋白之前从靶mrna翻译的肽的水平。在一些实施方式中,翻译相对于对照增加约1.1倍,约1.2倍,约1.3倍,约1.4倍,约1.5倍,约1.6倍,约1.7倍,约1.8倍,约1.9倍,约2倍,约2.5倍,约3倍,约4倍,约5倍,约6倍,约7倍,约8倍,约9倍,约10倍,约20倍,约50倍,约100倍,约1000倍或约10,000倍。在一些方面,本文提供了用于转录后降低或下调基因表达的方法,该方法包括使靶mrna与融合蛋白接触,由其组成或基本上由其组成,所述融合蛋白包括以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e-bp1蛋白,其中所述向导核苷酸序列可编程rna结合蛋白结合与靶rna的区域杂交的grna或crrna。在一些实施方式中,降低或下调基因表达是指与对照相比,从靶mrna翻译的肽的量减少。在一些实施方式中,对照包含在不存在融合蛋白的情况下从靶mrna翻译的肽的水平。在一些实施方式中,对照包含在添加融合蛋白之前从靶mrna翻译的肽的水平。在一些实施方式中,翻译相对于对照降低约1.1倍,约1.2倍,约1.3倍,约1.4倍,约1.5倍,约1.6倍,约1.7倍,约1.8倍,约1.9倍,约2倍,约2.5倍,约3倍,约4倍,约5倍,约6倍,约7倍,约8倍,约9倍,约10倍,约20倍,约50倍,约100倍,约1000倍或约10,000倍。可以通过本领域已知的任何方法确定翻译的肽的量。合适的检测方法的非限制性实例包括western印迹,elisa,质谱,免疫组织化学,免疫荧光和使用报告基因例如荧光报告基因。在本文描述的方法的一些实施方式中,靶mrna包含pam序列。在其他实施方式中,靶mrna不包含pam序列。该方法进一步包括提供含pam的寡核苷酸。在其他实施方式中,该方法不包括提供含pam的寡核苷酸。在一些实施方式中,靶mrna在细胞中。在一些实施方式中,细胞是真核细胞。在一些实施方式中,细胞是原核细胞。在一些实施方式中,所述细胞是哺乳动物细胞。在一些实施方式中,细胞是牛,鼠,猫,马,猪,犬,猿或人细胞。在一些实施方式中,细胞是植物细胞。在一些实施方式中,细胞在对象中。在一些实施方式中,细胞是体内,体外,离体或原位的。在一些实施方式中,组合物包含载体,所述载体包含包含本公开的向导rna和本公开的融合蛋白的组合物。在一些实施方式中,载体是aav。在一些方面中,本公开提供了治疗疾病或病症的方法,其包括向对象给药治疗有效量的本公开的组合物。本文还提供了用于治疗有此需要的对象的疾病或病状的方法,该方法包括向对象给予融合蛋白,由其组成或基本上由组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e-bp1蛋白,编码融合蛋白的多核苷酸,包含编码融合蛋白的多核苷酸的载体,或包含该载体的病毒颗粒,从而降低或下调靶mrna在对象中的翻译。在一些实施方式中,靶mrna涉及对象的疾病或病症的病因。在一些方面,本文还提供了用于治疗有此需要的对象的疾病或病状的方法,该方法包括向对象给予融合蛋白,由其组成或基本上由组成,所述融合蛋白包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e蛋白,编码融合蛋白的多核苷酸,包含编码融合蛋白的多核苷酸的载体,或包含该载体的病毒颗粒,从而增加或上调靶mrna在对象中的翻译。在一些实施方式中,靶mrna的缺乏与对象的疾病或病症的病因相关。在本文描述的方法的一些实施方式中,对象是植物或动物。在一些实施方式中,对象是哺乳动物。在一些实施方式中,哺乳动物是牛,马,猪,犬,猫,猿,鼠或人。在一些实施方式中,所述对象是人。在本文所述方法的一些实施方式中,进一步给予对象(i)与靶mrna互补的grna,或(ii)与靶mrna和tracrrna互补的crrna。在一些实施方式中,互补序列是间隔区序列。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于遗传疾病或病症。在一些实施方式中,遗传疾病或病症是单基因疾病或病症。在一些实施方式中,单基因疾病或病症是常染色体显性疾病或病症,常染色体隐性遗传性疾病或病症,x染色体连锁(x连锁)疾病或病症,x连锁显性疾病或病症,x连锁隐性疾病或病症,y连锁疾病或病症或线粒体疾病或病症。在一些实施方式中,遗传疾病或病症是多基因疾病或病症。在一些实施方式中,遗传疾病或病症是多基因疾病或病症。在一些实施方式中,单基因疾病或病症是常染色体显性疾病或病症,包括但不限于亨廷顿氏病,1型神经纤维瘤病,2型神经纤维瘤病,马凡氏综合症,遗传性非息肉病性结直肠癌,多发性遗传性骨软骨瘤病,血管性血友病和急性间歇性卟啉症。在一些实施方式中,单基因疾病或病症是常染色体隐性遗传疾病或病症,包括但不限于白化病,中链酰基辅酶a脱氢酶缺乏症,囊性纤维化,镰状细胞病,泰-萨氏病,尼曼-匹克病,脊髓性肌萎缩症和罗伯茨综合征。在一些实施方式中,单基因疾病或病症是x连锁疾病或病症,包括但不限于肌肉营养不良,杜兴氏肌营养不良,血友病,肾上腺神经营养不良(ald),rett综合征和血友病a。单基因疾病或病症是线粒体病症,包括但不限于莱伯遗传性视神经病变。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于免疫疾病或病症。在一些实施方式中,免疫疾病或病症是免疫缺陷疾病或病症,包括但不限于b细胞缺陷,t细胞缺陷,中性粒细胞减少症,无精子症,补体缺陷,获得性免疫缺陷综合症(aids)和由于医学干预引起的免疫缺陷(免疫抑制是药物治疗的预期或不良作用)。在一些实施方式中,免疫疾病或病症是自身免疫疾病或病症,包括但不限于,眼盲症,阿迪生氏病,成人斯蒂尔氏病,血球蛋白血症,斑秃,淀粉样变性病,抗gbm/抗tbm肾炎,抗磷脂综合征,自身免疫性血管性水肿,自身免疫性自主神经异常,自身免疫性脑脊髓炎,自身免疫性肝炎,自身免疫性内耳疾病(aied),自身免疫性心肌炎,自身免疫性卵泡炎,自身免疫性睾丸炎,自身免疫性胰腺炎,自身免疫性视网膜病,自身免疫性荨麻疹,轴索病和神经元性神经病疾病(aman),baló病,白塞氏病,良性粘膜天疱疮,大疱性天疱疮,castleman病(cd),乳糜泻,查加斯病,慢性炎性脱髓鞘性多发性神经病(cidp),慢性复发性多灶性骨髓炎(crmo),churg-strauss综合征(css)或嗜酸性粒细胞瘤(egpa),瘢痕性天疱疮,科根氏综合症,冷凝集素病,先天性心脏传导阻滞,考克斯奇基心肌炎,crest综合征,克罗恩病,疱疹样皮炎,皮肌炎,迪维克氏病(视神经脊髓炎),盘状狼疮,德莱斯特氏综合症,子宫内膜异位症,嗜酸性食管炎(eoe),嗜酸性筋膜炎,嗜酸性筋膜炎,淋巴结炎,淋巴结炎纤维化性肺泡炎,巨细胞动脉炎(颞动脉炎),巨细胞心肌炎,肾小球肾炎,goodpasture综合征,肉芽肿性多血管炎,graves病,guillain-barre综合征,桥本甲状腺炎,溶血性贫血,henoch-schonleis紫癜(hsp),妊娠疱疹(pg),化脓性汗腺炎(hs)(反面痤疮),低血红蛋白球蛋白血症,iga肾病,igg4相关硬化性疾病,免疫性血小板减少性紫癜(itp),包涵体肌炎(ibm),间质性膀胱炎(ic),青少年关节炎,青少年糖尿病(1型糖尿病),青少年肌炎(jm),川崎病,lambert-eaton综合征,白细胞碎裂性血管炎,扁平苔藓,硬化性苔藓,木样结膜炎,线性iga病(lad),狼疮,慢性莱姆病,美尼尔氏病,显微镜下多血管炎(mpa),混合性结缔组织病(mctd),mooren溃疡,mucha-habermann病,多灶性运动神经病(mmn)或mmncb,多发性硬化症,重症肌无力,肌炎,嗜睡症,新生儿狼疮,视神经脊髓炎,中性粒细胞减少症,眼瘢痕性类天疱疮,视神经炎,复发性风湿病(pr),pandas,副肿瘤性小脑变性(pcd),阵发性夜间血红蛋白尿(pnh),parryromberg综合征,扁平部炎(周围葡萄膜炎),parsonnage-turner综合征,天疱疮,周围神经病变,围发性脑脊髓炎,恶性贫血(pa),poems综合征,结节性多动脉炎,i,ii,iii型多腺综合征,风湿性肌痛,多肌炎,心肌梗塞后综合征,心包切开术后综合征,原发性胆汁性肝硬化,原发性硬化性胆管炎,孕酮皮炎,牛皮癣,牛皮癣性关节炎,纯红细胞发育不良(prca),坏疽性脓皮病,雷诺现象,反应性关节炎,反射性交感神经营养不良,复发性多发性软骨炎,不宁腿综合症(rls),腹膜纤维化,风湿热,类风湿性关节炎,结节病,施密特综合征,巩膜炎,硬皮病,干燥综合征,精子和睾丸自身免疫性,僵人综合征(sps),亚急性细菌性心内膜炎(sbe),苏萨克氏综合征,交感性眼炎(so),多发性大动脉炎,颞动脉炎/巨细胞动脉炎,血小板减少性紫癜(ttp),tolosa-hunt综合征(ths),横贯性脊髓炎,1型糖尿病,溃疡性结肠炎(uc),未分化结缔组织病(uctd),葡萄膜炎,血管炎,白癜风,vogt-koyanagi-harada病或wegener肉芽肿病。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于炎性疾病或病症。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于代谢性疾病或病症。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于退行性或进行性疾病或病症。在一些实施方式中,退行性或进行性疾病或病症包括但不限于肌萎缩性侧索硬化症(als),亨廷顿氏病,阿尔茨海默氏病和衰老。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于传染性疾病或病症。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于儿科或发育性疾病或病症。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于心血管疾病或病症。在本公开的组合物和方法的一些实施方式中,本公开的疾病或病症包括但不限于增殖性疾病或病症。在一些实施方式中,所述增殖性疾病或病症是癌症。在一些实施方式中,癌症包括但不限于急性淋巴细胞白血病(all),急性髓细胞性白血病(aml),肾上腺皮质癌,aids相关癌症,卡波济肉瘤(软组织肉瘤),aids相关淋巴瘤(淋巴瘤),原发性中枢神经系统淋巴瘤(淋巴瘤),肛门癌,阑尾癌,胃肠道类癌,星形细胞瘤,非典型类畸形/类瘤,中枢神经系统(脑癌),基底细胞癌,胆管癌,膀胱癌,骨癌,尤因肉瘤,骨肉瘤,恶性纤维组织细胞瘤,脑肿瘤,乳腺癌,伯基特淋巴瘤,类癌瘤,癌,心脏(心)肿瘤,胚性肿瘤,生殖细胞肿瘤,原发性中枢神经系统淋巴瘤,宫颈癌,胆管癌,脊索瘤,慢性淋巴细胞白血病(cll),慢性粒细胞性白血病(cml),慢性骨髓增生性肿瘤,结直肠癌,颅咽管瘤,皮肤t细胞淋巴瘤,原位导管癌,胚胎肿瘤,子宫内膜癌症(子宫癌),室管膜瘤,食道癌,嗅神经母细胞瘤(头颈癌),尤因肉瘤(骨癌),颅外生殖细胞瘤,性腺外生殖细胞瘤,眼癌,儿童眼内黑素瘤,眼内黑素瘤,视网膜母细胞瘤,输卵管癌癌症,骨,恶性和骨肉瘤的纤维组织细胞瘤,胆囊癌,胃癌(胃),胃肠道类癌,胃肠道间质瘤(gist)(软组织肉瘤),儿童胃肠道间质瘤,生殖细胞瘤,儿童颅外生殖细胞瘤肿瘤,性腺外生殖细胞肿瘤,卵巢生殖细胞肿瘤,睾丸癌,妊娠滋养细胞疾病,毛细胞白血病,头颈癌,心脏肿瘤,肝细胞(肝)癌,组织细胞增多症,霍奇金淋巴瘤,下咽喉癌(头颈癌),眼内黑素瘤,胰岛细胞瘤,胰腺神经内分泌肿瘤,卡波济肉瘤(软组织肉瘤),肾癌(肾细胞),朗格汉斯细胞组织细胞增生症,喉癌(头颈癌),白血病,嘴唇和口腔癌(头颈癌),肝癌,肺癌(非小细胞和小细胞癌),儿童肺癌,淋巴瘤,男性乳腺癌,骨和骨肉瘤的恶性纤维组织细胞瘤,黑色素瘤,默克尔细胞癌(皮肤癌),间皮瘤,原发性隐匿性转移性鳞癌(头颈癌),nut基因改变的中线癌,口腔癌(头颈癌),多发性内分泌肿瘤,多发性骨髓瘤/血浆细胞瘤,蕈样真菌病(淋巴瘤),骨髓增生异常综合征,骨髓增生异常/骨髓增生性肿瘤,鼻腔和鼻旁鼻窦癌(头颈癌),鼻咽癌(头颈癌),神经母细胞瘤,非霍奇金淋巴瘤,非小细胞肺癌,口腔癌,嘴唇和口腔癌和口咽癌,骨肉瘤和骨恶性纤维组织细胞瘤,卵巢癌,胰腺癌,胰腺神经内分泌肿瘤(胰岛细胞瘤),乳头状瘤病,副神经节瘤,甲状旁腺癌,阴茎癌,咽癌(头颈癌),嗜铬细胞瘤,浆细胞瘤/多发性骨髓瘤,胸膜肺母细胞瘤,妊娠和乳腺癌,原发性中枢神经系统(cns)淋巴瘤,原发性腹膜癌,前列腺癌,直肠癌,复发性癌症,肾细胞(肾)癌,视网膜母细胞瘤,横纹肌肉瘤,儿童期(软组织肉瘤),唾液腺癌(头颈癌),肉瘤,儿童期横纹肌肉瘤(软组织肉瘤),儿童期血管肿瘤(软组织肉瘤),尤因肉瘤(骨癌),卡波西肉瘤(软组织肉瘤),骨肉瘤(骨癌),子宫肉瘤,塞氏综合征,淋巴瘤,皮肤癌,小细胞肺癌,小肠癌,软组织肉瘤,皮肤鳞状细胞癌,鳞状颈癌,胃(胃部)癌,t细胞淋巴瘤,睾丸癌,喉癌(头颈癌),鼻咽癌,口咽癌,下咽喉癌,胸腺瘤和胸腺癌,甲状腺癌,肾盂和输尿管移行细胞癌,肾细胞癌,尿道癌,子宫肉瘤,阴道癌,血管肿瘤(软组织肉瘤),外阴癌,威尔姆斯瘤和其他儿童期肾脏肿瘤。在本公开的方法的一些实施方式中,已经诊断本公开的对象患有疾病或病症。在一些实施方式中,本公开的对象表现出疾病或病症的至少一种体征或症状。在一些实施方式中,对象具有可预测发生疾病或病症的风险的生物标志物。在一些实施方式中,生物标志物是遗传突变。在本公开的方法的一些实施方式中,本公开的对象是雌性。在本公开的方法的一些实施方式中,本公开的对象是雄性。在一些实施方式中,本公开的对象具有两个xx或xy染色体。在一些实施方式中,本公开的对象具有两个xx或xy染色体和第三染色体,x或y。在本公开的方法的一些实施方式中,本公开的对象是新生儿,婴儿,儿童,成人,中老年人或老年人。在本公开的方法的一些实施方式中,本公开的对象的日龄为至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或31天。在本公开的方法的一些实施方式中,本公开的对象的月龄为至少1、2、3、4、5、6、7、8、9、10、11或12个月。在本公开的方法的一些实施方式中,本公开的对象年龄为至少1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100岁或其间的任何年数或部分年数。在本公开的方法的一些实施方式中,本公开的对象是哺乳动物。在一些实施方式中,本公开的对象是非人哺乳动物。在本公开的方法的一些实施方式中,本公开的对象是人。在本公开的方法的一些实施方式中,治疗有效量包括单剂量的本公开的组合物。在一些实施方式中,治疗有效量包括治疗有效量,其包括至少一剂本公开的组合物。在一些实施方式中,治疗有效量包括治疗有效量,其包括至少一剂或多剂本公开的组合物。在本公开的方法的一些实施方式中,治疗有效量能消除疾病或病症的体征或症状。在一些实施方式中,治疗有效量降低疾病或病症的体征或症状的严重性。在本公开的方法的一些实施方式中,治疗有效量能消除疾病或病症。在本公开的方法的一些实施方式中,治疗有效量预防疾病或病症的发作。在一些实施方式中,治疗有效量延迟疾病或病症的发作。在一些实施方式中,治疗有效量降低疾病或病症的体征或症状的严重性。在一些实施方式中,治疗有效量改善了对象的预后。在本公开的方法的一些实施方式中,将本公开的组合物全身性给予对象。在一些实施方式中,本公开的组合物通过静脉内途径给予对象。在一些实施方式中,本公开的组合物通过注射或输注给予对象。在本公开的方法的一些实施方式中,将本公开的组合物局部给予对象。在一些实施方式中,本公开的组合物通过骨内,眼内,脑脊髓内或脊髓内途径给予对象。在一些实施方式中,将本公开的组合物直接给予中枢神经系统的脑脊髓液。在一些实施方式中,将本公开的组合物直接给予眼睛的组织或流体,并且在眼结构之外不具有生物利用度。在一些实施方式中,本公开的组合物通过注射或输注给予对象。病毒颗粒在其他方面,本文提供的病毒颗粒包含载体,或由载体组成,或基本上由载体组成,所述载体包含编码融合蛋白的多核苷酸,由其组成或基本上由其组成,所述融合蛋白包含(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e蛋白,由其组成或基本上由其组成。在其他方面,本文提供的病毒颗粒包含载体,或由载体组成,或基本上由载体组成,所述载体包含编码融合蛋白的多核苷酸,由其组成或基本上由其组成,所述融合蛋白包含(i)向导核苷酸序列可编程rna结合蛋白;和(ii)eif4e-bp1蛋白,由其组成或基本上由其组成。在一些实施方式中,多核苷酸还包含编码接头肽的核酸序列。通常,将遗传材料例如rna或dna包装到一种或多种载体中的方法是本领域众所周知的。例如,可以使用包装载体和细胞系包装遗传物质,并通过传统的重组方法引入。在一些实施方式中,包装载体可以包括但不限于逆转录病毒载体,慢病毒载体,腺病毒载体和腺相关病毒载体。包装载体包含促进遗传物质向细胞内递送的元件和序列。例如,逆转录病毒构建体是包装质粒,其包含至少一个逆转录病毒辅助dna序列,其衍生自无复制能力的逆转录病毒基因组,其反式编码包装无复制能力的逆转录病毒载体所需的所有病毒体蛋白,并用于产生能够以高滴度包装无复制能力的逆转录病毒载体的病毒体蛋白,而不会产生具有复制能力的辅助病毒。逆转录病毒dna序列缺少编码病毒的病毒5′ltr的天然增强子和/或启动子的区域,并且缺少负责包装辅助基因组的psi功能序列和3′ltr,但编码外源聚腺苷酸化位点,例如,sv40聚腺苷酸化位点,和外来的增强子和/或启动子,其在需要产生病毒的细胞类型中引导高效转录。逆转录病毒是白血病病毒,例如莫洛尼鼠白血病病毒(mmlv),人免疫缺陷病毒(hiv)或长臂猿白血病病毒(galv)。外源增强子和启动子可以是人巨细胞病毒(hcmv)即早(ie)增强子和启动子,莫洛尼鼠肉瘤病毒(mmsv)的增强子和启动子(u3区域),劳斯肉瘤病毒(rsv)的u3区域,脾灶形成病毒(sffv)的u3区域或连接天然莫洛尼鼠白血病病毒(mmlv)启动子的hcmvie增强子。逆转录病毒包装质粒可以由基于质粒的表达载体编码的两个逆转录病毒辅助dna序列组成,例如,其中第一辅助序列包含编码亲嗜性mmlv或galv的gag和pol蛋白的cdna,第二辅助序列包含编码env蛋白的cdna。决定宿主范围的env基因可以来自编码异种,两亲,亲嗜,多变(形成水貂病灶)或10a1鼠白血病病毒env蛋白,或长臂猿白血病病毒(galv)env蛋白,人类免疫缺陷病毒env(gp160)蛋白,水泡性口炎病毒(vsv)g蛋白,i和ii型人t细胞白血病(htlv)env基因产物,由一种或多种上述env基因的组合衍生的嵌合包膜基因或编码上述env基因产物的细胞质和跨膜的嵌合包膜基因,以及针对所需靶细胞上特定表面分子的单克隆抗体。类似的基于载体的系统可以采用其他载体,例如睡美人载体或转座子元件。然后可以通过适当的给药途径引入所得的包装表达系统,该给药途径相对于本文公开的方法方面进行了详细讨论。组合物本发明还提供了一种包含任何一种或多种融合蛋白或编码融合蛋白的核酸序列以及运载体的组合物。在一些实施方式中,组合物可以是编码向导核苷酸序列可编程rna结合蛋白和翻译修饰蛋白的一种或多种多核苷酸。在一些实施方式中,组合物可以是本文所述的任何融合蛋白。在一些实施方式中,组合物可以是本文所述的任何多核苷酸。在一些实施方式中,运载体是药学上可接受的运载体。在一些实施方式中,组合物是药物组合物,其包含一种或多种融合蛋白,或一种或多种编码融合蛋白的核酸序列,以及药学上可接受的运载体。在一些实施方式中,组合物或药物组合物还包含一种或多种grna,crrna和/或tracrrna。简而言之,本发明的药物组合物可以与一种或多种药学或生理学上可接受的运载体,稀释剂或赋形剂组合,包含融合蛋白或编码所述融合蛋白的多核苷酸,其任选地包含在aav中,其也任选地是免疫正交的。这样的组合物可以包括缓冲液,如中性缓冲盐水、磷酸盐缓冲盐水等;糖类,如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇;蛋白质;多肽或氨基酸,如甘氨酸;抗氧化剂;螯合剂,如edta或谷胱甘肽;佐剂(例如,氢氧化铝);和防腐剂。本公开的组合物可以配制用于口服,静脉内,局部,肠内和/或肠胃外给药。在某些实施方式中,将本公开的组合物配制用于静脉内给药。试剂盒在一些方面,本文提供了试剂盒,其包含以下,由以下组成或基本上由以下组成:一种或多种融合蛋白,编码融合蛋白的多核苷酸,包含该多核苷酸的载体,或包含该载体的病毒颗粒,其中该融合蛋白包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e蛋白;或其中所述融合蛋白包含以下,由以下组成或基本上由以下组成:(a)向导核苷酸序列可编程rna结合蛋白;和(b)eif4e-bp1蛋白。在一些实施方式中,试剂盒进一步包含使用说明书,由其组成或基本上由其组成。在本文所述试剂盒的一些实施方式中,试剂盒进一步包含以下,由以下组成或基本上由以下组成:选自以下的一种或多种核酸:(i)grna;(ii)crrna和tracrrna;(iii)含pam的寡核苷酸;和(iv)用于表达(i),(ii)或(iii)的核酸的载体。在一些实施方式中,试剂盒进一步包含一种或多种用于实施本公开的方法的试剂,由其组成或基本上由其组成。这种试剂的非限制性实例包括病毒包装细胞,病毒载体,载体主链,grna,转染试剂,转导试剂,病毒颗粒和pcr引物。因此,其它实施方式包括在所附权利要求书的范围内。示例性实施方式:实施方式1是包含一种或多种编码以下物质的多核苷酸的组合物:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)翻译修饰蛋白。实施方式2是实施方式1的组合物,其中所述向导核苷酸序列可编程rna结合蛋白包含cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,casm及其各自的生物学等同物中的至少一种。实施方式3是实施方式2的组合物,其中所述向导核苷酸序列可编程rna结合蛋白包含以下的至少一种:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式4是实施方式2或3的组合物,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式5是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白是以下的至少一种:真核翻译起始因子4e(eif4e)(seqidno:52-59),翻译起始因子4e结合蛋白(eif4e-bp1)(seqidno:61-62),泛素相关蛋白2-样(ubap2l)(seqidno:64-71)及其各自的生物学等同物。实施方式6是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白由具有包含seqidno:52-55,seqidno:61,seqidno:64-67,seqidno:94-193,seqidno:285,seqidno:320-348及其各自的生物学等同物中的至少一种的全部或部分的序列的多核苷酸编码。实施方式7是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白具有氨基酸序列,该氨基酸序列包含以下序列的至少一种的全部或部分:seqidno:56-59,seqidno:62,seqidno:68-71及其各自的生物学等同物。实施方式8是前述实施方式中任一项的组合物,还包含接头。实施方式9是实施方式8的组合物,其中所述接头是肽接头。实施方式10是实施方式9的组合物,其中所述肽接头包含三肽ggs的一个或多个重复。实施方式11是实施方式8的组合物,其中所述接头是非肽接头。实施方式12是实施方式11的组合物,其中所述非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。实施方式13是前述实施方式中任一项的组合物,其中所述向导核苷酸序列可编程rna结合蛋白与向导rna(grna),crisprna(crrna)或反式激活crrna(tracrrna)结合。实施方式14是前述实施方式中任一项的组合物,其中所述真核翻译修饰蛋白的一个或多个激酶磷酸化结构域被突变。实施方式15是前述实施方式中任一项的组合物,还包含载体。实施方式16是实施方式15的载体,其中所述载体是腺病毒载体,腺相关病毒载体或慢病毒载体。实施方式17是实施方式15或16的载体,还包含表达控制元件。实施方式18是实施方式15-17的载体,还包含可选择标志物。实施方式19是实施方式15-18中任一项的载体,还包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸。实施方式20是实施方式19的载体,其中所述grna或crrna包含与靶rna互补的核苷酸序列。实施方式21是一种用于转录后基因调控的系统,该系统包括:(i)实施方式1-20中任一项的组合物;和(ii)grna;或(iii)crrna和tracrrna;其中grna或crrna包含与靶mrna互补的序列。实施方式22是一种用于转录后调节基因表达的方法,所述方法包括使靶mrna与实施方式1-20中任一项的组合物接触,其中所述向导核苷酸序列可编程rna结合蛋白结合与靶rna的区域杂交的grna或crrna。实施方式23是一种融合蛋白,其包含:(i)rna结合蛋白;和(ii)翻译修饰蛋白。实施方式24是实施方式23的融合蛋白,其中rna结合蛋白选自pumilio和fbf(puf)蛋白,基于pumilio的装配体(pumby)蛋白,五肽重复序列(ppr)蛋白以及其各自的生物学等同物。实施方式25是实施方式23的融合蛋白,其中rna结合蛋白是pumilio和fbf(puf)蛋白。实施方式26是实施方式23的融合蛋白,其中所述rna结合蛋白是基于pumilio的装配体(pumby)蛋白。实施方式27是实施方式23的融合蛋白,其中rna结合蛋白是五肽重复序列(ppr)蛋白。实施方式28是实施方式23-27中任一项的组合物,其中所述翻译修饰蛋白是以下物质的至少一种:真核翻译起始因子4e(eif4e)(seqidno:52-59),翻译起始因子4e结合蛋白(eif4e-bp1)(seqidno:61-62),泛素相关蛋白2-样(ubap2l)(seqidno:64-71)及其各自的生物学等同物。实施方式29是实施方式23-28中任一项的组合物,其中所述翻译修饰蛋白由具有包含seqidno:52-55,seqidno:61,seqidno:64-67,seqidno:94-193,seqidno:285,seqidno:320-348及其各自的生物学等同物中至少一个的全部或部分的序列的多核苷酸编码。实施方式30是实施方式23-29中任一项的组合物,其中所述翻译修饰蛋白具有氨基酸序列,该氨基酸序列包含以下的至少一种的全部或部分:seqidno:56-59,seqidno:62,seqidno:68-71,及其各自的生物学等同物。实施方式31是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白是真核蛋白。实施方式32是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白是人蛋白。实施方式33是前述实施方式中任一项的组合物,其中所述翻译修饰蛋白是原核的。实施方式34是一种融合蛋白,其包含:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)真核翻译起始因子4e(eif4e)蛋白。实施方式35是实施方式34的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,及其各自的生物学等同物。实施方式36是实施方式35的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式37是实施方式35或36的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式38是实施方式34-37中任一项的融合蛋白,还包含接头。实施方式39是实施方式38的融合蛋白,其中所述接头是肽接头。实施方式40是实施方式39的融合蛋白,其中所述肽接头包含三肽ggs的一个或多个重复。实施方式41是实施方式38的融合蛋白,其中所述接头是非肽接头。实施方式42是实施方式41的融合蛋白,其中所述非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。实施方式43是实施方式38-42中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[eif4e]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。实施方式44是实施方式38-42中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[eif4e]-cooh。实施方式45是实施方式34-44中任一项的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白与向导rna(grna),crisprna(crrna)或反式激活crrna(tracrrna)结合。实施方式46是实施方式34-45中任一项的融合蛋白,其中所述eif4e蛋白由具有包含选自以下序列的全部或部分的序列的多核苷酸编码:seqidno:52,seqidno:53,seqidno:54,seqidno:55,及其各自的生物学等同物。实施方式47是实施方式34-46中任一项的融合蛋白,其中所述eif4e蛋白具有包含选自以下序列的全部或部分的氨基酸序列:seqidno:56,seqidno:57,seqidno:58,seqidno:59,及其各自的生物学等同物。实施方式48是实施方式34-47中任一项的融合蛋白,其中eif4e的一个或多个激酶磷酸化结构域被突变。实施方式49是实施方式48的融合蛋白,其中突变的eif4e是组成性活性的。实施方式50是一种融合蛋白,其包含:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)真核翻译起始因子4e结合蛋白1(eif4e-bp1)蛋白。实施方式51是实施方式50的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,及其各自的生物学等同物。实施方式52是实施方式51的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新凶手弗朗西丝氏菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式53是实施方式51或52的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式54是实施方式50-53中任一项的融合蛋白,还包含接头。实施方式55是实施方式54的融合蛋白,其中所述接头是肽接头。实施方式56是实施方式55的融合蛋白,其中所述肽接头包含三肽ggs的一个或多个重复。实施方式57是实施方式54的融合蛋白,其中所述接头是非肽接头。实施方式58是实施方式57的融合蛋白,其中所述非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。实施方式59是实施方式54-58中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[eif4e-bp1]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。实施方式60是实施方式54-58中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[eif4e-bp1]-cooh。实施方式61是实施方式50-60中任一项的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白与向导rna(grna),crisprna(crrna)或反式激活crrna(tracrrna)结合。实施方式62是实施方式50-61中任一项的融合蛋白,其中所述eif4e-bp1蛋白由具有包含seqidno:61的全部或部分或其生物学等同物的序列的多核苷酸编码。实施方式63是实施方式50-62中任一项的融合蛋白,其中所述eif4e-bp1蛋白具有包含seqidno:62的全部或部分或其生物学等同物的氨基酸序列。实施方式64是实施方式50-63中任一项的融合蛋白,其中eif4e-bp1蛋白的一个或多个激酶磷酸化结构域被突变。实施方式65是实施方式64的融合蛋白,其中突变的eif4e-bp1是组成性活性的。实施方式66是编码实施方式34-65中任一项的融合蛋白的多核苷酸。实施方式67是包含实施方式66的多核苷酸的载体,任选地其中该载体是腺病毒载体,腺相关病毒载体或慢病毒载体。实施方式68是实施方式67的载体,还包含表达控制元件。实施方式69是实施方式67或68的载体,还包含可选择标志物。实施方式70是实施方式67-69中任一项的载体,还包含编码(i)grna或(ii)crrna和tracrrna的多核苷酸。实施方式71是实施方式70的载体,其中所述grna或crrna包含与靶rna互补的核苷酸序列。实施方式72是一种病毒颗粒,其包含实施方式34-65中任一项的融合蛋白,实施方式66的多核苷酸或实施方式67-71中任一项的载体。实施方式73是一种细胞,其包含实施方式34-65中任一项的融合蛋白,实施方式66的多核苷酸,实施方式67-71中任一项的载体,或实施方式72的病毒颗粒。实施方式74是实施方式73的细胞,其中该细胞是真核细胞。实施方式75是实施方式73的细胞,其中该细胞是原核细胞。实施方式76是实施方式74的细胞,其中所述细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猿或人细胞。实施方式77是一种用于转录后基因调控的系统,该系统包括:(i)实施方式34-65中任一项的融合蛋白;和(ii)grna;或(iii)crrna和tracrrna;其中grna或crrna包含与靶mrna互补的序列。实施方式78是用于增加靶mrna翻译的系统,该系统包括:(i)实施方式34-39中任一项的融合蛋白;和(ii)grna;或(iii)crrna和tracrrna;其中grna或crrna包含与靶mrna互补的序列。实施方式79是用于降低靶mrna翻译的系统,该系统包括:(i)实施方式50-65中任一项的融合蛋白;和(ii)grna;或(iii)crrna和tracrrna;其中grna或crrna包含与靶mrna互补的序列。实施方式80是根据实施方式77-79中任一项的系统,还包括含pam的寡核苷酸。实施方式81是实施方式77-79中任一项的系统,其中靶mrna不包含pam序列或其互补序列。实施方式82是一种用于转录后增加基因表达的方法,所述方法包括使靶mrna与实施方式34-49中任一项的融合蛋白接触,其中所述向导核苷酸序列可编程rna结合蛋白结合与靶rna的区域杂交的grna或crrna。实施方式83是一种用于转录后降低基因表达的方法,所述方法包括使靶mrna与实施方式50-65中任一项的融合蛋白接触,其中所述向导核苷酸序列可编程rna结合蛋白结合与靶rna的区域杂交的grna或crrna。实施方式84是实施方式82或83的方法,其中靶mrna包含pam序列或其互补序列。实施方式85是实施方式82或83的方法,其中靶mrna不包含pam序列或其互补序列。实施方式86是实施方式82-85中任一项的方法,其中靶mrna在细胞中。实施方式87是实施方式86的方法,其中该细胞是真核细胞。实施方式88是实施方式86的方法,其中该细胞是原核细胞。实施方式89是实施方式87的方法,其中所述真核细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猿或人细胞。实施方式90是实施方式86-89中任一项的方法,其中所述细胞在对象中。实施方式91是一种用于治疗有此需要的对象的疾病或病症的方法,该方法包括向对象给予实施方式34-65中任一项的融合蛋白,实施方式66的多核苷酸,实施方式67-71中任一项的载体,或实施方式72的病毒颗粒,从而增加或降低对象中靶mrna翻译。实施方式92是实施方式90或91的方法,其中所述对象是人。实施方式93是实施方式91的方法,还包括向对象给予:(i)与mrna互补的grna,或(ii)与mrna和tracrrna互补的crrna。实施方式94是实施方式93的方法,还包括向所述对象给予含pam的寡核苷酸。实施方式95是试剂盒,其包含以下一个或多个:实施方式34-65中任一项的融合蛋白,实施方式66的多核苷酸,实施方式67-71中任一项的载体,或实施方式72的病毒颗粒,以及任选的使用说明书。实施方式96是实施方式95的试剂盒,还包含选自以下的一种或多种核酸:(i)grna;(ii)crrna和tracrrna;(iii)含pam的寡核苷酸;和(iv)用于表达(i),(ii)或(iii)的核酸的载体。实施方式97是一种包含本文所述的融合蛋白或病毒载体的非人转基因动物。实施方式98是一种融合rna,其包含:(i)向导核苷酸序列可编程rna;和(ii)一个或多个内部核糖体进入位点(ires)。实施方式99是实施方式98的融合rna,其中所述向导核苷酸序列可编程rna是向导rna(grna)或crisprna(crrna)。实施方式100是实施方式99的融合rna,其中所述向导核苷酸序列可编程rna衍生自来自化脓性链球菌,金黄色葡萄球菌,新凶手弗朗西丝氏菌,脑膜炎奈瑟氏球菌,嗜热链球菌或侧孢短芽孢杆菌的向导rna支架。实施方式101是实施方式98-100中任一项的融合rna,其中ires是i型或ii型ires。实施方式102是实施方式98-101中任一项的融合rna,其中ires是病毒ires或真核ires。实施方式103是实施方式98-102中任一项的融合rna,其中所述ires选自:脊髓灰质炎ires,鼻病毒ires,脑心肌炎病毒ires(emcv-ires),小核糖核酸病毒ires,口蹄疫病毒ires(fmdv-ires),口咽病毒ires,卡波西氏肉瘤相关疱疹病毒ires(kshv-ires),甲型肝炎ires,丙型肝炎ires,经典猪瘟病毒ires,瘟病毒ires,牛病毒性腹泻病毒ires,弗云德鼠白血病ires,莫洛尼鼠白血病ires(mmlv-ires),劳斯肉瘤病毒ires,人类免疫缺陷病毒ires(hiv-ires),小珀椿象肠病毒ires,双顺反子病毒(cripavirus)ires,蟋蟀麻痹病毒ires,锥蝽病毒ires,禾谷缢管蚜病毒ires,马立克氏病病毒ires,成纤维细胞生长因子(fgf-1ires和fgf-2ires),血小板衍生生长因子b(pdgf/c-sisires),血管内皮生长因子(vegfires)和胰岛素样生长因子2(igf-iiires)。实施方式104是实施方式98-103中任一项的融合rna,还包含位于所述向导核苷酸序列可编程rna和ires之间的接头序列rna。实施方式105是实施方式104的融合rna,其中所述融合rna包含结构5’-[向导核苷酸序列可编程rna]-[接头序列]-[ires]-3’。实施方式106是实施方式104的融合rna,其中所述融合rna包含结构5’-[ires]-[接头序列]-[向导核苷酸序列可编程rna]-3’。实施方式107是实施方式98-106中任一项的融合rna,其中所述向导核苷酸序列可编程rna包含与靶rna互补的核苷酸序列。实施方式108是编码实施方式98-107中任一项的融合rna的多核苷酸。实施方式109是包含实施方式108的多核苷酸的载体,任选地其中该载体是腺病毒载体,腺相关病毒载体或慢病毒载体。实施方式110是实施方式109的载体,还包含表达控制元件。实施方式111是实施方式109或110的载体,还包含可选择标志物。实施方式112是实施方式109-111中任一项的载体,还包含编码tracrrna的多核苷酸。实施方式113是一种病毒颗粒,其包含实施方式98-107中任一项的融合rna,实施方式108的多核苷酸或实施方式109-112中任一项的载体。实施方式114是一种细胞,其包含实施方式98-107中任一项的融合rna,实施方式108的多核苷酸,实施方式109-112中任一项的载体,或实施方式113的病毒颗粒。实施方式115是实施方式114的细胞,其中该细胞是真核细胞。实施方式116是实施方式114的细胞,其中该细胞是原核细胞。实施方式117是实施方式115的细胞,其中所述细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猿或人细胞。实施方式118是一种用于转录后基因调控的系统,该系统包括:(i)实施方式98-107中任一项的融合rna;和(ii)向导核苷酸序列可编程rna结合蛋白,其中融合rna包含与靶mrna互补的序列。实施方式119是用于增加靶mrna翻译的系统,该系统包括:(i)实施方式98-107中任一项的融合rna;和(ii)向导核苷酸序列可编程rna结合蛋白,其中融合rna包含与靶mrna互补的序列。实施方式120是实施方式118或119的系统,还包含含pam的寡核苷酸。实施方式121是实施方式118或119的系统,其中靶mrna不包含pam序列或其互补序列。实施方式122是实施方式118-121中任一项的系统,其中所述向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,及其各自的生物学等同物。实施方式123是实施方式118-122中任一项的系统,其中所述向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新弗朗西斯菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式124是实施方式118-123中任一项的系统,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式125是一种用于转录后增加基因表达的方法,该方法包括使靶mrna与根据实施方式98-107中任一项的融合rna和向导核苷酸序列可编程rna结合蛋白接触。实施方式126是一种用于转录后降低基因表达的方法,该方法包括使靶mrna与根据实施方式98-107中任一项的融合rna和向导核苷酸序列可编程rna结合蛋白接触。实施方式127是实施方式125或126的方法,还包括使所述向导核苷酸序列可编程rna结合蛋白与含pam的寡核苷酸接触。实施方式128是实施方式125或126的方法,其中靶mrna不包含pam序列。实施方式129是实施方式125-128中任一项的方法,其中所述向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,及其各自的生物学等同物。实施方式130是实施方式125-129中任一项的方法,其中所述向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新弗朗西斯菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式131是实施方式125-130中任一项的方法,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式132是实施方式125-131中任一项的方法,其中靶mrna在细胞中。实施方式133是实施方式132的方法,其中该细胞是真核细胞。实施方式134是实施方式132的方法,其中该细胞是原核细胞。实施方式135是实施方式133的方法,其中所述真核细胞是哺乳动物细胞,任选地是牛,鼠,猫,马,猪,犬,猿或人细胞。实施方式136是实施方式125-135中任一项的方法,其中所述细胞在对象中。实施方式137是一种用于在有此需要的对象中治疗疾病或病症的方法,该方法包括向该对象给予:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)实施方式98-107中任一项的融合rna,实施方式108的多核苷酸,实施方式109-112中任一项的载体或实施方式113的病毒颗粒,其中所述融合rna与所述对象的靶mrna互补,从而增加对象中靶mrna翻译。实施方式138是实施方式137的方法,其中所述对象是人。实施方式139是实施方式137或138的方法,还包括向对象给予以下一种或多种:(i)tracrrna和(ii)含pam的寡核苷酸。实施方式140是试剂盒,其包含以下一个或多个:实施方式98-107中任一项的融合rna,实施方式108的多核苷酸,实施方式109-112中任一项的载体,或实施方式113的病毒颗粒,以及任选的使用说明书。实施方式141是实施方式140的试剂盒,还包含选自以下的一种或多种核酸:(i)含pam的寡核苷酸;(ii)tracrrna;和(iii)用于表达(i)或(ii)的核酸的载体。实施方式142是实施方式140或141的试剂盒,还包含向导核苷酸序列可编程rna结合蛋白。实施方式143是一种融合蛋白,其包含:(i)向导核苷酸序列可编程rna结合蛋白;和(ii)泛素相关蛋白2样(ubap2l)蛋白。实施方式144是实施方式143的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:cas9,修饰的cas9,cas13a,cas13b,casrx/cas13d,及其各自的生物学等同物。实施方式145是实施方式144的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白选自:化脓性链球菌(steptococcuspyogenes)cas9(spcas9),金黄色葡萄球菌(staphylococcusaureus)cas9(sacas9),新弗朗西斯菌(francisellanovicida)cas9(fncas9),脑膜炎奈瑟氏球菌(neisseriameningitidis)cas9(nmcas9),嗜热链球菌(streptococcusthermophilus)1cas9(st1cas9),嗜热链球菌(streptococcusthermophilus)3cas9(st3cas9)和侧孢短芽孢杆菌(brevibacilluslaterosporus)cas9(blatcas9)。实施方式146是实施方式144或145的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白是核酸酶失活的。实施方式147是实施方式143-146中任一项的融合蛋白,还包含接头。实施方式148是实施方式147的融合蛋白,其中所述接头是肽接头。实施方式149是实施方式148的融合蛋白,其中所述肽接头包含三肽ggs的一个或多个重复。实施方式150是实施方式147的融合蛋白,其中所述接头是非肽接头。实施方式151是实施方式150的融合蛋白,其中所述非肽接头包括聚乙二醇(peg),聚丙二醇(ppg),共聚(乙二醇/丙二醇),聚氧乙烯(poe),聚氨酯,聚磷腈,多糖,葡聚糖,聚乙烯醇,聚乙烯基吡咯烷酮,聚乙烯基乙醚,聚丙烯酰胺,聚丙烯酸酯,聚氰基丙烯酸酯,脂质聚合物,几丁质,透明质酸,肝素或烷基接头。实施方式152是实施方式147-151中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[ubap2l]-[接头]-[向导核苷酸序列可编程rna结合蛋白]-cooh。实施方式153是实施方式147-151中任一项的融合蛋白,其中所述融合蛋白包含以下结构:nh2-[向导核苷酸序列可编程rna结合蛋白]-[接头]-[ubap2l]-cooh。实施方式154是实施方式143-153中任一项的融合蛋白,其中所述向导核苷酸序列可编程rna结合蛋白与向导rna(grna),crisprna(crrna)或反式激活crrna(tracrrna)结合。实施方式155是实施方式143-154中任一项的融合蛋白,其中所述ubap2l蛋白由具有包含选自以下序列的全部或部分的序列的多核苷酸编码:seqidno:64,seqidno:65,seqidno:66,seqidno:67,及其各自的生物学等同物。实施方式156是实施方式34-46中任一项的融合蛋白,其中所述ubap2l蛋白具有包含选自以下序列的全部或部分的氨基酸序列:seqidno:68,seqidno:69,seqidno:70,seqidno:71,及其各自的生物学等同物。实施方式157是实施方式143-156中任一项的融合蛋白,其中ubap2l的一个或多个激酶磷酸化结构域被突变。实施方式158是实施方式157的融合蛋白,其中突变的ubap2l是组成性活性的。实施例下述实施例为非限制性和说明性的过程,其可以用于在各种情况中实现本公开内容。表3列出了本文所述实施例中使用的示例性多核苷酸和多肽序列。表3实施例1:eif4e融合蛋白此实施例基于eif4e蛋白的5’cap结合生物学,其增强靶mrna的翻译。在该实施例中,eif4e蛋白包含已知由细胞激酶调节的突变氨基酸残基,以使其调节成为组成性调节。使用核酸酶失活的cas9(dcas9)进行实验,将蛋白质效应物融合到c末端。只要选择针对每个crispr-cas系统特异性的适当的mrna靶向间隔区序列,就可以使用该系统靶向任何目标信使rna。一个示例性系统包含与修饰的eif4e(图1)融合的核酸酶失活的cas9(dcas9)蛋白,其可以增强翻译。这些dcas9融合蛋白结合由u6聚合酶iii启动子驱动的单向导rna(sgrna),并且可以共结合由2′omerna和dna碱基交替组成的反义合成寡核苷酸(含pam的寡核苷酸)。这些组分一起形成了结合信使rna的rcas9-rna识别复合物。不受理论的束缚,含pam的寡核苷酸可能在体内和体外都增加了dcas9对rna的结合亲和力,但是可能并非是rna靶向绝对需要的。在没有含pam的寡核苷酸的情况下进行了初步实验。预期机理的示意图如图1所示。不受理论的束缚,dcas9-eif4e靶向代表性靶转录物mrna的3’utr。修饰的eif4e有助于转录物环化以及eif4g和核糖体起始前复合物的招募。如图3a和图3b所示制备dna构建体。cas9-eif4e的表达水平与效应物质粒上共表达的cfp荧光团相关。yfp和rfp由报告物上的不同启动子共同表达。但是,只有yfp信使rna带有与单向导rna(sgrna)的间隔区互补的靶位点(luc靶位点)。实验结果如图3c所示:(i)热图显示相对于报告物(x轴)和效应物(y轴)dna构建体水平的yfp/rfp比如何倍数变化。用于热图的数据点表示落入定义箱中的单个细胞的平均荧光。(ii)与(i)中提供的数据相同,但yfp/rfp比绘制为第三变量(z轴)。(iii)用于生成热图的数据点的残差。实施例2:eif4e-bp1融合蛋白该技术基于eif4e-bp1的5’帽结合生物学,其抑制翻译。为了使该蛋白质适应本文所述的特定应用,使已知受细胞激酶调节的氨基酸残基突变,以使其调节成为组成性调节。使用核酸酶失活的cas9(dcas9)进行实验,将蛋白质效应物融合到c末端。只要选择针对每个crispr-cas系统特异性的适当的grna间隔区序列,就可以靶向任何目标靶信使rna。一个示例性系统包含与修饰的eif4e-bp1(图2)融合的核酸酶失活的cas9(dcas9)蛋白,其可以分别增强或抑制翻译。这些dcas9融合蛋白结合由u6聚合酶iii启动子驱动的单向导rna(sgrna),并且可以共结合由2′omerna和dna碱基交替组成的反义合成寡核苷酸(含pam的寡核苷酸)。这些组分一起形成了结合信使rna的rcas9-rna识别复合物。图2描述了该系统的预期机制。不受理论的束缚,dcas9与修饰的eif4e-bp1融合。示意图显示dcas9-eif4e-bp1靶向代表性靶转录物的3′utr。修饰的eif4e-bp1有助于转录物mrna环化,并防止eif4e-bp1从eif4e脱离。组成性结合阻止eif4g和核糖体起始前复合物的招募。如图4a和4b所示,制备用于表征研究的效应物和报告物构建体的dna构建体。cas9-eif4e-bp1的表达水平与效应物上共表达的cfp荧光团相关。yfp和rfp由报告物上的不同启动子共同表达。但是,只有yfp信使rna带有与单向导rna(sgrna)的间隔子互补的靶位点(luc靶位点)。这些实验的结果如图4c所示:(i)热图显示相对于报告物(x轴)和效应物(y轴)dna构建体水平的yfp/rfp比如何倍数变化。用于热图的数据点表示落入定义箱中的单个细胞的平均荧光。(ii)与(i)中提供的数据相同,但yfp/rfp比绘制为第三变量(z轴)。(iii)用于生成热图的数据点的残差。实施例3:ubap2l融合蛋白该实施例基于一个筛选,该筛选提示泛素相关蛋白2-样(ubap2l)作为增强翻译的先前未知的rna结合蛋白(rbp)。用带有融合到c末端的ubap2l的rna靶向cas9(rcas9)进行实验。只要选择针对每个crispr-cas系统特异性的适当的mrna靶向间隔区序列,就可以使用该系统靶向任何目标信使rna。一个示例性系统包含与ubap2l融合的rna靶向cas9(rcas9),其可以增强翻译(图8)。通过伴rcas9-ubap2l或rcas9表达盒的质粒构建体的转座酶介导的搭载式(piggyback)基因组整合驱动仅表达cas9-ubap2l融合或cas9的hek293t细胞系。然后转染第二构建体,其中包含稳定地表达不受cas9调控的rfp转录物的报告物,向导rna和具有该向导rna靶序列的四环素诱导型yfp转录物。设计了七个不同的向导rna,它们靶向yfp转录物中的不同位置,并设计了非靶向向导rna。使用分析流式细胞术以标准化yfp/rfp荧光比率的变化测量转录后调节。由于背负式介导的整合在构建体整合位点和数量方面具有随机性,因此在数以千计的数据点(细胞)中对各种rcas9构建体水平(cfp)和报告物构建体水平(rfp)的调节进行了定量。观察到ubap2l对yfp报告物表达的影响程度取决于直接靶向编码区域内位点的ubap2l(图9)。实施例4:融合rna该实施例涉及能够增强细胞中特定信使rna翻译的融合rna平台。该技术取决于crispr-cas系统通过单链向导结合靶信使rna的能力,核糖核酸序列与单链向导融合,从而将翻译起始前复合物募集到结合的信使rna。因此,该技术可以启动反式翻译。这项技术建立在crispr-cas系统的rna靶向能力之上,该系统使用单链向导rna提供一个简单且快速可编程系统来调控细胞中的信使rna分子。crispr-cas系统还对信使rna的稳定性产生中性影响,这使得基因表达的任何测量变化是融合到向导rna的核酸效应物的变量。由于其高度可编码的性质以及对多种crispr/cas系统的适应性,与其他方法相比,示例性融合rna平台具有很高的实用性和多功能性。设计融合rna,其包含基于i型或ii型病毒内部核糖体进入序列(ires)融合到核糖核酸序列的单链rna向导(sgrna)或单链crisprrna(crrna)。这些修饰的sgrna和crrna分别被核酸酶失活的cas9(dcas9)蛋白和核酸酶失活的cas13b(dcas13b)结合。信使rna靶标特异性是由合适的间隔区序列赋予的,该序列存在于sgrna和crrna的5′端。当融合rna在细胞中表达时,它与靶信使rna特异性结合。融合的核糖核酸序列效应物然后将起始前复合物募集到结合的信使rna上以促进蛋白质翻译,如图5所示。使用源自ii型脑心肌炎病毒(emcv-ires)的核糖核酸序列进行示例性表征。但是,该技术不限于特定类型的ires,并且可以包含任何具有ires的功能能力和/或结构性质的核糖核酸序列。对于基于dcas9的融合rna系统,还可以提供包含2′omerna和dna碱基交替的反义合成寡核苷酸(含pam的寡核苷酸)。但是,为了简化递送策略,在没有含pam的寡核苷酸的情况下进行了涉及dcas9的初步实验。不受理论的束缚,认为含pam的寡核苷酸可能在体内和体外都增加了dcas9对rna的结合亲和力,但是已发现这并非是rna靶向绝对需要的。在没有含pam的寡核苷酸的情况下进行了初步实验。基于dcas13b的系统不要求含pam的寡核苷酸。用融合到pv-ires,fmdv-ires或emcc-ires的sgrna或crrna制备融合rna系统。在该实施例中,除了包括核输出序列以外,没有对dcas9或dcas13b进行任何具体的修饰。为了对融合rna的调控进行定量,开发了基于黄色荧光蛋白(yfp)和红色荧光蛋白(rfp)表达的双重荧光测定法(图6a和图6b)。设计间隔区序列以将融合rna靶向yfpmrna并调节yfp表达(图6c)。相反,rfpmrna保持未结合状态,因此允许rfp荧光和蛋白质水平用作转染对照。ha标签附加到yfp的c末端,其可用于分析不同yfp翻译阅读框的调控,这是在其他(alternative)起始密码子处引发的结果。可以通过western印迹来区分不同的yfp同种型。总体转录后调控的变化也可以表示为yfp与rfp荧光比率的变化。如图7a-7b所示,使用emcv-ires的dcas9和dcas13b融合rna的调控成功介导了蛋白质翻译的增强(图7a和图7b)。参考文献本文和整个公开中公开的所有参考文献均通过引用全文并入。1.cooke等,2011.“使用puf蛋白家族支架进行靶向翻译调控(targetedtranslationalregulationusingthepufproteinfamilyscaffold)”pnas108(38):15870-15875.2.cao等,2015.“调节原核和真核细胞mrna翻译的通用策略(auniversalstrategyforregulatingmrnatranslationinprokaryoticandeukaryoticcells)”nars43(8):4353-4362.3.wo/2015/0892774.wo/2016/183402当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1