一种蛋氨酸亚砜还原酶及其编码基因、制备方法和用途与流程
本发明涉及基因工程技术领域,具体涉及一种蛋氨酸亚砜还原酶、蛋氨酸亚砜还原酶基因、重组表达载体、重组细胞系或重组菌株及其用途,以及蛋氨酸亚砜还原酶基因的cdna序列的制备方法、蛋氨酸亚砜还原酶的制备方法、蛋氨酸亚砜还原酶的检测引物和检测探针、芯片或试剂盒。
背景技术:
生物体内氧气在正常代谢时经过不完全还原可生成活性氧化合物(ros,reactiveoxygenspecies),主要包括超氧阴离子自由基、过氧化氢、过氧亚硝基阴离子、次氯酸、单线态氧和羟基自由基等。ros可以与一系列生物分子作用,引起氧化损伤或者影响许多信号转导过程,调控细胞增殖、分化和凋亡,同时,ros也与一系列的疾病,如心脑血管疾病、癌症、阿尔兹海默症以及渐冻症(als)等疾病的发生、发展和治疗密切相关。
细胞受胁迫后形成ros的主要目标是两种含硫氨基酸半胱氨酸(cys)和蛋氨酸(met),cys和met对活性氧非常敏感,其硫原子极易被氧化。met被氧化导致蛋白质中蛋氨酸亚砜(meto)的形成,met作为蛋白质合成中通用的起始氨基酸,meto的产生可能导致蛋白结构改变和催化功能异常,影响细胞的正常功能。为了抵消ros的破坏,生物体进化出了多种ros清除和修复机制,包括低分子量化合物和抗氧化应激的抗氧化酶。蛋氨酸亚砜还原酶(msrs)是目前唯一确定的蛋白质蛋氨酸亚砜残基特征性还原酶,能够将蛋氨酸亚砜(meto)还原为蛋氨酸(met),起到调节蛋白质的功能、调控相关信号通路、修复氧化损伤蛋白、防止氧化应激等作用。目前,已有研究表明msrs在机体的衰老、神经退行性疾病、白内障等相关生理和病理过程中发挥保护作用。
蛋氨酸亚砜还原酶(msrs)广泛存在于大多数原核和真核生物中如细菌和人类等,生物体内已经发现的也是研究最多的msrs主要有蛋氨酸亚砜还原酶a(msra)和蛋氨酸亚砜还原酶b(msrb)两种。msra能够特异性地还原蛋白质和游离的蛋氨酸-s-亚砜,而msrb只能还原蛋白质中的蛋氨酸-r-亚砜。msra的保守催化位点中含有硒代半胱氨酸残基(sec或u)的为硒蛋白msra,与保守位点为半胱氨酸(cys)的不含硒msra相比,硒蛋白msra的催化活性有10-50倍幅度提升,表明硒代半胱氨酸残基(sec或u)改善了氧化还原的催化活性。目前,在细菌、藻类和无脊椎动物中均发现了msra的含硒形式。
获得具有高催化活性的硒蛋白msra,对于抗氧化剂、msrs相关药物的疗法的开发、利用具有重要意义。由于硒蛋白msra在动植物中的含量极低,从动植物中大量提取msra不仅成本高,且破坏生态资源。因此,如何获得大量表达的硒蛋白msra是现阶段亟待解决的重要问题。
技术实现要素:
因此,本发明要解决的技术问题在于克服现有技术中的硒蛋白msra的提取成本高、无法实现其大量生产、表达的缺陷,从而提供一种能够用于基因工程表达的蛋氨酸亚砜还原酶。
为此,本发明提供如下技术方案:
第一方面,本发明提供了一种蛋氨酸亚砜还原酶,所述蛋氨酸亚砜还原酶选自如下(a1)-(a3)中的任一种:
(a1)其氨基酸序列如seqidno.1所示;
(a2)为与seqidno.1所示的氨基酸序列具有至少85%同源性的氨基酸序列;
(a3)具有(a)或(b)所示的氨基酸序列的不丧失生物活性的同系物、衍生物、片段或突变体。
第二方面,本发明提供了一种蛋氨酸亚砜还原酶基因,所述蛋氨酸亚砜还原酶基因编码如权利要求1所述的蛋氨酸亚砜还原酶。
可选地,上述的蛋氨酸亚砜还原酶基因,所述蛋氨酸亚砜还原酶基因选自如下(b1)-(b2)所示的任一种:
(b1)其cdna序列如seqidno.2所示;
(b2)为与seqidno.2所示的核苷酸序列具有至少85%同源性的核苷酸序列。
第三方面,本发明提供了包含上述的蛋氨酸亚砜还原酶基因的重组表达载体、重组细胞系或重组菌株。
第四方面,本发明提供了一种药物,所述药物包含上述的蛋氨酸亚砜还原酶,或上述的蛋氨酸亚砜还原酶基因。
第五方面,本发明提供了上述的蛋氨酸亚砜还原酶、蛋氨酸亚砜还原酶基因,或者蛋氨酸亚砜还原酶基因的重组表达载体、重组细胞系或重组菌株在如下(c1)-(c3)中至少一种的用途:
(c1)还原蛋氨酸亚砜,或制备用于还原蛋氨酸亚砜的产品;
(c2)作为抗氧化剂,或制备用于抗氧化的产品;
(c3)制备治疗msrs相关疾病的药物。
第六方面,本发明提供了上述的蛋氨酸亚砜还原酶的制备方法,包括:
s1,构建表达如权利要求1所述蛋氨酸亚砜还原酶的重组表达载体;
s2,以所述重组表达载体转化目标菌株,获得重组菌株;
s3,对所述重组菌株进行发酵培养,诱导蛋白表达;
s4,分离纯化所述重组菌株表达的蛋白,获得蛋氨酸亚砜还原酶。
第七方面,本发明提供了一种制备上述的蛋氨酸亚砜还原酶基因的cdna序列的方法,其特征在于,包括如下步骤:
(1)提取雨生红球藻的总rna并逆转录为cdna;
(2)以雨生红球藻的cdna为模板进行扩增,获得蛋氨酸亚砜还原酶基因的cdna片段;
(3)对所述蛋氨酸亚砜还原酶基因的cdna片段进行5’-race扩增和3’-race扩增,获得5’-race扩增片段和3’-race扩增片段;
(4)将所述5’-race扩增片段和所述3’-race扩增片段测序后,进行序列拼接,获得所述蛋氨酸亚砜还原酶基因的cdna序列;
优选地,所述蛋氨酸亚砜还原酶基因的cdna片段的扩增引物包括:hpmsra-f,其核苷酸序列如seqidno.3所示;hpmsra-r,其核苷酸序列如seqidno.4所示;
优选地,所述5’-race扩增片段的扩增引物包括:gsp5-1,其核苷酸序列如seqidno.5所示;gsp5-2,其核苷酸序列如seqidno.6所示;gsp5-3,其核苷酸序列如seqidno.7所示;
优选的,所述3’-race扩增片段的扩增引物包括:gsp3-1,其核苷酸序列如seqidno.8所示;gsp3-2,其核苷酸序列如seqidno.9所示;gsp3-3,其核苷酸序列如seqidno.10所示。
第八方面,本发明提供了一种蛋氨酸亚砜还原酶的检测引物,所述检测引物基于权利要求2或3所述的蛋氨酸亚砜还原酶基因设计;
优选的,所述检测引物包括:hpmsra-qf,其核苷酸序列如seqidno.11所示;hpmsra-qr,其核苷酸序列如seqidno.12所示。
第九方面,本发明提供了一种用于检测上述的蛋氨酸亚砜还原酶,或蛋氨酸亚砜还原酶基因的探针、芯片或试剂盒。
本发明技术方案,具有如下优点:
1.本发明提供的蛋氨酸亚砜还原酶,选自如下(a1)-(a3)中的任一种:(a1)其氨基酸序列如seqidno.1所示;(a2)为与seqidno.1所示的氨基酸序列具有至少85%同源性的氨基酸序列;(a3)具有(a)或(b)所示的氨基酸序列的不丧失生物活性的同系物、衍生物、片段或突变体。
具有seqidno.1所示氨基酸序列的蛋氨酸亚砜还原酶来源自雨生红球藻,雨生红球藻是一种单细胞淡水微藻,是一种具有极强抗逆能力的单细胞生物。雨生红球藻在受到高温、高光照等环境条件的胁迫下雨生红球藻的细胞内积累高含量的虾青素,虾青素作为一种“超级抗氧化剂”在增强机体健康、抗衰老等方面具有重要意义。本发明首次提供了雨生红球藻的蛋氨酸亚砜还原酶的序列,并研究发现在蛋氨酸亚砜还原酶的氨基酸序列中具有高度保守的gufw的催化中心,其中具有能够明显改善氧化还原催化活性的硒代半胱氨酸残基(u),说明具有seqidno.1所示氨基酸序列的蛋氨酸亚砜还原酶是一种具有高催化活性的硒蛋白msra。本发明通过提供来源雨生红球藻的蛋氨酸亚砜还原酶的氨基酸序列,为这种硒蛋白msra的基因工程表达奠定基础,有利于实现具有高催化活性的蛋氨酸亚砜还原酶的大规模工业生产,降低了蛋氨酸亚砜还原酶的获得成本,进而为高效抗氧化剂、神经退行型疾病、白内障等msrs相关疾病的治疗药物的研发和利用提供条件。
2.本发明提供的蛋氨酸亚砜还原酶基因,编码上述的蛋氨酸亚砜还原酶,蛋氨酸亚砜还原酶基因选自如下(b1)-(b2)所示的任一种:(b1)其cdna序列如seqidno.2所示;(b2)为与seqidno.2所示的核苷酸序列具有至少85%同源性的核苷酸序列。利用上述核苷酸序列,有利于构建蛋氨酸亚砜还原酶的体外表达载体,筛选高效表达蛋氨酸亚砜还原酶的重组菌株,从而实现蛋氨酸亚砜还原酶的体外高效表达,降低蛋氨酸亚砜还原酶的生产成本。
3.本发明提供的包含蛋氨酸亚砜还原酶基因的重组表达载体,适于筛选稳定高表达蛋氨酸亚砜还原酶的重组细胞系或重组菌株,通过重组菌株的发酵培养,能够实现蛋氨酸亚砜还原酶的大规模体外表达、生产。
4.本发明提供的蛋氨酸亚砜还原酶通过还原蛋氨酸亚砜,修复氧化损伤蛋白,能够实现抗氧化的作用。因此,蛋氨酸亚砜还原酶可以作为抗氧化剂或制备用于抗氧化的产品。此外,研究表明msrs蛋白在神经退行性疾病等相关疾病的发生发展过程中发挥作用,本发明提供的蛋氨酸亚砜还原酶为msrs相关疾病的治疗药物的开发提供条件。
5.本发明提供的蛋氨酸亚砜还原酶的制备方法,采用基因工程方法,实现了蛋氨酸亚砜还原酶的体外表达,降低了蛋氨酸亚砜还原酶的生产成本,有利于实现蛋氨酸亚砜还原酶大规模的工业化量产。
6.本发明提供的蛋氨酸亚砜还原酶的检测引物、探针、芯片或试剂盒,能够用于检测蛋氨酸亚砜还原酶的表达水平,本发明通过研究发现,受环境胁迫因素(草甘膦、重金属镉、硒等)影响,雨生红球藻中蛋氨酸亚砜还原酶的表达量发生明显变化,因此,通过检测水体中雨生红球藻内蛋氨酸亚砜还原酶的表达情况,能够实现对环境不利因素的监测控制,有利于对环境中不利因素的管理控制。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
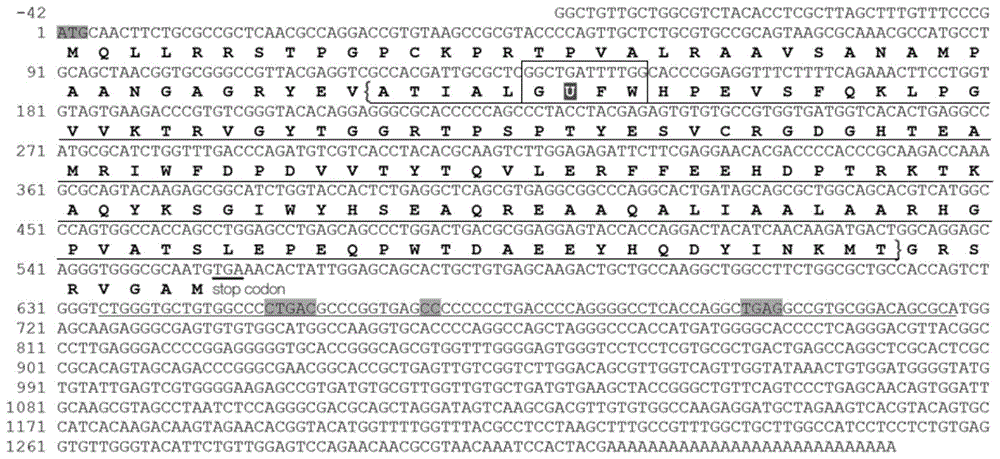
图1是本发明实施例1提供的雨生红球藻蛋氨酸亚砜还原酶基因的cdna序列及其对应的氨基酸序列图;
图2是本发明实施例1提供的雨生红球藻蛋氨酸亚砜还原酶基因的secis元件结构图;
图3是本发明实施例1提供的雨生红球藻的msra序列与多物种的蛋氨酸亚砜还原酶的序列比对结果;
图4是本发明实验例1提供的雨生红球藻的蛋氨酸亚砜还原酶基因在不同环境胁迫因素的影响下表达变化情况;
图5是本发明实验例2提供的雨生红球藻的蛋氨酸亚砜还原酶基因在不同浓度的亚硒酸盐中影响下表达变化情况及酶活性变化情况。
具体实施方式
下面将对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。此外,下面所描述的本发明不同实施方式中所涉及的技术特征只要彼此之间未构成冲突就可以相互结合。
下述实施例中使用的实验试剂均为常规实验试剂,可由市场直接获得;
实施例1
本实施例提供一种雨生红球藻蛋氨酸亚砜还原酶基因的克隆方法,具体包括以下步骤:
(1)提取雨生红球藻的总rna,利用
(2)以雨生红球藻的cdna为模板,使用扩增引物hpmsra-f和hpmsra-r进行扩增,获得雨生红球藻中蛋氨酸亚砜还原酶基因的cdna扩增片段。其中,hpmsra-f的核苷酸序列如seqidno.3所示,hpmsra-r的核苷酸序列如seqidno.4所示。pcr扩增条件为:95℃2min;(95℃30s,58℃45s,72℃1min,35个循环);72℃10min。
(3)对步骤(2)中的cdna片段进行5’-race扩增和3’-race扩增,其中,5’-race扩增使用的引物包括:gsp5-1,其核苷酸序列如seqidno.5所示;gsp5-2,其核苷酸序列如seqidno.6所示;gsp5-3,其核苷酸序列如seqidno.7所示;3’-race扩增使用的引物包括:gsp3-1,其核苷酸序列如seqidno.8所示;gsp3-2,其核苷酸序列如seqidno.9所示;gsp3-3,其核苷酸序列如seqidno.10所示。经5’-race扩增和3’-race扩增,获得5’-race扩增片段和3’-race扩增片段。pcr扩增条件为:94℃30s,68℃30s,72℃3min,25个循环。
(4)将步骤(3)中的5’-race扩增片段和3’-race扩增片段测序后,进行序列拼接,得到蛋氨酸亚砜还原酶基因的cdna序列,其cdna序列如seqidno.2所示,对应的蛋氨酸亚砜还原酶的氨基酸序列如seqidno.1所示。
图1显示雨生红球藻蛋氨酸亚砜还原酶基因的cdna序列及其对应的氨基酸序列,图中密码子u表示硒代半胱氨酸的编码位点,由氨基酸序列可以发现在蛋氨酸亚砜还原酶中具有保守的gufw的催化中心。氨基酸序列中下划线标注的开放阅读框区域对应为多肽蛋氨酸亚砜还原酶家族(peptidemethioninesulfoxidereductase,psmr),cdna序列中下划线标注的为硒半胱氨酸插入序列(selenocysteineinsertionsequence,secis)。图2显示secis元件的二级结构,由图中可看出蛋氨酸亚砜还原酶基因的secis元件具有标志性的顶环和ag/ga四重奏等保守结构,在secis元件的存在下,蛋氨酸亚砜还原酶基因的mrna中的uga能够用作硒半胱氨酸的密码子,编码得到硒代半胱氨酸,使雨生红球藻的蛋氨酸亚砜还原酶作为一种具有高催化活性的硒蛋白msra。雨生红球藻的msra与团藻同源基因蛋白质序列的一致性达到65.5%,具有显著的硒蛋白基因结构。
图3显示雨生红球藻的msra序列与下述物种的蛋氨酸亚砜还原酶的序列比对结果:b.floridae,n.vectensis_b,t.adhaerens,d.vulgaris,h.pluvialis,m.commoda,d.rerio,h.sapiens,e.coli,s.cerevisiae,a.thaliana。深色阴影表示完全一致序列,浅色阴影表示保守替代序列,高度保守gufw基序是msra基因的催化中心,其中具有硒代半胱氨酸u。
本实施例中首次获得了雨生红球藻的蛋氨酸亚砜还原酶基因的全长cdna序列,并提供了雨生红球藻的蛋氨酸亚砜还原酶的序列。通过序列分析发现在蛋氨酸亚砜还原酶的氨基酸序列中具有高度保守的gufw的催化中心,其中具有能够明显改善氧化还原催化活性的硒代半胱氨酸残基(u),说明具有seqidno.1所示氨基酸序列的蛋氨酸亚砜还原酶是一种具有高催化活性的硒蛋白msra。本发明通过提供来源雨生红球藻的蛋氨酸亚砜还原酶的氨基酸序列,为这种硒蛋白msra的基因工程表达奠定基础,有利于实现具有高催化活性的蛋氨酸亚砜还原酶的大规模工业生产,降低了蛋氨酸亚砜还原酶的获得成本,进而为高效抗氧化剂、神经退行型疾病、白内障等msrs相关疾病的治疗药物的研发和利用提供条件。
实施例2
本实施例提供一种蛋氨酸亚砜还原酶的制备方法,具体包括如下步骤:
s1,构建表达如seqidno.1所示氨基酸序列的蛋氨酸亚砜还原酶的重组表达载体,具体为:
在蛋氨酸亚砜还原酶基因的cdna片段的两端引入xbai和xhoi的酶切位点,以pet-28a(购自solarbio)为载体,利用xbai和xhoi的限制性内切酶分别对pet-28a和msra的基因片段进行酶切,将酶切后的片段进行胶回收,得到5’xbai-pet-28a-3’xhoi的线性质粒片段和5’xbai-msra-3’xhoi的基因片段。
在10μl的t4连接酶体系中加入酶切回收的5’xbai-pet-28a-3’xhoi和5’xbai-msra-3’xhoi,16℃过夜连接。以连接产物转化dh5a感受态细胞,涂平板后进行筛选,通过菌液pcr筛选阳性克隆,获得msra的重组表达载体,将其命名为pet-28a-msra。
s2,以所述重组表达载体转化目标菌株,获得重组菌株;具体为:以重组表达载体pet-28a-msra转化bl21感受态细胞,筛选重组转化子,获得含有msra基因的重组菌株。
s3,对所述重组菌株进行发酵培养,诱导蛋白表达;具体为:将转化后的bl21感受态细胞接种到lb培养基中,37℃条件下进行振荡,对重组菌株进行发酵培养,以iptg诱导重组菌株表达蛋白,确定蛋白表达量高的适宜iptg添加量及蛋白诱导条件。
s4,分离纯化所述重组菌株表达的蛋白,获得蛋氨酸亚砜还原酶。具体为:将步骤s3中诱导蛋白表达后的重组菌株进行破碎,分离菌株中表达的蛋白,通过柱层析的亲和层析方法对重组菌株中表达的蛋氨酸亚砜还原酶进行纯化,获得目标蛋白。
实施例3
本实施例提供一种包含蛋氨酸亚砜还原酶基因的重组表达载体和重组菌株,其中,蛋氨酸亚砜还原酶基因具体为具有seqidno.2所示的核苷酸序列的cdna片段。
具体地,重组表达载体是实施例2中构建的以pet-28a为载体,以xbai和xhoi为克隆位点构建的重组表达载体pet-28a-msra;重组菌株是将重组表达载体pet-28a-msra转化至bl21感受态细胞获得的重组转化子。
本实施例提供的重组表达载体pet-28a-msra和重组菌株能够用于蛋氨酸亚砜还原酶的体外诱导表达,以降低蛋氨酸亚砜还原酶的生产成本,实现大规模的工业化量产。
实施例4
本实施例提供一种抗氧化剂,包含实施例2中纯化的蛋氨酸亚砜还原酶。实施例2中蛋氨酸亚砜还原酶具有seqidno.1所示的氨基酸序列,是一种以gufw为活性中心的硒蛋白msra,硒蛋白msra催化蛋氨酸亚砜还原的活性强、具有高的抗氧化性,能够作为一种高效的抗氧化剂。
实验例1
1、实验目的:检测监测环境胁迫因素雨生红球藻内蛋氨酸亚砜还原酶基因表达水平的影响。
2、实验方法:
1)以h2o2,强光,亚硝酸镉和草甘膦基除草剂作为代表对红球藻细胞处理,对于每个因子设计三种浓度的处理,包括:过氧化氢h2o2(20、40、80mg/l),高光(80、150、350mol光子m-2s-1),草甘膦(2、4、8mg/l)和亚硝酸镉(3、6、12mg/l)设计用于处理组。每种处理重复三次,采样并记录暴露处理后3、6和12小时的表达水平。
2)根据雨生红球藻msra基因序列设计qrt-pcr引物,得到如下检测引物:hpmsra-qf,其核苷酸序列如seqidno.11所示;hpmsra-qr,其核苷酸序列如seqidno.12所示。利用上述的检测引物,以荧光定量pcr对处于指数生长期的雨生红球藻细胞(密度约为每毫升3×105个细胞)处理组与对照组的样品进行分析,荧光定量pcr的内参蛋白为actin,检测actin蛋白表达量的引物为actin-qf:5’-agcgggagatagtgcgggaca-3’,actin-qr:5’-atgcccaccgcctcaatgc-3’。qrt-pcr扩增条件为:95℃30s;95℃10s,60℃30s,40个循环。
3、实验结果
实验结果如图4所示,具体如下:
图4a显示在h2o2暴露不同时间后msra表达水平的检测结果,由图图4a可知,h2o2暴露3小时,所有处理组与对照组均无显著改变,并且随着处理时间的延长,与相应对照组相比,所有40和80mg/l处理组均达到显著水平,而在处理12小时后,hpmsra表达提升到最高水平(分别为对照组的1.8倍和3.4倍,p<0.01),而20mg/lh2o2组与对照组一致。
图4b显示在不同光照强度下msra表达水平随时间变化的检测结果,藻类细胞对增加的光强度敏感,因为与对照(20mol光子m-2s-1光强度)相比,高光处理可能会诱导细胞内ros积累,3小时到6小时范围,从80到350mol光子m-2s-1光强度条件下,hpmsra转录本水平显著上调。到12h时恢复正常,所有高光组保持相同的水平。
图4c显示在不同浓度草甘膦曝露后msra表达水平随时间变化的检测结果,草甘膦作为广谱内吸性除草剂可能会干扰芳香族氨基酸的合成。hpmsra表达随时间变化呈现上升模式而不受剂量变化影响,处理后3小时转录本比对照略有增加,但无显著差异,草甘膦从6小时到12小时继续促进msra表达。8mg/l草甘膦处理后hpmsra表达量在12小时达到峰值,是对照的9倍以上。
图4d显示在不同浓度cd2+曝露后msra表达水平随时间变化的检测结果,镉(cd)作为一种污染水生环境的有害金属,对hpmsra表达量的效应呈剂量依赖性。在每个处理组中,转录本在不同时间段稳定表达。对照组和3mg/l硝酸镉处理组之间无显著差异,6小时和12小时的转录水平是对照组的两倍。6mg/l硝酸镉处理可迅速增加转录本表达,并在6h达到最高水平,但是12mg/l组始终低于6mg/l组。
实验例2
1、实验目的:检测硒处理条件下雨生红球藻内蛋氨酸亚砜还原酶基因表达水平的变化,及酶活性变化。
2、实验方法
1)将雨生红球藻暴露于不同浓度的在亚硒酸盐(0,3,13,23mg/ml)中,在亚硒酸盐暴露3、6和12小时后,以荧光定量pcr检测雨生红球藻内msra基因的mrna转录水平。
2)应用特定的比色法监测亚硒酸钠处理后msra的活性,在msra反应系统中,二硫醇化合物的氧化与甲基亚砜还原为甲基硫醚的反应同时发生,因此可以通过二硫醇底物减少量来监测msra的催化活性。该反应基于ellman的试剂(二硫代双硝基苯甲酸,dtnb)与二硫苏糖醇(dtt)反应并产生颜色,从而能通过分光光度法在od412波长进行检测(wu等,2013)。以相同的时间间隔研究酶活性。
3、实验结果
检测结果如图5所示:
图5a显示暴露于不同浓度的亚硒酸盐中的雨生红球藻蛋氨酸亚砜还原酶基因表达随时间变化结果。检测结果表明红球藻细胞对亚硒酸盐具有很高的敏感性,hpmsramrna表达显著高于对照(10-40倍)。每个处理组中的表达水平均随时间而提高,在使用13mg/l亚硒酸盐处理12小时后达到峰值。结果表明在对照组中没有观察到显著性差异。
图5a显示暴露于不同浓度的亚硒酸盐中的雨生红球藻蛋氨酸亚砜还原酶活性随时间变化结果。在亚硒酸盐存在下,酶活性显著增加,相比对照组有1.8倍以上增加。此外,值得注意的是,在暴露6小时后,hpmsra酶活水平在23mg/l组中大约升高了7倍,随后在12小时后下降。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
sequencelisting
<110>深圳大学
<120>一种蛋氨酸亚砜还原酶及其编码基因、制备方法和用途
<130>zha202000043
<160>12
<170>patentinversion3.3
<210>1
<211>185
<212>prt
<213>雨生红球藻(msra1)
<400>1
metglnleuleuargargserthrproglyprocyslysproargthr
151015
provalalaleuargalaalavalseralaasnalametproalaala
202530
asnglyalaglyargtyrgluvalalathrilealaleuglysecphe
354045
trphisprogluvalserpheglnlysleuproglyvalvallysthr
505560
argvalglytyrthrglyglyargthrproserprothrtyrgluser
65707580
valcysargglyaspglyhisthrglualametargiletrppheasp
859095
proaspvalvalthrtyrthrglnvalleugluargphephegluglu
100105110
hisaspprothrarglysthrlysalaglntyrlysserglyiletrp
115120125
tyrhisserglualaglnargglualaalaglnalaleuilealaala
130135140
leualaalaarghisglyprovalalathrserleugluproglugln
145150155160
protrpthraspalagluglutyrhisglnasptyrileasnlysmet
165170175
thrglyargserargvalglyalamet
180185
<210>2
<211>558
<212>dna
<213>雨生红球藻(msra1_orf)
<400>2
atgcaacttctgcgccgctcaacgccaggaccgtgtaagccgcgtaccccagttgctctg60
cgtgccgcagtaagcgcaaacgccatgcctgcagctaacggtgcgggccgttacgaggtc120
gccacgattgcgctcggctgattttggcacccggaggtttcttttcagaaacttcctggt180
gtagtgaagacccgtgtcgggtacacaggagggcgcacccccagccctacctacgagagt240
gtgtgccgtggtgatggtcacactgaggccatgcgcatctggtttgacccagatgtcgtc300
acctacacgcaagtcttggagagattcttcgaggaacacgaccccacccgcaagaccaaa360
gcgcagtacaagagcggcatctggtaccactctgaggctcagcgtgaggcggcccaggca420
ctgatagcagcgctggcagcacgtcatggcccagtggccaccagcctggagcctgagcag480
ccctggactgacgcggaggagtaccaccaggactacatcaacaagatgactggcaggagc540
agggtgggcgcaatgtga558
<210>3
<211>20
<212>dna
<213>人工序列(hpmsra-f)
<400>3
tttacgccaggaccgtgtaa20
<210>4
<211>20
<212>dna
<213>人工序列(hpmsra-r)
<400>4
cttggcagcagtcttgctca20
<210>5
<211>18
<212>dna
<213>人工序列(gsp5-1)
<400>5
cgtcattcgcgtttgcgg18
<210>6
<211>20
<212>dna
<213>人工序列(gsp5-2)
<400>6
cgagttgcggtcctggcaca20
<210>7
<211>19
<212>dna
<213>人工序列(gsp5-3)
<400>7
acgaccgcagatgtggagc19
<210>8
<211>18
<212>dna
<213>人工序列(gsp3-1)
<400>8
ggaagagccgtgatgtgc18
<210>9
<211>18
<212>dna
<213>人工序列(gsp3-2)
<400>9
acagtgccatcacaagac18
<210>10
<211>18
<212>dna
<213>人工序列(gsp3-3)
<400>10
tttgccgtttggctgctt18
<210>11
<211>17
<212>dna
<213>人工序列(hpmsra-qf)
<400>11
gctcggctgattttggc17
<210>12
<211>21
<212>dna
<213>人工序列(hpmsra-qr)
<400>12
tgtaggtgacgacatctgggt21
- 还没有人留言评论。精彩留言会获得点赞!