一种基于RT-PCR及毛细电泳的同步检测19种脑炎脑膜炎病原体的试剂盒及检测方法与流程
本发明涉及病原体核酸检测技术领域,具体涉及一种基于rt-pcr及毛细电泳的同步检测19种脑炎脑膜炎病原体的试剂盒及检测方法。
背景技术:
脑膜炎(meningitis)是指包裹大脑和脊髓的保护薄膜急性炎症,而这些保护薄膜被统称为脑膜。脑膜发炎可由病毒、细菌或其他微生物的感染所引致,而在少数情况下或可由某种药物引发。脑膜炎由于其发炎位置接近大脑和脊髓,因此可以致命;所以此病为内科急诊的一种。
脑膜炎最常见的症状是头痛和颈部僵直,伴随发烧、精神错乱或意识改变、呕吐、畏光(恐光症)或响亮的声音(声音恐惧症)。儿童通常只会出现非特异性的症状,如易怒和精神萎靡。按照病因可分为:细菌性脑膜炎、病毒性脑膜炎、真菌性脑膜炎、寄生性脑膜炎和非感染性脑膜炎。
细菌性脑膜炎是一种发病率低,但是症状非常严重,可能致死的疾病。脑膜炎奈氏菌(neisseriameningitidis)、肺炎链球菌(streptococcuspneumoniae)和流感嗜血杆菌(haemophilusinfluenzae)是引起细菌性脑膜炎的常见的3种病原体。肺炎链球菌主要感染2岁以下的儿童和免疫低下/缺陷的成年人,肺炎球菌性脑膜炎是细菌性脑膜炎中最严重的,患者通常会有神经损伤,例如耳聋,脑损伤。流行性脑脊髓膜炎是由脑膜炎奈氏菌引起的,患者可能会有脑损伤等其他后遗症。嗜血杆菌脑膜炎也是发病率很高的疾病,但是随着b型流感嗜血杆菌疫苗的使用,发病率已经大大降低。其他类型的细菌性脑膜炎的细菌还有李斯特氏菌脑膜炎(listeriamonocytogenesmeningitis)、大肠杆菌脑膜炎(escherichiacolimeningitis)、结核分枝杆菌脑膜炎(mycobacteriumtuberculosismeningitis)。
病毒性脑膜炎(viralmeningitis)通常是由肠道病毒引起的,病毒通过口传入身体中,并传染到脑及周边组织,并在那里繁殖。其他病毒包括水痘带状疱疹病毒、单纯性疱疹病毒、腮腺炎病毒等等。
引起真菌性脑膜炎最常见的病原体是新型隐球菌(cryptococcusneoformans),尽管是可治愈的,但是感染过新型隐球菌的人中接近一半的人可能复发。
脑炎(encephalitis)是指脑实质受病原体侵袭导致的炎症性病变。由于发病原因复杂、诊断难度大,加之起病急、病情凶险,如果治疗不及时,会对身体健康和生命安全造成严重危害,尤其是婴幼儿,影响其生长发育。脑炎的感染病原体繁多,通常由病毒感染造成,也可由细菌、霉菌、螺旋体、立克次氏体、寄生虫等感染引起,有的可能是变态反应性疾病,如急性播散性脑脊髓炎。但是60%的脑炎都是未确诊的,这是个值得探索的领域。最常见的致病菌有脑膜炎奈瑟氏菌、肺炎链球菌、b型流感嗜血杆菌、葡萄球菌、结核分枝杆菌、李斯特氏菌、大肠杆菌等。最常见的病毒感染有肠道病毒、单纯性疱疹病毒、腮腺炎病毒、巨细胞病毒、日本脑炎病毒、柯萨奇病毒和虫媒病毒等。
临床常用的脑炎脑膜炎检测方法,包括脑脊液检查、影像学检查、分子生物学法、二代测序技术等。具体如下:
(1)脑脊液检查
脑脊液(cerebrospinalfluid,csf)可行常规、生化、细菌学和免疫学检查。腰椎穿刺术常用于检查脑脊液的性质,对诊断脑膜炎、脑炎、脑血管病变、肿瘤以及其他全身疾病有重要意义。将脑脊液分别收集于3个无菌试管中,第一管作细菌培养,第二管作化学分析和免疫学检查,第三管作一般性状及显微镜检查。每管收集1~2ml。csf检查是脑炎脑膜炎病原学检查的首要手段。csf动力学检查可以了解脑脊髓腔通畅情况;细胞学检查可了解炎症反应的程度;生化检查可有助于区别细菌性或病毒性感染;免疫抗体及核酸检测有助于病毒性疾病的诊断;考虑到可能是细菌感染,必须做脑脊液的细菌培养和药物敏感试验,明确感染源。细菌培养是金标准,也是目前实验室常规检测手段,革兰氏染色、墨汁染色、抗酸染色等检测手段也用于细菌检测。这些方法都存在灵敏度低的缺陷,同时培养法耗时长。
(2)影像学检查
通过电子仪器进行检波、放大,将脑电记录下来的图形即为脑电图。脑电图是反映大脑细胞电活动的最敏感指标,其异常脑电活动改变及转归与临床病情及预后有较高的一致性。作为众多辅助检查手段的一种,具有敏感度高等特点,对脑炎的诊断具有不可替代的作用。而脑电图也有一定的弊端:有文献报道脑电图异常多于中枢神经系统受累后3~5天出现,发病早期检查可能无明显异常,需要根据病情变化进行复查并与前次检查对比分析。
头颅ct检查可显示炎症导致的脑水肿、脑容积的变化,脑皮质和髓质的密度改变。ct值的变化对于是否伴有出血、反映病变的严重程度,辅助医师对病情作出更准确的判断有重要意义。
磁共振成像(magneticresonanceimaging,mri)在脑炎的诊断比ct更准确,这是因为mri对脑髓质水分含量较敏感,组织分辨率更高,可以显示ct看不到的一些异常,如发病早期较轻的脑水肿、脱髓鞘病变等。mri检查病人免受x线照射,但由于其费用较高,检查时间较长,噪音较大,对于有精神异常的病人,检查时易受噪音的刺激引发精神激越发作。
(3)分子生物学法
pcr技术克服了病原体分离和抗原、抗体免疫学检测的缺点,已成为微生物感染快速诊断的重要手段,国外有学者称其为cns感染病原诊断的金标准,也有学者称其为临床常规实验室的“first-linediagnostictest”。目前常用的方法有pcr、多重pcr、实时pcr及生物芯片等。pcr方法与培养法相比,敏感性和特异性更高,病原诊断所需时间由原来的数天减少为数小时。其高效性、灵敏性、特异性,为临床用药提供更有效的信息,可以抓住治疗时机。
(4)二代测序技术
二代测序技术(nextgenerationsequencing,ngs),可一次性对几百万到十亿条dna分子进行并行测序,是一种较一代测序通量更高、成本更低、用时更短且自动化程度更高的测序技术。ngs有潜力成为神经感染性疾病的诊断工具。对于并非临床常见而没有在多数医院常规开展检测的囊虫、布氏杆菌、螺旋体等病原体,或者培养方法较复杂或非常规开展的李斯特氏菌、奴卡菌等病原体,ngs检测可以规避常规检查的不足。尽管脑脊液ngs检测给神经系统感染的病原学检查带来了很大变革,但目前ngs的检测和解读仍然存在很多问题。感染性疾病待测标本的成分复杂、病原微生物核酸浓度较低等因素均制约了脑脊液病原微生物的ngs检测。
技术实现要素:
本发明所要解决的技术问题是克服背景技术的技术缺陷,提供一种基于一步法rt-pcr及毛细电泳的同步检测19种脑炎脑膜炎病原体的试剂盒及其检测方法,该试剂盒能对患者的脑脊液样本进行检测,并给出分析,帮助临床医师确诊病原体并有效治疗。
本发明解决上述技术问题所采用的技术方案如下:
本试剂盒包含以下几个组分:me预混液、rt-pcr酶液、me阳性对照、阴性对照、反应内参和无核酸酶水。其中的me预混液由5×一步法rt-pcr缓冲液、22对引物、dntp、mgcl2混合而成。引物包含扩增19种病原体靶基因、1个人基因组dna内参、1个人rna内参和1个反应内参的引物序列。上述引物序列及其pcr产物长度详见表1。
表1本试剂盒检测靶点、内参引物序列
具体地,本发明公开了一种基于一步法rt-pcr及毛细电泳的同步检测19种脑炎脑膜炎病原体的检测方法,包括如下步骤:
(1)采集患者脑脊液样本;
(2)样本和ic核酸提取;
(3)配制反应体系,加入提取好的核酸;
取me预混液4.6μl,加入rt-pcr酶液0.4μl,混合均匀后加入提取好的样本核酸5μl;
(4)一步法rt-pcr扩增;
本试剂盒的pcr扩增反应条件见表2:
表2一步法rt-pcr扩增条件
(5)对扩增产物进行毛细电泳分析,并根据峰型图进行结果判读。
取3500dx遗传分析仪配套高度去离子甲酰胺(hidi)8.75μl、size-500plus0.25μl,混合后加入pcr产物1μl进行毛细电泳分离样品。根据峰型图的出峰位置大小判断脑炎脑膜炎病原体种类。
与现有技术相比,本发明的有益效果是:
(1)本试剂盒可对患者脑脊液样本提取核酸进行一步法多重rt-pcr扩增,同时检测19种脑炎脑膜炎病原体;
(2)本试剂盒通过靶点特异性引物的设计,可以精确测出感染的病原体,包括同步提供交叉感染信息;
(3)本试剂盒人基因组dna内参和人rna内参可有效监控核酸提取样本质量,防止因样本不合格造成的假阴性结果;
(4)本试剂盒反应内参可有效监控核酸提取、rt-pcr扩增和毛细电泳过程;
(5)本试剂盒利用3500dx遗传分析仪灵敏、准确、快速、高通量的技术优势,将为疾控中心、医院及其他医疗机构提供一种灵敏、准确、快速的多重脑炎脑膜炎病原体检测方案;
(6)本试剂盒可同步对19种脑炎脑膜炎病原体进行检测,并同时提供交叉感染信息,具有灵敏度高、特异性强、重复性好、快速准确的优势。
附图说明
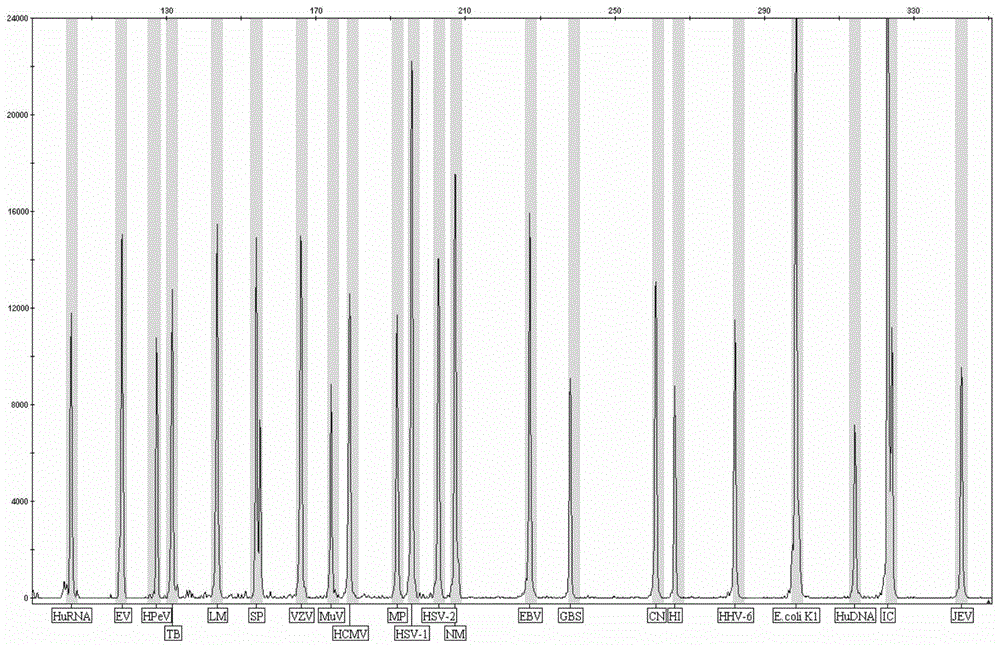
图1为本试剂盒阳性对照扩增图谱,19种脑炎脑膜炎病原体、人dna内参、人rna内参和反应内参均在相应位置出现特征峰;
图2为本试剂盒阴性对照扩增图谱,人dna内参、反应内参出现特征峰;
图3为脑膜炎患者1脑脊液提取核酸扩增图谱,人dna内参、人rna内参、反应内参和结核分枝杆菌(tb)靶点出现特征峰;
图4为脑膜炎患者2脑脊液提取核酸扩增图谱,人dna内参、人rna内参、反应内参、肠道病毒(ev)和单纯疱疹病毒2型(hsv-2)靶点出现特征峰。
具体实施方式
为了更好地理解本发明的内容,下面结合具体实施例和附图作进一步说明。应理解,这些实施例仅用于对本发明进一步说明,而不用于限制本发明的范围。此外应理解,在阅读了本发明所述的内容后,该领域的技术人员对本发明作出一些非本质的改动或调整,仍属于本发明的保护范围。
检测19种脑炎脑膜炎病原体包括如下步骤:
(1)采集患者脑脊液样本;
(2)样本及ic核酸提取;
(3)配制反应体系,加入提取好的核酸;
取me预混液4.6μl,加入rt-pcr酶液0.4μl,混合均匀后加入提取好的样本核酸5μl;
(4)一步法rt-pcr扩增;
本试剂盒的pcr扩增反应条件见表2。
(5)对扩增产物进行毛细电泳分析,并根据峰型图进行结果判读。
取3500dx遗传分析仪配套高度去离子甲酰胺(hidi)8.75μl、size-500plus0.25μl,混合后加入pcr产物1μl进行毛细电泳分离样品。根据峰型图的出峰位置大小判断脑炎脑膜炎病原体数量和种类。
本试剂盒包含以下几个组分:me预混液、rt-pcr酶液、me阳性对照、阴性对照、反应内参和无核酸酶水。其中的me预混液由5×一步法rt-pcr缓冲液、引物、dntp、mgcl2混合而成。引物包含19种病原体靶基因、1个人基因组dna内参、1个人rna内参和1个反应内参的引物组,详见表1。
在实施例1中,所述的样本为患者脑脊液样本。
在实施例1中,通过毛细管电泳对扩增产物进行电泳,并结合分析软件给出扩增图谱并给出分析,判断患者感染的脑炎脑膜炎病原体数量和种类。
实施例1
(1)所选样本:患者脑脊液样本。
(2)样本采集
采集方法:采用腰椎穿刺采集脑脊液样本。病人取卧位,颈部前屈,两侧髋关节和膝关节屈曲以便脊椎间隙增宽。穿刺点在第3、4腰椎间隙。
有效样本:外观应无色透明液体,样本量1ml以上,无血液污染。
(3)核酸提取:取300μl脑脊液样本进行核酸提取,me阳性对照和阴性对照各取80μl进行提取,每个参与提取的样本需加入2μl的ic共同提取。
(4)配制反应体系
根据说明书,按照每个反应me预混液4.6μl、rt-pcr酶液0.4μl的比例配制反应体系,涡旋混匀后,用离心机进行离心,然后分装于pcr反应管中。
(5)加入核酸模板:将提取好的核酸加入到装有配制好的反应体系的pcr反应管中,每人份加入5μl核酸。
(6)一步法rt-pcr扩增
一步法rt-pcr扩增条件见表2。
(7)毛细电泳
由高纯度去离子甲酰胺与系统中分子量内标(size-500plus)组成上样混合物[(0.25μlsize-500plus+8.75μl高纯度去离子甲酰胺)×(进样数)]。将9μl上样混合物与1μl扩增产物混合,避免产生气泡,尽快电泳。用abi3500遗传分析仪(购自美国abi公司)检测分析,具体分析参数为进样电压:1.2kv,进样时间:15s,电泳时间1210-1500s。检测结果分别为图1、图2、图3和图4。
(8)分析数据
本次实验中所使用的是患者样本,根据各目的峰在图谱中出现的位置,确定该患者感染的病原体类型。
图1为阳性对照的分析图谱,图2为阴性对照的分析图谱,图3为脑膜炎患者1的分析图谱,图4为脑膜炎患者2的分析图谱。
结果分析如下:
图1为阳性对照扩增结果图谱,19种脑炎脑膜炎病原体、人dna内参、人rna内参和反应内参均在相应位置出现特征峰。
图2为阴性对照扩增结果图谱,人dna内参和反应内参均出现特征峰。
图3为脑膜炎患者1脑脊液样本的分析图谱。
脑膜炎患者1脑脊液样本扩增产物电泳图谱出现以下特征峰:人dna内参、人rna内参、反应内参、结核分枝杆菌(tb)。表明该患者感染了结核分枝杆菌。
图4为脑膜炎患者2脑脊液样本的分析图谱。
脑膜炎患者2脑脊液样本扩增产物电泳图谱出现以下特征峰:人dna内参、人rna内参、反应内参、肠道病毒(ev)、单纯疱疹病毒2型(hsv-2)。表明该患者感染了肠道病毒和单重疱疹病毒2型,为交叉感染类型。
上述说明并非对本发明的限制,本发明也并不限于上述举例。本技术领域的普通技术人员在本发明的实质范围内,做出的变化、改型、添加或替换,也应属于本发明的保护范围。
sequencelisting
<110>宁波海尔施基因科技有限公司
<120>一种基于rt-pcr及毛细电泳的同步检测19种脑炎脑膜炎病原体的试剂盒及检测方法
<130>2020-05-26
<160>44
<170>patentinversion3.3
<210>1
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>脑膜炎奈瑟氏菌正向引物
<400>1
caagatcgccgttctgatgcgc22
<210>2
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>脑膜炎奈瑟氏菌反向引物
<400>2
atacaatacatctttattcttc22
<210>3
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>流感嗜血杆菌正向引物
<400>3
tatcaacgtaacggcattggt21
<210>4
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>流感嗜血杆菌反向引物
<400>4
cataacgcataggagggaaat21
<210>5
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>结核分枝杆菌正向引物
<400>5
tggtttcctgcgtgggcatgat22
<210>6
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>结核分枝杆菌反向引物
<400>6
cctggattatcccgggctgcac22
<210>7
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>肺炎支原体正向引物
<400>7
cctccgcggggaatcccgact21
<210>8
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>肺炎支原体反向引物
<400>8
gcgcgctgcgcgttgttctt20
<210>9
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>肺炎链球菌正向引物
<400>9
ttgccgaaaacgcttgataca21
<210>10
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>肺炎链球菌反向引物
<400>10
tcaatatcatgcttaaactgc21
<210>11
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>无乳链球菌正向引物
<400>11
aaaggtactattgacatcgaca22
<210>12
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>无乳链球菌反向引物
<400>12
tgatatctgcaatgttattaatt23
<210>13
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>大肠杆菌k1正向引物
<400>13
aagatgtcagtcttattcaatag23
<210>14
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>大肠杆菌k1反向引物
<400>14
aaaatcatttccatcctcttcaa23
<210>15
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>李斯特氏菌正向引物
<400>15
gcctaacatatccaggtgctct22
<210>16
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>李斯特氏菌反向引物
<400>16
tttacaacatttttattgtctt22
<210>17
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>肠道病毒正向引物
<400>17
tgctgtatccacggcagaagt21
<210>18
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>肠道病毒反向引物
<400>18
ctgaactacactggggttgct21
<210>19
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>腮腺炎病毒正向引物
<400>19
ttcagggaaccaactcgttga21
<210>20
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>腮腺炎病毒反向引物
<400>20
cttcggaggatgagaccatgat22
<210>21
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>单纯疱疹病毒1型正向引物
<400>21
cttcgatcgccctcctcacaa21
<210>22
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>单纯疱疹病毒1型反向引物
<400>22
gtccccaataaacaaaaggt20
<210>23
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>单纯疱疹病毒2型正向引物
<400>23
ctggcccaccttatctacgtc21
<210>24
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>单纯疱疹病毒2型反向引物
<400>24
gttacaggagggtgcccagta21
<210>25
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>水痘带状疱疹病毒正向引物
<400>25
tttagcaactctctattatga21
<210>26
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>水痘带状疱疹病毒反向引物
<400>26
aagatgtggcgaaggataaa20
<210>27
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>非洲淋巴细胞瘤病毒正向引物
<400>27
ctgacactttagagctctggag22
<210>28
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>非洲淋巴细胞瘤病毒反向引物
<400>28
gccctgacctttggtgaagtca22
<210>29
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>人类巨细胞病毒正向引物
<400>29
ggagccgacgctgaaaacgcc21
<210>30
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>人类巨细胞病毒反向引物
<400>30
gccgtgtcacctaacgccgctat23
<210>31
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>人类疱疹病毒6型正向引物
<400>31
tccttgggattgggcaaaatatc23
<210>32
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>人类疱疹病毒6型反向引物
<400>32
agacgaccatggatctctcggc22
<210>33
<211>23
<212>dna
<213>人工序列(unknown)
<220>
<223>新型隐球菌正向引物
<400>33
ctagaaatgttagtcacaattac23
<210>34
<211>24
<212>dna
<213>人工序列(unknown)
<220>
<223>新型隐球菌反向引物
<400>34
accccatcaaatttcttggtgtga24
<210>35
<211>24
<212>dna
<213>人工序列(unknown)
<220>
<223>乙型脑炎病毒正向引物
<400>35
tgtgatgaaagatggaaggagcat24
<210>36
<211>25
<212>dna
<213>人工序列(unknown)
<220>
<223>乙型脑炎病毒反向引物
<400>36
gtgattggagtcttgtccatcatcc25
<210>37
<211>21
<212>dna
<213>人工序列(unknown)
<220>
<223>人双埃可病毒正向引物
<400>37
ggattggttcaaacctgaatt21
<210>38
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>人双埃可病毒反向引物
<400>38
atagtgtctcttgttacctacg22
<210>39
<211>19
<212>dna
<213>人工序列(unknown)
<220>
<223>人dna内参正向引物
<400>39
gagtctctgggatgtccct19
<210>40
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>人dna内参反向引物
<400>40
tccgagcctccacggcgctt20
<210>41
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>人rna内参正向引物
<400>41
gaaccatgtgactttgtcac20
<210>42
<211>19
<212>dna
<213>人工序列(unknown)
<220>
<223>人rna内参反向引物
<400>42
accttaagtaggttaggtt19
<210>43
<211>22
<212>dna
<213>人工序列(unknown)
<220>
<223>反应内参正向引物
<400>43
atgattgaacaagatggattgc22
<210>44
<211>20
<212>dna
<213>人工序列(unknown)
<220>
<223>反应内参反向引物
<400>44
gcaaggtgagatgacaggag20
- 还没有人留言评论。精彩留言会获得点赞!