一种TEMPO催化的以肟类化合物为原料合成螺异噁唑啉的新型反应方法与流程
本发明属于化学合成技术领域,具体涉及一种以tempo作为催化剂,肟类化合物作为原料,合成螺异噁唑啉的新型反应方法。
背景技术:
螺异噁唑啉是一类重要的天然产物骨架,比如在海绵动物中发现的subereamollines、purealidins。此外,螺异噁唑啉还表现出较为广泛的生物活性,如抗菌、抗病毒、抗肿瘤等。正因如此,螺异噁唑啉及其衍生物吸引了众多科学家的研究兴趣。
目前为止,螺异噁唑啉常通过预制备的酚肟化合物为原料,在过量氧化剂的作用下实现产物的合成。这一方法存在这较大的缺陷,首先酚肟化合物合成复杂,存在众多上保护与去保护步骤;其次已报道的氧化剂存在毒性大或产生废物多等问题;最后,酚肟制备螺异噁唑啉的例子少,产率也不高。
本发明所述的新型螺异噁唑啉合成方法,开创性的实现了肟类化合物的催化去芳构化,以空气中的氧气作为氧化剂,操作简单,条件绿色温和,底物范围广,产率高。
技术实现要素:
本部分的目的在于概述本发明的实施例的一些方面以及简要介绍一些较佳实施例。在本部分以及本申请的说明书摘要和发明名称中可能会做些简化或省略以避免使本部分、说明书摘要和发明名称的目的模糊,而这种简化或省略不能用于限制本发明的范围。
鉴于上述和/或现有螺异噁唑啉类化合物的合成方法的技术空白,提出了本发明。
因此,本发明其中的一个目的是解决现有技术中的不足,提供一种条件绿色温和,产率高的合成螺异噁唑啉的新方法。
为解决上述技术问题,本发明提供了如下技术方案:将原料肟类化合物、亚硝酸钠、浓盐酸、tempo、水和1,2-二氯乙烷加入反应瓶中,以400-1200rpm的转速敞口搅拌0.5至48小时。反应结束后,浓缩反应液,再经柱层析分离得到目标产物。
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应所述的原料肟类化合物,其结构通式如式i所示:
式i中r1基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),酯基、酮基、醛基、烷基等;式i中r2基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等;式i中r3基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等;式i中xr4基团处于芳香环支链的邻位或对位,x为硫原子或氧原子,r4基团包括但不限于氢、烷基、硅基等;式i中r5基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等。
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应所述的亚硝酸钠,可以使用其他亚硝源代替,包括但不限于亚硝酸银、亚硝酸钾、亚硝酸特丁酯、亚硝酸异戊酯、浓硝酸等,其用量与所述肟类化合物的比例为1:100至10:1;
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应中所述的浓盐酸,可以使用其它酸代替,包括但不限于甲酸、乙酸、磷酸、硫酸、三氟甲磺酸、对甲苯磺酸、三氯化铝、三氯化铁等,其用量与所述肟类化合物的比例为1:10至30:1;
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应中所述的tempo,其化学名称为2,2,6,6-四甲基哌啶-1-氧基自由基,可以使用其它类似化合物代替,包括但不限4-氨基-2,2,6,6-四甲基哌啶氧自由基、tempo甲基丙烯酸甲酯、4-氰基-2,2,6,6-四甲基哌啶-1-氧基自由基等,其用量与所述肟类化合物的比例为1:100至99:100;
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应中所述的水,其用量与所述肟类化合物的比例为1:10至1000:1;反应中所述的1,2-二氯乙烷,可以使用其它溶剂代替,包括但不限于乙醚、二氯甲烷、乙腈、n,n-二甲基甲酰胺、四氢呋喃等,反应液浓度为0.05至1m。
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:反应中所述的反应温度,在0至75℃之间。
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:所述浓缩反应液,其转速为100至200rpm,温度为38至40℃,真空为0.09至0.10mpa,处理时间为3至5min;所述柱层析,其是采用200至300目柱层析硅胶,洗脱剂为石油醚与乙酸乙酯的混合溶液。
作为本发明所述合成螺异噁唑啉的新方法的一种优选方案,其中:所述产物螺异噁唑啉,其结构通式如式ii所示:
当原料肟类化合物中所含xr4基团处于芳香环支链的邻位时,所得产物对应式ii-a,当原料肟类化合物中所含xr4基团处于芳香环支链的对位时,所得产物对应式ii-b。
式ii中r1基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),酯基、酮基、醛基、烷基等;式ii中r2基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等;式ii中r3基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等;式ii中r5基团包括但不限于苯基,取代苯基(包括单取代苯基以及多取代苯基,取代基包括但不限于卤素、羰基、酯基、醛基、硝基、三氟甲基、三氟甲氧基、甲巯基、烷基、甲氧基、二甲氨基、羟基、烯基、炔基等),杂环取代基(包括但不限于呋喃环,噻吩环,吡啶环等),烷基等。
本发明的有益效果:
(1)本发明所提供的一种以肟类化合物类化合物为原料合成螺异噁唑啉的新型反应方法,开创性地使用tempo作为催化剂,以空气作为氧化剂,实现了螺异噁唑啉地绿色高效合成。
(2)操作简单,产率高,纯度在95%以上。
(3)条件温和,底物范围广。
(4)如式i中所示,原料无需使用特定的xr4为羟基地酚肟类化合物。各类x为氧或硫原子,r4为氢、烷基、硅基的肟类化合物均可以在此条件下顺利反应。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其它的附图。其中:
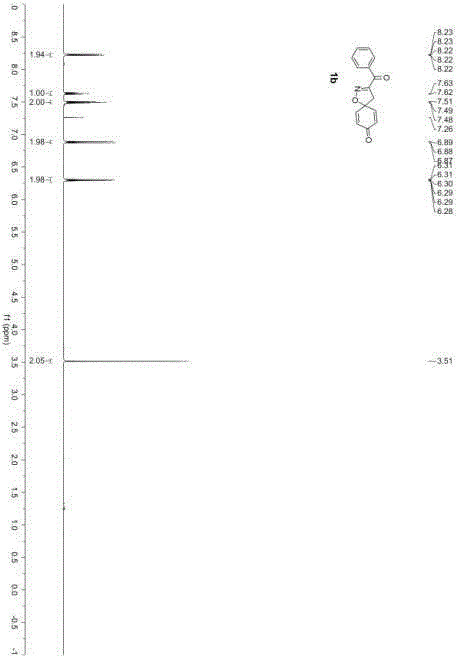
图1为化合物1b的核磁谱图h谱,图1表明化合物1b结构正确;
图2为化合物1b的核磁谱图c谱,图2表明化合物1b结构正确;
图3为化合物2b的核磁谱图h谱,图3表明化合物2b结构正确。
图4为化合物2b的核磁谱图c谱,图1表明化合物2b结构正确;
图5为化合物3b的核磁谱图h谱,图2表明化合物3b结构正确;
图6为化合物3b的核磁谱图c谱,图3表明化合物3b结构正确。
具体实施方式
为使本发明的上述目的、特征和优点能够更加明显易懂,下面结合具体实施例对本发明的具体实施方式做详细的说明。
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是本发明还可以采用其他不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似推广,因此本发明不受下面公开的具体实施例的限制。
其次,此处所称的“一个实施例”或“实施例”是指可包含于本发明至少一个实现方式中的特定特征、结构或特性。在本说明书中不同地方出现的“在一个实施例中”并非均指同一个实施例,也不是单独的或选择性的与其他实施例互相排斥的实施例。
通用实验步骤
将亚硝酸钠、原料肟类化合物、浓盐酸、tempo、水和四氢呋喃加入预先干燥的100ml反应瓶中。反应体系在室温下搅拌48小时,待反应结束后,浓缩反应液,再经柱层析分离得到预期产物。
实施例1:
根据通用实验步骤,使用原料1a得到产物1b,产率为79%。(经hplc分析纯度为98%,从核磁图谱外形、信号、噪声等方面也可以反映出产品纯度极高)
rf=0.4(20%eainpe)
1hnmr(600mhz,cdcl3)δ8.29–8.15(m,2h),7.68–7.58(m,1h),7.53–7.44(m,2h),6.93–6.82(m,2h),6.35–6.25(m,2h),3.51(s,2h).
13cnmr(150mhz,cdcl3)δ185.2,184.4,157.4,144.0,135.3,134.2,130.5,129.5,128.7,82.3,44.3.
hrms-esi(m/z)[m+h]+calculatedforc15h12no3254.0812,found254.0806.
实施例2:
根据通用实验步骤,使用原料2a得到产物2b,产率为69%。(经hplc分析纯度为98%,从核磁图谱外形、信号、噪声等方面也可以反映出产品纯度极高)
rf=0.3(20%eainpe)
1hnmr(400mhz,cdcl3)δ8.32(dd,j=3.9,1.1hz,1h),7.79(dd,j=4.9,1.1hz,1h),7.20(dd,j=4.9,4.0hz,1h),6.88(d,j=10.1hz,2h),6.31(d,j=10.0hz,2h),3.49(s,2h).
13cnmr(100mhz,cdcl3)δ184.4,176.7,157.2,143.9,140.7,136.4,136.4,129.6,128.8,82.6,43.9.
hrms-esi(m/z)[m+na]+calculatedforc13h9nnao3s282.0195,found282.0196.
实施例3:
根据通用实验步骤,使用原料3a得到产物3b,产率为89%。(经hplc分析纯度为98%,从核磁图谱外形、信号、噪声等方面也可以反映出产品纯度极高)
rf=0.3(40%eainpe)
1hnmr(600mhz,cdcl3)δ6.85(d,j=10.1hz,2h),6.28(d,j=10.1hz,2h),3.91(s,3h),3.35(s,2h).
13cnmr(150mhz,cdcl3)δ184.3,160.2,151.1,143.7,129.5,83.3,53.3,43.6.
hrms-esi(m/z)[m+na]+calculatedforc10h9nnao4230.0424,found230.0430。
- 还没有人留言评论。精彩留言会获得点赞!