一种N-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺的制备方法与流程
丙基-2-吡咯烷乙酰胺(bi-ii751xx)的制备方法,以方便更好的进行普拉克索的质量研究。
8.为了实现上述发明目的,本发明提供以下技术方案:
9.本发明提供了一种n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺的制备方法,包括以下步骤:
10.步骤1:在无机酸催化、加热条件下,焦谷氨酸与甲醇发生酯化反应生成5-(羧酸甲酯)-2-吡咯烷酮;
11.步骤2:非质子性溶剂中,在强碱催化、回流条件下,5-(羧酸甲酯)-2-吡咯烷酮和1-碘丙烷发生亲电取代反应生成5-(羧酸甲酯)-n-丙基-2-吡咯烷酮;
12.步骤3:质子性溶剂中,在室温条件、碱的作用下,5-(羧酸甲酯)-n-丙基-2-吡咯烷酮发生水解反应,生成5-羧甲基-n-丙基-2-吡咯烷酮;
13.步骤4:5-羧甲基-n-丙基-2-吡咯烷酮在氯化亚砜作用下先生成酰氯类物质,然后在非质子性溶剂中、加热条件下与硫脲发生亲核取代反应生成n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺。
14.作为优选,步骤1中,无机酸为浓硫酸。
15.作为优选,步骤1中,酯化反应的温度为40℃
±
5℃,酯化反应的时间为2~5小时,反应在持续搅拌状态下发生。
16.优选地,步骤1中,酯化反应的温度为40℃,酯化反应的时间为4小时。
17.作为优选,步骤2中,强碱为氢化钠和/或甲醇钠;非质子性溶剂为四氢呋喃、二甲基甲酰胺、乙腈、四氯化碳、二硫化碳、苯、甲苯、氯仿、二氯甲烷中的一种或几种。
18.优选地,步骤2中,强碱为氢化钠,非质子性溶剂为四氢呋喃。
19.作为优选,步骤2中,5-(羧酸甲酯)-2-吡咯烷酮与1-碘丙烷的摩尔比为1∶(1~2);亲电取代反应的时间为4~8小时。
20.优选地,步骤2中,5-(羧酸甲酯)-2-吡咯烷酮与1-碘丙烷的摩尔比为1∶1,亲电取代反应的时间为6小时。
21.作为优选,步骤3中,质子性溶剂为甲醇、乙醇、水中的一种或几种;强碱为氢氧化钠和/或氢氧化钾。
22.优选地,步骤3中,质子性溶剂为乙醇;强碱为氢氧化钠。
23.作为优选,步骤3中,水解反应的温度为20℃
±
5℃,水解反应的时间为2~4小时。
24.优选地,步骤3中,水解反应的时间为3小时。
25.作为优选,步骤4中,5-羧甲基-n-丙基-2-吡咯烷酮与硫脲的摩尔比为1∶(1.5~2.5)。
26.作为优选,步骤4中,亲核取代反应的温度为80℃
±
10℃,亲核取代反应的时间为4~8小时。
27.优选地,亲核取代反应的温度为回流温度,亲核取代反应的时间为6小时。
28.作为优选,步骤4中,氯化试剂为氯化亚砜和/或草酰氯,非质子性溶剂为二甲基甲酰胺、乙腈、四氯化碳、苯、甲苯中的一种或几种。
29.优选地,步骤4中,氯化试剂为氯化亚砜,非质子性溶剂为乙腈。
30.本发明提供了一种n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺(bi-ii751xx)的制备方法。该制备方法包括以下步骤:在无机酸催化、加热条件下,焦谷氨酸与
甲醇发生酯化反应生成5-(羧酸甲酯)-2-吡咯烷酮;非质子性溶剂中,在强碱催化、回流条件下,5-(羧酸甲酯)-2-吡咯烷酮和1-碘丙烷发生亲电取代反应生成5-(羧酸甲酯)-n-丙基-2-吡咯烷酮;质子性溶剂中,在室温条件、碱的作用下,5-(羧酸甲酯)-n-丙基-2-吡咯烷酮发生水解反应,生成5-羧甲基-n-丙基-2-吡咯烷酮;5-羧甲基-n-丙基-2-吡咯烷酮在氯化亚砜作用下先生成酰氯类物质,然后在非质子性溶剂中、加热条件下与硫脲发生亲核取代反应生成n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺。
31.与已知专利及其它现有技术相比,本发明具有如下优势:
32.(1)本专利以焦谷氨酸为原料避免使用氰化钾剧毒物质,绿色环保。
33.(2)本专利避免了原专利需要自制氯化氢气体造成实验操作繁琐的缺点,简化了实验操作。
34.(3)本专利反应步骤为四步(已知专利为六步),总收率提高,且极大减少了制备杂质bi-ii751xx所需时间。
附图说明
35.图1目标产物bi-ii751xx质谱结果;
36.图2目标产物bi-ii751xx hplc图。
具体实施方式
37.本发明公开了一种n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺的制备方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本
技术实现要素:
、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
38.本发明具体步骤如下:
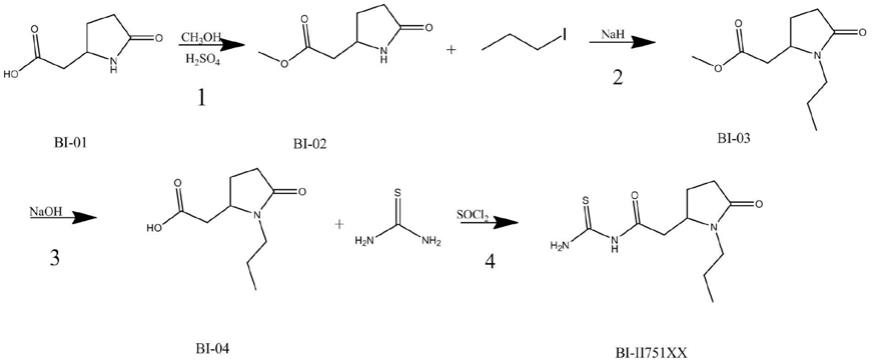
39.一种n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺(bi-ii751xx)的制备路线如下所示:
[0040][0041]
n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺(bi-ii751xx)的制备方法包括以下步骤:
[0042]
步骤1:化合物bi-01(焦谷氨酸)与甲醇为原料在无机酸催化下,加热条件持续搅拌生成化合物bi-02(5-(羧酸甲酯)-2-吡咯烷酮)。
[0043]
步骤2:化合物bi-02(5-(羧酸甲酯)-2-吡咯烷酮)和1-碘丙烷为原料在非质子性溶剂中,回流条件下经强碱催化下生成(5-(羧酸甲酯)-n-丙基-2-吡咯烷酮)。
[0044]
步骤3:化合物bi-03(5-(羧酸甲酯)-n-丙基-2-吡咯烷酮)在质子性溶剂中,室温条件在碱的作用下发生水解反应生成化合物bi-04(5-羧甲基-n-丙基-2-吡咯烷酮)。
[0045]
步骤4:化合物bi-04(5-羧甲基-n-丙基-2-吡咯烷酮)在与氯化亚砜作用下生成酰氯类物质,再与硫脲反应在非质子性溶剂中加热条件下生成目标产物bi-ii751xx(n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺)。
[0046]
步骤1中以焦谷氨酸(bi-01)为原料,在(40℃
±
5℃)条件下进行反应,在浓硫酸(0.5~1ml)的作用下与甲醇进行酯化反应得到5-(羧酸甲酯)-2-吡咯烷酮(bi-02)。本反应中所用甲醇既是反应原料,也是反应溶剂。反应时间2-5小时,优选4小时。
[0047]
步骤2中以5-(羧酸甲酯)-2-吡咯烷酮(bi-02)与1-碘丙烷为原料,摩尔比为1∶1~2。5-(羧酸甲酯)-2-吡咯烷酮(bi-02)在强碱活化下与1-碘丙烷在回流条件下进行亲电取代反应得到5-(羧酸甲酯)-n-丙基-2-吡咯烷酮(bi-03)。本反应所用强碱包括氢化钠、甲醇钠,优选氢化钠。反应选用的非质子性溶剂包括四氢呋喃、二甲基甲酰胺、乙腈、四氯化碳、二硫化碳、苯、甲苯、氯仿、二氯甲烷等溶剂,优选四氢呋喃。反应时间4-8小时,优选6小时。
[0048]
步骤3中以5-(羧酸甲酯)-n-丙基-2-吡咯烷酮(bi-03)为原料。5-(羧酸甲酯)-n-丙基-2-吡咯烷酮(bi-02)在室温(20℃
±
5℃)碱性条件下水解得到5-羧甲基-n-丙基-2-吡咯烷酮(bi-04)。本反应所用强碱包括氢氧化钠、氢氧化钾,优选氢氧化钠。反应选用的质子性溶剂包括甲醇、乙醇、水等溶剂,优选乙醇。反应时间2-4小时,优选3小时。
[0049]
步骤4中以5-(羧甲基)-n-丙基-2-吡咯烷酮(bi-04)与硫脲为原料,摩尔比为1∶1.5~2.5。5-(羧甲基)-2-吡咯烷酮(bi-02)在氯化试剂活化后与硫脲在非质子性溶剂中(80℃
±
10℃)条件下发生亲核取代反应生成n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺(bi-ii751xx)。本反应所用氯化试剂包括氯化亚砜、草酰氯,优选氯化亚砜。反应选用的非质子性溶剂包括二甲基甲酰胺、乙腈、四氯化碳、苯、甲苯等溶剂,优选乙腈。反应时间4-8小时,优选6小时。
[0050]
本发明最后制备出纯度大于98%的杂质(bi-ii751xx)的标准品。
[0051]
本发明提供的n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺的制备方法中所用原料或试剂均可由市场购得。
[0052]
下面结合实施例,进一步阐述本发明:
[0053]
实施例1:bi-ii751xx的制备
[0054]
步骤1、5-(羧酸甲酯)-2-吡咯烷酮(bi-02)的合成
[0055]
方法(1)将35.8g焦谷氨酸溶于100ml甲醇中,加入2ml浓h2so4。40℃条件下搅拌2.0h。tlc监控反应(石油醚:乙酸乙酯=1:1,碘熏),待原料反应完毕加饱和碳酸钠溶液调节ph值至中性。蒸干甲醇用二氯甲烷三次萃取,分出有机层分别用水和饱和食盐水洗,无水硫酸钠干燥,滤液蒸干得白色固体33.5g,收率85.3%。
[0056]
方法(2)将35.8g焦谷氨酸溶于100ml甲醇中,加入2ml浓h2so4。40℃条件下搅拌3.0h。tlc监控反应(石油醚:乙酸乙酯=1:1,碘熏),待原料反应完毕加饱和碳酸钠溶液调
节ph值至中性。蒸干甲醇用二氯甲烷三次萃取,分出有机层分别用水和饱和食盐水洗,无水硫酸钠干燥,滤液蒸干得白色固体36.8g,收率93.6%。
[0057]
方法(3)将35.8g焦谷氨酸溶于100ml甲醇中,加入2ml浓h2so4。40℃条件下搅拌4.0h。tlc监控反应(石油醚:乙酸乙酯=1:1,碘熏),待原料反应完毕加饱和碳酸钠溶液调节ph值至中性。蒸干甲醇用二氯甲烷三次萃取,分出有机层分别用水和饱和食盐水洗,无水硫酸钠干燥,滤液蒸干得白色固体37.7g,收率97%。
[0058]
方法(4)将35.8g焦谷氨酸溶于100ml甲醇中,加入2ml浓h2so4。40℃条件下搅拌5.0h。tlc监控反应(石油醚:乙酸乙酯=1:1,碘熏),待原料反应完毕加饱和碳酸钠溶液调节ph值至中性。蒸干甲醇用二氯甲烷三次萃取,分出有机层分别用水和饱和食盐水洗,无水硫酸钠干燥,滤液蒸干得白色固体37.2g,收率95.8%。
[0059]
步骤2、5-(羧酸甲酯)-n-丙基-2-吡咯烷酮(bi-03)的合成
[0060]
方法(1)将15.7g 5-(羧酸甲酯)-2-吡咯烷酮溶于无水50ml四氢呋喃中,分批加入4.8g氢化钠,室温下搅拌30min,加入34g碘丙烷,回流条件下反应6.0h,tlc监测反应(石油醚∶乙酸乙酯=1∶1,碘熏),原料反应完全后缓慢降至室温。过滤,滤液旋干得油状物。甲醇重结晶得14.9g白色固体,收率75%。
[0061]
方法(2)将15.7g 5-(羧酸甲酯)-2-吡咯烷酮溶于无水50ml乙腈中,分批加入4.8g氢化钠,室温下搅拌30min,加入34g碘丙烷,回流条件下反应6.0h,tlc监测反应(石油醚∶乙酸乙酯=1∶1,碘熏),原料反应完全后缓慢降至室温。过滤,滤液旋干得油状物。甲醇重结晶得13.8g白色固体,收率69.3%。
[0062]
方法(3)将15.7g 5-(羧酸甲酯)-2-吡咯烷酮溶于无水50ml二氯甲烷中,分批加入4.8g氢化钠,室温下搅拌30min,加入34g碘丙烷,回流条件下反应6.0h,tlc监测反应(石油醚∶乙酸乙酯=1∶1,碘熏),原料反应完全后缓慢降至室温。过滤,滤液旋干得油状物。甲醇重结晶得14.3g白色固体,收率72.2%。
[0063]
方法(4)将15.7g 5-(羧酸甲酯)-2-吡咯烷酮溶于无水50ml氯仿中,分批加入4.8g氢化钠,室温下搅拌30min,加入34g碘丙烷,回流条件下反应6.0h,tlc监测反应(石油醚∶乙酸乙酯=1∶1,碘熏),原料反应完全后缓慢降至室温。过滤,滤液旋干得油状物。甲醇重结晶得13.9g白色固体,收率70.2%。
[0064]
步骤3、5-(羧甲基)-n-丙基-2-吡咯烷酮(bi-04)的合成
[0065]
方法(1)将10g 5-(羧酸甲酯)-n-丙基-2-吡咯烷酮溶于30ml乙醇中,反应液中加入0.5mol/l氢氧化钠3ml。室温条件下搅拌3h。tlc监测反应(二氯甲烷∶甲醇.=8∶1,碘熏)。原料反应完后用稀盐酸水溶液将反应液ph值调至5~6。蒸干甲醇用二氯甲烷分三次萃取,合并有机层分别用水和饱和食盐水洗,无水硫酸钠干燥。滤液蒸干得白色固体8.6g,收率92%。
[0066]
方法(2)将10g 5-(羧酸甲酯)-n-丙基-2-吡咯烷酮溶于30ml乙醇中,反应液中加入0.5mol/l氢氧化钾3ml。室温条件下搅拌3h。tlc监测反应(二氯甲烷∶甲醇.=8∶1,碘熏)。原料反应完后用稀盐酸水溶液将反应液ph值调至5~6。蒸干甲醇用二氯甲烷分三次萃取,合并有机层分别用水和饱和食盐水洗,无水硫酸钠干燥。滤液蒸干得白色固体8.2g,收率88%。
[0067]
步骤4、n-(氨基硫代甲基)-5-氧代-1-丙基-2-吡咯烷乙酰胺(bi-ii751xx)的合成
[0068]
方法(1)将5g 5-(羧甲基)-n-丙基-2-吡咯烷酮溶于20ml氯化亚砜中,氮气保护,室温条件下搅拌3h,旋干剩余氯化亚砜后溶于20ml无水乙腈中。将4.9g硫脲溶于20ml无水乙腈中,回流搅拌至全溶。回流条件下滴入上述酰氯的乙腈溶液,滴加完毕后持续搅拌6h。tlc监测反应(二氯甲烷∶甲醇.=10∶1,254nm紫外显色)。待反应原料反应完毕。反应液降至室温,旋干溶剂得黑色油状物,柱层析(流动相二氯甲烷∶甲醇.=20∶1)分离得到2.9g目标产物bi-ii751xx,收率56%。
[0069]
方法(2)将5g 5-(羧甲基)-n-丙基-2-吡咯烷酮溶于20ml草酰氯中,氮气保护,室温条件下搅拌3h,旋干剩余氯化亚砜后溶于20ml无水乙腈中。将4.9g硫脲溶于20ml无水乙腈中,回流搅拌至全溶。回流条件下滴入上述酰氯的乙腈溶液,滴加完毕后持续搅拌6h。tlc监测反应(二氯甲烷∶甲醇.=10∶1,254nm紫外显色)。待反应原料反应完毕。反应液降至室温,旋干溶剂得黑色油状物,柱层析(流动相二氯甲烷∶甲醇.=20∶1)分离得到2.6g目标产物bi-ii751xx,收率51%,hplc测出纯度为99.22%。
[0070]
目标产物bi-ii751xx质谱如图1,液相图如图2所示。
[0071]
由上述试验数据可知,本发明制备方法的最高总收率可达37.4%。
[0072]
对比例1cn103012233a实施例一:
[0073]
参照对比专利cn103012233a的公开实施例一方法制备目标产物bi-ii751xx,总收率14.7%。
[0074]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1