一种含酰胺的曼尼希型化合物的制备方法与流程
[0001]
本发明属于有机化合物技术领域,具体涉及一种含酰胺的曼尼希型化合物的制备方法。
背景技术:
[0002]
曼尼希型反应是有机合成中最重要的c-c、c-n成键反应之一。它能提供β-氨基化合物,是各种药物和天然产品的重要合成中间体。然而,经典的曼尼希反应存在许多严重的缺点,受限于胺类化合物亲核性的影响,传统的曼尼希反应底物选取范围相对有限,比如酰胺由于羰基的影响亲核性减弱,难以进行曼尼希反应得到相应产物。尽管不对称曼尼希反应的合成路线多种多样。但是,总的来说,改进的方法仍然依赖于使用预先形成的亲电试剂(如亚胺)和稳定的亲核试剂(如烯醇和烯醇醚)的双组分体系。对于如何让低亲核性的胺类参与反应缺少报道。
[0003]
据申请人所知,各种各样的胺源,如苯胺、伯胺和仲胺,已被用于与醛的亲核反应中。然而,由于羰基对氨基的影响,酰胺的亲核性相对较低,醛与酰胺的氨基烷基化曼尼希型反应在以往的文献中鲜有报道。
技术实现要素:
[0004]
本发明的目的是提供一种含酰胺的曼尼希型化合物的制备方法,该方法解决了现有条件下,由于酰胺亲核性较低,难以进行传统的曼尼希反应的问题,且反应条件温和,操作过程简单,成本低廉且绿色环保,具有推广的应用价值。
[0005]
为了达到上述技术目的,本发明具体通过以下技术方案实现:
[0006]
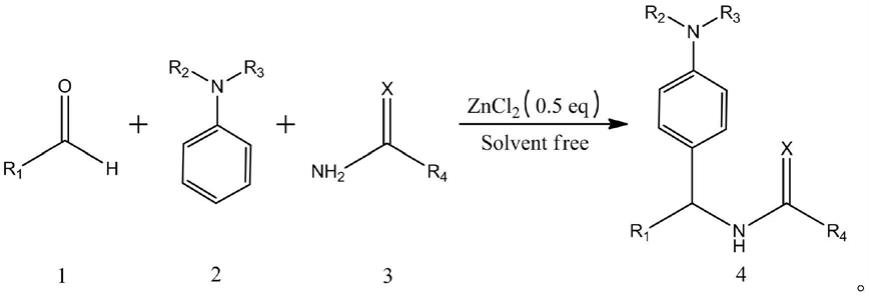
一种含酰胺的曼尼希型化合物的制备方法,通过将醛、n取代苯胺、酰胺类化合物以及催化剂于80℃下搅拌反应,即可得到含酰胺的产物;该方法的合成路线为:
[0007][0008]
进一步的,所述的醛具有如化合物1所示的结构,r1选自芳基或烷基;
[0009]
优选的,r1选自无取代苯基、取代苯基、呋喃、噻吩以及饱和烷基。
[0010]
进一步的,所述n取代苯胺具有如化合物2所示的结构,r2,r3各自独立的选自芳基、烷基以及h。
[0011]
优选的,r2、r3各自独立的选自无取代苯基、饱和烷基以及h。
[0012]
进一步的,所述酰胺类化合物具有如化合物3所示的结构,r4选自烷基或芳基,x选自s或o。
[0013]
优选的,r4选自无取代苯基、取代苯基以及烷基,x选自s或o。
[0014]
进一步的,所述的催化剂氯化锌的用量为0.5个当量。
[0015]
进一步的,反应结束后采用柱色谱分离进行处理,并在低温真空条件下干燥。
[0016]
优选的,所述的干燥温度为30~50℃。
[0017]
优选的,柱色谱分离的洗脱剂采用乙酸乙酯和石油醚,所述乙酸乙酯和石油醚的体积比为1:2或2∶1。
[0018]
本发明的有益效果为:
[0019]
(1)本发明的制备方法,在氯化锌条件下,不添加任何溶剂,绿色环保,合成了一种新的化合物,反应条件温和,容易控制,安全性高;
[0020]
(2)本发明的制备方法,操作简单、成本低廉,且后处理简便,目标产物易分离,整个制备系统容易构建且绿色环保,与传统的曼尼希反应相比,使用不活泼的酰胺参与反应,在氮原子上引入了一个羰基,是曼尼希反应上的一个重大突破。
具体实施方式
[0021]
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0022]
实施例1
[0023]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0024][0025]
具体包括以下步骤:
[0026]
(1)取10ml试管,加入0.2mmol苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0027]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0028]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0029]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0030]1h nmr(500mhz,cdcl3)δ7.35
–
7.27(m,2h),7.26
–
7.21(m,3h),7.06(d,j=8.7hz,2h),6.67(d,j=8.7hz,2h),6.16(d,j=8.0hz,1h),6.10(d,j=7.5hz,1h),2.92(s,6h),2.02(s,3h).
[0031]
13
c nmr(126mhz,cdcl3)δ168.97,149.91,142.06,129.46,128.45,128.44,127.15,127.06,112.55,56.44,40.55,23.39.
[0032]
hrms calcd.for c
17
h
20
n2o[m+h]
+
m/z 269.1648,found 269.1651.
[0033]
实施例2
[0034]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0035]
具体包括以下步骤:
[0036]
(1)取10ml试管,加入0.2mmol对硝基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0037]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0038]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0039]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0040]1h nmr(500mhz,cdcl3)δ8.17(d,j=8.8hz,2h),7.42(d,j=8.6hz,2h),7.02(d,j=8.7hz,2h),6.67(d,j=8.7hz,2h),6.14(d,j=7.1hz,1h),6.06(d,j=6.8hz,1h),2.94(s,6h),2.07(s,3h).
[0041]
13
c nmr(126mhz,cdcl3)δ169.31,150.31,149.64,146.95,128.68,127.67,123.71,112.61,56.73,40.41,23.28.
[0042]
hrms calcd.for c
17
h
19
n3o3[m+h]
+
m/z 314.1499,found 314.1489.
[0043]
实施例3
[0044]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0045][0046]
具体包括以下步骤:
[0047]
(1)取10ml试管,加入0.2mmol对溴苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0048]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0049]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,
体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0050]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0051]1h nmr(500mhz,cdcl3)δ7.43(d,j=8.4hz,2h),7.11(d,j=8.3hz,2h),7.03(d,j=8.6hz,2h),6.67(d,j=8.4hz,2h),6.08(d,j=7.7hz,1h),5.99(d,j=7.2hz,1h),2.93(s,6h),2.03(s,3h).
[0052]
13
c nmr(126mhz,cdcl3)δ169.03,150.04,141.15,131.51,128.81,128.51,120.93,112.58,56.14,40.52,23.37.
[0053]
hrms calcd.for c
17
h
19
brn2o[m+h]
+
m/z 347.0754,found 347.0750.
[0054]
实施例4
[0055]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0056][0057]
具体包括以下步骤:
[0058]
(1)取10ml试管,加入0.2mmol对氯苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0059]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0060]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0061]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0062]1h nmr(500mhz,cdcl3)δ7.29
–
7.26(m,2h),7.17(d,j=8.4hz,2h),7.03(d,j=8.7hz,2h),6.67(d,j=8.6hz,2h),6.06(dd,j=35.5,7.6hz,2h),2.93(s,6h),2.03(s,3h).
[0063]
13
c nmr(126mhz,cdcl3)δ169.04,150.01,140.62,132.80,128.56,128.50,128.45,112.60,56.06,40.54,23.36.
[0064]
hrms calcd.for c
17
h
19
cln2o[m+h]
+
m/z 303.1259,found 303.1256.
[0065]
实施例5
[0066]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0067][0068]
具体包括以下步骤:
[0069]
(1)取10ml试管,加入0.2mmol对甲基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0070]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0071]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0072]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0073]1h nmr(500mhz,cdcl3)δ7.13(d,j=8.7hz,4h),7.07(d,j=8.6hz,2h),6.67(d,j=8.7hz,2h),6.12(d,j=8.0hz,1h),6.03(d,j=7.8hz,1h),2.92(s,6h),2.32(s,3h),2.02(s,3h).
[0074]
13
c nmr(126mhz,cdcl3)δ168.89,149.85,139.13,136.70,129.15,128.36,127.10,112.58,56.17,40.60,23.43,21.04.
[0075]
hrms calcd.for c
18
h
22
n2o[m+h]
+
m/z 283.1805,found 283.1800.
[0076]
实施例6
[0077]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0078][0079]
具体包括以下步骤:
[0080]
(1)取10ml试管,加入0.2mmol对甲氧基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0081]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0082]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0083]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0084]1h nmr(500mhz,cdcl3)δ7.15(d,j=8.4hz,2h),7.07(d,j=8.4hz,2h),6.84(d,j=8.5hz,2h),6.68(d,j=8.4hz,2h),6.11(d,j=7.9hz,1h),5.99(d,j=7.3hz,1h),3.78(s,3h),2.92(s,6h),2.03(s,3h).
[0085]
13
c nmr(126mhz,cdcl3)δ168.89,158.68,149.88,134.31,128.36,128.33,113.87,112.60,55.88,55.30,40.62,23.47.
[0086]
hrms calcd.for c
18
h
22
n2o2[m+h]
+
m/z 299.1754,found 299.1759.
[0087]
实施例7
[0088]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0089][0090]
具体包括以下步骤:
[0091]
(1)取10ml试管,加入0.2mmol对氰基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0092]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0093]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0094]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0095]1h nmr(500mhz,cdcl3)δ7.60(d,j=8.2hz,2h),7.36(d,j=8.2hz,2h),7.01(d,j=8.7hz,2h),6.67(d,j=8.6hz,2h),6.11(d,j=7.2hz,1h),6.03(d,j=6.7hz,1h),2.94(s,6h),2.06(s,3h).
[0096]
13
c nmr(126mhz,cdcl3)δ169.25,150.24,147.60,132.28,128.67,127.63,118.87,112.60,110.80,56.77,40.43,23.28.
[0097]
hrms calcd.for c
18
h
19
n3o[m+h]
+
m/z 294.1601,found 294.1599.
[0098]
实施例8
[0099]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0100][0101]
具体包括以下步骤:
[0102]
(1)取10ml试管,加入0.2mmol 3-硝基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0103]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0104]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0105]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0106]1h nmr(500mhz,cdcl3)δ8.33
–
7.91(m,2h),7.58(d,j=7.5hz,1h),7.47(t,j=7.9hz,1h),7.03(d,j=8.5hz,2h),6.67(d,j=8.3hz,2h),6.16(t,j=7.6hz,2h),2.94(s,6h),2.07(s,3h).
[0107]
13
c nmr(126mhz,cdcl3)δ169.40,150.26,148.44,144.52,133.38,129.35,
128.65,127.75,122.10,121.42,112.65,56.47,40.43,23.28.
[0108]
hrms calcd.for c
17
h
19
n3o3[m+h]
+
m/z 314.1499,found 314.1483.
[0109]
实施例9
[0110]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0111][0112]
具体包括以下步骤:
[0113]
(1)取10ml试管,加入0.2mmol 2-硝基苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0114]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0115]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0116]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0117]1h nmr(500mhz,cdcl3)δ7.92(d,j=8.2hz,1h),7.73
–
7.56(m,2h),7.44(t,j=8.4hz,1h),6.98(d,j=8.7hz,2h),6.68(d,j=7.5hz,1h),6.63(d,j=7.8hz,2h),6.26(d,j=6.7hz,1h),2.91(s,6h),2.06(s,3h).
[0118]
13
c nmr(126mhz,cdcl3)δ169.18,148.76,136.82,133.20,129.71,128.27,128.06,125.48,112.45,54.21,40.47,23.30.
[0119]
hrms calcd.for c
17
h
19
n3o3[m+h]
+
m/z 314.1499,found 314.1485.
[0120]
实施例10
[0121]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0122][0123]
具体包括以下步骤:
[0124]
(1)取10ml试管,加入0.2mmol 2-噻吩甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0125]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0126]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0127]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0128]1h nmr(500mhz,cdcl3)δ7.24
–
7.08(m,3h),6.93(dd,j=5.0,3.6hz,1h),6.83(d,j=3.5hz,1h),6.71(d,j=8.3hz,2h),6.37(d,j=8.2hz,1h),6.11(d,j=7.3hz,1h),2.95(s,6h),2.03(s,3h).
[0129]
13
c nmr(126mhz,cdcl3)δ168.75,150.12,146.81,128.09,126.80,125.30,124.68,112.56,52.56,40.60,23.39.
[0130]
hrms calcd.for c
15
h
18
n2os[m+h]
+
m/z 275.1213,found 275.1218.
[0131]
实施例11
[0132]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0133][0134]
具体包括以下步骤:
[0135]
(1)取10ml试管,加入0.2mmol糠醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0136]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应6h得到该产品;
[0137]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0138]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0139]1h nmr(500mhz,cdcl3)δ7.36(s,1h),7.14(d,j=5.0hz,2h),6.69(d,j=2.5hz,2h),6.31(s,1h),6.25
–
5.96(m,3h),2.93(s,6h),2.02(s,3h).
[0140]
13
c nmr(126mhz,cdcl3)δ168.84,154.21,150.17,142.15,128.01,112.58,110.23,107.13,50.68,40.58,23.38.
[0141]
hrms calcd.for c
15
h
18
n2o2[m+h]
+
m/z 259.1441,found 259.1447.
[0142]
实施例12
[0143]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0144][0145]
具体包括以下步骤:
[0146]
(1)取10ml试管,加入0.2正戊醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0147]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h
得到该产品;
[0148]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0149]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0150]1h nmr(500mhz,cdcl3)δ7.17(d,j=8.6hz,2h),6.73(d,j=7.3hz,2h),5.56(d,j=7.4hz,1h),4.86(q,j=7.7hz,1h),2.94(s,6h),1.95(s,3h),1.84
–
1.70(m,2h),1.37
–
1.21(m,4h),0.86(t,j=7.1hz,3h).
[0151]
13
c nmr(126mhz,cdcl3)δ168.92,149.90,130.08,127.54,112.71,52.96,40.66,35.61,28.49,23.60,22.54,13.99.
[0152]
hrms calcd.for c
15
h
24
n2o[m+h]
+
m/z 249.1961,found 249.1967.
[0153]
实施例13
[0154]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0155][0156]
具体包括以下步骤:
[0157]
(1)取10ml试管,加入0.2异戊醛、0.2mmol n,n-二甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0158]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0159]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0160]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0161]1h nmr(500mhz,cdcl3)δ7.18(d,j=8.7hz,2h),6.71(d,j=8.7hz,2h),5.72(d,j=8.2hz,1h),4.98(q,j=7.9hz,1h),2.93(s,6h),1.93(s,3h),1.65(dtd,j=20.8,13.5,7.5hz,2h),1.49(td,j=13.4,6.7hz,1h),0.92(dd,j=8.8,6.6hz,6h).
[0162]
13
c nmr(126mhz,cdcl3)δ168.92,149.79,130.57,127.55,112.79,51.02,45.10,40.74,25.09,23.57,22.79,22.42.
[0163]
hrms calcd.for c
15
h
24
n2o[m+h]
+
m/z 249.1961,found 249.1964.
[0164]
实施例14
[0165]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0166]
[0167]
具体包括以下步骤:
[0168]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n-甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0169]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0170]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0171]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0172]1h nmr(500mhz,cdcl3)δ7.34
–
7.28(m,2h),7.24(t,j=6.5hz,3h),7.02(d,j=8.5hz,2h),6.55(d,j=8.5hz,2h),6.14(d,j=8.0hz,1h),6.00(d,j=7.3hz,1h),3.66(s,1h),2.81(s,3h),2.04(s,3h).
[0173]
13
c nmr(126mhz,cdcl3)δ168.95,148.70,142.04,130.26,128.62,128.48,127.16,127.12,112.44,56.55,30.74,23.46.
[0174]
hrms calcd.for c
16
h
18
n2o[m+h]
+
m/z 255.1492,found 255.1493.
[0175]
实施例15
[0176]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0177][0178]
具体包括以下步骤:
[0179]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二乙甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0180]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0181]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0182]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0183]1h nmr(500mhz,cdcl3)δ7.35
–
7.28(m,2h),7.26
–
7.17(m,3h),7.02(d,j=8.3hz,2h),6.60(d,j=8.3hz,2h),6.14(d,j=7.9hz,1h),5.98(d,j=6.6hz,1h),3.32(q,j=6.9hz,4h),2.04(s,3h),1.14(t,j=7.0hz,6h).
[0184]
13
c nmr(126mhz,cdcl3)δ168.90,147.15,142.07,128.74,128.43,128.14,127.11,127.02,111.61,56.49,44.32,23.47,12.55.
[0185]
hrms calcd.for c
19
h
24
n2o[m+h]
+
m/z 297.1961,found 297.1964.
[0186]
实施例16
[0187]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0188][0189]
具体包括以下步骤:
[0190]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n-乙甲基苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0191]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0192]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0193]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0194]1h nmr(500mhz,cdcl3)δ7.31(dd,j=17.5,9.6hz,2h),7.23(t,j=6.3hz,3h),6.99(d,j=8.5hz,2h),6.54(d,j=8.5hz,2h),6.14(dd,j=22.5,7.9hz,2h),3.64(s,1h),3.12(q,j=7.1hz,2h),2.00(s,3h),1.23(t,j=7.1hz,3h).
[0195]
13
c nmr(126mhz,cdcl3)δ169.05,147.62,142.05,130.31,128.63,128.43,127.17,127.07,112.83,56.52,38.57,23.35,14.77.
[0196]
hrms calcd.for c
17
h
20
n2o[m+h]
+
m/z 269.1648,found 269.1649.
[0197]
实施例17
[0198]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0199][0200]
具体包括以下步骤:
[0201]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n-甲基二苯胺、0.4mmol乙酰胺和0.1mmol氯化锌;
[0202]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0203]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为1:2,在30℃下真空干燥3h得到缩醛化合物。
[0204]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0205]1h nmr(500mhz,cdcl3)δ7.33
–
7.22(m,7h),7.08(d,j=8.6hz,2h),7.03(d,j=7.7hz,2h),6.98(t,j=7.3hz,1h),6.92(d,j=8.6hz,2h),6.19(dd,j=16.5,7.9hz,2h),
3.28(s,3h),2.02(s,3h).
[0206]
13
c nmr(126mhz,cdcl3)δ169.15,148.71,148.28,141.79,133.71,129.31,128.62,128.37,127.34,127.32,122.04,121.41,119.46,56.60,40.27,23.38.
[0207]
hrms calcd.for c
22
h
22
n2o[m+h]
+
m/z 331.1805,found 249.331.1810.
[0208]
实施例18
[0209]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0210][0211]
具体包括以下步骤:
[0212]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol苯甲酰胺和0.1mmol氯化锌;
[0213]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0214]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为2∶1,在30℃下真空干燥3h得到缩醛化合物。
[0215]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0216]1h nmr(500mhz,cdcl3)δ7.81(d,j=7.2hz,2h),7.49(t,j=7.4hz,1h),7.42(t,j=7.5hz,2h),7.38
–
7.28(m,4h),7.28
–
7.26(m,1h),7.15(d,j=8.6hz,2h),6.73(d,j=7.7hz,2h),6.64(d,j=7.3hz,1h),6.36(d,j=7.7hz,1h),2.94(s,6h).
[0217]
13
c nmr(126mhz,cdcl3)δ166.46,149.94,142.01,134.50,131.56,129.51,128.62,128.59,128.58,127.28,127.22,127.09,112.73,56.99,40.65.
[0218]
hrms calcd.for c
22
h
22
n2o[m+h]
+
m/z 331.1805,found 331.1812.
[0219]
实施例19
[0220]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0221][0222]
具体包括以下步骤:
[0223]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol 4-溴苯甲酰胺和0.1mmol氯化锌;
[0224]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0225]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,
体积比为2∶1,在30℃下真空干燥3h得到缩醛化合物。
[0226]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0227]1h nmr(500mhz,cdcl3)δ7.67(d,j=8.3hz,2h),7.55(d,j=8.3hz,2h),7.35-7.28(m,5h),7.13(d,j=8.4hz,2h),6.70(d,j=7.7hz,2h),6.60(d,j=7.0hz,1h),6.33(d,j=7.6hz,1h),2.93(s,6h).
[0228]
13
c nmr(126mhz,cdcl3)δ165.44,149.97,141.73,133.28,131.81,128.69,128.61,128.58,127.31,127.21,126.24,112.69,57.12,40.61.
[0229]
hrms calcd.for c
22
h
21
brn2o[m+h]
+
m/z 409.0910,found 409.0907.
[0230]
实施例20
[0231]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0232][0233]
具体包括以下步骤:
[0234]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol 4-氯苯甲酰胺和0.1mmol氯化锌;
[0235]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0236]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为2∶1,在30℃下真空干燥3h得到缩醛化合物。
[0237]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0238]1h nmr(500mhz,cdcl3)δ7.74(d,j=8.4hz,2h),7.38(d,j=8.5hz,2h),7.36
–
7.26(m,5h),7.13(d,j=8.6hz,2h),6.69(d,j=8.4hz,2h),6.61(d,j=7.3hz,1h),6.33(d,j=7.6hz,1h),2.93(s,6h).
[0239]
13
c nmr(126mhz,cdcl3)δ165.35,150.00,141.77,137.79,132.83,128.83,128.60,128.58,128.51,127.29,127.21,112.65,57.11,40.58.
[0240]
hrms calcd.for c
22
h
21
cln2o[m+h]
+
m/z 365.1415,found 365.1420
[0241]
实施例21
[0242]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0243][0244]
具体包括以下步骤:
[0245]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol对甲苯酰胺
和0.1mmol氯化锌;
[0246]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0247]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为2∶1,在30℃下真空干燥3h得到缩醛化合物。
[0248]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0249]1h nmr(500mhz,cdcl3)δ7.71(d,j=8.1hz,2h),7.37
–
7.25(m,5h),7.22(d,j=8.0hz,2h),7.14(d,j=8.7hz,2h),6.70(d,j=8.3hz,2h),6.59(d,j=7.4hz,1h),6.35(d,j=7.7hz,1h),2.93(s,6h),2.39(s,3h).
[0250]
13
c nmr(126mhz,cdcl3)δ166.31,149.89,142.06,141.96,131.60,129.21,128.59,128.53,127.24,127.15,127.03,112.70,56.88,40.63,21.45.
[0251]
hrms calcd.for c
23
h
24
n2o[m+h]
+
m/z 345.1961,found 345.1962.
[0252]
实施例22
[0253]
一种含酰胺的曼尼希型化合物的制备方法,其合成路线如下:
[0254][0255]
具体包括以下步骤:
[0256]
(1)取10ml试管,加入0.2苯甲醛、0.2mmol n,n-二甲基苯胺、0.4mmol硫脲和0.1mmol氯化锌;
[0257]
(2)将步骤(1)中的试管在磁力搅拌器上搅拌,在80℃下,转速为250r/min,反应8h得到该产品;
[0258]
(3)将步骤(2)中得到的粗产品进行柱色谱分离,洗脱剂采用乙酸乙酯和石油醚,体积比为2∶1,在30℃下真空干燥3h得到缩醛化合物。
[0259]
对制得的目标产物进行核磁共振氢谱和碳谱以及高分辨质谱的测定:
[0260]1h nmr(500mhz,cdcl3)δ7.31(dd,j=28.2,7.2hz,5h),7.11(d,j=8.5hz,2h),6.66-6.74(m,3h),5.74(s,2h),5.52(s,1h),2.94(s,6h).
[0261]
13
c nmr(126mhz,cdcl3)δ181.71,150.36,139.66,129.08,129.01,128.23,128.18,127.18,112.63,40.41,29.69.
[0262]
hrms calcd.for c
16
h
19
n3s[m+h]
+
m/z 286.1372,found 286.1373.
[0263]
研究反应底物对本发明合成化合物产率的影响,结果如表1所示,对于芳香醛而言,在对位上,给电子基团的醛明显优于吸电子基团的,空间效应的影响没有明显规律,而对于化合物2来说,氮原子上连给电子基团会有益于该反应,最后在化合物3的底物中,无取代基的苯甲酰胺产率最高,对甲苯酰胺产率次之,对氯苯甲酰胺和对溴苯甲酰胺产率偏低。
[0264]
表1不同底物合成含酰胺的曼尼希型化合物的产率情况
[0265]
序号123产率
1苯甲醛n,n-二甲基苯胺乙酰胺82%24-硝基苯甲醛n,n-二甲基苯胺乙酰胺58%34-溴苯甲醛n,n-二甲基苯胺乙酰胺74%44-氯苯甲醛n,n-二甲基苯胺乙酰胺80%54-甲基苯甲醛n,n-二甲基苯胺乙酰胺86%64-甲氧基苯甲醛n,n-二甲基苯胺乙酰胺87%74-氰基苯甲醛n,n-二甲基苯胺乙酰胺54%83-硝基苯甲醛n,n-二甲基苯胺乙酰胺71%92-硝基苯甲醛n,n-二甲基苯胺乙酰胺32%102-噻吩甲醛n,n-二甲基苯胺乙酰胺60%11糠醛n,n-二甲基苯胺乙酰胺78%12正戊醛n,n-二甲基苯胺乙酰胺45%13异戊醛n,n-二甲基苯胺乙酰胺46%14苯甲醛n甲基苯胺乙酰胺56%15苯甲醛n,n-二乙基苯胺乙酰胺70%16苯甲醛n-乙基苯胺乙酰胺59%17苯甲醛n-甲基二苯胺乙酰胺50%18苯甲醛n,n-二甲基苯胺苯甲酰胺74%19苯甲醛n,n-二甲基苯胺对溴苯甲酰胺42%20苯甲醛n,n-二甲基苯胺对氯苯甲酰胺50%21苯甲醛n,n-二甲基苯胺对甲苯酰胺67%22苯甲醛n,n-二甲基苯胺硫脲42%
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1