一种呋喃甲酰胺基β-咔啉类化合物及其制备方法和应用
一种呋喃甲酰胺基
β
‑
咔啉类化合物及其制备方法和应用
技术领域
1.本发明属于药物化学合成和药物治疗学领域,特别涉及一种呋喃甲酰胺基β
‑ꢀ
咔啉类化合物及其制备方法和应用。
技术背景
[0002][0003]
β
‑
咔啉是一种在植物和动物中形成的吲哚类生物碱,具有常见的三环吡啶 [3,4
‑
b]吲哚环结构,自然生成和合成的β
‑
咔啉生物碱由于具有广泛的重要药理和生物学特性而被广泛研究,如抗锥虫体和抗利什曼,抗阿尔茨海默病,抗血小板聚集和抗血栓形成、抗帕金森和作为dyrk1a抑制剂。值得一提的是,β
‑
咔啉类生物碱具有强大的抗肿瘤活性。β
‑
咔啉生物碱存在能够在dna碱基对之间堆叠的多环芳香族平面药效团,因此可以插入dna,改变dna复制保真度并且影响dna修复过程中酶的活性。
[0004]
我们通过采用活性结构拼接和结构改造方法,将溴化呋喃酮骨架改造为5
‑ꢀ
芳基
‑2‑
甲酰基呋喃骨架,并将其与β
‑
咔啉相结合,得到了一系列结构新颖的呋喃甲酰胺化合物
ⅰ‑
1~
ⅰ‑
13。
[0005]
生物活性测试结果表明,该类化合物具有显著的抑制a549人非小细胞肺癌细胞、hepg2人肝癌细胞、mcf
‑
7人乳腺癌细胞、hala人宫颈癌细胞、caco
‑
2 人克隆结肠腺癌细胞和hct
‑
116人结肠癌细胞等增殖的作用,对癌细胞表现出明显的细胞毒性。
技术实现要素:
[0006]
本发明的目的在于提供一种呋喃甲酰胺基β
‑
咔啉类化合物及其制备方法和应用,该化合物具有良好的抗肿瘤活性,对a549人非小细胞肺癌细胞、hepg2 人肝癌细胞、mcf
‑
7人乳腺癌细胞、hala人宫颈癌细胞、caco
‑
2人克隆结肠腺癌细胞和hct
‑
116人结肠癌细胞等恶性肿瘤细胞的细胞增殖有较好的抑制效果,具有较好的抗肿瘤药物的开发利用前景。
[0007]
本发明采用的技术方案:
[0008]
本发明提供一种式ⅰ所示呋喃甲酰胺基β
‑
咔啉类化合物:
[0009][0010]
式ⅰ中r基为单取代或多取代,所述r基为甲氧基、卤素或硝基;所述卤素为氟、氯或溴。
[0011]
进一步,所述r基优选为4
‑
甲氧基、2
‑
氟基、3
‑
氟基、4
‑
氟基、2
‑
氯基、3
‑ꢀ
氯基、4
‑
氯
基、2
‑
硝基、3
‑
硝基、4
‑
硝基、2,4
‑
二氟基、2,6
‑
二氟基、4
‑
溴基。
[0012]
本发明还提供一种所述呋喃甲酰胺基β
‑
咔啉类化合物的制备方法,所述方法包括如下步骤:
[0013]
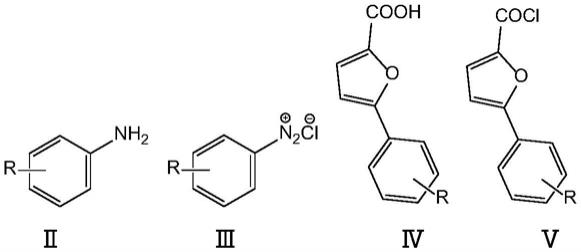
(1)式ⅱ化合物与hcl和nano2,0~5℃反应,制备式ⅲ化合物反应液;向式ⅲ化合物反应液中加入2
‑
呋喃甲酸丙酮溶液、氯化铜二水合物水溶液,0~5℃下反应6小时,随后再在室温下反应16小时,纯化分离得到式ⅳ化合物;
[0014]
(2)在二氯甲烷和氯化亚砜存在下,式ⅳ化合物,45℃下回流反应生成式
ⅴ
化合物;
[0015]
(3)在二氯甲烷、三乙胺存在下,式
ⅴ
化合物与9h
‑
吡啶[3,4
‑
b]吲哚(β
‑ꢀ
咔啉),室温反应结束后,除去反应溶剂,用体积浓度50%乙酸乙酯水溶液萃取后,水相用乙酸乙酯萃取,乙酸乙酯相用饱和食盐水洗涤后无水硫酸钠干燥,以体积比8:1的石油醚/乙酸乙酯为洗脱剂进行硅胶柱层析,收集rf值为0.3的组分,得到式ⅰ化合物;
[0016][0017][0018]
式ⅱ中r基为单取代或多取代,所述r基为甲氧基、卤素或硝基;所述卤素为氟、氯或溴;式ⅲ、ⅳ和
ⅴ
中r同式ⅱ中r。
[0019]
本发明制备呋喃甲酰胺基β
‑
咔啉类化合物的反应式为:
[0020][0021]
本发明所述呋喃甲酰胺基β
‑
咔啉类化合物的制备方法,具体按如下步骤进行:
[0022]
(1)化合物ⅳ的制备:将式ii化合物加入质量浓度15%的盐酸水溶液,置于冰水混合物中充分搅拌直至对甲氧基苯胺完全溶解,随后在0~5℃下滴加质量浓度30%的亚硝酸钠水溶液,滴加完毕后,搅拌15分钟,获得含式ⅲ化合物的反应液;往含式ⅲ化合物的反应液中加入2
‑
呋喃甲酸的丙酮溶液和氯化铜二水合物的去离子水溶液,0~5℃下反应6小时,随后再在室温(25
‑
30℃)下反应16 小时;反应结束后,抽滤,滤饼用水洗涤后再用饱和碳酸氢钠水溶液溶解至ph 为7~8,随后加入盐酸酸化直至无固体析出,过滤,收集滤饼,干燥(优选50
‑
90℃) 后,得到式ⅳ化合物;所述盐酸水溶液体积用量以式ii化合物重量计为2
‑
10ml/g,优选5
‑
6ml/g;所述亚硝酸钠水溶液体积用量以式ii化合物重量计为2
‑
10ml/g,优选4
‑
5ml/g;所述2
‑
呋喃甲酸与式ii化合物重量比为1:0.5
‑
2.0,优选1:1;所述丙酮体积用量以式ii化合物重量计为2
‑
10ml/g,优选5
‑
6ml/g;所述氯化铜二水合物与式ii化合物重量比为0.1
‑
1.0,优选1:0.5;所述去离子水体积用量以式ii化合物重量计为2
‑
10ml/g,优选4
‑
5ml/g;
[0023]
(2)化合物
ⅴ
的制备:将式ⅳ化合物加入二氯甲烷和氯化亚砜中,在45℃下回流反应2小时后用旋转蒸发仪除去反应溶剂,得到式
ⅴ
化合物,无需进一步分离纯化;所述二氯甲烷总体积用量以式ⅳ化合物重量计为100
‑
300ml/g,优选 200ml/g;所述氯化亚砜体积用量以式ⅳ化合物重量计为1
‑
10ml/g,优选5ml/g;
[0024]
(3)化合物i的制备:加入二氯甲烷溶解步骤(2)全部式
ⅴ
化合物,随后缓慢滴加用二氯甲烷和三乙胺溶解的9h
‑
吡啶[3,4
‑
b]吲哚(β
‑
咔啉),室温下搅拌, tlc监测反应进程(展开剂:石油醚/乙酸乙酯体积比为1/1),反应结束后用旋转蒸发仪除去反应溶剂,加入体积浓度50%乙酸乙酯水溶液进行萃取,水相再用乙酸乙酯萃取(优选3次),乙酸乙酯相用饱和食盐水洗涤后无水硫酸钠干燥,硅胶柱层析(洗脱剂为体积比8:1的石油醚/乙酸乙酯),收集rf值为0.3的组分,浓缩至干,得到式i化合物;所述二氯甲烷总体积用量以式ⅳ化合物重量计为10
‑
100 ml/g,优选41ml/g;所述三乙胺体积用量式以ⅳ化合物重量计为0.1
‑
1.0ml/g,优选0.5ml/g;所述9h
‑
吡啶[3,4
‑
b]吲哚与式ⅳ化合物重量比为1:0.5
‑
1.5,优选 1:0.8。
[0025]
本发明还提供一种所述呋喃甲酰胺基β
‑
咔啉类化合物在制备肿瘤细胞增殖抑制剂中的应用。
[0026]
进一步,所述肿瘤细胞包括a549人非小细胞肺癌细胞、hepg2人肝癌细胞、 mcf
‑
7人乳腺癌细胞、hala人宫颈癌细胞、caco
‑
2人克隆结肠腺癌细胞或hct
‑
116人结肠癌细胞。
[0027]
进一步,肿瘤细胞为a549人非小细胞肺癌细胞时,r为4
‑
meo、2
‑
no2、 4
‑
no2、2,4
‑
di
‑
f;肿瘤细胞为hepg2人肝癌细胞或mcf
‑
7人乳腺癌细胞时,r 为4
‑
meo、4
‑
cl、4
‑
no2;肿瘤细胞为hala人宫颈癌细胞时,r为4
‑
meo、4
‑
cl、 2
‑
no2、4
‑
no2;肿瘤细胞为caco
‑
2人克隆结肠腺癌细胞时,r为4
‑
meo、3
‑
f、 2,4
‑
f;肿瘤细胞为hct
‑
116人结肠癌细胞时,r为4
‑
meo、3
‑
f、2
‑
cl、4
‑
cl、 4
‑
no2。
[0028]
本发明还提供一种所述呋喃甲酰胺基β
‑
咔啉类化合物在制备抗肿瘤药物中的应用。
[0029]
进一步,所述抗肿瘤药物为治疗非小细胞肺癌、肝癌、乳腺癌、宫颈癌、结肠腺癌或结肠癌的药物。
[0030]
与现有技术相比,本发明具有如下有益效果:
[0031]
本发明公开一种结构新颖的呋喃甲酰胺基β
‑
咔啉类化合物,具有良好的生物活性,对多种癌细胞的增殖活性有明显的抑制活性。所述呋喃甲酰胺基β
‑
咔啉类化合物的制备方法简单,产率较高。所述呋喃甲酰胺基β
‑
咔啉类化合物在临床上可作为治疗包括非小细胞肺癌、肝癌、乳腺癌、宫颈癌、结肠腺癌和结肠癌在内的恶性肿瘤药物,拓展了呋喃和咔啉类结构在肿瘤抑制剂方面的应用前景。
附图说明
[0032]
图1为实施例1中目标产物(
ⅰ‑
1)核磁氢谱图,仪器型号bruker avance drx spectrometer at 600mhz。
[0033]
图2为实施例1中目标产物(
ⅰ‑
1)核磁碳谱图,仪器型号bruker avance drxspectrometer at 600mhz。
具体实施方式
[0034]
下面结合具体实施例对本发明作进一步的解释说明,但具体实施例并不对本发明作任何限定。除非特别说明,实施例中所涉及的试剂、方法均为本领域常用的试剂和方法。
[0035]
本发明所述室温为25
‑
30℃。
[0036]
实施例1:(5
‑
(4
‑
甲氧基苯基)呋喃
‑2‑
基)(9h
‑
吡啶并[3,4
‑
b]吲哚
‑9‑
基)甲酮(i
‑
1) 的制备
[0037][0038]
(1)化合物
ⅳ‑
1的制备
[0039]
在250ml的单口瓶中加入5.6g对甲氧基苯胺(ii
‑
1)以及30ml的质量浓度15%的盐酸水溶液,置于冰水混合物中充分搅拌直至对甲氧基苯胺完全溶解。随后 0~5℃滴加25ml的质量浓度30%的亚硝酸钠水溶液,滴加完毕后,搅拌15分钟,获得含(
ⅲ‑
1)化合物的反应液。往含(
ⅲ‑
1)化合物的反应液中加入 5.6g(0.05mol)2
‑
呋喃甲酸的30ml丙酮溶液和3g氯化铜二水合物的20ml去离子水溶液,0~5℃下反应6小时,随后再在室温下反应16小时。反应结束后,抽滤分离出悬浮的固体,滤饼用水洗涤后再用饱和碳酸氢钠水溶液溶解至ph为7~ 8,随后加入盐酸酸化直至无固体析出,最终过滤,收集滤饼,80℃干燥后,得到棕黄色固体5.34g,即为5
‑
(4
‑
甲氧基苯基)呋喃
‑2‑
羧酸(
ⅳ‑
1),质量产率51.6%。产物无需进一步纯化,可直接用于下一步反应。
[0040]
(2)化合物(
ⅴ‑
1)的制备
[0041]
在100ml的两口烧瓶里加入200mg的5
‑
(4
‑
甲氧基苯基)呋喃
‑2‑
羧酸(
ⅳ‑
1) 和20ml的二氯甲烷和1ml(13mmol)的氯化亚砜,在45℃下回流反应2小时后用旋转蒸发仪除去反应溶剂,得到褐色油状物
ⅴ‑
1,化合物
ⅴ‑
1对水敏感,无需进一步分离纯化;
[0042]
(3)化合物(i
‑
1)的制备
[0043]
加入6.4ml的二氯甲烷溶解步骤(2)全部化合物
ⅴ‑
1。随后缓慢滴加用2ml 二氯甲烷和0.1ml三乙胺溶解的168.2mg(1mmol)9h
‑
吡啶[3,4
‑
b]吲哚,室温下搅拌,tlc监测反应进程(展开剂:石油醚/乙酸乙酯体积比为1/1)。反应结束后旋蒸除去反应溶剂,加入10ml水和10ml乙酸乙酯进行萃取,水相再用乙酸乙酯 (10ml)萃取3次,合并乙酸乙酯相,饱和食盐水洗涤后无水硫酸钠干燥。最后硅胶柱层析(洗脱剂为体积比8:1的石油醚/乙酸乙酯),收
集rf值为0.3的组分,浓缩至干,得到160mg的黄色固体,即为化合物i
‑
1,质量产率44.9%,核磁氢谱见图1,核磁碳谱见图2。
[0044]
同样条件下,分别将步骤(1)中ii
‑
1中4
‑
meo替换为表1中r;分别制备得到产物i
‑
2~i
‑
13,详情见表1和表2。
[0045]
表1式ⅰ所示化合物的理化常数及高分辨质谱数据
[0046][0047]
表2式i所示化合物的核磁共振氢谱和核磁共振碳谱数据
[0048]
[0049]
[0050][0051]
实施例2、式ⅰ所示呋喃甲酰胺基β
‑
咔啉类化合物对肿瘤细胞的细胞毒性
[0052]
1、人非小细胞肺癌细胞a549
[0053]
细胞株:人非小细胞肺癌细胞a549,购自购自南京凯基生物科技发展有限公司。
[0054]
受试化合物:实施例1制备的式i
‑
1~i
‑
13化合物,用pbs(购自碧云天生物,上海)配制成浓度10mm的溶液。
[0055]
试验方法:采用cck
‑
8(四唑单钠盐)法,进行化合物的抗细胞增殖活性试验。
[0056]
a549细胞用含10%小牛血清的rpmi 1640培养基在37℃、5%co2饱和湿度的条件下培养。取对数生长期的细胞,加入10%小牛血清(购自gbico)的 rpmi 1640培养基(购自gbico),以1
×
105/ml密度接种于96孔培养板中,每孔100μl,在37℃、5%co2饱和湿度的条件下培养,分为对照组、空白组、实验组。实验组中加入不同的受试化合物,终浓度分别为50μm、25μm、5μm、1μm、 0.5μm、0.1μm;空白组给予等体积的pbs,对照组分别加入50μm、25μm、5μm、 1μm、0.5μm、0.1μm、0.01μm的多柔比星(dox)和喜树碱(cpt)。培养48h,加入10μl cck
‑
8工作液(购自碧云天生物,上海),放入恒温箱孵育20min后,在酶标仪上于波长450nm处读取
吸光度,计算化合物对细胞增殖的抑制率,结果见表3。
[0057]
根据下式计算抑制率:
[0058]
抑制率=(对照组od值
‑
实验组od值)/(对照组od值
‑
空白组od值)
×
100%
[0059]
由表3数据可知:针对a549细胞,i
‑
1、i
‑
8、i
‑
10、i
‑
11有较强的细胞毒作用,其它化合物基本没有明显细胞毒活性。
[0060]
2、其他肿瘤细胞
[0061]
将步骤1中a549细胞分别替换为hepg2人肝癌细胞、mcf
‑
7人乳腺癌细胞、hala人宫颈癌细胞、caco
‑
2人克隆结肠腺癌细胞和hct
‑
116人结肠癌细胞 (均购自南京凯基生物科技发展有限公司),每种细胞培养时均按常规方法,在培养基中添加含10%小牛血清,其中hepg2培养基为1640培养基;mcf
‑
7培养基为1640培养基;hala培养基为dmem培养基(购自gibco);caco
‑
2培养基为dmem培养基(购自gibco);hct
‑
116培养基为1640培养基。其他操作同步骤1,结果见表3所示,表明化合物
ⅰ‑
1有较为广谱的抗癌细胞增殖活性,有开发为抗肿瘤药物的前景。
[0062]
表3式ⅰ所示化合物及两个阳性对照药对六种癌细胞的ic
50
(μm)测定
[0063][0064]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1