PM
pm
2.5
致呼吸系统损伤的检测方法
技术领域
1.本发明涉及生物医药领域,主要是涉及甲基转移酶dnmt1、dnmt3a和dnmt3b在pm
2.5
致呼吸系统损伤的检测。
背景技术:
2.大气细颗粒物(fine particulate matter,pm
2.5
)是指空气动力学直径≤2.5μm的大气悬浮颗粒物。pm
2.5
是大气污染物中危害性极大的成分,流行病学研究发现,pm
2.5
每升高10μg/m3,全因死亡率、肺心病死亡率、肺癌死亡率分别增加4%、6%和8%;目前研究发现,pm
2.5
对呼吸系统的损伤机制主要包括氧化应激、炎症反应、免疫损伤、dna损伤、细胞周期阻滞、细胞凋亡、细胞自噬、细胞焦亡等。但具体机制有待进一步研究发现,对其深入研究具有极高的环境卫生学意义。
3.随着表观遗传学研究的不断深入,大量研究发现在pm
2.5
相关的毒性损伤中常涉及特定基因和/或全基因组甲基化水平异常。dna甲基化是由dna甲基转移酶(dna methyltransferase,dnmt)催化完成的。哺乳动物细胞中已知有活性的dnmt有3种,它们是dnmt1、dnmt3a和dnmt3b。dnmt1的主要功能是作为dna复制复合物(dna synthesome)中的组分,催化子链dna半甲基化位点甲基化,维持复制过程中甲基化位点的遗传稳定性;dnmt3a和dnmt3b主要催化从头甲基化,以非甲基化的dna为模板,催化新的甲基化位点形成,在胚胎发育中起重要作用。人群流行病学研究也证实短期或者长期吸入pm
2.5
可导致机体dna甲基化水平的改变。这提示pm
2.5
诱导的dna甲基化异常可能是pm
2.5
相关毒性损伤发生发展过程中的重要环节。
4.非专利文献《particulate matter
‑
induced senescence of skin keratinocytes involves oxidative stress
‑
dependent epigenetic modifications》中研究了pm
2.5
暴露对dnmt1、dnmt3b和tet1产生影响进而影响皮肤衰老,未涉及dnmt3a以及呼吸系统损伤的研究。
5.非专利文献《repeated pm2.5 exposure inhibits beas
‑
2b cell p53 expression through ros
‑
akt
‑
dnmt3b pathway
‑
mediated promoter hypermethylation》中研究了pm
2.5
暴露对dna甲基化的影响,但结果表明pm
2.5
对dnmt1和dnmt3b产生影响,但对dnmt3a的表达无明显影响,并且pm
2.5
暴露时间较短。
6.而本申请是基于pm
2.5
致呼吸系统损伤研究进一步认识其分子机制,以dnmt1、dnmt3a和dnmt3b作为pm
2.5
致呼吸系统损伤的生物标志物为pm
2.5
致呼吸系统损伤的检测提供理论基础和指导意义。
技术实现要素:
7.本发明的第一方面,提供了一种pm
2.5
致呼吸系统损伤的生物标志物,所述的生物标志物为dna甲基化转移酶,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
8.优选的,所述的呼吸系统损伤选自由氧化应激、炎症反应、免疫损伤、dna损伤、细胞周期阻滞、细胞凋亡、细胞自噬或细胞焦亡导致的呼吸系统损伤。
9.优选的,所述的呼吸系统损伤为肺损伤。
10.本发明所述的各生物标志物均可单独作为诊断或评估pm
2.5
致呼吸系统损伤的依据。
11.优选的,pm
2.5
致呼吸系统损伤诊断的依据为各dna甲基化转移酶或其组合的表达量的多少或编码各dna甲基化转移酶或其组合的mrna的表达量的多少。
12.本发明的第二方面,提供了一种检测生物标志物的试剂在制备诊断/预防pm
2.5
致呼吸系统损伤的产品中的应用,或者,在诊断呼吸系统损伤与否、解释呼吸系统损伤病因、筛选治疗或预防pm
2.5
致呼吸系统损伤的药物及为临床治疗提供决策支持的产品中的应用。
13.优选的,所述的试剂选自探针组、引物组、试剂盒、蛋白芯片、基因芯片或药物。
14.优选的,所述的引物组包含seq id no:7
‑
12或seq id no:19
‑
24所示序列。
15.优选的,所述的生物标志物为dna甲基化转移酶,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
16.在本发明的一个具体实施方式中,所述的检测生物标志物的试剂为检测各dna甲基化转移酶或其组合或编码各dna甲基化转移酶或其组合的mrna的表达量的试剂。
17.本发明的第三方面,提供了一种筛选用于治疗或预防pm
2.5
致呼吸系统损伤的药物的方法,包括如下步骤:
18.a)将生物样品置于pm
2.5
染毒剂量且存在候选药物的条件下培养;
19.b)将生物样品置于pm
2.5
染毒剂量且不存在候选药物的条件下培养;
20.c)检测步骤a)和步骤b)的生物样品中的pm
2.5
致呼吸系统损伤的生物标志物或编码生物样品中的pm
2.5
致呼吸系统损伤的生物标志物的mrna的表达水平;
21.或者c)确定生物样品在步骤a)和步骤b)两种情况下的呼吸系统炎症因子以及动物死亡率变化,以此结果指示候选药物是否可以用于治疗或预防pm
2.5
致呼吸系统损伤。
22.优选的,所述的呼吸系统炎症因子选自il
‑
6、tnf
‑
α或il
‑
1β。
23.优选的,所述的生物样品为动物模型,进一步优选的,所述的动物模型选自大鼠、小鼠、兔或猴。
24.本发明的第四方面,提供了生物标志物在制备诊断pm
2.5
致呼吸系统损伤的产品中的应用,所述的生物标志物为dna甲基化转移酶,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
25.优选的,所述的呼吸系统损伤选自由氧化应激、炎症反应、免疫损伤、dna损伤、细胞周期阻滞、细胞凋亡、细胞自噬或细胞焦亡导致的呼吸系统损伤。
26.优选的,所述的呼吸系统损伤为肺损伤。
27.本发明的第五方面,提供了一种检测pm
2.5
致呼吸系统损伤的生物标志物的试剂,所述的生物标志物为dna甲基化转移酶,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合;或者,所述的试剂选自探针组、引物组、蛋白芯片、基因芯片或试剂盒。
28.优选的,所述的引物组包含seq id no:7
‑
12或seq id no:19
‑
24所示序列。
29.本发明的第六方面,提供了一种治疗或预防pm
2.5
致呼吸系统损伤的药物,所述的
药物以上述各生物标志物或生物标志物的组合作为靶点。
30.本发明的第七方面,提供了一种探针组,所述探针组检测dna甲基化转移酶或编码dna甲基化转移酶的mrna,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
31.优选的,根据上述dna甲基化转移酶或编码上述dna甲基化转移酶的mrna通过公知、通用的方法设计合成或选择合适的探针分子,对目的蛋白进行特异性捕获或对目的片段进行特异性捕获、扩增、测序,以达到检测样本的目的。
32.优选的,所述的检测dna甲基化转移酶的探针选自与pm
2.5
致呼吸系统损伤的生物标志物特异性结合的抗原、抗体、酶、吸水或疏水物质、结合阳离子或阴离子的化学集团、受体或免疫复合物。
33.本发明所述的dna甲基化转移酶或各dna甲基化转移酶的组合或编码dna甲基化转移酶的mrna或编码各dna甲基化转移酶的mrna的组合可以用于治疗或预防pm
2.5
致呼吸系统损伤的药物的筛选。
34.本发明的第九方面,提供了一种含有本发明所述的探针组的芯片,所述的芯片为基因芯片或蛋白芯片。
35.优选的,所述的芯片还包括固相载体。进一步优选的,所述的固相载体选自硝酸纤维素膜、尼龙膜、聚苯乙烯、玻璃片、硅片或聚丙烯膜中的一种或两种以上的组合。
36.优选的,所述探针固定在固相载体上的方法选自原位合成法、点样法或其他固定方法。
37.其中,将芯片中的探针固定在所述的固相载体上。优选的,将探针序列密集有序地排列固定在固相载体预先设置的区域内,形成微型检测器件。
38.本发明的第十方面,提供了一种检测pm
2.5
致呼吸系统损伤的试剂盒,所述的试剂盒中包含检测生物标志物的表达量的试剂,所述生物标志物为dna甲基化转移酶,优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
39.优选的,所述的生物标志物的表达量为生物标志物的mrna或蛋白的表达量。
40.优选的,所述的呼吸系统损伤选自由氧化应激、炎症反应、免疫损伤、dna损伤、细胞周期阻滞、细胞凋亡、细胞自噬或细胞焦亡导致的呼吸系统损伤。
41.优选的,所述的呼吸系统损伤为肺损伤。
42.本发明的第十一方面,提供了一种所述的含有探针组的试剂盒的制备方法,包括:
43.1)根据上述pm
2.5
致呼吸系统损伤的标志物选择相应的探针分子;
44.2)为步骤1)获得的探针分子加上生物素标记;
45.3)配制所需杂交液和/或缓冲液和/或洗涤液。
46.本发明的第十二方面,提供了一种pm
2.5
致呼吸系统损伤的检测方法,所述的检测方法包括检测编码pm
2.5
致呼吸系统损伤的生物标志物的mrna表达量,优选的,所述的生物标志物为dna甲基化转移酶,进一步优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
47.优选的,所述的检测方法包括:
48.(1)提取肺部细胞或组织中总rna;
49.(2)以步骤(1)获得的总rna为模板进行cdna逆转录,并扩增获得目的基因;
50.(3)对步骤(2)获得的cdna进行荧光定量rt
‑
pcr,采用2
‑
δδct法对编码pm
2.5
致呼吸系统损伤的生物标志物的mrna进行相对定量分析。
51.本发明的第十三方面,提供了一种pm
2.5
致呼吸系统损伤的检测方法,所述的检测方法包括检测pm
2.5
致呼吸系统损伤的生物标志物的表达量,优选的,所述的生物标志物为dna甲基化转移酶,进一步优选的,所述的dna甲基化转移酶选自dnmt1、dnmt3a或dnmt3b中的一种或两种以上的组合。
52.优选的,所述的检测方法包括:
53.(1)提取肺部细胞或组织蛋白;
54.(2)采用bicinchoninicacid(bca)蛋白定量法测定蛋白浓度;
55.(3)采用western blot蛋白免疫印迹法检测pm
2.5
致呼吸系统损伤的生物标志物表达量;
56.本发明的第十四方面,提供了一种本发明所述的探针组、或本发明所述的基因芯片或蛋白芯片,或本发明所述的试剂盒在制备检测/预防pm
2.5
致呼吸系统损伤的产品中的应用,或者,在诊断呼吸系统损伤与否、解释呼吸系统损伤病因、筛选治疗或预防pm
2.5
致呼吸系统损伤的药物及为临床治疗提供决策支持的产品中的应用。
57.本发明所述的产品包括本发明所述的试剂,优选的,所述的产品选自探针组、引物组、试剂盒、基因芯片、蛋白芯片或药物。
58.优选的,所述的引物组包含seq id no:7
‑
12或seq id no:19
‑
24所示序列。
59.本发明所述的“呼吸系统”为人体与外界空气进行气体交换的一系列器官的总称,包括鼻、咽、喉、气管、支气管及由大量的肺泡、血管、淋巴管、神经构成的肺,以及胸膜等组织。临床上常将鼻、咽、喉称为上呼吸道,气管以下的气体通道(包括肺内各级支气管)部分称为下呼吸道。
60.本研究从表观遗传层面发现dna甲基化转移酶可作为pm
2.5
致呼吸系统损伤的检测指标,以dnmt1、dnmt3a和dnmt3b作为pm
2.5
致呼吸系统损伤的生物标志物为pm
2.5
致呼吸系统损伤的检测提供理论基础和指导意义。
61.以上只是概括了本发明的一些方面,不是也不应该认为是在任何方面限制本发明。
62.本说明书提到的所有专利和出版物都是通过参考文献作为整体而引入本发明的。本领域的技术人员应认识到,对本发明可作某些改变并不偏离本发明的构思或范围。
63.下面的实施例进一步详细说明本发明,不能认为是限制本发明或本发明所说明的具体方法的范围。
附图说明
64.以下,结合附图来详细说明本发明的实施例,其中:
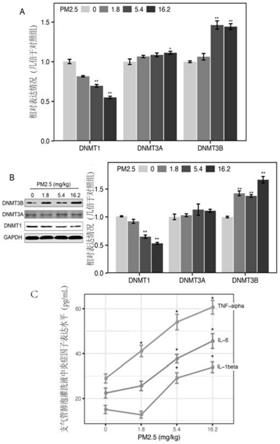
65.图1:pm
2.5
染毒30天后sd大鼠肺组织检测结果,其中,a为sd大鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测结果,b为sd大鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b蛋白表达检测结果,c为sd大鼠肺泡灌洗液炎症因子检测结果;
66.图2:pm
2.5
染毒30天后sd大鼠肺组织在暴露停止后的6、12、18个月的检测结果,其中,a为sd大鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测结果,b、c为sd大
鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b蛋白表达检测结果;
67.图3:pm
2.5
染毒24h后,beas
‑
2b细胞检测结果,其中,a为beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测结果,b为beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a和dnmt3b蛋白表达检测结果,c为beas
‑
2b细胞中炎症因子il
‑
6和tnf
‑
α的mrna表达情况,d为beas
‑
2b细胞上清炎症因子il
‑
6和tnf
‑
α表达水平检测结果。
68.图4:pm
2.5
连续染毒30代次beas
‑
2b细胞模型,其中,a为pm
2.5
染毒24h对细胞存活率的影响;b
‑
g为beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a、dnmt3b和炎症因子il
‑
6和tnf
‑
α蛋白表达检测结果。
具体实施方式
69.下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
70.在下述每一实施例中,设备和材料是从以下所指出的几家公司获得:
71.spf级雄性sd大鼠购自北京维通利华实验动物有限公司;
72.细胞株购于美国组织培养库(americantissueculturecollection,atcc);
73.procartaplex multiplex immunoassays试剂盒购自thermofisher(生物公司完成)
74.direct
‑
zolrnaminiprep试剂盒购自zymo research,货号:r2050;
75.premixextaqtmⅱ试剂盒购自takara;货号:rr820a
76.mrna逆转录试剂盒购自takara。货号:r2050;rr037a
77.dnmt3b抗体购自abcam,货号:ab79822
78.dnmt3a抗体购自proteintech,货号:20954
‑1‑
ap
79.dnmt1抗体购自proteintech,货号:24206
‑1‑
ap
80.tnf
‑
α抗体购自cst,货号:6945
81.il
‑
6抗体购自novus,货号:nb600
‑
1131
82.anti
‑
rabbit igg(h+l)(dylight
tm
680 conjugate)购自cst,货号:5366
83.human il
‑
6quantikine elisakit购自r&d systems,货号:d6050
84.human tnf
‑
alpha quantikine elisakit购自r&d systems,货号:dta00d
85.实施例1pm
2.5
重复剂量暴露sd大鼠实验设计
86.选择spf级雄性sd大鼠,6周龄,体重200
±
20g。饲养条件:每笼3只大鼠,饲养于首都医科大学实验动物房,每周更换2
‑
3次垫料,自由饮食、饮水。实验动物房温度24℃
±
1℃,湿度50%
±
5%,饲养房内每天光照时间12h,24h不间断通风。
87.pm
2.5
染毒剂量根据who给出的pm
2.5
年平均浓度过渡时期目标
‑
1(it
‑
1)限值、大鼠的体重、呼吸量、呼吸次数以及毒理学外推安全系数计算得出(表1),单位体重每天pm
2.5
暴露剂量为1.8mg/kg,中等剂量和高剂量分别确定为低剂量的3倍和9倍,即5.4mg/kg和16.2mg/kg。
88.表1体内实验染毒剂量推算
[0089][0090]
采用非暴露式支气管滴注:支气管镜配合导针将pm
2.5
悬液定向滴入大鼠气管。具体操作如下:
[0091]
①
每次气管滴注前12h对大鼠禁食,不禁水;
[0092]
②
10%的水合氯醛以0.3ml/100g进行腹腔注射麻醉;
[0093]
③
待大鼠无明显挣扎时,将大鼠仰面吊牙固定于操作台上,使用镊子将舌头拉出,暴露咽喉深部,通过喉镜定位会厌软骨开口处,将套有软导丝的软质塑料插管插入气道;
[0094]
④
将导丝拔出,使用配套注射器将定量好的pm
2.5
悬液沿塑料插管缓缓推入气道,完成滴注;
[0095]
⑤
待大鼠清醒后自由进食饮水;
[0096]
⑥
滴注过程中注意:使用棉签将大鼠口内分泌物清理干净,导丝尽量少露出软管,防止对大鼠的会厌及气管造成机械损伤。
[0097]
实验设计如图1所示,将大鼠随机分为对照、低、中、高(1.8、5.4和16.2mg/kg)剂量染毒组,每组8
‑
10只,根据大鼠体重,分别滴入等体积的生理盐水和pm
2.5
悬液,每三天滴注一次,重复滴注10次,即染毒时间共30天,最后一次滴注完成48h后处死大鼠,检测滴注完成时pm
2.5
的各项肺毒性指标;随后将中剂量组(5.4mg/kg)和生理盐水对照组各30只大鼠进行常规饲养,分别在滴注染毒完成后的6、12和18个月,每个时间点处死8只/组,以观察重复染毒停止后pm
2.5
的长期毒性效应。
[0098]
(1)sd大鼠肺泡灌洗液炎症因子检测
[0099]
sd大鼠采血处死之后,打开胸腔,暴露气管,采用止血钳夹紧右肺主支气管,对左肺进行灌洗。采用5ml无菌注射器从主支气管缓慢推入灭菌生理盐水3ml,缓慢反复抽吸3次,将样本在4℃,1500rpm离心5min,分装于离心管中冻存于
‑
80℃备用。
[0100]
使用procarta plex multiplex immunoassay试剂盒检测肺泡灌洗液中促炎因子(tnf
‑
α、il
‑
6和il
‑
1β)。
[0101]
测定原理:procarta plex multiplex immunoassay试剂盒采用液相芯片实现多重检测的基础。通过独有的微球表面化学技术,实现了在96/384孔板的每一个单孔中同时检测多个指标的研究。对每一个微球进行2
‑
3种荧光染料的着色,通过精确的染料比例产生100
‑
500种不同的微珠,每一种颜色的微珠上偶联一种特异性的蛋白抗体。检测时,不同颜色的微珠上偶联针对不同待测分析物的特异性“捕获”抗体,通过最终荧光标记的“检测”抗体(双抗夹心原理),通过平台,轻松实现对单个样本中的多种待测分析物的精确
检测。
[0102]
具体步骤如下:
[0103]
①
试剂稀释:
[0104]
wash buffer(10
×‑1×
):采用ddh2o进行9:1稀释;
[0105]
beads(50
×‑1×
):将beads涡旋30s,每管50
×
beads各取出100μl,加入1
×
wash buffer至最终体积5ml,混匀;
[0106]
detection antibody(50
×‑1×
):每管50
×
detection antibody各取60μl,加入detection antibody diluent至最终体积3ml。
[0107]
②
溶解标准品
[0108]
1)将标准品取出,2000g离心10s;
[0109]
2)向标准品管中各自加入50μl的universal assay buffer;
[0110]
3)轻轻混匀30s;
[0111]
4)置于冰上5
‑
10min;
[0112]
5)将标准品混合到一管里,加入universal assay buffer,最终获得250μl混合标准品,具体混合情况如表2所示。
[0113]
表2标准品混合情况
[0114][0115]
③
标准品的稀释
[0116]
1)取出试剂盒中提供的pcr 8联管用于稀释标准品;
[0117]
2)向第一管中加入200μl的混合标准品做为标准品1;
[0118]
3)向管2
‑
8中分别加入150μl的universalassay buffer;
[0119]
4)从管1中取50μl混合标准品加入管2中,上下吹打10次混匀,尽量避免气泡的产生;
[0120]
5)更换新的枪头,从管2中吸取50μl的稀释标准品转移到管3中,上下吹打10次混匀。依次转移,完成混合标准品的梯度稀释,置于冰上备用。
[0121]
④
准备微球:
[0122]
1)涡旋微球30s;
[0123]
2)向96孔板中的每孔中加入50μl预混微球;
[0124]
3)将96孔板放入磁性分离板中,确保孔板被牢牢卡住。待板静止2min,让微球沉底。然后将磁板快速倒置,倒出孔板中的液体。此过程中不可将96孔板从磁性分离板中取出;
[0125]
4)向每孔中加入150μl 1x的wash buffer,静置30s,然后将磁板倒置,倒出孔板中的液体;
[0126]
5)在倒置的状态下,用纸巾吸附孔板表面的残留液体,其中,所述的微球已分别偶联tnf
‑
α抗体、il
‑
6抗体和il
‑
1β抗体。
[0127]
⑤
微球与样本孵育:
[0128]
1)每孔中分别加入25μl的universal assay buffer;
[0129]
2)向指定的孔中分别加入25μl的标准品或样本;
[0130]
3)向空白对照中加入25μluniversalassay buffer;
[0131]
4)孔板封膜,500rpm室温下震荡孵育30min,于4℃静置过夜。第二天取出,500rpm室温下震荡孵育30min。
[0132]
⑥
洗板:
[0133]
1)将96孔板置于磁性分离板中,静置2min;
[0134]
2)轻轻去除封膜,避免液体飞溅,将孔板中的液体倒置去掉;
[0135]
3)向每孔中加入150μl 1x wash buffer,静置30s,将孔板中的液体倒置去掉。重复步骤,共洗3次;
[0136]
4)最后一次清洗结束时,用纸巾吸附残留液体。
[0137]
⑦
加入detectionantibody:
[0138]
1)向每孔中加入25μl 1x detection antibody混合液;
[0139]
2)使用新的封膜密封孔板;
[0140]
3)将96孔板从磁性分离板中取出,至于孔板荡器中500rpm室温震荡30min。
[0141]
⑧
洗板:重复步骤
⑥
。
[0142]
⑨
加入sa
‑
pe:
[0143]
1)向每孔中加入50μl sa
‑
pe,使用新的密封膜密封孔板;
[0144]
2)将96孔板从磁性分离板中取出,至于孔板荡器中500rpm室温震荡30min。
[0145]
⑩
洗板:重复步骤
⑥
。
[0146]
上机检测:
[0147]
1)向每孔中加入120μlreading buffer;
[0148]
2)使用新的密封膜密封孔板;
[0149]
3)将96孔板从磁性分离板中取出,至于孔板震荡器中500rpm室温震荡5min;
[0150]
4)轻轻去除密封膜,采用luminex 200instrument(luminex corporation,austin,tx)仪器中读数,获得tnf
‑
α、il
‑
6和il
‑
1β表达情况。
[0151]
(2)sd大鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测
[0152]
1)总rna的提取:本实验使用direct
‑
zol rnaminiprep试剂盒和trizol试剂。
[0153]
实验步骤:
[0154]
①
每只sd大鼠的肺组织取大约30mg,放入研磨器中,并加入300μl的trizol试剂,置于冰上充分研磨,12000r/min,4℃离心5min,取上清液,转移至1.5ml的离心管内;
[0155]
②
加入与上清液等量的无水乙醇充分混匀;
[0156]
③
将充分混匀的液体加入direct
‑
zol rnaminiprep试剂盒的纯化柱中,12000r/min,4℃离心5min;
[0157]
④
加入400μl的rna洗液,12000r/min,4℃离心5min,重复2次;
[0158]
⑤
按dnase稀释液:dnaseⅰ=45μl:5μl,配制dnase孵育混合物,在每个纯化柱中加
入50μl的dnase孵育混合物,室温孵育15min;
[0159]
⑥
孵育结束后每个纯化柱中加入400μl的rna前洗液,12000r/min,4℃离心5min;
[0160]
⑦
随后每个纯化柱中加入400μl的rna洗液,12000r/min,4℃离心5min;
[0161]
⑧
扭掉纯化柱的盖子,将纯化柱套在新的1.5ml洗脱管上,每个纯化柱中加入20
‑
50μl的depc水,12000r/min,4℃离心5min,收集离心液;
[0162]
⑨‑
80℃保存或者立刻进行mrna的cdna逆转录。
[0163]
2)肺组织mrna的cdna逆转录:采用mrna逆转录试剂盒,以样本总rna的mrna为模板,在逆转录酶的作用下,将mrna逆转录成cdna,再以cdna为模板扩增,得到目的基因。按试剂盒说明书,配制逆转录体系如表3所示,其中*表示10μl逆转录体系中total rna最大为500ng。
[0164]
表3 mrna逆转录体系
[0165][0166][0167]
反应条件:
[0168]
37℃15min(逆转录反应)
[0169]
85℃5sec(逆转录酶的失活反应)
[0170]
4℃
[0171]
3)肺组织的cdna荧光定量rt
‑
pcr:肺组织cdna荧光定量rt
‑
pcr采用premix ex taq tmⅱ试剂盒,荧光定量pcr包括变性
‑
退火
‑
延伸三个基本步骤。经过反复的变性
‑
退火
‑
延伸循环,可以得到更多的“半保留复制链”,新合成链可以参与到下一次的循环,最后基因可以扩增到几百万倍以上,实现目的基因体外扩增。荧光定量rt
‑
pcr按试剂盒说明书,配制反应体系如表4所示:
[0172]
表4 rt
‑
pcr体系
[0173][0174]
反应条件:
[0175]
预变性:1个循环95℃30sec
[0176]
pcr反应:40个循环95℃5sec
[0177]
60℃30sec
[0178]
融解曲线:95℃60sec
[0179]
55℃30sec
[0180]
95℃30sec
[0181]
在荧光定量pcr仪的系统上进行数据收集,采用2
‑
δδct法进行数据的相对定量分析(以gapdh的表达量为内参),实验中所用到的引物序列(pcr forward primer及pcr reverse primer)如表5所示。
[0182]
表5大鼠肺组织相关基因引物序列
[0183][0184]
(3)sd大鼠肺组织甲基转移酶dnmt1、dnmt3a和dnmt3b蛋白表达检测
[0185]
1)肺组织蛋白提取:将
‑
80℃冰箱中冻存的肺组织取出,置于冰上保存,使用电子天平快速称取50mg的组织,放入2ml的圆底离心管中,用剪刀将组织剪碎,加入500μl预冷的蛋白裂解液(含蛋白酶和蛋白磷酸酶抑制剂),置于冰上使用研磨器匀浆,之后将组织匀浆液移至预冷的1.5ml的离心管中,12000rpm,4℃,离心5min,上清液即为肺组织蛋白提取物,将上清液移至新的预冷的离心管内,进行蛋白定量。
[0186]
2)蛋白浓度测定:采用bicinchoninicacid(bca)蛋白定量法测定蛋白浓度,将bca碱性溶液a与硫酸铜溶液b(50:1的体积比)配制成工作液,充分混匀备用。制作bca标准曲线,将蛋白标准品按照0,1,2,4,6,8,10μl的量分别加入到标准孔中,每组2个复孔,不足10μl加去离子水补齐至10μl;将待测样品每组2个复孔,加入到96孔板中;最后在标准品孔和待测样品孔中分别加入200μl的bca工作液,37℃温箱中孵育30min,酶标仪562nm处检测各孔的吸光度值。根据标准孔的吸光度值制作标准曲线,根据标准曲线公式计算出待测样品的蛋白浓度。将5
×
的上样缓冲液与蛋白提取样品(1:4)充分混匀,并在100℃金属浴中10min进行蛋白变性,将变性后的蛋白分装,储存于
‑
80℃备用。
[0187]
3)dnmt1、dnmt3a和dnmt3b表达检测:
[0188]
①
制胶:按比例配制分离胶,缓缓地摇动溶液进行混合,将分离胶溶液平缓地注入两层玻璃板中,在胶液面上小心注入一层去离子水,以阻止氧气进入分离胶溶液中,静置40min使分离胶凝固。同前按比例配制浓缩胶,混匀溶液时不要过于剧烈以免引入过多的氧气。倒掉玻璃板中的水,连续平稳的注入浓缩胶溶液,然后小心插入梳子并注意不得在齿尖留有气泡,静制20min以上保证浓缩胶凝固以及分离胶和浓缩胶完全聚合;
[0189]
②
加样:依次加入标准品(marker)和待分析样品(加样时间要尽量短,以免样品扩散)可在未加样的孔中加入等量的样品缓冲液,可避免边缘效应。每个泳道加入10μl待测样品;
[0190]
③
电泳:加样完毕后,选择80v恒压进行电泳,电泳直至溴酚蓝染料进入分离胶,并且可以看到marker在分离胶中分离出清晰的分子量指示条带(一般约20min),更换至140v恒压电泳,电泳直至溴酚蓝染料移至分离胶末端处,停止电泳(一般约为1.5h);
[0191]
④
转膜:将电泳完毕的胶完整的放在盛有电转液的玻璃皿中,将目的蛋白所在区域切下,测量其长宽,并记录。按胶的尺寸剪nc膜和滤纸(滤纸长宽较凝胶大0.5
‑
1cm,nc膜
长宽较凝胶大0.5cm),滤纸在电转液中充分浸湿,nc膜放入新配好的含10%甲醇的电转液中充分浸透。按如下顺序制作“三明治”,从正极到负极按如下顺序排列:正极;海绵;双层滤纸;nc膜;凝胶;双层滤纸;海绵;负极。(其中不能留有气泡)卡紧转膜板,电转槽中倒满新的含10%甲醇的电转液,将转膜板浸入电转槽中(注意正负极要正确),插上电源,电转槽放入事先准备的冰盒内,设定恒流300ma转膜90
‑
120min(根据分子量大小调整转膜时间);
[0192]
⑤
封闭:转膜之后将nc膜放入5%脱脂奶粉封闭液中(不加tween
‑
20),摇床震动,70r/min,室温封闭1.5h;
[0193]
⑥
一抗孵育:按相应抗体的效价配制一抗稀释液,将封闭后的膜放入孵育盒内,加入配好的一抗,4℃摇床过夜,其中,所述的一抗分别为dnmt3b抗体、dnmt3a抗体和dnmt1抗体;
[0194]
⑦
二抗孵育:一抗孵育结束后用tbst洗涤膜10min,3次。按相应二抗的效价配制二抗稀释液。nc膜放入二抗中,室温摇床70r/min避光孵育1h。孵育结束后用tbst洗涤10min,3次,洗涤全程避光进行,其中,所述的二抗为anti
‑
rabbit igg(h+l);
[0195]
⑧
曝光:使用odyssey clx红外荧光扫描成像系统进行曝光处理,先开仪器,再开软件。开机后进行初始化,该段时间不要进行其他操作。将nc膜放在扫描平面上,用吸水纸将大部分液体洗去,避免液体渗入仪器内部。扫描结束后,在扫描平面上滴去离子水并用无尘纸擦拭晾干。扫描结果导出用image j软件进行分析。
[0196]
(4)动物实验结果
[0197]
如图1所示,pm
2.5
染毒30天后sd大鼠肺组织dnmt1的mrna和蛋白表达量呈剂量依赖性下调且中、高剂量组与对照组相比差异有统计学意义(p<0.05);dnmt3a的mrna表达呈剂量依赖性上调,高剂量组与对照组相比差异有统计学意义(p<0.05),而蛋白表达量表达无明显变化;dnmt3b的mrna和蛋白表达量呈剂量依赖性上调且中、高剂量组与对照组相比差异有统计学意义(p<0.05),dnmt3b的mrna表达量的低剂量组与对照组相比差异也有统计学意义(p<0.05)。il
‑
6、tnf
‑
α和il
‑
1β的表达量呈剂量依赖性上调。这表明pm
2.5
可通过影响sd大鼠肺组织甲基转移酶的表达进而激活下游炎症信号通路,诱导炎症因子的表达,引起肺部炎症损伤。
[0198]
如图2所示,在暴露停止后的6、12个月时间点,暴露组dnmt1的mrna和蛋白水平在暴露组显著高于对照组,并且随时间推移呈下调趋势(p<0.05),在暴露停止后的18个月时间点,两组相比没有显著性差异;dnmt3a的mrna和蛋白水平同样在6个月时间点高于对照(p<0.05),在12个月时间点dnmt3a的mrna较对照组低(p<0.05),蛋白表达较对照组高(p<0.05),在18个月时间点dnmt3a的mrna和蛋白表达均低于对照(p<0.05);在暴露停止后6个月时间点dnmt3b的mrna水平高于对照(p<0.05),蛋白表达无明显差异,在12、18个月时间点dnmt3b的mrna和蛋白水平均高于对照(p<0.05),在这表明pm
2.5
可持续影响sd大鼠肺组织甲基转移酶的表达。
[0199]
实施例2 pm
2.5
重复剂量暴露人支气管上皮细胞实验
[0200]
(1)本研究采用人支气管上皮细胞(beas
‑
2b)作为体外细胞实验模型。
[0201]
1)细胞复苏:实验前超净工作台紫外消毒30min,所需试剂放入37℃水浴加热,超净台中点燃酒精灯。取出液氮中冻存的细胞,在37℃水浴中快速解冻,并转移至已预热的完全培养液(含10%胎牛血清、100u/ml青霉素和100μg/ml链霉素的dmem)中,用移液枪缓慢吹
匀,1200r/min,室温离心3min,弃上清,完全培养液重悬后种于100mm培养皿内,放入37℃、5%co2的细胞培养箱中进行培养,24h后更换新的完全培养液继续培养。待细胞密度达到培养皿底面积的90%时,用预热的胰蛋白酶(不含edta)消化细胞1
‑
2min,使细胞松动脱落,加入完全培养液去消化,并将脱落的细胞转移至无菌离心管中,1200r/min,室温离心3min,弃上清后用完全培养液重悬,以1:3的比例进行传代。
[0202]
2)细胞传代:实验前超净工作台紫外消毒30min,所需试剂放入37℃水浴加热。超净台中点燃酒精灯,弃去原培养液,无菌pbs洗2遍,用移液枪彻底吸干净残留的pbs,加入1ml胰蛋白酶(不含edta)消化细胞1
‑
2min,使细胞松动脱落,加入完全培养液去消化,并将脱落的细胞转移至无菌离心管中,1200r/min,室温离心3min,弃上清后用完全培养液重悬,重悬后种于100mm培养皿内,放入37℃、5%co2的细胞培养箱中进行培养,24h后观察细胞密度,若需传代则以1:3的比例进行传代,新复苏的细胞需传代3次以上才可用于后续实验检测。
[0203]
3)细胞冻存:实验前超净工作台紫外消毒30min,所需试剂放入37℃水浴加热。超净台中点燃酒精灯,弃去原培养液,无菌pbs洗2遍,用移液枪彻底吸干残留的pbs,加入1ml胰蛋白酶(不含edta)消化细胞1
‑
2min,使细胞松动脱落,加入完全培养液去消化,并将脱落的细胞转移至无菌离心管中,1200r/min,室温离心3min,弃上清。按胎牛血清:二甲基亚砜=9:1的体积比,配制细胞冻存液,每管1.5ml细胞冻存液,按需配制,细胞重悬于冻存液中并分装于冻存管内,梯度降温之后保存于液氮中。
[0204]
4)细胞实验分组和染毒:细胞实验分组根据cck
‑
8实验结果得出。确定本研究pm
2.5
浓度采用0、6.25、12.5、25、50、100μg/ml。当人支气管上皮细胞密度达到培养皿底面积的80%时,即可染毒。染毒前将pm
2.5
母液先超声15min,随后将母液进行稀释,配制实验所需的不同浓度的染毒液。染毒前,超净工作台紫外消毒30min,所需试剂放入37℃水浴加热。弃去原培养液,无菌pbs洗2遍,移液枪彻底吸干净pbs,然后加入配好的染毒液,放入37℃、5%co2的细胞培养箱,染毒培养24h。
[0205]
5)采用不同浓度的pm
2.5
分别暴露于人正常肺支气管上皮beas
‑
2b细胞24h后,其存活率变化如图4a所示。beas
‑
2b细胞存活率在50、100、200μg/ml处理组与对照组相比存在显著差异(p<0.05)。说明pm
2.5
可以剂量依赖性地降低beas
‑
2b细胞的存活率。此外,根据此结果,本研究选择了25μg/ml,即无可见有害作用水平,作为beas
‑
2b细胞pm
2.5
长期暴露模型的暴露剂量。
[0206]
(2)beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测
[0207]
1)总rna的提取:
[0208]
①
细胞种板:取对数生长期的beas
‑
2b细胞,消化后接种到6孔板中,细胞浓度为5
×
105个/孔,每孔加入2ml细胞悬液,每组设置3
‑
6个平行复孔,放置在37℃、5%co2的细胞培养箱中培养24h;
[0209]
②
染毒:待细胞密度达到培养皿底面积的80%左右时,进行染毒操作。弃去原培养液,用pbs洗2次。根据实验设计,向6孔板中加入不含血清的dmem配制成的不同浓度的pm
2.5
染毒液(0、25、50、100μg/ml),37℃、5%co2的细胞培养箱中培养24h;
[0210]
③
本实验使用direct
‑
zol rnaminiprep试剂盒和trizol试剂。弃去染毒液,psb洗两次,彻底吸干孔内pbs,每孔加入300μl的trizol试剂,置于冰上进行晃动,充分裂解细胞
5min;
[0211]
④
将孔内trizol液体移入1.5ml离心管中,加入等量的无水乙醇充分混匀;
[0212]
⑤
将充分混匀的液体加入direct
‑
zol rnaminiprep试剂盒的纯化柱中,12000r/min,4℃离心5min;
[0213]
⑥
加入400μl的rna洗液,12000r/min,4℃离心5min,重复2次;
[0214]
⑦
按dnase稀释液:dnaseⅰ=45μl:5μl,配制dnase孵育混合物,在每个纯化柱中加入50μl的dnase孵育混合物,室温孵育15min;
[0215]
⑧
孵育结束后每个纯化柱中加入400μl的rna前洗液,12000r/min,4℃离心5min;
[0216]
⑨
随后每个纯化柱中加入400μl的rna洗液,12000r/min,4℃离心5min;
[0217]
⑩
扭掉纯化柱盖子,将纯化柱套在新的1.5ml洗脱管上,每个纯化柱中加入20
‑
50μl的depc水,12000r/min,4℃离心5min,收集离心液;
[0218]
‑
80℃保存或者立刻进行mrna的cdna逆转录。
[0219]
2)beas
‑
2b细胞mrna的cdna逆转录:采用mrna逆转录试剂盒,以样本总rna的mrna为模板,在逆转录酶的作用下,将mrna逆转录成cdna,再以cdna为模板扩增,得到目的基因。具体操作步骤同大鼠肺组织中mrna的cdna逆转录。
[0220]
3)beas
‑
2b细胞mrna的cdna荧光定量rt
‑
pcr:采用premix ex taq tmⅱ试剂盒,以样本总rna的mrna为模板,在逆转录酶的作用下,将mrna逆转录成cdna,再以cdna为模板扩增,得到目的基因,即编码dnmt1、dnmt3a和dnmt3b的基因。按试剂盒说明书,配制逆转录体系如表6所示,其中,*表示10μl逆转录体系中total rna最大为500ng。
[0221]
表6:逆转录体系配置情况
[0222][0223]
反应条件:
[0224]
37℃15min(逆转录反应)
[0225]
85℃5sec(逆转录酶的失活反应)
[0226]
4℃
[0227]
3)beas
‑
2b细胞cdna荧光定量rt
‑
pcr:荧光定量rt
‑
pcr采用premix ex taq tmⅱ试剂盒,荧光定量pcr包括变性
‑
退火
‑
延伸三个基本步骤。经过反复的变性
‑
退火
‑
延伸循环,可以得到更多的“半保留复制链”,新合成链可以参与到下一次的循环,最后基因可以扩增到几百万倍以上,实现目的基因体外扩增。荧光定量rt
‑
pcr按试剂盒说明书,配制反应体系如表7所示:
[0228]
表7:荧光定量rt
‑
pcr反应体系配置情况
[0229][0230][0231]
反应条件:
[0232]
预变性:1个循环95℃30sec
[0233]
pcr反应:40个循环95℃5sec
[0234]
60℃30sec
[0235]
融解曲线:95℃60sec
[0236]
55℃30sec
[0237]
95℃30sec
[0238]
在荧光定量pcr仪的系统上进行数据收集,采用2
‑
δδct法进行数据的相对定量分析(以gapdh的表达量为内参)。
[0239]
(3)beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a和dnmt3b蛋白表达检测
[0240]
1)beas
‑
2b细胞全蛋白提取:
[0241]
①
细胞传代:取对数生长期的人支气管上皮细胞,消化后接种到100mm的培养皿中,细胞浓度为7
×
105个/皿,每皿加入1ml细胞悬液,完全培养液补足至10ml,放置在37℃、5%co2的细胞培养箱中,培养24h;
[0242]
②
染毒:待细胞密度达到培养皿底面积的80%左右时,进行染毒操作。弃去原培养液,用pbs洗2次。根据实验设计,每个剂量组3皿细胞,保证细胞量,向培养皿中加入不含血清的dmem配制成的不同浓度的pm
2.5
染毒液(0、25、50、100μg/ml)10ml,放置在37℃、5%co2的细胞培养箱中培养24h;
[0243]
③
将细胞从培养箱取出,置于冰上,用冷pbs洗两遍,彻底吸干净皿内洗液,加入200μl预冷的蛋白裂解液(含蛋白酶和蛋白磷酸酶抑制剂),在冰上用细胞刮将培养皿内的细胞刮下,随后转移至预冷的1.5ml的离心管中,每间隔15min,剧烈震荡15sec,在冰上充分裂解30min,之后12000r/min,4℃,离心5min,上清液即为蛋白提取物,将上清液移至新的预冷的离心管内,进行蛋白定量。
[0244]
2)蛋白浓度测定:采用bicinchoninicacid(bca)蛋白定量法测定蛋白浓度,将bca碱性溶液a与硫酸铜溶液b(50:1的体积比)配制成工作液,充分混匀备用。制作bca标准曲线,将蛋白标准品按照0,1,2,4,6,8,10μl的量分别加入到标准孔中,每组2个复孔,不足10μl加去离子水补齐至10μl;将待测样品每组2个复孔,加入到96孔板中;最后在标准品孔和待测样品孔中分别加入200μl的bca工作液,37℃温箱中孵育30min,酶标仪562nm处检测各孔的吸光度值。根据标准孔的吸光度值制作标准曲线,根据标准曲线公式计算出待测样品的蛋白浓度。将5
×
的上样缓冲液与蛋白提取样品(1:4)充分混匀,并在100℃金属浴中10min进行蛋白变性,将变性后的蛋白分装,储存于
‑
80℃备用。
[0245]
3)dnmt1、dnmt3a和dnmt3b表达检测:
[0246]
①
制胶:按比例配制分离胶,缓缓地摇动溶液进行混合,将分离胶溶液平缓地注入两层玻璃板中,在胶液面上小心注入一层去离子水,以阻止氧气进入分离胶溶液中,静置40min使分离胶凝固。同前按比例配制浓缩胶,混匀溶液时不要过于剧烈以免引入过多的氧气。倒掉玻璃板中的水,连续平稳的注入浓缩胶溶液,然后小心插入梳子并注意不得在齿尖留有气泡,静制20min以上保证浓缩胶凝固以及分离胶和浓缩胶完全聚合;
[0247]
②
加样:依次加入标准品(marker)和待分析样品(加样时间要尽量短,以免样品扩散)可在未加样的孔中加入等量的样品缓冲液,可避免边缘效应。每个泳道加入10μl待测样品;
[0248]
③
电泳:加样完毕后,选择80v恒压进行电泳,电泳直至溴酚蓝染料进入分离胶,并且可以看到marker在分离胶中分离出清晰的分子量指示条带(一般约20min),更换至140v恒压电泳,电泳直至溴酚蓝染料移至分离胶末端处,停止电泳(一般约为1.5h);
[0249]
④
转膜:将电泳完毕的胶完整的放在盛有电转液的玻璃皿中,将目的蛋白所在区域切下,测量其长宽,并记录。按胶的尺寸剪nc膜和滤纸(滤纸长宽较凝胶大0.5
‑
1cm,nc膜长宽较凝胶大0.5cm),滤纸在电转液中充分浸湿,nc膜放入新配好的含10%甲醇的电转液中充分浸透。按如下顺序制作“三明治”,从正极到负极按如下顺序排列:正极;海绵;双层滤纸;nc膜;凝胶;双层滤纸;海绵;负极。(其中不能留有气泡)卡紧转膜板,电转槽中倒满新的含10%甲醇的电转液,将转膜板浸入电转槽中(注意正负极要正确),插上电源,电转槽放入事先准备的冰盒内,设定恒流300ma转膜90
‑
120min(根据分子量大小调整转膜时间);
[0250]
⑤
封闭:转膜之后将nc膜放入5%脱脂奶粉封闭液中(不加tween
‑
20),摇床震动,70r/min,室温封闭1.5h;
[0251]
⑥
一抗孵育:按相应抗体的效价配制一抗稀释液,将封闭后的膜放入孵育盒内,加入配好的一抗,4℃摇床过夜,其中,所述的一抗分别为dnmt3b抗体、dnmt3a抗体和dnmt1抗体;
[0252]
⑦
二抗孵育:一抗孵育结束后用tbst洗涤膜10min,3次。按相应二抗的效价配制二抗稀释液。nc膜放入二抗中,室温摇床70r/min避光孵育1h。孵育结束后用tbst洗涤10min,3次,洗涤全程避光进行,其中,所述的二抗为anti
‑
rabbit igg(h+l);
[0253]
⑧
曝光:使用odyssey clx红外荧光扫描成像系统进行曝光处理,先开仪器,再开软件。开机后进行初始化,该段时间不要进行其他操作。将nc膜放在扫描平面上,用吸水纸将大部分液体洗去,避免液体渗入仪器内部。扫描结束后,在扫描平面上滴去离子水并用无尘纸擦拭晾干。扫描结果导出用image j软件进行分析。
[0254]
(4)beas
‑
2b细胞炎症因子il
‑
6和tnf
‑
α检测
[0255]
1)上清elisa实验
[0256]
elisa检测步骤:分别使用human il
‑
6quantikine elisa kit和human tnf
‑
alpha quantikine elisakit进行实验。首先,取染毒结束后各组细胞的上清样本,1200rpm,4℃离心5min置于冰上待用;将所有试剂平衡至室温并充分混匀;按elisa试剂盒说明书将标准品进行梯度稀释;设置并记好样品孔,空白孔,用dilutionbuffer r稀释样本;样本100μl/孔添加至样品孔中;加入预先稀释好的生物素标记抗体50μl/孔;混匀后封膜密闭,在37℃条件下孵育1.5h;吸去孔内液体,添加洗液洗脱3次;洗板完成后向孔中加入预先稀释后的streptavidin
‑
hrp 100μl/孔;封膜密闭后在37℃条件下孵育1h;重复前述洗板步骤3次;终
止反应及显色,向孔中加入tmb 100μl/孔,在37℃条件下避光孵育20min,向孔中加入终止工作液100μl/孔;在450nm波长下上机检测。
[0257]
2)炎症因子il
‑
6和tnf
‑
α的mrna表达检测具体步骤与beas
‑
2b细胞甲基转移酶dnmt1、dnmt3a和dnmt3b的mrna表达检测一致,其中,所使用的il
‑
6的引物序列如seq id no:15、16所示,tnf
‑
α的引物序列如seq id no:17、18所示。
[0258]
本实施例中所用到的引物序列(pcr forward primer及pcr reverse primer)如表8所示。
[0259]
表8 beas
‑
2b细胞相关基因引物序列
[0260][0261]
(5)细胞实验结果
[0262]
如图3所示,pm
2.5
染毒24h后beas
‑
2b细胞dnmt1的mrna和蛋白表达量随着染毒浓度的升高呈下调趋势且差异有统计学意义(p<0.05);dnmt3a的mrna和蛋白表达量表达无明显变化;dnmt3b的mrna和蛋白表达量随着染毒浓度的升高呈上调趋势且差异有统计学意义(p<0.05),il
‑
6和tnf
‑
α的mrna表达量以及细胞上清液中的表达量均呈剂量依赖性上调(p<0.05)。这表明pm
2.5
可通过影响beas
‑
2b细胞甲基转移酶的表达进而激活下游炎症信号通路,诱导炎症因子的表达,引起炎症损伤。
[0263]
如图4所示pm
2.5
连续染毒30代次的beas
‑
2b细胞模型中,dnmt1蛋白表达量在10、20和30代次均呈现下调趋势差异无统计学意义;dnmt3a和dnmt3b蛋白表达量在10、20和30代次均呈上调,且30代次蛋白的表达量与其对照组差异有统计学意义(p<0.05),il
‑
6和tnf
‑
α蛋白的表达量在10、20和30代次均呈上调,其中il
‑
6在20和30代次蛋白的表达量与其对照组差异有统计学意义(p<0.05),tnf
‑
α在30代次蛋白的表达量与其对照组差异有统计学意义(p<0.05)。这表明pm
2.5
长期暴露可通过影响beas
‑
2b细胞甲基转移酶的表达进而激活下游炎症信号通路,诱导炎症因子的表达,引起炎症损伤。
[0264]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0265]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
[0266]
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1