一种荧光染料亚磷酰胺单体的制备方法与流程
1.本发明属于生物医学检测领域,涉及荧光染料的制备方法,具体涉及荧光素染料亚磷酰胺同分异构体的分离方法以及荧光素亚磷酰胺单体的合成方法。
背景技术:
2.荧光探针就是以荧光物质为指示剂,在一定波长激发下使荧光物质产生荧光,通过检测所产生的荧光对被检测物质进行定量或定性分析。在生物医学检测方面,荧光探针相对于其他检测法,具有高灵敏度,高选择性,响应快,重复性好,操作简便,成本低等优点,因而在分子诊断,基因检测,抗体免疫分析等方面得到广泛的应用。荧光探针由识别基团、荧光基团和连接体三部分组成,识别基团决定探针的选择性特异性,荧光基团决定探针的灵敏度,连接体部分在探针中起到连接枢纽的作用。荧光染料在荧光探针中都以荧光基团的身份存在,它的光物理性质是探针性能的重要体现。
3.目前,用于标记或衍生的荧光探针主要有罗丹明类、荧光素类、邻苯二甲醛类等,其中荧光素类化合物在生物研究领域中占有及其重要的位置。荧光素类染料化学合成方法简单,一般是通过富电子的间苯二酚与邻苯二甲酸酐在酸性条件下缩合而成,但是在合成过程中会产生5,6-羧基同分异构体(如下式),所以荧光素染料异构体的拆分是至关重要的。
[0004][0005]2’
,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(英文简称-joe)是荧光探针的一种常用的荧光素染料,它的激发/发射波长为520/550nm。衍生后的joe的亚磷酰胺单体可以直接用于dna自动合成仪上,用于修饰dna探针的5’端,同时joe也可以衍生化后负载于cpg或ps上,直接标记dna探针的3’端。但是不管修饰dna探针的任何位置,必须要用单一的异构体去衍生化,用单一的异构体去修饰,因为混合异构会对dna探针的纯化造成干扰。
[0006]
从分子结构上讲,joe属于呫吨染料类,呫吨类染料5,6-羧基异构体分离一般用方法如下:在异构混合物中加入乙醇溶解,加入二异丙胺与羧基成盐,零下20度放置24小时,有结晶固体析出,过滤收集固体得6-位异构体,纯度大于90%,然后用同样方法二次结晶,纯度提高到95%以上。我们在joe的5, 6-羧基异构体分离中,也尝试过该方法,但效果不佳,需要经过反复多次结晶也未能得到单一的6-羧基joe异构体。目前有报道(organic process research &development 2001,5,45-49),joe的5,6-羧基异构体的分离可以在joe稠环后的第一步反应,即化合物1合成后(如图1),采用硅胶柱层析分离得到6
‑ꢀ
羧基joe,但是这个方法中化合物1是个大极性物质,在硅胶上吸附较大,5, 6-羧基异构体的分
离收率低,这样的收率会对下游产品衍生化造成一定阻碍,不易于规模化生产。
[0007]
鉴于上述缺陷,设计一种简单易行、分离方便、收率提高的joe的5,6
‑ꢀ
同分异构体的分离方法以及joe的亚磷酰胺单体的合成方法,具有十分重要的意义。
技术实现要素:
[0008]
本发明要解决的技术问题是提供一种新的joe的5,6-同分异构体的分离方法,以及一种6-羧基joe亚磷酰胺单体的合成方法,以上方法简单,易于规模化生产。
[0009]
本发明所要解决的技术问题是通过以下技术方案来实现的:
[0010]
一种2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(joe)的5,6-羧基异构体的分离方法,包括如下步骤:
[0011]
s1、2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(joe)在稠环后衍生化得到化合物a;
[0012]
s2、将上述化合物a与羟基化合物反应生成两种异构体的活化酯,将活化酯通过纯化分离得到单一的6-joe活化酯。
[0013]
优选地,步骤s1中,稠环后衍生化的方法包括:称取一定量2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1),加入吡啶溶解,滴加特戊酰氯,低温反应至完全,加水淬灭,减压蒸除溶剂,残留物加入二氯甲烷,加水萃取分层,收集有机相,得到化合物a。
[0014]
优选地,步骤s2中,所述化合物a与羟基化合物的反应过程包括:称取步骤s1的粗品于一个干燥的烧瓶中,加入第一有机溶剂溶解,加入羟基化合物,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物经过纯化,分别收得5-joe活化酯和6-joe活化酯。
[0015]
优选地,所述步骤s1中,所述的低温为0-30℃。
[0016]
优选地,步骤s2中,所述的第一有机溶剂选自dmf,二氯甲烷,三氯甲烷,乙酸乙酯或乙腈中的任意一种。
[0017]
优选地,步骤s2中,所述的羟基化合物选自n-羟基琥珀酰亚胺,n-羟基邻苯酰亚胺,n-羟基-5-降冰片稀-2,3-二酰亚胺,苯酚,对硝基苯酚,邻硝基苯酚,四氯苯酚,五氟苯酚,2,3,5,6-四氟苯酚,2,4,5-三氯苯酚,3,5
‑ꢀ
二(三氟甲基)苯酚,2,6-二叔丁基-4甲氧基苯酚或3,5-双(三氟甲基)苯酚的任意一种。
[0018]
优选地,步骤s2中的反应过程中还包括缩合剂;优选地,所述的缩合剂在羟基化合物前加入;更优选地,缩合物选自dcc,edc,hobt,hbtu,hatu 或pybop中的任意一种。
[0019]
优选地,所述步骤s2中,纯化方法是柱层析纯化。
[0020]
作为本发明的另一技术方案,本发明还涉及一种2’,7
’‑
二甲氧基-4’,5
’‑
二氯 5(6-)羧基荧光素(joe)的亚磷酰胺单体的合成方法,包括如下步骤:
[0021]
s1、2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(joe)在稠环后衍生化成化合物a;
[0022]
s2、将上述化合物a与羟基化合物反应生成活化酯的两种异构体,将活化酯通过纯化方法分离得到单一的6-joe活化酯;
[0023]
s3、将上述步骤s2获得的6-joe活化酯与6-胺基-1-己醇进行衍生化反应,加水萃取分层,收集有机相,除去溶剂,残留物经过纯化,得到化合物b;
[0024]
s4、将步骤s3纯化后得到的化合物b与磷试剂、活化剂反应,加水萃取分层,收集有机相,除去溶剂,残留物经过纯化,即得2’,7
’‑
二甲氧基-4’,5
’‑ꢀ
二氯-6-荧光素亚磷酰胺单体。
[0025]
优选地,步骤s1中,稠环后衍生化的方法包括:称取一定量2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1),加入吡啶溶解,滴加特戊酰氯,低温反应至完全,加水淬灭,减压蒸除溶剂,残留物加入二氯甲烷,加水萃取分层,收集有机相,得到化合物a。
[0026]
优选地,步骤s2中,化合物a与羟基化合物的反应过程包括:称取步骤 s1的粗品于一个干燥的烧瓶中,加入第一有机溶剂溶解,加入羟基化合物,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物经过纯化,分别收得5-joe活化酯和6-joe活化酯。
[0027]
优选地,所述步骤s1中,所述的低温为0-30℃。
[0028]
优选地,步骤s2中,所述的第一有机溶剂选自dmf,二氯甲烷,三氯甲烷,乙酸乙酯或乙腈中的任意一种。
[0029]
优选地,步骤s2中,所述的羟基化合物选自n-羟基琥珀酰亚胺,n-羟基邻苯酰亚胺,n-羟基-5-降冰片稀-2,3-二酰亚胺,苯酚,对硝基苯酚,邻硝基苯酚,四氯苯酚,五氟苯酚,2,3,5,6-四氟苯酚,2,4,5-三氯苯酚,3,5
‑ꢀ
二(三氟甲基)苯酚,2,6-二叔丁基-4甲氧基苯酚或3,5-双(三氟甲基)苯酚的任意一种。
[0030]
优选地,步骤s2中,反应过程中还包括缩合剂;优选地,所述的缩合剂在羟基化合物前加入;更优选地,缩合物选自dcc,edc,hobt,hbtu,hatu 或pybop中的任意一种。
[0031]
优选地,步骤s2中,纯化方法是柱层析纯化。
[0032]
优选地,步骤s3中,衍生化反应过程包括:称取s2步骤中的6-joe活化酯于一个干燥的烧瓶中,加入二氯甲烷溶解,然后加入6-胺基-1-己醇,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物结晶纯化,即得化合物b。
[0033]
所述步骤s4的反应包括:称取s3步骤中的化合物b,加入一定量的第二有机溶剂溶解,然后加入一定量磷试剂和活化剂,室温搅拌反应,tlc监控,反应完成后,加水淬灭,萃取分层收集有机相,干燥后减压蒸除溶剂,残留物纯化得2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体。
[0034]
优选地,步骤s3以及步骤s4中,所述的纯化方法是结晶或柱层析。
[0035]
优选地,步骤s4中,所述的第二有机溶剂选自dmf,二氯甲烷,三氯甲烷,乙腈,乙酸乙酯中的任意一种。
[0036]
优选地,步骤s4中,所述的活化剂选自四氮唑,四氮唑二异丙基胺盐中的任意一种。
[0037]
优选地,本发明涉及的2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素亚磷酰胺单体合成步骤如下:
[0038]
(1)称取一定量2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素于一个干燥的烧瓶中,加入吡啶溶解,滴加特戊酰氯,0-25℃反应至完全,加水淬灭,减压蒸除溶剂,残留物加入二氯甲烷,加水萃取分层,收集有机相,粗品用于下步反应。
[0039]
(2)称取一定量2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯于一个干燥的烧瓶中,加入二氯甲烷溶解,依次加入缩合剂、n-羟基-5-降冰片稀
ꢀ‑
2,3-二酰亚胺,室
温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,分别收得2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素(5
‑ꢀ
降冰片稀基)活化酯和2’,7
’‑
二甲氧基-4’,5
’‑
二氯-5-荧光素(5-降冰片稀基)活化酯。
[0040]
(3)称取一定量2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯于一个干燥的烧瓶中,加入二氯甲烷溶解,然后加入6-胺基-1-己醇,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,得中间产物。
[0041]
(4)称取一定量中间产物于干燥的烧瓶中,加入一定量的第二有机溶剂溶解,然后加入一定量磷试剂和四氮唑,室温搅拌反应,tlc监控,反应完成后,加水淬灭,萃取分层收集有机相,干燥后减压蒸除溶剂,残留物柱层析纯化得 2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体。
[0042][0043]
与现有技术相比,本发明的有益效果是:本发明所提供的异构体拆分方法,能够获得单一的6-羟基joe异构体,简便易行、分离效率高、易于规模化生产;进一步地,将该异构体衍生化通过两步反应得到的6-joe亚磷酰胺单体,得到的荧光素染料单体的提取率高,作为荧光探针使用,标记效率高。
附图说明
[0044]
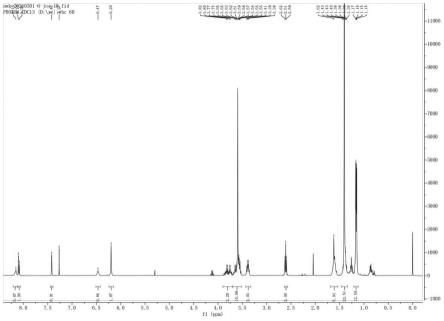
图1为2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体的氢谱;
[0045]
图2为2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体的磷谱。
具体实施方式
[0046]
为使本技术的目的、技术方案和优点更加清楚,下面将结合本技术具体实施例及附图对本技术技术方案进行清楚、完整地描述。显然,所描述的实施例仅是本技术一部分实施例,而不是全部的实施例,不用来限制本发明的范围。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
[0047]
实施例一
[0048]2’
,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素的5,6-羧基异构体的分离方法:
[0049]
(1)2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2):
[0050]
称取100克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1)于一个干燥的烧瓶中,加入600毫升吡啶溶解,滴加70克特戊酰氯,0℃反应至完全,加50毫升水淬灭,减压蒸除溶剂,残留物加入600毫升二氯甲烷,加水萃取分层,收集有机相,粗品用于下步反应。
[0051][0052]
(2)2’,7
’‑
二甲氧基-4’,5
’‑
二氯6-荧光素(5-降冰片稀基)活化酯(化合物 3a):
[0053]
称取90克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2) 于一个干燥的烧瓶中,加入750毫升乙酸乙酯溶解,依次加入24克dcc、21克 n-羟基-5-降冰片稀-2,3-二酰亚胺,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,分别收得40克2’,7
’‑
二甲氧基
ꢀ‑4’
,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯3a和45克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-5-荧光素(5-降冰片稀基)活化酯3b。其中:2’,7
’‑
二甲氧基-4’,5
’‑
二氯
ꢀ‑
6-荧光素亚磷酰胺单体的氢谱如图1所示;2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6
‑ꢀ
荧光素亚磷酰胺单体的磷谱如图2所示。
[0054][0055]
实施例二
[0056]2’
,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素的5,6-羧基异构体的分离方法:
[0057]
(1)2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2):
[0058]
称取100克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1)于一个干燥
的烧瓶中,加入600毫升吡啶溶解,滴加70克特戊酰氯,10℃反应至完全,加50毫升水淬灭,减压蒸除溶剂,残留物加入600毫升二氯甲烷,加水萃取分层,收集有机相,粗品用于下步反应。
[0059]
(2)2’,7
’‑
二甲氧基-4’,5
’‑
二氯6-荧光素(5-降冰片稀基)活化酯(化合物 3a):
[0060]
称取90克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2) 于一个干燥的烧瓶中,加入750毫升二氯甲烷溶解,依次加入24克hbtu、21克3, 5-二(三氟甲基)苯酚,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,分别收得40克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6
‑ꢀ
荧光素(5-降冰片稀基)活化酯3a和45克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-5-荧光素(5
‑ꢀ
降冰片稀基)活化酯3b。
[0061]
实施例三
[0062]2’
,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素亚磷酰胺单体的合成方法:
[0063]
(1)2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2):
[0064]
称取100克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1)于一个干燥的烧瓶中,加入600毫升吡啶溶解,滴加70克特戊酰氯,0℃反应至完全,加50毫升水淬灭,减压蒸除溶剂,残留物加入600毫升二氯甲烷,加水萃取分层,收集有机相,粗品用于下步反应。
[0065][0066]
(2)2’,7
’‑
二甲氧基-4’,5
’‑
二氯6-荧光素(5-降冰片稀基)活化酯(化合物 3a):
[0067]
称取90克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2) 于一个干燥的烧瓶中,加入750毫升乙酸乙酯溶解,依次加入24克dcc、21克 n-羟基-5-降冰片稀-2,3-二酰亚胺,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,分别收得40克2’,7
’‑
二甲氧基
ꢀ‑4’
,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯3a和45克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-5-荧光素(5-降冰片稀基)活化酯3b。
[0068][0069]
(3)称取40克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯于一个干燥的烧瓶中,加入250毫升二氯甲烷溶解,然后加入5克6-胺基-1-己醇,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物用乙酸乙酯/正己烷结晶纯化,
得25克化合物4。
[0070][0071]
(4)称取14.5克化合物4于干燥的烧瓶中,加入180毫升二氯甲烷,加入4.2 克四氮唑二异丙基胺盐,6.3克磷试剂2-氰乙基-n,n,n’,n
’‑
四异丙基亚磷酰二胺室温搅拌反应至完成后,加水淬灭,萃取分层收集有机相,干燥后减压蒸除溶剂,残留物柱层析纯化得16克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体。1h nmr(cdcl3)δ1.16(dd,12h),1.43(m,22h),1.62(m,4h),2.61(t,2h), 3.41(dd,2h),3.62(m,10h),3.7(m,2h),6.20(s,2h),6.47(m,1h),7.45(s,1h), 8.10(m,1h),8.16(m,1h)。31p nmr(cdcl3)δ147。
[0072][0073]
实施例四
[0074]2’
,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素亚磷酰胺单体的合成方法:
[0075]
(1)2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2):
[0076]
称取100克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素(化合物1)于一个干燥的烧瓶中,加入600毫升吡啶溶解,滴加70克特戊酰氯,20℃反应至完全,加50毫升水淬灭,减压蒸除溶剂,残留物加入700毫升二氯甲烷,加水萃取分层,收集有机相,粗品用于下步反应。
[0077][0078]
(2)2’,7
’‑
二甲氧基-4’,5
’‑
二氯6-荧光素(5-降冰片稀基)活化酯(化合物 3a):
[0079]
称取90克2’,7
’‑
二甲氧基-4’,5
’‑
二氯5(6-)羧基荧光素特戊酸酯(化合物2) 于一个干燥的烧瓶中,加入750毫升dmf溶解,依次加入24克edc、21克对硝基苯酚,室温反应至
完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物柱层析纯化,分别收得40克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯3a和45克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-5-荧光素(5-降冰片稀基) 活化酯3b。
[0080]
(3)称取40克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素(5-降冰片稀基)活化酯于一个干燥的烧瓶中,加入250毫升二氯甲烷溶解,然后加入5克6-胺基-1-己醇,室温反应至完全,加水淬灭,萃取分层,收集有机相,减压蒸除溶剂,残留物用乙酸乙酯/正己烷柱层析纯化,得25克化合物4。
[0081]
(4)称取14.5克化合物4于干燥的烧瓶中,加入180毫升三氯甲烷,加入4.2 克四氮唑,6.3克磷试剂2-氰乙基-n,n
’‑
二异丙基胺基氯化磷室温搅拌反应至完成后,加水淬灭,萃取分层收集有机相,干燥后减压蒸除溶剂,残留物柱层析纯化得16克2’,7
’‑
二甲氧基-4’,5
’‑
二氯-6-荧光素亚磷酰胺单体。1h nmr(cdcl3) δ1.16(dd,12h),1.43(m,22h),1.62(m,4h),2.61(t,2h),3.41(dd,2h),3.62(m, 10h),3.7(m,2h),6.20(s,2h),6.47(m,1h),7.45(s,1h),8.10(m,1h),8.16(m,1h)。 31p nmr(cdcl3)δ147。
[0082]
虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施方式中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
[0083]
上文所列出的一系列的详细说明仅仅是针对本发明的可行性实施方式的具体说明,它们并非用以限制本发明的保护范围,凡未脱离本发明技艺精神所作的等效实施方式或变更均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1