再生丝素蛋白/ε-聚赖氨酸复合水凝胶的制备方法及其产品和应用
再生丝素蛋白/
ε-聚赖氨酸复合水凝胶的制备方法及其产品和应用
技术领域
1.本发明涉及生物材料领域,具体涉及再生丝素蛋白/ε-聚赖氨酸复合水凝胶的制备方法,还涉及制得的再生丝素蛋白/ε-聚赖氨酸复合水凝胶和应用。
背景技术:
2.目前,蚕丝由于来源广、产量大、生物相容性好、可生物降解、可修饰等性质,因此正从传统的纺织领域向具有重要前景的仿生材料、生物医用材料和光电材料等诸多先进领域拓展,蚕丝经脱胶后可得到丝素纤维,将丝素纤维溶解得到的再生丝素蛋白经过各种加工工艺可得到各种形态的材料以更好的复合其应用场景,目前用再生丝素蛋白(rsf)的制备的材料形式主要有电纺膜、纳米颗粒、薄膜、水凝胶、微管、海绵状支架等;其中水凝胶形式的再生丝素蛋白材料具有柔软、保水、性状稳定、可修饰后功能化的特点,并且提供了一个可模拟细胞外基质的三维环境从而调节细胞的行为和组织功能,此外,再生丝素蛋白水凝胶还具有独特的生物降解性和生物相容性,因而在包括创伤修复等在内的生物医学方面具有重要的应用前景。
3.再生丝素蛋白水凝胶虽然有各种优点,但是作为一种非生物活性的结构蛋白,难以满足各种实际应用的需要。因此,急需改进再生丝素蛋白水凝胶的特性,以期达到创伤修复的效果。目前,研究工作者通常利用rsf和其他生物大分子如胶原蛋白、壳聚糖、羧甲基纤维素等交联制备水凝胶,未见直接利用rsf和ε-聚赖氨酸(ε-pll)制备水凝胶材料的报道。
技术实现要素:
4.有鉴于此,本发明的目的之一在于提供一种再生丝素蛋白/ε-聚赖氨酸复合水凝胶的制备方法,由于rsf分子中缺少高反应活性的氨基酸残基,因此制备rsf化学交联水凝胶的过程非常缓慢,为此采取的策略是将高浓度的rsf与ε-pll混合,为edc的交联提供更多的反应基团;本发明的目的之二在于提供由所述制备方法制得的再生丝素蛋白/ε-聚赖氨酸复合水凝胶;本发明的目的之三在于提供所述再生丝素蛋白/ε-聚赖氨酸复合水凝胶在制备创伤修复材料中的应用。
5.为达到上述目的,本发明提供如下技术方案:
6.1、再生丝素蛋白/ε-聚赖氨酸复合水凝胶的制备方法,将浓度高于55mg/ml的再生丝素蛋白与ε-聚赖氨酸充分混合,然后edc/nhs作为交联剂,充分混合发生交联得到再生丝素蛋白/ε-聚赖氨酸复合水凝胶。
7.本发明优选的,所述再生丝素蛋白与ε-聚赖氨酸的质量比为15:0~11:4。
8.本发明优选的,所述交联剂中加入edc后终浓度为0.04mg/ml,加入nhs后终浓度为0.04mg/ml。
9.本发明优选的,所述再生丝素蛋白的浓度为55~75mg/ml,所述ε-聚赖氨酸的浓度为0~20mg/ml。
10.本发明优选的,所述再生丝素蛋白与ε-聚赖氨酸的总浓度为75mg/ml。
11.本发明优选的,所述再生丝素蛋白与ε-聚赖氨酸的质量比为14:1~13:2。
12.2、由所述制备方法制得的再生丝素蛋白/ε-聚赖氨酸复合水凝胶。
13.3、所述再生丝素蛋白/ε-聚赖氨酸复合水凝胶在制备创伤修复材料中的应用。
14.本发明的有益效果在于:本发明制得的再生丝素蛋白/ε-聚赖氨酸复合水凝胶具有如下优点:
15.1)制备的水凝胶截面为典型的胶状物质的微观形貌,并且呈现了相对均一多孔的三维网状结构,而未加入交联剂的复合水凝胶制备体系样品并未显示出三维网状结构,而是片层的形貌。该结果表明交联剂edc/nhs成功将rsf和ε-pll之间交联从而形成了三维网状的骨架结构,而同时这个骨架又与周围的水分子相互作用制约水分子的运动从而成为水凝胶,这样的结构为养分、药物以及其他营养物质提供了通道,能与外界进行高效的物质交换,并具有良好的机械性能。
16.2)制备的复合水凝胶制备体系中加入交联剂edc/nhs从而使得样品从粘弹性液体转变为粘弹性固体,含少量ε-pll的水凝胶enrp141强度最高,为3848.69pa,而随着体系内ε-pll的继续增多,复合水凝胶的强度下降,enrp132和enrp114的水凝胶强度分别为580.9pa和33.48pa,与此相比,不含ε-pll的水凝胶enrp150强度最低,为5.37pa,并且其频率扫描的结果中g”值和g’值十分接近,这再一结果说明了纯rsf在edc/nhs交联后形成的水凝胶不稳定且强度低,表明在制备中加入ε-pll对制备更高强度且更稳定的水凝胶具有十分重要的意义。除此以外,振幅扫描的结果显示水凝胶能经受较大的形变,尤其是含有大量ε-pll的样品,其碎裂剪切应变显著增大并超过1000%,表明将其注射或将其像药膏一样挤出时水凝胶不容易碎裂成颗粒,这有利于其使用后能很好的贴合以及覆盖住创伤部位。
17.3)红外光谱测试,本发明制备的水凝胶rsf分子主要以α-螺旋/无规卷曲为主,在受到外力时分子链可以通过变形将能量储存,并且由于交联的键主要是分布均匀的酰胺键,因此在受到外力时不易断裂,三维网状结构将外力分散,所以水凝胶无色透明且具有弹性。
18.4)通过对水凝胶形成的时间作出统计,结果显示相对传统自组装的物理交联方式,利用交联剂edc/nhs的化学交联方式能极显著的缩短水凝胶形成时间,这意味着在相同的时间内能制备出更多的rsf/pll水凝胶,更具有工业化的前景。并且在含ε-pll的实验组样品中,少量的ε-pll能很好的和rsf交联形成三维网状结构,缩短水凝胶形成的时间,而更多的ε-pll在复合水凝胶制备体系内的引入反而会延长水凝胶形成的时间,但均短于利用纯rsf经交联剂edc/nhs化学交联制备水凝胶所需的时间。
19.5)制备的rsf/ε-pll复合水凝胶能有效地被多种蛋白酶降解,具备良好的生物降解性。并且降解速率高,复合水凝胶体系内rsf的无规卷曲高,以及结晶度低,因此酶切位点更容易暴露出,从而酶接触结合进行切割。因此制备的水凝胶在酶的作用下快速降解能,表明水凝胶并不会阻碍创伤修复过程中的组织再生和伤口收缩等过程。
20.6)对制备的rsf/ε-pll复合水凝胶的溶胀度进行研究,溶胀动力学结果显示前1h内复合水凝胶快速发生溶胀,此后溶胀速率减缓,然后在15h时基本达到溶胀平衡,且平衡溶胀度的结果显示制备的水凝胶具有较高的溶胀度,所有水凝胶平衡溶胀度超过250%,但是少量ε-pll的加入会导致水凝胶的平衡溶胀度下降,而随着水凝胶中ε-pll含量的增加,
水凝胶的平衡溶胀度会升高,这可能是因为少量ε-pll引入时,提供的氨基很好的rsf的羧基交联形成酰胺键,体系内极性基团减少,而当ε-pll继续增多时,未反应的亲水性氨基大量剩余,能够使水凝胶吸收更多的水分并增大溶胀度,并最终在ε-pll含量最高的水凝胶得到超过400%的溶胀度。水凝胶具备合适的溶胀度不仅有利于伤口的水化以及吸取多余的伤口渗出液,还能具备较好的粘性从而形成密闭的环境,防止伤口被外界微生物感染,并有利于血管和肉芽组织的生成。
21.7)对制备的rsf/ε-pll复合水凝胶的抗菌性进行探索,利用挖孔法将固体培养基去掉后填充制备的水凝胶,结果显示不含或者含少量ε-pll的水凝胶不具备明显的抑菌效果,而含大量ε-pll的水凝胶enrp114周围出现了抑菌圈,表明其对金黄色葡萄球菌和大肠杆菌dh5α具备明显的抑菌效果。因此,可以作为创伤修复材料。
22.8)制得的材料具有促进成纤维细胞的粘附作用,可能会加快成纤维细胞募集到伤口处,然后再在细胞因子ifn-γ、tgf-β的调节下,进行上皮化、血管形成以及肉芽组织的的生成,从而加快创伤修复。
23.9)制备的水凝胶中enrp132和enrp114对巨噬细胞无不良刺激,在创伤修复的炎症反应中理论上不会引起炎症反应加剧,有利于创伤修复的正常进行。
附图说明
24.为了使本发明的目的、技术方案和有益效果更加清楚,本发明提供如下附图进行说明:
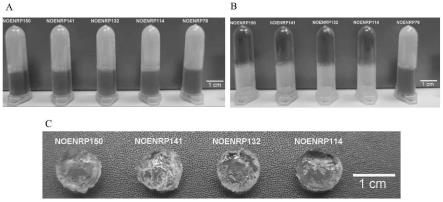
25.图1为rsf/ε-pll复合水凝胶的宏观形态(a:不含交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系;b:含有交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系;c:成功制备的rsf/ε-pll复合水凝胶的形态)。
26.图2为rsf/ε-pll复合合水凝胶的微观截面形貌(a:noenrp150的微观截面形貌;b:noenrp141的微观截面形貌;c:noenrp132的微观截面形貌;d:noenrp114的微观截面形貌;e:enrp150的微观截面形貌;f:enrp141的微观截面形貌;g:enrp132的微观截面形貌;h:enrp114的微观截面形貌)。
27.图3为rsf/ε-pll复合水凝胶的流变学表征(a:不含交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系样品的频率扫描;b:含交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系的频率扫描;c:不同水凝胶的硬度;d:不同水凝胶的振幅扫描;e:不同水凝胶的断裂剪切应变;f:enrp114的手指按压测试)。
28.图4为rsf/ε-pll复合水凝胶的红外光谱表征表征(a:所有样品的红外光谱原始数据;b:不含交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系样品的酰胺i分峰图;c:含交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系样品的酰胺i分峰图;d:原材料比例一致的样品的二级结构含量对比)。
29.图5为rsf/ε-pll复合水凝胶的形成时间。
30.图6为rsf/ε-pll复合水凝胶的生物降解性(a:样品在pbs、酶溶液中浸泡后质量变化;b:样品在胶原蛋白酶酶降解前后的截面微观形貌)。
31.图7为rsf/ε-pll复合水凝胶的溶胀度(a:各水凝胶样品在pbs中的溶胀动力学;b:各水凝胶样品的平衡溶胀度)。
32.图8为rsf/ε-pll复合水凝胶的抗菌性(a:rsf/ε-pll复合水凝胶对金黄色葡萄球菌的抑菌效果;b:rsf/ε-pll复合水凝胶对大肠杆菌dh5α的抑菌效果)。
33.图9为rsf/ε-pll复合水凝胶的促细胞粘附特性。
34.图10为rsf/ε-pll复合水凝胶的炎症反应(a:巨噬细胞raw264.7在各材质上的形态;b:巨噬细胞raw264.7在各材质上no的分泌量以及tnf-α、il-1β、il-6的表达量)。
具体实施方式
35.下面结合附图和具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好的理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
36.实施例1、rsf/ε-pll复合水凝胶制备
37.将再生丝素蛋白(rsf)和ε-聚赖氨酸(ε-pll)按照质量比分别为15∶0、14∶1、13∶2、11∶4、7∶8,并控制rsf和ε-pll的总浓度为75mg/ml,先加入rsf溶液后再加入ε-pll溶液,加ddh2o补足体积至820μl,将混合液旋转混合仪上翻转使体系充分混合,条件为4℃中,6rpm的条件下翻转10min;再向体系中加入100μl的10
×
pbs溶液,然后继续加入40μl的100mg/ml edc溶液和40μl的100mg/ml nhs溶液;继续在旋转混合仪上翻转使体系充分混合,条件为4℃中,6rpm的条件下翻转5min。
38.同时设置不含交联剂edc/nhs的体系为对照,区别是加入edc和nhs溶液换成等体积的ddh2o。
39.将含交联edc/nhs、rsf和ε-pll质量比为15∶0、14∶1、13∶2、11∶4、7∶8的复合水凝胶制备体系样品分别命名为enrp150、enrp141、enrp132、enrp114、enrp78,并作为以下实验组;将不含交联剂edc/nhs、rsf和ε-pll质量比为15∶0、14∶1、13∶2、11∶4、7∶8的水凝胶制备体系样品分别命名为noenrp150、noenrp141、noenrp132、noenrp114、noenrp78,并作为以下对照组。
40.本实施例中,即控制加入edc后终浓度为0.04mg/ml,加入nhs后终浓度为0.04mg/ml。再生丝素蛋白的浓度为55~75mg/ml,所述ε-聚赖氨酸的浓度为0~20mg/ml,可实现发明目的。
41.实施例2、复合水凝胶的表征
42.1)rsf/ε-pll复合水凝胶的宏观形态
43.将实施例1制备的样品置于-20℃冰箱内放置12h以上,将其取出后迅速打开离心管盖子并放入提前降温的冻干机内进行冻干,冻干的时间为48h;将冻干后的海绵状支架小心取出,用刀片小心在内部切出一块薄片,注意不要挤压截面导致发生变形;将薄片的样品平整粘附在含导电胶带的电镜样品台上,镀金90s;将电镜样品台正确放置后打开仪器进行观察,选取合适倍数进性拍照并保存图片。
44.结果如图1所示,结果显示不含交联剂edc/nhs的所有对照组样品在室温放置过夜后,仍然为液体状态,当试管倒置后,样品会像高粘度流体一样缓慢流动到底部(图1中a)。而含有交联剂edc/nhs的实验组样品(图1中b)中,除了enrp78未形成水凝胶外,其余的样品已经形成无色透明的水凝胶(体系内加入了少许溴酚蓝来作为标记),在试管倒置后,位于上方的试管底部,说明在交联剂为低浓度、缓冲液为pbs(ph 7.4)的条件下成功将rsf和ε-pll交联,制备出化学交联水凝胶。将enrp150、enrp141、enrp132、enrp114在形成水凝胶后
取出时的状态,相对均一且无色透明(图1中c)。因此,后续实验只使用rsf∶ε-pll为15∶0、14∶1、13∶2、11∶4这4个比例进行实验。
45.上述实验说明edc/nhs交联剂是形成水凝胶必须的,并且当rsf的浓度在35mg/ml时无法形成水凝胶,而在再生丝素蛋白浓度高于55mg/ml时能够形成水凝胶,表明再生丝素蛋白的浓度高于为55mg/ml即可实现发明目的,优选的再生丝素蛋白的浓度为55~75mg/ml,ε-聚赖氨酸的浓度为0~20mg/ml,可实现发明目的。
46.2)rsf/ε-pll复合水凝胶的微观截面形貌
47.将实施例1制备的样品置于-20℃冰箱内放置12h以上;将其取出后迅速打开离心管盖子并放入提前降温的冻干机内进行冻干,冻干的时间为48h;将冻干后的海绵状支架小心取出,用刀片小心在内部切出一块薄片,注意不要挤压截面导致发生变形;将薄片的样品平整粘附在含导电胶带的电镜样品台上,镀金90s;将电镜样品台正确放置后打开仪器进行观察,选取合适倍数进性拍照并保存图片,结果如图2所示。结果显示,rsf/ε-pll复合水凝胶样品横截面呈现出了典型的胶状物质的微观形貌(图2中e-h);对比不含交联剂edc/nhs的对照组样品(图2中a-d),除了rsf∶ε-pll为15∶0的体系样品微观形貌在加入交联剂后并没有显著的变化外,其余三个含ε-pll的样品在加入交联剂edc/nhs后横截面微观形貌出现了明显地改变,由不均一的片层结构变成了相对均一多孔的三维网状结构。
48.3)rsf/ε-pll复合水凝胶的流变学性能
49.为了进一步证明交联剂edc/nhs在rsf/ε-pll复合水凝胶形成中的关键作用,以及了解rsf/ε-pll复合水凝胶的粘弹性和机械性能,通过在流变仪上原位交联制备水凝胶然后进行了流变学表征,即将样品置于流变仪上作剪切运动并分析其力学特征。
50.首先,将实施例1制备的样品进行频率扫描,图3中a为不含交联剂edc/nhs的对照组样品在频率扫描下的结果,其中红色的线代表样品在不同剪切频率下的储能模量(g”),g”是描述材料在发生形变时,由于弹性(可逆)形变而储存能量的大小,反映材料弹性大小或者描述其固体性质;蓝色的线代表样品在不同剪切频率下的损耗模量(g’),g’是描述材料在发生形变时,由于粘性形变(不可逆)而损耗的能量大小,反映材料粘性大小或者描述其液体性质。在剪切低频率下时,所有对照组样品g’》g”,因此这些样品在流变学上归属于粘弹性液体,这和我们先的观察一致。并且两者比较接近,当剪切频率增大到一定程度时,g”》g’。图3中b为含有交联剂edc/nhs的rsf/ε-pll复合水凝胶制备体系样品在频率扫描下的结果,所有的样品在整个测试的剪切频率下都有g”》g’,属于粘弹性固体,说明交联剂edc/nhs的加入使得样品体系内部发生交联,其状态由粘弹性液体转变为粘弹性固体。通过横向比较发现,区别于含有ε-pll的实验组样品enrp141、enrp132、enrp114中g”值为g’值的数倍甚至数十倍,只含有rsf的样品enrp150在交联后g”值和g’值相对较为接近,说明enrp150水凝胶内部结构不稳固,其状态并不稳定。根据低剪切频率下的剪切模量来比较制备的水凝胶的强度,或者说硬度,结果如表1所示,强度由强到弱的顺序是enrp141》enrp132》enrp114》enrp150。由此说明,ε-pll加入到体系内与rsf交联能显著的提高水凝胶的强度和稳定性,并且少量的ε-pll的加入使得水凝胶强度最高,随着体系内ε-pll的增多,水凝胶的强度开始减弱,但均大于不含ε-pll的水凝胶。图3中c详细的反应了水凝胶的强度,enrp150与沙拉酱相当,enrp114与涂料和油漆相当,enrp132高于牛奶布丁,enrp141介于奶油乳酪和软糖之间。总的来说,制备出来的rsf/ε-pll复合水凝胶相对较软。
51.表1、不同水凝胶的初始剪切模量
[0052][0053]
为了了解rsf/ε-pll复合水凝胶在受力后的是否不易被破坏,又对其进行振幅扫描测试,结果如图3中d所示,随着振荡应变的增大,水凝胶的储能模量缓慢下降,振荡应力逐渐上升,而当振荡应变增大到某一程度时,储能模量和振荡应力出现剧烈下滑,此时水凝胶发生塑性形变并立刻开始碎裂,而对应的振荡应变则为断裂剪切应变,图3中e显示了各水凝胶对应的断裂剪切应变大小,结果显示当少量ε-pll的加入对水凝胶断裂剪切应变无太大影响,而当其加入量达到某一程度时,如在样品enrp114中的高含量时,水凝胶断裂剪切应变显著增大,达到1000%以上,即在其受到形变后最难碎裂,这与我们用手指对水凝胶揉搓时的直观感受一致,如图3中f。至于enrp150和enrp114样品随着振荡应变增大时g”值下降的趋势相对更大,可能是因为相对不够稳固的三维网状结构中rsf分子更容易受到剪切影响从而导致二级结构的改变,因此储能模量也出现了下滑。
[0054]
4)rsf/ε-pll复合水凝胶的红外光谱特征
[0055]
将实施例1得到的样品体系置于-20℃冰箱内放置12h以上,将其取出后迅速打开离心管盖子并放入提前降温的冻干机内进行冻干,冻干的时间为48h;取出固体样品。用刀片切出1-2mg的碎片,连同200mg高纯度的kbr颗粒放入玛瑙研钵中朝同一方向进行充分研磨,细至200目以下;利用压片机将适量样品和高纯度的kbr混合粉末压片,将得到的无色透明压片放入药品夹中;采集背景后放入压片开始测试,范围为4000cm-1
到400cm-1
,分辨率为4cm-1
,扫描次数为256次,样品测试温度为25℃。利用omnic picta去除水峰,将数据导出为excel格式,利用peakfit对酰胺i区(1580-1720)进行直线基线校正,然后进行高斯方程自动拟合,参数设置为峰位固定峰宽可变。结果如图4所示,其中图4中a为各个样品经红外光扫描后得到的吸收峰图,选取其中经常用于分析的酰胺i(1580-1720cm-1
)进行分析并分峰,结果如图4中b和图4中c显示,在rsf和ε-pll质量比一致的样品中,加入交联剂edc/nhs实验组样品和未加交联剂edc/nhs的对照组样品红外光谱的酰胺i峰形十分相似,在低波数区段没有发现明显的肩峰出现,说明利用交联剂edc/nhs的化学交联没有导致体系内再生丝素蛋白β-折叠含量的上升,其各二级结构没有明显变化,利用peakfit软件对酰胺i分峰后对比各类二级结构含量也印证了这一点(图4中d),利用交联剂edc/nhs的化学交联的方式使得样品体系内rsf的二级结构和溶液中一样仍然以α-螺旋和无规卷曲为主。
[0056]
5)rsf/ε-pll复合水凝胶的形成时间
[0057]
传统rsf自组装形成水凝胶耗时长,目前以后多种技术来加快水凝胶的形成速度,以涡旋、超声等为代表的物理交联方式主要是诱导rsf的β-折叠快速形成来实现,而化学交联则是在rsf链间快速形成共价键来加快形成水凝胶。为了证明edc/nhs交联的高效率能加快水凝胶的形成,我们对加入交联剂edc/nhs的实验组样品形成水凝胶的时间进行统计,并和不加入交联剂edc/nhs的对照组样品在室温放置自组装形成水凝胶的时间进行对比。结果如表2和图5所示,利用edc/nhs的化学交联方式极显著的缩短了水凝胶形成的时间,并且,即使在含交联剂edc/nhs的实验组样品中,因ε-pll的含量不同,水凝胶的形成时间也不
一样,不含ε-pll的样品enrp150水凝胶形成时间最长,而含有少量的ε-pll的样品enrp141形成水凝胶所需时间最短,仅仅需要半小时,随着ε-pll的加入量增多,水凝胶的形成时间又再次延长,但是,在edc/nhs交联的实验组中,含有ε-pll的水凝胶形成时间始终远远低于纯rsf水凝胶的形成时间。
[0058]
实施例3、再生丝素蛋白/ε-聚赖氨酸复合水凝胶的特性与功能
[0059]
1)rsf/ε-pll复合水凝胶的生物降解性
[0060]
将实施例1制备的水凝胶样品冻干后置于pbs、或酶溶液中进行体外降解测试,结果如图6所示。结果显示,所有样品在前两天降解的最快,此后除了在pbs中的样品保持基本稳定,其余浸泡在酶溶液的样品仍然会缓慢的降解(图6中a)。样品在酶溶液中降解得明显更快于在pbs中,尤其是胶原蛋白酶和木瓜蛋白酶中,说明制备的rsf/ε-pll复合水凝胶能有效地被多种蛋白酶降解。图6中b为在胶原蛋白酶溶液中水解10d后的样品截面微观形貌,结果显示,未经胶原蛋白酶降解的复合水凝胶冻干后的截面孔洞内表面十分光滑,而被酶水解后出现裂缝,以及微米级别的颗粒,说明酶降解复合水凝胶的过程是先将材料降解为微米级别的颗粒,然后再进一步降解为多肽、氨基酸。
[0061]
2)rsf/ε-pll复合水凝胶的溶胀度
[0062]
水凝胶是由网状结构的聚合物和溶剂水组成的,因此水凝胶在水中可呈现出显著的溶胀现象,即水凝胶在吸收溶剂后自身体积增大而不至于溶解。具备良好溶胀度的水凝胶,能处理伤口产生的过多的渗出液,维持伤口的湿润环境,还能牢固的贴合、封闭伤口伤口,而封闭的环境又能防止外界微生物的感染、加速新生肉芽组织和血管的再生。rsf/ε-pll复合水凝胶在pbs中的溶胀度如图7所示,图7中a为样品在接触pbs后24h内的溶胀动力学,在前1h内水凝胶快速发生溶胀,在10h后溶胀速率明显变慢,15h后基本达到溶胀平衡,图7中b为各水凝胶的平衡溶胀度,可以看出,所有的水凝胶溶胀度很高,均达到了250%以上,并且复合水凝胶制备体系内加入少量ε-pll导致得到的水凝胶的平衡溶胀度下降,而随着体系内ε-pll的增多,样品的溶胀度再次增大,含ε-pll最多的水凝胶enrp114甚至具有超过400%的溶胀度。总的来说,制备rsf/ε-pll复合水凝胶具有相对良好的溶胀度,能够使其适用于创伤修复。
[0063]
3)rsf/ε-pll复合水凝胶的抗菌性能
[0064]
ε-pll是由白色链霉菌属代谢产生的、聚合度为25-30、具有广泛抑菌性的多肽类代谢物。将其与rsf复合后经edc/nhs交联制备了水凝胶并采用挖孔法探索其抗菌性。图8展示了rsf/ε-pll复合水凝胶对金黄色葡萄球菌(革兰氏阳性菌)和大肠杆菌dh5α(革兰氏阴性菌)的抑菌效果,结果发现,当rsf/ε-pll复合水凝胶中不含ε-pll或含量较少时,图8中a和图8中b表明水凝胶对金黄色葡萄球菌和大肠杆菌dh5α均不具备明显的抑菌效果,而当rsf/ε-pll复合水凝胶中ε-pll含量较多时,即在水凝胶enrp114周围出现了明显的抑菌圈,显示出了对金黄色葡萄球菌和大肠杆菌dh5α明显的抑制效果。
[0065]
4)rsf/ε-pll复合水凝胶的促细胞粘附性能
[0066]
利用小鼠胚胎来源的成纤维细胞nih/3t3在制备的水凝胶上体外接种实验,并利用tcp平板作为对照,在白光、绿色荧光、红色荧光下来观察制备的rsf/ε-pll复合水凝胶对细胞的影响,结果如图9所示,细胞能够在所有的水凝胶表面和tcp平板上生长,但是,长在各水凝胶上的细胞数目和形态并不一致,其中不含ε-pll的水凝胶enrp150上细胞数目最
少,且细胞形态仍未铺展开,呈圆形或椭圆形,而当复合水凝胶中ε-pll含量越来越高,粘附在水凝胶表面的细胞越来越多,细胞的形态也越来越趋于贴壁细胞的梭形或长条状,水凝胶enrp132展现和tcp平板相当的细胞粘附能力,而enrp114的促细胞粘附能力甚至高于tcp平板,活死细胞染色更加清晰的显示这一结果,发出绿色荧光的活细胞密集的粘附在enrp114上并大部分显示出梭形或长条状,而在tcp上粘附相同时间的细胞相对更少,并且含有大部分细胞仍然未铺展开,表明enrp114具备促细胞粘附的特性。需要说明的是,我们未在水凝胶上看到死细胞核发出的红色荧光,说明水凝胶对粘附上的细胞无毒害作用,另外,由于enrp150结构的不稳定性,置于37℃的环境加速了其二级结构无规卷曲向β-折叠的转变,因此水凝胶变得浑浊,荧光因为光散射而无法看清活细胞的形态。
[0067]
5)rsf/ε-pll复合水凝胶的炎症反应
[0068]
对于宿主而言,材料植入体内最普通的反应就是炎症反应。利用常用的炎症模型小鼠巨噬细胞样细胞系raw264.7进行体外接触实验,以检测制备的rsf/ε-pll复合水凝胶是否会引起炎症反应,结果如图10所示,首先从形态上进行观察,图10中a显示复合水凝胶以及tcp平板与材料接触后,raw 264.7细胞形态仍然为圆形,而加入lps的阳性对照组中细胞出现了不规则的分化,而且作为半贴壁的细胞在复合水凝胶上的粘附与先前nih/3t3细胞的规律类似,但始终不及在tcp上粘附的细胞多。对巨噬细胞分泌的一氧化氮(no)和产生的主要促炎因子tnf-α、il-1β、il-6进行检测,检测引物如表3所示。
[0069]
表3、促炎因子定量pcr检测引物
[0070][0071]
结果显示,阳性对照组中raw 264.7细胞受到lps刺激后,无论是no的分泌量还是三种促炎因子表达量都出现明显的上升,说明巨噬细胞raw 264.7细胞对刺激有反应并可用于检测,在这些水凝胶中,enrp150会引起一氧化氮的分泌量和三种促炎因子表达量的上升,尤其是no合成量和il-1β表达量上升十分明显,而水凝胶enrp141引起的炎症反应程度低于enrp150,但是也高于tcp平板的水平,而和enrp132、enrp114接触的raw 264.7细胞no的分泌量和三种促炎因子的表达量则与tcp平板水平较为一致,说明这两种水凝胶对巨噬细胞raw 264.7细胞无明显刺激,不会导致炎症的发生。
[0072]
以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1