一种靶向CCR8的嵌合抗原受体T细胞及其制备方法和应用与流程
一种靶向ccr8的嵌合抗原受体t细胞及其制备方法和应用
技术领域
1.本发明属于生物技术领域,具体涉及一种靶向ccr8的嵌合抗原受体t细胞及其制备方法和应用。
背景技术:
2.t细胞恶性肿瘤是由克隆生长和t细胞功能障碍所产生的肿瘤,该类病人常被定义为高危人员,该类病人的造血功能衰竭、髓质和髓外浸润,并有很高的可能性影响患者的中枢神经系统。其中成人t细胞白血病/淋巴瘤(atll)是常见的t细胞恶性肿瘤之一,atll是一个由htlv-1病毒引来的恶性肿瘤。atll患者临床分期主要有急性、淋巴瘤、慢性以及冒烟型,其四年生存期分别为11%、16%、36%和52%。
3.嵌合抗原受体(cars)是基因修饰的受体,可将t细胞重定向至各种肿瘤的表面抗原。car分子最初产生于1980年代末,到2010年代初得到迅猛发展。目前,常见的car分子通常包含细胞外抗原结合结构域,细胞内信号传导结构域和一个或两个额外的细胞内共刺激信号传导结构域。临床使用时,首先从患者或健康供体中收获t细胞,对其进行基因编辑以表达特定的受体蛋白,然后在体外扩增后注入患者体内。作为活体药物,car-t细胞疗法正在迅速发展成为治疗血液学和非血液学恶性肿瘤最有前景的新疗法之一。
4.2017年,fda批准了诺华的tisagenlecleucel用于治疗儿童b细胞前体急性淋巴细胞白血病(all),fda批准了kite的axicabtagene ciloleucel用于成人弥漫性大b细胞淋巴瘤,car-t细胞疗法得到迅猛发展。car-t疗法在治疗血液肿瘤中取得了巨大的成功,鼓励和激发着更多的人投入到实体瘤的car-t疗法研究中。人们期待,car-t疗法也能在实体瘤中获得相似的成功。目前,t细胞肿瘤的治疗面临的挑战主要包括缺乏肿瘤特异性抗原、t细胞扩增受限以及需要第三方供者或t细胞受体α位点(trac)基因编辑,因此迫切需要研究治疗肿瘤的新靶标。
5.有研究报道,anti-cd7 car-t可以用于治疗血液肿瘤,但是需要在t细胞基础上敲除cd7并在第三方供者中表达trac,且很多患者接受治疗后会发生复发,同时atll中不表达cd7。目前,靶向atll的car-t疗法的靶点只有ccr4,但ccr4是一个t细胞激活后会显著上调的标记物,靶向ccr4的car-t细胞损耗较大,因此car-t细胞的制备需要更大的基数。而ccr8主要表达在肿瘤浸润的treg细胞上,其次会表达在一部分th2型细胞,但不表达在th1型细胞,是一个理想的潜在靶点。因此,提供将ccr8作为car-t的靶点的新的治疗血液瘤的car-t细胞及其制备方法具有重要应用价值。
技术实现要素:
6.针对现有技术存在的不足,本发明的目的在于提供一种靶向ccr8的嵌合抗原受体t细胞及其制备方法和应用。本发明中所述嵌合抗原受体以ccr8作为靶点,构建了靶向ccr8的car-t细胞,证明了ccr8不会影响t细胞的增殖,所述靶向ccr8的car-t细胞在atll细胞模型或动物模型中表现出明显的抗肿瘤效果,并且对表达ccr8的t-all的细胞具有明显的杀
伤特性。为靶向atll和表达ccr8的t-all等肿瘤的car-t治疗方案提供新的靶点和治疗策略。
7.本发明首次提出将ccr8作为成人t淋巴细胞白血病的靶点,第一次构建靶向ccr8的car-t细胞,且所述靶向ccr8的car-t细胞具有良好的抗肿瘤效果,在体内外均对肿瘤细胞有良好的杀伤效果,为成人t淋巴细胞白血病的治疗提供了新靶点、新策略。
8.为达到此发明目的,本发明采用以下技术方案:
9.第一方面,本发明提供一种嵌合抗原受体,所述嵌合抗原受体特异性结合ccr8;
10.所述嵌合抗原受体包括信号肽、胞外识别结构域、跨膜结构域和信号传导结构域;
11.所述胞外识别结构域包括抗ccr8单链抗体,所述抗ccr8单链抗体包括seq id no.1或seq id no.2所示的氨基酸序列。
12.seq id no.1:
13.eivmtqspatlsvspgeratlscrssksllhsngntylywyqqkpgqaprlliyrvsnlasgiparfsgsgsgteftltisslqsedfavyycmqhleypftfgqgtkleikgsggggsggggsggggsevqlvesggalvkpggslrlscaasgftfstyamywvrqapgkglewvgrirsksnnyatyyadsvkdrftisrddskntlylqmnslktedtavyyctrggygnyryamdywgqgttvtvss。
14.seq id no.2:
15.divmtqspdslavslgeratincrssksllhsngntylywyqqkpgqppklliyrmsnlasgvpdrfsgsgsgtdfiltisslqaedvavyycmqhleypltfgqgtkleikrtgsggggsggggsggggsevqlvesggalvkpggslrlscaasgftfstyalywvrqapgkglewvgrirsksnnyatyyadsvkdrftisrddskntlylqmnslktedtavyyctrarfyysdygyamdywgqgtlvtvss。
16.优选地,所述跨膜结构域包括cd28 tm。
17.优选地,所述信号传导结构域包括cd28、cd3ζ和tlr2的组合。
18.优选地,所述嵌合抗原受体由信号肽、抗ccr8单链抗体、cd28 tm、cd28、cd3ζ和tlr2依次串联组成。
19.优选地,所述嵌合抗原受体包括seq id no.3或seq id no.4所示的氨基酸序列。
20.seq id no.3:
21.mlllvtslllcelphpafllipeivmtqspatlsvspgeratlscrssksllhsngntylywyqqkpgqaprlliyrvsnlasgiparfsgsgsgteftltisslqsedfavyycmqhleypftfgqgtkleikgsggggsggggsggggsevqlvesggalvkpggslrlscaasgftfstyamywvrqapgkglewvgrirsksnnyatyyadsvkdrftisrddskntlylqmnslktedtavyyctrggygnyryamdywgqgttvtvsstrievmypppyldneksngtiihvkgkhlcpsplfpgpskpfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalpprqakrkprkapsrnicydafvsyserdaywvenlmvqelenfnppfklclhkrdfipgkwiidniidsiekshktvfvlsenfvksewckyeldfshfrlfdenndaailillepiekkaipqrfcklrkimntktylewpmdeaqregfwvnlraaiks。
22.seq id no.4:
23.mlllvtslllcelphpafllipdivmtqspdslavslgeratincrssksllhsngntylywyqqkpgqppklliyrmsnlasgvpdrfsgsgsgtdfiltisslqaedvavyycmqhleypltfgqgtkleikrtgsggggsggggsggggsevqlvesggalvkpggslrlscaasgftfstyalywvrqapgkglewvgrirsksnnyatyyadsvk
drftisrddskntlylqmnslktedtavyyctrarfyysdygyamdywgqgtlvtvsstrievmypppyldneksngtiihvkgkhlcpsplfpgpskpfwvlvvvggvlacysllvtvafiifwvrskrsrllhsdymnmtprrpgptrkhyqpyapprdfaayrsrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalpprqakrkprkapsrnicydafvsyserdaywvenlmvqelenfnppfklclhkrdfipgkwiidniidsiekshktvfvlsenfvksewckyeldfshfrlfdenndaailillepiekkaipqrfcklrkimntktylewpmdeaqregfwvnlraaiks。
24.第二方面,本发明提供一种核酸分子,所述核酸分子编码第一方面所述的嵌合抗原受体。
25.优选地,所述核酸分子包括seq id no.5或seq id no.6所示的核苷酸序列。
26.seq id no.5:
27.atgcttctcctggtgacaagccttctgctctgtgagttaccacacccagcattcctcctgatcccagagatcgtgatgacacagagccccgccacactgagcgtgagccccggcgagcgggccaccctgagctgccggagcagcaagagcctgctgcacagcaacgggaacacctacctgtactggtaccagcagaagcccggccaggcccccaggctgctgatctacagggtgagcaacctggccagcggcatccccgcccggttcagcgggagcgggagcggcaccgagttcacactgaccatcagcagcctgcagagcgaggatttcgccgtgtactactgcatgcagcacctggagtaccccttcacattcgggcaggggacaaagctggagatcaagggatccggtggcggtggcagcggcggtggtggttccggaggcggcggttctgaagtgcagctggtggagagcgggggggccctggtgaagcccggcggcagcctgaggctgagctgcgccgccagcgggttcaccttctccacctacgccatgtactgggtgaggcaggcccccggcaaggggctggagtgggtggggcggattaggagcaagagcaacaactacgccacatactacgccgatagcgtgaaggataggttcaccatcagccgggacgatagcaagaacacactgtacctgcagatgaacagcctcaagaccgaggacaccgccgtgtactactgcacaaggggcggctacggcaactaccggtacgccatggactactgggggcaggggacaacagtgacagtgagcagcacgcgtattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttgggggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgccaggccaaaaggaagcccaggaaagctcccagcaggaacatctgctatgatgcatttgtttcttacagtgagcgggatgcctactgggtggagaaccttatggtccaggagctggagaacttcaatccccccttcaagttgtgtcttcataagcgggacttcattcctggcaagtggatcattgacaatatcattgactccattgaaaagagccacaaaactgtctttgtgctttctgaaaactttgtgaagagtgagtggtgcaagtatgaactggacttctcccatttccgtctttttgatgagaacaatgatgctgccattctcattcttctggagcccattgagaaaaaagccattccccagcgcttctgcaagctgcggaagataatgaacaccaagacctacctggagtggcccatggacgaggctcagcgggaaggattttgggtaaatctgagagctgcgataaagtcc。
28.seq id no.6:
29.atgcttctcctggtgacaagccttctgctctgtgagttaccacacccagcattcctcctgatcccagatatcgtgatgacacagagccccgatagcctggccgtgagcctgggcgagcgggccacaatcaactgcaggagcagc
aagagcctgctgcacagcaacgggaacacatacctgtactggtaccagcagaagcccggccagccccccaagctgctgatctaccggatgagcaacctggcctccggggtgcccgataggttcagcgggagcgggagcgggaccgacttcatcctgaccatcagcagcctgcaggccgaggacgtggccgtgtactactgcatgcagcacctggagtaccccctgaccttcggccagggcacaaagctggagatcaagaggacaggatccggtggcggtggcagcggcggtggtggttccggaggcggcggttctgaggtgcagctggtggagagcggcggcgccctggtgaagcccggcgggagcctgaggctgagctgcgccgccagcgggttcaccttcagcacatacgccctgtactgggtgaggcaggcccccggcaagggcctggagtgggtggggcggatcaggagcaagagcaacaactacgccacctactacgccgatagcgtgaaggataggttcacaatcagccgggatgatagcaagaacacactgtacctgcagatgaacagcctcaagaccgaggacaccgccgtgtactactgcacaagggcccggttctactacagcgactacgggtacgccatggactactgggggcagggcacactggtgacagtgagcagcacgcgtattgaagttatgtatcctcctccttacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgtccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttgggggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctccagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgccaggccaaaaggaagcccaggaaagctcccagcaggaacatctgctatgatgcatttgtttcttacagtgagcgggatgcctactgggtggagaaccttatggtccaggagctggagaacttcaatccccccttcaagttgtgtcttcataagcgggacttcattcctggcaagtggatcattgacaatatcattgactccattgaaaagagccacaaaactgtctttgtgctttctgaaaactttgtgaagagtgagtggtgcaagtatgaactggacttctcccatttccgtctttttgatgagaacaatgatgctgccattctcattcttctggagcccattgagaaaaaagccattccccagcgcttctgcaagctgcggaagataatgaacaccaagacctacctggagtggcccatggacgaggctcagcgggaaggattttgggtaaatctgagagctgcgataaagtcc。
30.第三方面,本发明提供一种表达载体,所述表达载体包括至少一个拷贝的第二方面所述的核酸分子。
31.优选地,所述表达载体包括病毒载体。
32.优选地,所述病毒载体包括慢病毒载体、逆转录病毒载体或腺相关病毒载体中的任意一种,优选为慢病毒载体。
33.第四方面,本发明提供一种重组慢病毒,所述重组慢病毒采用第三方面所述的表达载体与包装质粒共转染病毒包装细胞制备得到。
34.第五方面,本发明提供一种靶向ccr8的嵌合抗原受体t细胞,所述靶向ccr8的嵌合抗原受体t细胞表达第一方面所述的嵌合抗原受体。
35.第六方面,本发明提供一种第五方面所述的靶向ccr8的嵌合抗原受体t细胞的制备方法,所述制备方法包括如下步骤:
36.(1)构建编码嵌合抗原受体的表达载体;
37.(2)将步骤(1)中的表达载体与包装质粒共转染病毒包装细胞,制备重组慢病毒;
38.(3)将步骤(2)中的重组慢病毒导入t细胞中,制备表达靶向ccr8的嵌合抗原受体t
细胞。
39.第七方面,本发明提供一种药物组合物,所述药物组合物包括第五方面所述的靶向ccr8的嵌合抗原受体t细胞。
40.优选地,所述药物组合物还包括药学上可接受的载体、赋形剂或稀释剂中的任意一种或至少两种的组合。
41.第八方面,本发明提供第五方面所述的靶向ccr8的嵌合抗原受体t细胞和/或第七方面所述的药物组合物在制备肿瘤治疗药物中的应用。
42.优选地,所述肿瘤包括ccr8阳性肿瘤。
43.优选地,所述ccr8阳性肿瘤包括t淋巴细胞白血病。
44.相对于现有技术,本发明具有以下有益效果:
45.(1)本发明中所述靶向ccr8的car-t细胞在atll细胞模型或动物模型中表现出明显的抗肿瘤效果,ccr8不会影响t细胞的增殖,并且所述car-t细胞对表达ccr8的t-all的细胞具有明显的杀伤作用。
46.(2)本发明首次提出将ccr8作为成人t淋巴细胞白血病的靶点,第一次构建靶向ccr8的car-t细胞,且所述靶向ccr8的car-t细胞具有良好的抗肿瘤效果,在体内外均对肿瘤细胞有良好的杀伤效果,为成人t淋巴细胞白血病的治疗提供了新靶点、新策略。
附图说明
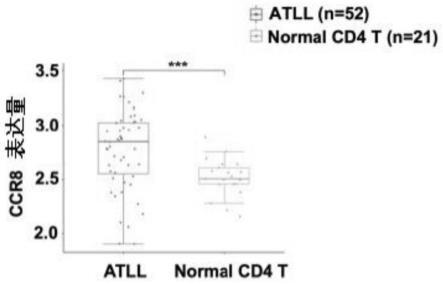
47.图1a和图1b是实施例1中atll患者cd4 t细胞与正常cd4 t细胞中ccr8和cd7的表达水平。
48.图1c和图1d是实施例1中mt-4细胞和c8166细胞中ccr8和cd7的表达水平。
49.图2是实施例2中c1928z质粒、c1028z质粒和1928z质粒的结构示意图。
50.图3是测试例1中car-t细胞的扩增曲线。
51.图4a是测试例2中car-t细胞对mt-4-gl细胞和c8166-gl细胞的杀伤活性检测图。
52.图4b是测试例2中car-t细胞与mt-4-gl细胞和c8166-gl细胞共培养后颗粒酶的分泌量统计图。
53.图4c是测试例2中car-t细胞与mt-4-gl细胞和c8166-gl细胞共培养后ifn-γ的分泌量统计图。
54.图5a、图5b和图5c是测试例3中car-t细胞的抗肿瘤活性的检测结果;图5a为小鼠活体成像的结果图,图5b为mt-4-gl细胞在小鼠体内的扩增结果统计图,图5c为mt-4-gl小鼠生存曲线。
55.图6a是测试例4中jurkat细胞和molt-4细胞中ccr8的表达水平。
56.图6b是测试例4中car-t细胞对jurkat细胞杀伤活性检测图。
57.图6c是测试例4中car-t细胞与jurkat细胞共培养后颗粒酶的分泌量统计图。
58.图6d是测试例4中car-t细胞与jurkat细胞共培养后ifn-γ的分泌量统计图。
59.图6e是测试例4中小鼠活体成像的结果图。
60.图6f是测试例4中jurkat细胞在小鼠体内扩增结果统计图。
61.图6g是测试例4中jurkat小鼠的生存曲线。
具体实施方式
62.下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
63.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
64.实施例1
65.本实施例验证ccr8在atll患者和atll细胞系中特异性表达
66.在geo database(gse33615)下载atll患者cd4 t细胞及正常cd4 t细胞(normal cd4t)的数据进行t检验分析,分析结果如图1a和图1b所示,与normal cd4 t相比atll患者cd4 t细胞中高表达ccr8。
67.流式检测atll细胞系(包括mt-4细胞系和c8166细胞系)中cd7和ccr8的表达情况:
68.采用rpmi-1640培养基+10%fbs+1%p/s分别培养mt-4细胞系和c8166细胞系,培养条件为37℃、5%co2,每两天进行半换液,确保培养的细胞浓度不超过3
×
106细胞/ml。
69.将mt-4细胞系和c8166细胞系的培养液分别使用pbs缓冲液稀释成2
×
105细胞/ml的细胞悬浮液;分别向所述细胞悬浮液中加入0.5μl cd7流式抗体和0.5μl ccr8流式抗体,在4℃下染色30min,染色后使用1ml pbs缓冲液清洗,300g离心5min后加入100μl pbs缓冲液上机检测。
70.检测结果如图1c和图1d所示,检测结果表明,ccr8在mt-4细胞系和c8166细胞系中高表达。
71.实施例2
72.本实施例构建慢病毒表达载体(c1928z质粒、c1028z质粒和1928z质粒)
73.慢病毒表达载体构建:将合成的序列anti-ccr8(19d7)-cd28-cd3ζ-tlr2和序列anti-ccr8(10a11)-cd28-cd3ζ-tlr2(由生工生物工程(上海)股份有限公司合成)分别使用mssi和bcui两个限制性内切酶进行酶切,同时使用mssi和bcui酶切带有egfp报告基因的pwpxld-2a-egfp慢病毒骨架,酶切条件为:37℃酶切2h。
74.酶切后使用琼脂糖凝胶电泳分离目的片段,仪器设置为120v、30min。用凝胶回收试剂盒回收目的片段,然后用solutioni连接酶在16℃金属浴连接1h。将连接产物与感受态细胞transstbl3放在冰上孵育30min,42℃热激45s,在冰上放置3min,加入200μl无抗lb培养基,在37℃摇床培养45min后均匀涂布在带有氨苄抗性的lb平板上,倒放在培养箱37℃过夜培养。
75.挑取长势良好的圆形克隆菌斑,将克隆菌斑接种于氨苄抗性液体lb培养基中进行培养(15ml离心管中装2ml lb培养基),培养条件为:37℃摇床、220r/min培养8h。
76.培养结束后使用质粒小量提取试剂盒提取质粒,再用限制性内切酶mssi、bcui或ndei对提取的质粒进行鉴定并测序,取100μl鉴定正确的克隆菌液接种于氨苄抗性液体lb培养基中进行培养(50ml离心管中装30ml lb培养基),培养条件为:37℃摇床、220r/min培养20h。
77.培养结束后使用无内毒素质粒提取试剂盒提取质粒,再次用限制性内切酶mssi、bcui或ndei对提取的质粒进行鉴定并测序,将鉴定正确的质粒放在-20℃冰箱保存。
78.采用相同的方法构建含有靶向cd19单链抗体的car的编码序列的慢病毒载体(pwpxld-fmc63-cd28tm-cd28-cd3ζ-tlr2-2a-egfp),作为对照组(1928z质粒)。
79.构建后得到c1928z质粒、c1028z质粒和1928z质粒,其中c1928z质粒、c1028z质粒和1928z质粒的结构示意图如图2所示,图2中1928z质粒为对照组。
80.c1928z质粒pwpxld-ccr8(19d7)-cd28tm-cd28-cd3ζ-tlr2-2a-egfp的核苷酸序列如seq id no.5所示;
81.c1028z质粒pwpxld-ccr8(10a11)-cd28tm-cd28-cd3ζ-tlr2-2a-egfp的核苷酸序列如seq id no.6所示。
82.实施例3
83.本实施例制备c1928z重组慢病毒、c1028z重组慢病毒和1928z重组慢病毒
84.慢病毒包装:
85.(1)在100mm细胞培养皿中加入hek293t细胞(6
×
106个细胞左右)(货号icell-h237)和8ml dmem培养基(dmem+10%fbs+1%p/s),将细胞培养皿放置在细胞培养箱中培养。
86.(2)至细胞铺满培养皿底部的80%,在荧光倒置显微镜下观察细胞状态。如果细胞分布均匀且状态良好,则可用于病毒包装实验。吸除培养基上清,加入6ml dmem病毒包装培养基(dmem+1%fbs+1%p/s),放置在培养箱中饥饿处理2h。
87.(3)将辅助质粒pmd2.g质粒(货号p0262)、pspax2质粒(货号p0261)和实施例2中制备的慢病毒表达载体c1928z质粒混合,将c1928z质粒、辅助质粒pmd2.g和辅助质粒pspax2按质量(μg)9:3:12混合,并加到0.5ml opti-mem里(标记为a液),再将72μgpei(聚乙烯亚胺)加到0.5ml opti-mem中(标记为b液)室温放置5min;将a液和b液混合,室温放置20min;将混合液逐滴加到饥饿完成的hek 293t细胞培养皿中,轻轻摇匀后放置在培养箱中培养。
88.(4)培养6h后,在荧光倒置显微镜下观察细胞,应可见零星细胞发出绿色荧光。吸出培养基上清,加10ml新鲜预热的dmem病毒包装培养基(dmem+1%fbs+1%p/s),放回培养箱中继续培养。
89.(5)每过24h收集培养基上清,添加适量新鲜预热的dmem病毒包装培养基(dmem+1%fbs+1%p/s)后放回培养箱中;将收集的病毒上清用0.45μm过滤器过滤,得到c1928z重组慢病毒,保存在4℃冰箱,于一周内使用。
90.采用同样的方法制备c1028z重组慢病毒和1928z重组慢病毒。
91.实施例4
92.本实施例制备car-t细胞,包括c1928z t细胞、c1028z t细胞和1928z t细胞。
93.car-t细胞的制备步骤如下所示:
94.将激活的t细胞离心后去上清,用t细胞培养基(t551 h3+10%fbs+1%p/s+300iu/ml il-2)重悬后计数。
95.将t细胞稀释成约2
×
106细胞/ml,加入实施例3中所述的c1928z重组慢病毒(病毒颗粒数与细胞数的比例为5:1)和聚凝胺(8μg/ml),混合后放置在37℃、5%co2培养箱中感染24h,之后进行换液,用t细胞培养基(t551 h3+10%fbs+1%p/s+300iu/ml il-2)培养t细胞至换液后的第7天,确保t细胞的培养密度为(1~2)
×
106。将c1928z t细胞计数后离心,加入冻存液(90%fbs+10%dmso)后混匀,冻存密度为1
×
108细胞/ml;每个冻存管中加入
1ml细胞匀液。将冻存管放在梯度冻存盒中,于-80℃冰箱中降温;12h后转移至液氮罐中保存。
96.采用同样的方法制备c1028z t细胞和1928z t细胞。
97.测试例1
98.对实施例4中car-t细胞进行培养并制作car-t细胞的扩增曲线
99.将car-t细胞(包括c1928z t细胞、c1028z t细胞和1928z t细胞)稀释成1
×
106细胞/ml的细胞悬液,进行培养,培养条件为t551 h3+10%fbs+1%p/s+300u/ml il-2,每2天在倒置荧光显微镜下观察car-t细胞的状态和培养基的颜色;在第3、5、7和9天取细胞进行流式计数;在car-t细胞培养的过程中,一般每2天更换一次新鲜的t细胞培养基,在体外扩增培养10天;car-t细胞培养至第10天时,将car-t细胞转移至合适的离心管中,在室温下380g离心3.5min,吸走上清,用1ml t细胞培养基重悬,取10μl t细胞悬液进行细胞计数并记录car-t细胞数目。car-t细胞的扩增曲线如图3所示。
100.测试例2
101.实施例4中car-t细胞的杀伤作用验证和细胞因子分泌检测
102.取出适量实施例4中的car-t细胞至15ml离心管中,300g离心5min去上清,用pbs缓冲液重悬car-t细胞,清洗一遍后再次离心,用不含il-2的1640培养基(1640+10%fbs+1%p/s)重悬,计数,将car-t细胞稀释成合适的浓度。
103.在白底96孔板中加入100μl 1640培养基(1640+10%fbs+1%p/s),在第一排加入100μl调节好密度的car-t细胞。用排枪混匀后取100μl加入到下一排。然后依次倍比(2倍)稀释,一共设置7个梯度和一个只有培养基的空白梯度。
104.准备靶细胞(包括mt-4-gl细胞和c8166-gl细胞)离心后弃上清,用pbs缓冲液重悬后清洗一遍,离心弃上清,用1640培养基(1640+10%fbs+1%p/s)重悬,稀释至1
×
105细胞/ml。在白底96孔板中每孔加入100μl靶细胞。因此,最终浓度为car-t细胞:靶细胞(e:t)比例为8:1、4:1、2:1、1:1、1:2、1:4、1:8和0:1;将混合好的细胞放置在37℃培养箱中培养24h。
105.培养24h后,将白底96孔板取出,向白底96孔板中每孔加入稀释好的荧光素酶底物(150μg/ml)在荧光照度计上读取荧光值,计算不同e:t比下的细胞杀伤比例。
106.杀伤后取上清根据granzyme-b及ifn-γelisa试剂盒操作说明检测细胞因子分泌量。
107.检测结果如图4a、图4b和图4c所示。图4a为car-t细胞对mt-4-gl细胞和c8166-gl细胞的杀伤活性检测图;图4b为car-t细胞与mt-4-gl细胞和c8166-gl细胞共培养后颗粒酶的分泌量统计图;图4c为car-t细胞与mt-4-gl细胞和c8166-gl细胞共培养后ifn-γ的分泌量统计图。
108.将car-t细胞与mt-4细胞和c8166细胞共培养后,靶向ccr8的car-t细胞(c1928zt细胞和c1028z t细胞)表现出上调的激活标记,并分泌出丰富的细胞因子(颗粒酶b和ifn-γ),所述细胞因子对t细胞的免疫力至关重要。从低到高的e:t比,靶向ccr8的car-t细胞也发挥了越来越大的细胞毒性作用。
109.测试例3
110.实施例4中car-t细胞体内抗肿瘤活性验证
111.第一天取8周龄同一性别nsi小鼠,用胰岛素注射器吸取100μl mt-4-gl细胞悬液
(8
×
105细胞/鼠),尾静脉注射。第二天进行活体成像并根据成像数据进行分组。
112.复苏冻存的car-t细胞,以c1928z t细胞和c1028z t细胞实验组,以1928z t细胞为对照组,计数后重悬至car-t细胞密度为5
×
107细胞/ml,并分装成每管100μl。即每管5
×
106个car-t细胞,采用腹腔注射的方式将car-t细胞注射到小鼠体内。每周对三组小鼠进行活体成像,并且进行分析。
113.抗肿瘤活性的检测结果如图5a、图5b和图5c所示。图5a为小鼠活体成像的结果图,图5b为mt-4-gl细胞在小鼠体内的扩增结果统计图,图5c为mt-4-gl小鼠生存曲线。从图中可以看出实验组的car-t细胞能有效抑制mt-4-gl细胞在体内的扩增进展。
114.测试例4
115.验证实施例4中car-t细胞在体外和体内对ccr8阳性t细胞恶性肿瘤的生长的抑制作用。
116.(1)流式检测jurkat细胞和molt 4细胞中ccr8的表达情况
117.采用rpmi-1640培养基+10%fbs+1%p/s培养jurkat细胞和molt 4细胞,培养条件为37℃、5%co2,每两天进行半换液,确保培养细胞浓度不超过3
×
106细胞/ml。
118.将jurkat细胞和molt 4细胞的培养液分别使用pbs缓冲液稀释成2
×
105细胞/ml的悬浮液;分别加入0.5μl ccr8流式抗体,4℃进行染色30min,使用1ml pbs缓冲液清洗,300g离心5min后加入100μl pbs缓冲液上机检测。检测结果如图6a所示,图6a为jurkat细胞和molt-4细胞中ccr8的表达水平,其中ccr8在jurkat细胞中高表达。
119.(2)car-t细胞对jurkat细胞的杀伤验证和细胞因子分泌
120.取出适量的car-t细胞至15ml离心管中,300g离心5min去上清,用pbs缓冲液重悬清洗一遍后再次离心,用不含il-2的1640培养基(1640+10%fbs+1%p/s)重悬,计数,将car-t细胞稀释成合适的浓度。
121.在白底96孔板中加入100μl 1640培养基(1640+10%fbs+1%p/s),在第一排加入100μl调节好密度的car-t细胞。用排枪混匀后取100μl加入到下一排。然后依次倍比(2倍)稀释,一共设置7个梯度和一个只有培养基的空白梯度。
122.准备靶细胞(jurkat细胞)离心后弃上清,用pbs缓冲液重悬后清洗一遍,离心弃上清,用1640培养基(1640+10%fbs+1%p/s)重悬,稀释至1
×
105细胞/ml。在白底96孔板中每孔加入100μl靶细胞。因此,最终浓度为car-t细胞:靶细胞(e:t)比例为8:1、4:1、2:1、1:1、1:2、1:4、1:8和0:1;将混合好的细胞放置在37℃培养箱培养24h。
123.共培养24h后,将白底96孔板取出,然后向白底96孔板中每孔加入稀释好的荧光素酶底物(150μg/ml)在荧光照度计上读取荧光值,计算不同e:t比下的细胞杀伤比例。
124.杀伤后取上清根据granzyme-b及ifn-γelisa试剂盒操作检测细胞因子分泌。
125.检测结果如图6b、图6c和图6d所示。图6b为car-t细胞对jurkat细胞的杀伤活性检测图;图6c为car-t细胞与jurkat细胞共培养后颗粒酶的分泌量统计图;图6d为car-t细胞与jurkat细胞共培养后ifn-γ的分泌量统计图。
126.将car-t细胞与jurkat细胞共培养后,靶向ccr8的car-t细胞(c1928z t细胞和c1028z t细胞)表现出上调的激活标记,并分泌出丰富的细胞因子(颗粒酶b和ifn-γ),这些因子对t细胞的免疫力至关重要。从低到高的e:t比,靶向ccr8的car-t细胞也发挥了越来越大的细胞毒性作用。
127.(3)car-t细胞体内抗肿瘤活性:
128.第一天取8周龄同一性别nsi小鼠,用胰岛素注射器吸取100μl jurkat细胞混悬液(8
×
105细胞/鼠),尾静脉注射。第二天进行活体成像并根据成像数据进行分组。
129.复苏冻存的car-t细胞,以c1928z t细胞和c1028z t细胞实验组,以1928z-t细胞为对照组,计数后重悬至car-t细胞密度为5
×
107细胞/ml,并分装成每管100μl。即每管5
×
106个car-t细胞,采用腹腔注射的方式将car-t细胞注射到小鼠体内。每周对三组小鼠进行活体成像,并且进行分析。
130.抗肿瘤活性的检测结果如图6e、图6f和图6g所示。图6e为小鼠活体成像的结果图,图6f为jurkat细胞在小鼠体内扩增结果统计图,图6g是jurkat小鼠(注射jurkat的小鼠)的生存曲线。从图中可以看出实验组的car-细胞能有效抑制jurkat细胞在体内的扩增进展。
131.上述实验的结果表明car-t细胞在体外和体内均能显著抑制ccr8阳性t细胞恶性肿瘤的生长。
132.综上,本发明首次提出将ccr8作为成人t淋巴细胞白血病的靶点,并且第一次将ccr8作为car-t的靶点并具有良好的治疗效果,在体内外均对肿瘤细胞有良好的杀伤效果,为成人t淋巴细胞白血病的治疗提供了新靶点、新策略。本技术提供靶向ccr8的car-t细胞在atll细胞模型或动物模型中表现出明显的抗肿瘤效果,并且对表达ccr8的t-all的细胞具有明显的杀伤特性。
133.申请人声明,以上所述仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,所属技术领域的技术人员应该明了,任何属于本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1