瑞卢戈利关键中间体的制备的制作方法
1.本发明属于化学合成领域,具体涉及瑞卢戈利关键中间体1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮的制备。
背景技术:
[0002]
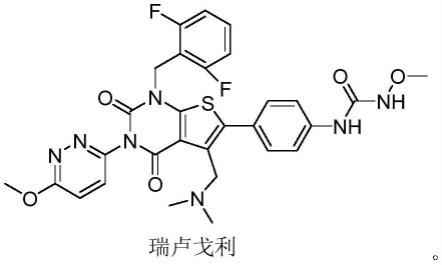
瑞卢戈利(relugolix,cas:737789-87-6)是由武田公司研制开发,由myovant sciences公司于2016年6月获得除日本和其他亚洲国家在外的全球独家授权的药物。2018年5月,aska pharmaceutical获得武田授权在日本独家开发和商业化瑞卢戈利的权利。2019年1月8日瑞卢戈利获日本医药品医疗器械综合机构(pmda)批准上市,由武田和aska pharmaceutical上市销售,商品名为被批准用于子宫肌瘤的治疗和症状缓解。瑞卢戈利是一种每日一次、口服、促性腺激素释放激素(gnrh)受体拮抗剂,能抑制睾丸睾酮的生成。此外,瑞卢戈利也可通过阻断垂体腺中的gnrh受体,减少卵巢雌二醇的生成,这种激素可刺激子宫肌瘤和子宫内膜异位症的生长。瑞卢戈利的化学名为:1-[4-[1-(2,6-二氟苄基)-5-二甲基氨基甲基-3-(6-甲氧基哒嗪-3-基)-2,4-二氧代-1,2,3,4-四氢噻吩并[2,3-d]嘧啶-6-基]苯基]-3-甲氧基脲,具有如下化学结构式:
[0003]
目前公开报道的制备瑞卢戈利的专利文献较多。在2013年武田药业(cn104703992)报道了以2-[(2,6-二氟苄基)乙氧基羰基氨基]-4-甲基-5-(4-硝基苯基)噻吩-3-甲酸乙酯为起始原料的合成路线,经溴代反应、二甲胺基亲核取代反应、酯的水解反应、酸胺缩合反应、分子内胺脂交换反应、硝基还原反应、成脲等步骤实现了瑞卢戈利的全合成。该路线路线长,且该路线步骤3、步骤4、步骤5会产生大量的酸性废水和含膦废水,环境不友好,该工艺有很大的环保压力,因此工业化生产受到局限。相关合成路线如下所示:
[0004]
四川伊诺达博医药科技有限公司(cn110194776)开发了以4-硝基苯丙酮为原料的合成路线。该路线通过gewald反应、酯的水解反应、缩合环化、亲核取代、胺脂交换、缩合环化、溴代、二甲胺基取代、硝基还原等10步反应完成了瑞卢戈利的合成。该路线在化合物6的合成中也同样进过了酯的水解、羧基活化、3-氨基-6-甲氧基哒嗪引入和关嘧啶环4个步骤,步骤繁琐,废水量较大。相关合成路线如下所示:
[0005]
江西青峰药业有限公司(cn111423452)在武田药业工艺基础上对反应顺序进行了调整,以化合物a为起始原料,经过酯的水解反应、3-氨基-6-甲氧基哒嗪引入、关环反应、溴
代反应、二甲氨基取代反应、硝基还原、成脲等7步反应完成了瑞卢戈利的合成。该工艺在化合物a到化合物d的合成中同样经过了酯的水解反应、3-氨基-6-甲氧基哒嗪引入和关嘧啶环三个步骤。该工艺具体合成路线如下所示:
[0006]
综合上述已公开报道的合成瑞卢戈利的方法,在引入3-氨基-6-甲氧基哒嗪和关嘧啶环过程中都涉及多步反应,步骤繁琐,大大增加了成本。为此,开发一条更简洁的适合工业化放大生产的瑞卢戈利合成路线对于瑞卢戈利的产业化尤其重要。上述几篇专利引入3-氨基-6-甲氧基哒嗪和关嘧啶环的路线汇总如下:
技术实现要素:
[0007]
本发明的目的在于新开发一条瑞卢戈利的合成方法,特别是关键中间体1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv)的合成工艺,创新点在于从2-((2,6-二氟苄基)(乙氧羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-羧酸乙酯(式iii)出发仅需一步即可实现3-氨基-6-甲氧基哒嗪的引入和关嘧啶环步骤,合成路线如下所示:
[0008]
研究发现,2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-甲基-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式i)在nbs/aibn的作用下进行溴代,可以制备得到4-(溴甲基)-2-((2,6-二氟苄基)(乙氧基羰基)氨基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式ii);4-(溴甲基)-2-((2,6-二氟苄基)(乙氧基羰基)氨基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯与盐酸二甲胺发生取代反应,制备得到2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式iii);2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式iii)在碱/溶剂作用下和3-氨基-6-甲氧基哒嗪反应,制备得到1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv),该步反应所使用的溶剂包括四氢呋喃、1,4-二氧六环、乙醚,所使用的碱包括二异丙基氨基锂、正丁基锂、仲丁基锂;1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv)经pd/c氢化反应制备得到6-(4-氨基苯基)-1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式v);最后,6-(4-氨基苯基)-1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式v)与羰基二咪唑/盐酸甲氧基胺发生缩合反应实现瑞卢戈利的制备。
[0009]
本发明制备瑞卢戈利的工艺路线优势明显,在引入3-氨基-6-甲氧基哒嗪片段继而关嘧啶环仅需一步完成,大大节省了工艺成本,减少了三废,具有明显的优势。
具体实施方式
[0010]
通过下面的实施例可以更具体的理解本发明,但其是举例说明而不是限制本发明
的范围。实施例1.制备4-(溴甲基)-2-((2,6-二氟苄基)(乙氧基羰基)氨基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式ii)
[0011]
2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-甲基-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式i)(10.0g,19.8mmol)加入至乙酸乙酯(100ml)中,加入n-溴代琥珀酰亚胺(5.3g,29.7mmol,1.5eq)和2,2'-偶氮二异丁腈(0.03g,0.2mmol,0.01eq)。投料完毕后体系加热至50℃搅拌反应1小时,然后将反应液冷却至20℃,加入饱和食盐水洗涤2次(2
×
100ml)。所得有机相减压脱除溶剂后加入庚烷(200ml)激烈搅拌24小时,过滤后固体50℃真空干燥,得到4-(溴甲基)-2-((2,6-二氟苄基)(乙氧基羰基)氨基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式ii)(黄色固体,11.0g,收率95.2%)。实施例2.制备2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式iii)
[0012]
将盐酸二甲胺(2.1g,25.7mmol,1.5eq)置于反应瓶中,加入n,n-二甲基甲酰胺(70.0ml)和三乙胺(17.3g,171.0mmol),氮气保护下向反应体系缓慢加入4-(溴甲基)-2-((2,6-二氟苄基)(乙氧基羰基)氨基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式ii)(10.0g,17.1mmol),体系在15
±
5℃反应1小时。然后加入乙醇(20ml)升温至45
±
5℃,加入水(25ml),搅拌30分钟,过滤收集固体,所得固体用乙醇/水(4/1,15ml)洗涤。洗涤后所得固体在50
±
5℃下干燥24小时得2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式iii)(黄色固体,8.6g,收率91.5%)实施例3.制备1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv)
[0013]
2-((2,6-二氟苄基)(乙氧基羰基)氨基)-4-((二甲氨基)甲基)-5-(4-硝基苯基)噻吩-3-甲酸乙酯(式iii)(5.0g,10.0mmol)置于反应瓶中,加入3-氨基-6-甲氧基哒嗪(1.0g,10.0mmol)和四氢呋喃(100ml),开启搅拌。氮气保护下体系降温至-78℃左右,向反应体系缓慢滴加入正丁基锂(2.5m in hexane,10ml,25mmol),滴加完毕后体系-78℃左右反应2小时。然后,体系缓慢滴加水(50ml)淬灭反应,体系自然升温至室温,随后滴加盐酸(1m)调节ph至5左右。体系使用乙酸乙酯萃取(2
×
100ml),合并的有机相加入饱和食盐水洗涤(2
×
100ml),有机相减压脱除溶剂后加入庚烷(200ml)激烈搅拌24小时。体系过滤后所得固体50℃真空干燥12小时得1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv)(浅黄色固体,4.5g,收率85.2%)。实施例4.制备6-(4-氨基苯基)-1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式v)
[0014]
1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)-6-(4-硝基苯基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式iv)(4.0g,6.9mmol)置于反应瓶中,加入钯碳(10%pd,300mg)和甲醇(30ml),滴加浓盐酸(12m,0.5g)。氢气置换三次,加氢(1atm)反应20小时。反应液滤除钯碳,母液浓缩干得6-(4-氨基苯基)-1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式v)(白色固体,3.6g,96.3%)。
实施例5.制备瑞卢戈利
[0015]
将6-(4-氨基苯基)-1-(2,6-二氟苄基)-5-((二甲基氨基)甲基)-3-(6-甲氧基哒嗪-3-基)噻吩并[2,3-d]嘧啶-2,4(lh,3h)-二酮(式v)(2.60g,4.8mmol),n,n'-羰基二咪唑(1.60g,9.6mmol),n,n'-二异丙基乙胺(6.0g,48mmol)和乙腈20(ml)加入到反应瓶中,体系加热至45℃反应30分钟,然后再加入甲氧基胺盐酸盐,继续反应6小时。体系降温至20℃左右,加入水(100ml),搅拌析晶,滤饼用乙醇/二氯甲烷(50ml/50ml)打浆纯化,过滤后固体50℃真空干燥12小时,得到瑞卢戈利(2.5g,86.3%)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1