酰胺化合物的合成及其用途
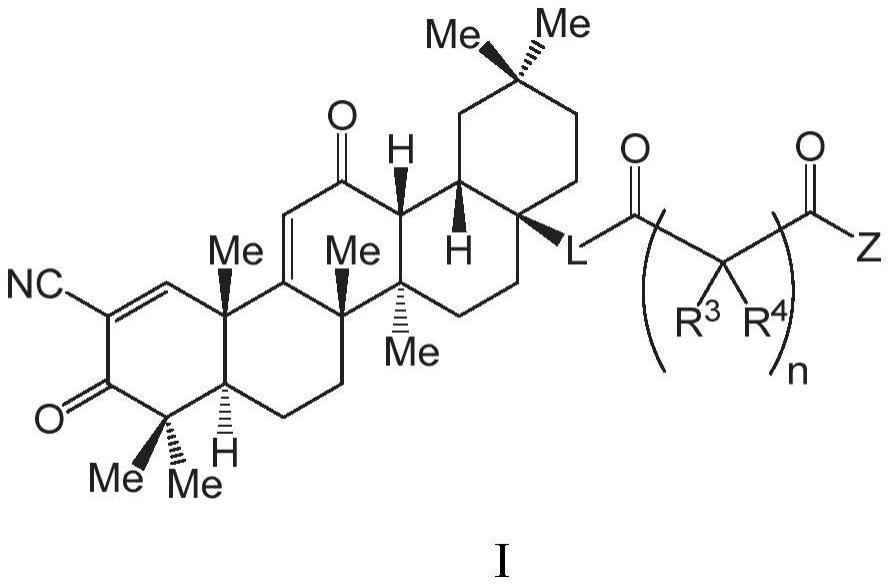
本发明涉及一种新型的齐墩果酸酰胺衍生物,特别涉及这类化合物的制备方法和用途。
背景技术:
0、技术背景
1、五环三萜类天然产物齐墩果酸(oleanolic acid,简称oa)具有多种潜在的药用价值,如器官保护、治疗慢性肾病、抗肿瘤、降血脂、降血糖、抗炎,抗溃疡等,其较弱的生物活性和不理想的物理性质限制了他的临床应用,因此以齐墩果酸为构架的化学修饰也成为药物研究的方向之一。特别是近年来的研究证明这类衍生物的抗炎药理活性是通过干预多个生化信号传导通路实现的,如抑制多个诱发炎症的媒介,包括ifn-γ诱导的一氧化氮的合成酶(inos)和cox-2的合成等,特别是激活keap/nrf2/are信号通路,诱导多种抗炎和抗氧化蛋白的生成,例如ho-1和nqo-1的上调。具有高活性、低毒性以及高生物利用度的齐墩果酸衍生物一直是当前待解决的问题。
技术实现思路
1、本发明的目的在于提供一种新型的齐墩果酸酰胺衍生物,用于治疗多发性硬化症(ms)、阿尔兹海默症(ad)、帕金森症(pd)、亨廷顿氏症(hd)、肌萎缩侧索硬化症(als)、弗里德莱西氏公济失调(frda)、脊髓性肌萎缩症(sma)、视神经脊髓炎(nmo)和脊髓小脑共济失调症(sca)以及其它神经退行性疾病,也可用于治疗脑卒中、自身免疫性疾病、糖尿病和肾病等其它慢性病。
2、本发明的另一目的在于提供该抑制剂的制备方法。
3、本发明的第一方面,提供了一种如通式i所示的化合物,或其各类异构体和药学上可以接受的盐:
4、
5、其中,z为c2-c10烯基、c1-c6羟基烷基、-c2-c6亚烷基-s-c1-c6烷基、-c2-c6亚烷基-o-c1-c6烷基、-c0-c6亚烷基-nr1r2、-nrg-so2nrarb、-nrg-s(o)2rc、-c0-c6亚烷基-c(o)nrarb、-c0-c6亚烷基-nhc(o)rc、-c0-c6亚烷基-nhc(o)c(o)nrarb、-c0-c6亚烷基-nhc(o)c(o)ora、-c0-c6亚烷基-nhc(o)nrarb、-c2-c6亚烷基-p(o)me2、-c2-c6亚烷基-p(o)(ome)2、-c0-c6亚烷基-3-10元非芳香性杂环基、-c0-c6亚烷基-取代或未取代的c6-c10芳基、或-c0-c6亚烷基-取代或未取代的c3-c10杂芳基;所述烷基、c6-c10芳基、c3-c10杂芳基、3-10元非芳香性杂环基、c3-c6环烷基、或c3-c10环烯基各自独立地为未取代或被一个、两个或多个各自独立地选自下列的取代基所取代:卤素、-oh、羰基、-c0-c6亚烷基-cn、-c0-c6亚烷基-cooh、c1-c6烷基、-c0-c6亚烷-c3-c6环烷基、-c0-c6亚烷基氧基-c1-c6烷基-、c1-c6卤代烷基、c1-c6亚烷基-oh、c0-c6亚烷基-b(oh)2、c1-c6卤代烷氧基、c2-c10烷氧基烷基、c2-c10卤代烷氧基烷基、c1-c6羟基烷基、-c0-c6亚烷基-s-c1-c6烷基-、-c0-c6亚烷基-c6-c10芳基、-c0-c6亚烷-x-c6-c10芳基、-c0-c6亚烷基-5-10元杂芳基、-c0-c6亚烷基-x-5-10元杂芳基、-c0-c6亚烷基-3-10元非芳香性杂环基(其中杂原子可独立为一个或多个硫、氧、nh或nrg)、-c0-c6亚烷基-c3-c10环稀基、-c0-c6亚烷基-corc、-c0-c6亚烷基-co2c1-c6烷基、-c0-c6亚烷基-conrarb、-c0-c6亚烷基-so2nrarb、-c0-c6亚烷基-s(o)2rc、sf5、-c0-c6亚烷基-nrarb、-c0-c6亚烷基-nhc(o)rc、-c0-c6亚烷基-nhc(o)c(o)nrarb、-c0-c6亚烷基-nhc(o)c(o)ora、-c0-c6亚烷基-nhc(o)nrarb、-c0-c6亚烷基-p(o)me2、-c0-c6亚烷基-p(o)(ome)2、-c0-c6亚烷基c3-c6环烷氧基、-c0-c6亚烷基c1-c6烷氧基、-c0-c6亚烷基c1-c6卤代烷氧基、-c0-c6亚烷基-c≡c-r2、-o-c1-c6亚烷基-c≡c-r2、-s-c1-c6亚烷基-c≡c-r2、-c0-c6亚烷基-c(ra)=c(rb)-r2;
6、r1和r2分别独立为氢、取代或未取代的c1-c10烷基、取代或未取代的c3-c10环烷基、取代或未取代的c2-c10烯基、c1-c6羟基烷基、-c2-c6亚烷基-s-c1-c6烷基、-c2-c6亚烷基-o-c1-c6烷基、-c2-c6亚烷基-conrarb、-c0-c6亚烷基-so2nrarb、-c0-c6亚烷基-s(o)2rc、-c0-c6亚烷基-nrarb、-c0-c6亚烷基-c(o)nrarb、-c0-c6亚烷基-nhc(o)rc、-c0-c6亚烷基-nhc(o)c(o)nrarb、-c0-c6亚烷基-nhc(o)c(o)ora、-c0-c6亚烷基-nhc(o)nrarb、-c2-c6亚烷基-p(o)me2、-c2-c6亚烷基-p(o)(ome)2、-c2-c6亚烷基-3-10元非芳香性杂环基、-c0-c6亚烷基-取代或未取代的c6-c10芳基、或-c0-c6亚烷基-取代或未取代的c3-c10杂芳基;所述烷基、c6-c10芳基、c3-c10杂芳基、3-10元非芳香性杂环基、c3-c6环烷基、或c3-c10环烯基各自独立地为未取代或被一个、两个或多个各自独立地选自下列的取代基所取代:rg、卤素或c0-c6亚烷基-b(oh)2;r1和r2可以与它们连接的氮原子或碳原子一起可以形成三至八元环或四至八元杂环,其中可含杂原子,比如硫、氧、nh或nrg;所述的三至八元环或四至八元杂环可被一个或多个re取代;
7、re为h、c1-c6烷基或c1-c6卤代烷基;
8、rg各自独立地为h、c1-c6烷基、c3-c6环烷基、c1-c6卤代烷基、c3-c10环烯基、c1-c6烷氧基、c1-c6环烷氧基、c6-c10芳基、5-10元杂芳基、3-10元非芳香性杂环基、-c0-c6亚烷基cf3、-c0-c6亚烷基cn、-c0-c6亚烷基-oh、-c1-c6亚烷-c1-c6烷氧基、-c1-c6亚烷-c1-c6环烷氧基、c2-c6亚烷基-nrarb、c2-c6亚烷基-nrbc(o)ra、c2-c6亚烷基-nrbs(o)2ra、c2-c6亚烷基-s(o)2ra、c2-c6亚烷基-s(o)2nrbra、c1-c6亚烷基-co2h、-c1-c6亚烷基-co2c1-c6烷基、c1-c6亚烷基-cora、-c0-c6亚烷基-conrarb,-c2-c6亚烷基-p(o)me2、-c2-c6亚烷基-p(o)(ome)2;所述c1-c6烷基、c3-c6环烷基、c1-c6环烷氧基、c6-c10芳基、5-10元杂芳基、3-10元非芳香性杂环基、或c3-c10环烯基各自独立地为未取代或被一个、两个或多个各自独立地选自下列的取代基所取代:卤素、c1-c6烷基、c3-c6环烷基、c1-c4烷氧基、c0-c6亚烷基nrarb、-c0-c6亚烷基cn、-c0-c6亚烷基oh;
9、ra、rb各自独立为氢、取代或未取代的c1-c10烷基、取代或未取代的c3-c10环烷基、取代或未取代的c2-c10烯基、取代或未取代的c6-c10芳基、或取代或未取代的c3-c10杂芳基;ra和rb可以它们连接的氮原子或碳原子一起可以形成三至八元环或四至八元杂环,其中可含杂原子,比如硫、氧、nh或nrg;所述的三至八元环或四至八元杂环可被一个或多个re取代;
10、l为-c0-c6亚烷基、-oc0-c6亚烷基、-c0-c6亚烷基-o-、-c0-c6亚烷基-nrg-c0-c6亚烷基或-nrg-c0-c6亚烷基-nrg;
11、r3和r4分别独立为氢、氟、取代或未取代的c1-c10烷基、取代或未取代的c3-c10环烷基、取代或未取代的c2-c10烯基、c1-c6羟基烷基、-c0-c6亚烷基-s-c1-c6烷基、-c0-c6亚烷基-o-c1-c6烷基、-c1-c6亚烷基-conrarb、-c1-c6亚烷基-so2nrarb、-c1-c6亚烷基-s(o)2rc、-c0-c6亚烷基-nrarb、-c1-c6亚烷基-c(o)nrarb、-c0-c6亚烷基-nhc(o)rc、-c0-c6亚烷基-nhc(o)c(o)nrarb、-c0-c6亚烷基-nhc(o)c(o)ora、-c0-c6亚烷基-nhc(o)nrarb、-c0-c6亚烷基-p(o)me2、-c0-c6亚烷基-p(o)(ome)2、-c2-c6亚烷基-3-10元非芳香性杂环基、-c0-c6亚烷基-c6-c10芳基、或-c0-c6亚烷基-c3-c10杂芳基;所述烷基、c6-c10芳基、c3-c10杂芳基、3-10元非芳香性杂环基、c3-c6环烷基、或c3-c10环烯基各自独立地为未取代或被一个、两个或多个各自独立地选自下列的取代基所取代:rg、卤素或c0-c6亚烷基-b(oh)2;r1和r2可以它们连接的氮原子或碳原子一起可以形成三至八元环或四至八元杂环,其中可含杂原子,比如硫、氧、nh或nrg;所述的三至八元环或四至八元杂环可被一个或多个re取代;r3和r4可以与它们连接的碳原子一起可以形成三至八元环或四至八元杂环,其中可含杂原子,比如硫、氧、nh或nrg;所述的三至八元环或四至八元杂环可被一个或多个re取代;
12、n为0或1至6的整数。
13、在另一优选中,所述通式i化合物为式ii所示化合物:
14、
15、其中rg、r3、r4和z如通式i所述。
16、在另一优选中,所述通式i化合物为式iii所示化合物:
17、
18、其中rg和z如通式i所述。
19、在另一优选中,所述通式i化合物为式iv所示化合物:
20、
21、其中rg如通式i所述;r6、r7和r8分别独立为氢、取代或未取代的c1-c10烷基、取代或未取代的c3-c10环烷基、取代或未取代的c6-c10芳基、取代或未取代的c3-c10杂芳基、取代或未取代的3-10元非芳香性杂环基。
22、在另一优选例中,所述通式i至通式iv化合物为:
23、
24、
25、
26、
27、
28、
29、
30、
31、
32、在另一优选例中,所述的通式i至通式iv的化合物包括所有立体异构体。
33、在另一优选例中,所述的立体异构体为顺反异构体。
34、在另一优选例中,所述的化合物为光学纯异构体。
35、在另一优选例中,所述的化合物是外消旋体。
36、在另一优选例中,所述的立体异构体是对映异构体。
37、在另一优选例中,所述的化合物中任一个或多个氢原子可被氘原子取代。
38、在另一优选例中,所述的通式i至通式iv的化合物包括其前药。
39、在另一优选例中,所述通式i至通式iv药学上可接受的盐选自下组:盐酸盐、氢溴酸盐、硫酸盐、磷酸盐、甲磺酸盐、三氟甲磺酸盐、苯磺酸盐、对甲苯磺酸盐(甲苯磺酸盐)、1-萘磺酸盐、2-萘磺酸盐、乙酸盐、三氟乙酸盐、苹果酸盐、酒石酸盐、柠檬酸盐、乳酸盐、草酸盐、琥珀酸盐、富马酸盐、马来酸盐、苯甲酸盐、水杨酸盐、苯乙酸盐、扁桃酸盐。
40、本发明的第二方面,提供第一方面所述的通式i至通式iv化合物的制备方法,其中,所属方法为选自以下方案之一。
41、路线1
42、
43、本发明的第三方面,提供第一方面所述的通式i至通式iv化合物的用途,用于治疗多发性硬化症(ms)、阿尔兹海默症(ad)、帕金森症(pd)、亨廷顿氏症(hd)、肌萎缩侧索硬化症(als)、弗里德莱西氏公济失调(frda)、脊髓性肌萎缩症(sma)、视神经脊髓炎(nmo)和脊髓小脑共济失调症(sca)以及其它神经退行性疾病,也可用于治疗脑卒中、自身免疫性疾病、糖尿病、肾病及其它慢性病。
44、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一赘述。
- 还没有人留言评论。精彩留言会获得点赞!