制备苯唑草酮中间体的方法与流程
本发明涉及农药中间体的制备领域,具体涉及一种制备苯唑草酮中间体的方法。
背景技术:
1、苯唑草酮是巴斯夫首创研制的苯甲酯吡唑酮类除草剂,属于对羟基苯基丙酮酸酯双氧化酶(hppd)类抑制剂。其英文通用名称为topramezone,中文名称为苯唑草酮或苯吡唑草酮,商品名为campusr或“苞卫”,能有效防除玉米地一年生禾本科杂草和阔叶杂草,对玉米安全,但其使用范围也已逐渐扩大至水稻及甘蔗等作物,且与其他农药可安全进行复配使用。2018年全球苯唑草酮市场规模约为1.09亿美元,原药应用总量约为269.35t,其中玉米田市场占比65.55%,其他作物约占34.45%。苯唑草酮具有优异的药效和广阔的市场前景,但其难度极高的合成工艺使其售价高昂并因此限制了它的广泛使用。
2、目前苯唑草酮的制备工艺主要包括以下两条路线:
3、路线1:
4、
5、路线2:
6、
7、其中,路线1中化合物(8)的制备(参见us20026469176)需要经过超低温反应构建异噁唑环,同时该路线还用到剧毒的一氧化碳和昂贵的金属钯催化剂,导致成本居高不下。
8、cn103788083a公开了制备路线2中化合物(7),制备路线如下,
9、
10、起始原料的来源困难,也是参照us20026469176中的方法制备,同时在转变为羧基的过程中用到正丁基锂在-100℃至-60℃的超低温条件下反应,工业化生产困难。
11、综上,现有技术中制备苯唑草酮及其中间体的方法存在起始原料来源困难、反应条件苛刻、收率和纯度低以及成本较高的技术问题;因此,需要寻求一种条件温和、收率和纯度以及成本较低的制备苯唑草酮及其中间体的方法。
技术实现思路
1、本发明的目的是为了克服现有技术存在的起始原料来源困难、反应条件苛刻、收率和纯度低以及成本较高的技术缺陷,提供一种制备苯唑草酮中间体的方法,该方法具有条件温和、收率和纯度以及成本较低的优势。
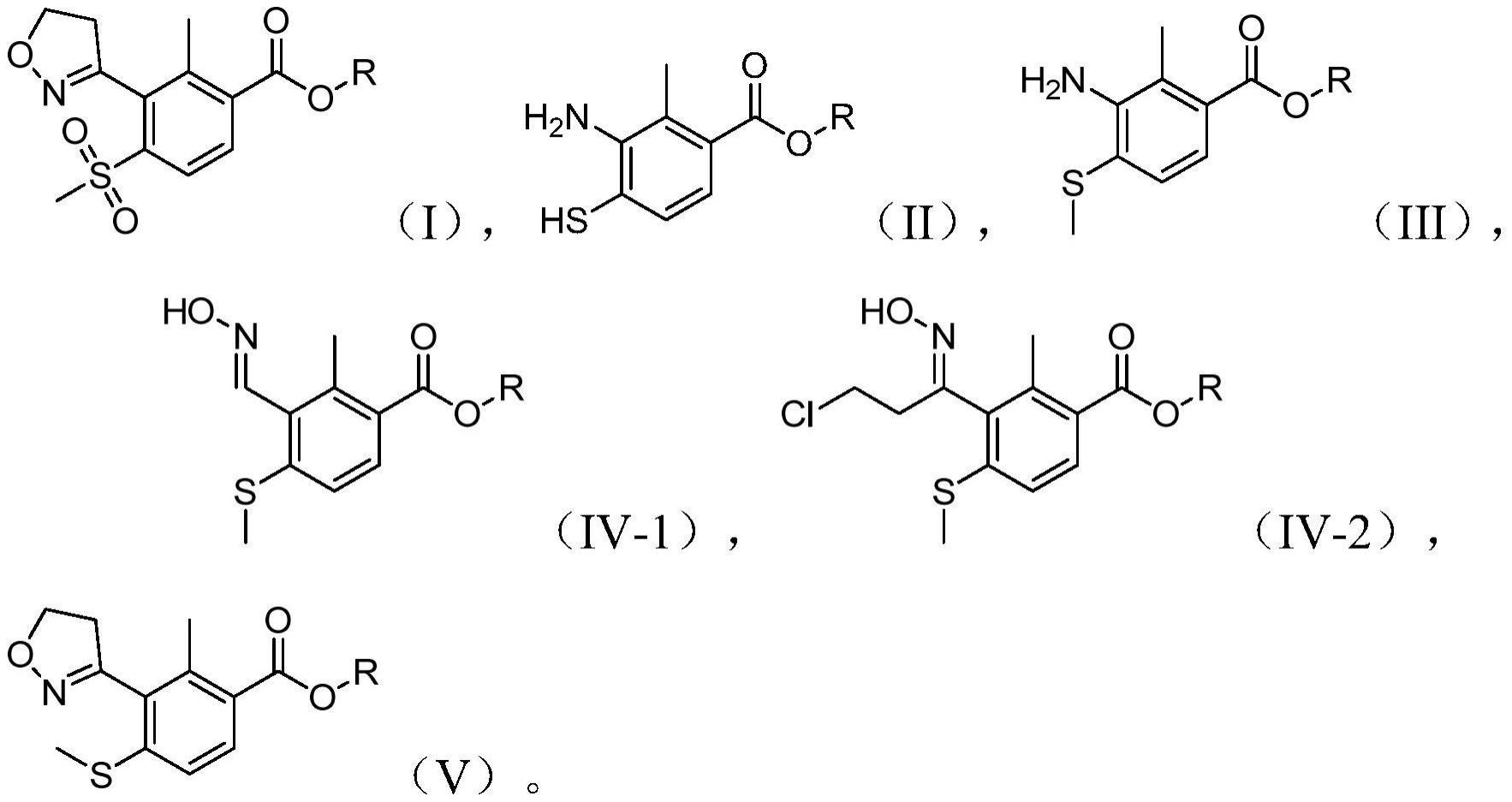
2、为了实现上述目的,本发明提供一种制备苯唑草酮中间体的方法,该方法包括以下步骤:
3、(1)在第一溶剂的存在下,将式(ii)所示的化合物与甲基化试剂进行甲基化反应,得到式(iii)所示的化合物,
4、
5、(2)将式(iii)所示的化合物经重氮化反应后,再与甲醛肟进行第一反应,得到式(iv-1)所示的化合物,
6、或者,
7、将式(iii)所示的化合物经重氮化反应后,再与氯代丙醛肟进行第二反应,得到式(iv-2)所示的化合物,
8、
9、(3)将式(iv-1)所示的化合物与次氯酸钠进行第三反应后,再与乙烯进行第四反应,得到式(v)所示的化合物;或者,
10、在碱性条件下,将式(iv-2)所示的化合物进行关环反应,得到式(v)所示的化合物,
11、
12、(4)将式(v)所示的化合物进行氧化反应,得到式(i)所示的苯唑草酮中间体,
13、
14、其中,式(i)-(v)中,r为c1-c6的烷基。
15、优选地,步骤(1)中,式(iii)所示的化合物还可以由以下方法制得:
16、i、在溶剂-i的存在下,将3,4-二氯甲苯和傅克烷基化试剂进行傅克烷基化反应后,再与硝化试剂进行硝化反应,得到式(vi)所示的化合物,
17、
18、ii、将式(vi)所示的化合物与酯化试剂进行酯化反应,得到式(vii)所示的化合物,
19、
20、iii、在非质子极性溶剂的存在下,将式(vii)所示的化合物与甲硫醇钠进行第五反应,得到式(viii)所示的化合物,
21、
22、iv、将式(viii)所示的化合物经过氢化还原反应,得到式(iii)所示的化合物。
23、与现有技术相比,本发明提供了一种制备苯唑草酮中间体(式(i)所示结构)的新方法(全新的工艺路线)。本发明选用式(ii)所示结构的化合物或者3,4-二氯甲苯作为起始原料,相对容易获得,并且通过巧妙的设计步骤(1)-(4),最终获得目标化合物,避免了例如插羰反应中条件苛刻以及成本高的缺陷,具有条件温和,反应收率和纯度较高以及成本较低的优势,利于工业化生产。
技术特征:
1.一种制备苯唑草酮中间体的方法,其特征在于,该方法包括以下步骤:
2.根据权利要求1所述的方法,其中,步骤(1)中,相对于1mol式(ii)所示的化合物,所述甲基化试剂的用量为0.95-2mol,优选为1-1.5mol;
3.根据权利要求1所述的方法,其中,步骤(1)中,式(iii)所示的化合物还可以由以下方法制得:
4.根据权利要求3所述的方法,其中,步骤i中,相对于1mol的3,4-二氯甲苯,所述傅克烷基化试剂的用量为0.95-2mol,优选为1-1.5mol;所述硝化试剂的用量为1-2mol,优选为1-1.5mol;
5.根据权利要求3或4所述的方法,其中,步骤ii中,相对于1mol式(vi)所示的化合物,所述酯化试剂的用量为1-2mol,优选为1-1.5mol;
6.根据权利要求3-5中任意一项所述的方法,其中,步骤iii中,相对于1mol式(vii)所示的化合物,甲硫醇钠的用量为1-2mol,优选为1-1.5mol;
7.根据权利要求1-6中任意一项所述的方法,其中,步骤(2)中,所述重氮化反应的条件包括:温度为-10℃至5℃,优选为-5℃至0℃;时间为1-10h,优选为2-5h;
8.根据权利要求1-7中任意一项所述的方法,其中,步骤(2)中,相对于1mol式(iii)所示的化合物,甲醛肟和氯代丙醛肟的用量各自独立地为1-5mol,优选为1-2mol;
9.根据权利要求1-8中任意一项所述的方法,其中,步骤(3)中,相对于1mol式(iv-1)所示的化合物,次氯酸钠的用量为1-5mol,优选为1-2mol;乙烯的用量为2-20mol,优选为2-5mol;
10.根据权利要求1-9中任意一项所述的方法,其中,步骤(4)中,所述氧化反应的条件包括:温度为50-100℃,优选为70-80℃;时间为1-15h,优选为2-8h;
技术总结
本发明涉及农药中间体的制备领域,公开了一种制备苯唑草酮中间体的方法,包括:(1)在第一溶剂的存在下,将式(II)所示的化合物经甲基化反应得到式(III)所示的化合物;(2)将式(III)所示的化合物经重氮化反应后,分别与甲醛肟、氯代丙醛肟反应,分别得到式(IV‑1)和式(IV‑2)所示的化合物;(3)将式(IV‑1)所示的化合物与次氯酸钠反应后,再与乙烯反应,或者,在碱性条件下,将式(IV‑2)所示的化合物关环,得到式(V)所示的化合物;(4)将式(V)所示的化合物经氧化反应得到式(I)所示的苯唑草酮中间体;其中,式(I)‑(V)中,R为C1‑C4的烷基。该方法条件温和、纯度和收率较高。
技术研发人员:焦体,李星强,王志会,李生学
受保护的技术使用者:帕潘纳(北京)科技有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!