一种用于治疗胃癌的药物及其制备方法
1.本发明涉及医药领域,具体来说,本发明涉及一种用于治疗胃癌的药物及其制备方法。
背景技术:
2.胃癌是全世界最常见的恶性肿瘤之一,虽然近年来其发病率和死亡率均有下降趋势,但在所有恶性肿瘤中,胃癌的发病率仍居第5位,死亡率居第3位。外科手术是胃癌惟一的根治性手段,但80%以上的胃癌患者确诊时已为晚期,大多数伴有广泛的侵犯和远处转移,失去了根治性手术的机会,此时需要更多的综合治疗,包括化疗、放疗、靶向治疗、免疫治疗等。胃癌的化疗药包括铂类化合物、氟嘧啶类、紫杉类、蒽环类和伊立替康等,其对胃癌的治疗均有疗效。联合化疗比单药化疗更能延长患者的总生存期。
3.咔啉(carbolines)类生物碱是广泛分布于自然界的一大类吲哚类生物碱,其属于由色氨酸衍生的非单萜吲哚类生物碱的一种,是一种由吲哚并吡啶构成的三环体系,包括α-咔啉、β-咔啉、γ-咔啉、δ咔啉,其中β-咔啉类(β-carbolines)生物碱是自然界中分布最广的,结构相对简单,数量众多,而且研究最为深入的一类咔啉类生物碱。已经报道的天然β-咔啉类生物碱多达数百种,广泛分布于自然界中,包括植物、海洋生物、蓝藻、蘑菇甚至动物中,代表性化合物有骆驼蓬碱、哈尔满碱、去甲基哈尔满碱等。不同的β-咔啉类生物碱具有不同生物活性,包括抗炎、抗菌、抗病毒、抗肿瘤、抗疟疾、杀皂,gabaa、5-ht2serotonin、imidazoline受体结合活性,pde5受体抑制活性等等。
技术实现要素:
4.本发明在现有β-咔啉类生物碱的基础上,提供了一种新颖的β-咔啉类生物碱衍生物,具有良好的胃癌细胞增殖抑制活性,能够用于胃癌的治疗。
5.本发明提供了一种式(i)所示化合物、其药学上可接受的盐、立体异构体、互变异构体、溶剂化物和前药:
[0006][0007]
其中,r0独立地选自氢、氘、卤素、氰基、硝基、氨基、羟基、c1-6烷基、c1-c6烷氧基、卤代c1-c6烷基、取代或未取代的c6-c14芳基;
[0008]
r1、r2独立地选自氢、c1-c6烷基、c3-c10环烷基、卤代c1-c6烷基,并且r1、r2中的至少一个不为氢;或者r1、r2一起形成-(ch2)
n-;
[0009]
r3选自c1-c6烷基、取代或未取代的c6-c14芳基、取代或未取代的c6-c14芳基-c1-2亚烷基;
[0010]
l选自c1-c6亚烷基;
[0011]
het选自取代或未取代的5-10元杂芳基;
[0012]
m选自1、2、3、4或5;
[0013]
n选自2、3、4、5或6。
[0014]
在一些优选的实施方案中,r0独立地选自氢、氘、氟、氯、溴、氰基、硝基、氨基、羟基、甲基、乙基、异丙基、叔丁基、甲氧基、乙氧基、三氟甲基、苯基。
[0015]
优选的,r0选自氢。
[0016]
在一些优选的实施方案中,r1、r2独立地选自氢、甲基、乙基、异丙基、正丙基、叔丁基、三氟甲基、环丙基、环丁基、环戊基、环己基,并且r1、r2中的至少一个不为氢;或者r1、r2一起形成-ch2ch
2-、-ch2ch2ch
2-、-ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch2ch
2-。
[0017]
优选的,r1选自氢、甲基,r2选自甲基、异丙基、环丙基;或者r1、r2一起形成-ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch
2-。
[0018]
优选的,r1选自氢,r2选自异丙基、环丙基;或者r1选自甲基、r2选自甲基;或者r1、r2一起形成-ch2ch2ch2ch2ch
2-。
[0019]
在一些优选的实施方案中,r3选自甲基、乙基、苯基、苄基。
[0020]
优选的,r3选自甲基、乙基。
[0021]
在一些优选的实施方案中,l选自-ch
2-、-ch2ch
2-、-ch2ch2ch
2-、-ch2ch2ch2ch
2-。
[0022]
优选的,l选自-ch
2-、-ch2ch
2-。
[0023]
在一些优选的实施方案中,het选自取代或未取代的5-7元杂芳基,所述“取代或未取代的”是指未被取代,或者被选自氘、卤素、氰基、硝基、氨基、羟基、c1-4烷基、c1-c4烷氧基、卤代c1-c4烷基的基团取代。
[0024]
优选的,het选自取代或未取代的:噁唑基、异噁唑基、噻唑基、异噻唑基、吡啶基、嘧啶基,所述“取代或未取代的”是指未被取代,或者被1-3个选自氘、氟、氯、溴、氰基、硝基、氨基、羟基、甲基、乙基、异丙基、正丙基、甲氧基、乙氧基、三氟甲基的基团取代。
[0025]
更优选的,het选自取代或未取代的:异噁唑基、异噻唑基、吡啶基、嘧啶基,所述“取代或未取代的”是指未被取代,或者被选自1-3个选自氟、氯、甲基、乙基、异丙基、正丙基、三氟甲基的基团取代。
[0026]
本发明中,所述“取代或未取代”是指未被取代或者被选自以下的基团取代:氘、卤素、氰基、硝基、氨基、羟基、c1-c4烷基、c1-c4烷氧基、卤代c1-c4烷基。
[0027]
优选的,所述“取代或未取代”是指未被取代或者被选自以下的基团取代:氘、氟、氯、溴、氰基、硝基、氨基、羟基、甲基、乙基、异丙基、正丙基、甲氧基、乙氧基、三氟甲基。
[0028]
在一些优选的实施方案中,所述式(i)所示化合物具有以下式(ii)所示结构:
[0029][0030]
其中,r1、r2独立地选自氢、甲基、乙基、异丙基、正丙基、叔丁基、三氟甲基、环丙基、
环丁基、环戊基、环己基,并且r1、r2中的至少一个不为氢;或者r1、r2一起形成-ch2ch
2-、-ch2ch2ch
2-、-ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch2ch
2-;
[0031]
r3选自甲基、乙基、苯基、苄基;
[0032]
l选自-ch
2-、-ch2ch
2-、-ch2ch2ch
2-、-ch2ch2ch2ch
2-;
[0033]
het选自取代或未取代的:噁唑基、异噁唑基、噻唑基、异噻唑基、吡啶基、嘧啶基,所述“取代或未取代的”是指未被取代,或者被1-3个选自氘、氟、氯、溴、氰基、硝基、氨基、羟基、甲基、乙基、异丙基、正丙基、甲氧基、乙氧基、三氟甲基的基团取代。
[0034]
在一些优选的实施方案中,r1选自氢、甲基,r2选自甲基、异丙基、环丙基;或者r1、r2一起形成-ch2ch2ch2ch
2-、-ch2ch2ch2ch2ch
2-;
[0035]
r3选自甲基、乙基;
[0036]
l选自-ch
2-、-ch2ch
2-;
[0037]
het选自取代或未取代的:异噁唑基、异噻唑基、吡啶基、嘧啶基,所述“取代或未取代的”是指未被取代,或者被选自1-3个选自氟、氯、甲基、乙基、异丙基、正丙基、三氟甲基的基团取代。
[0038]
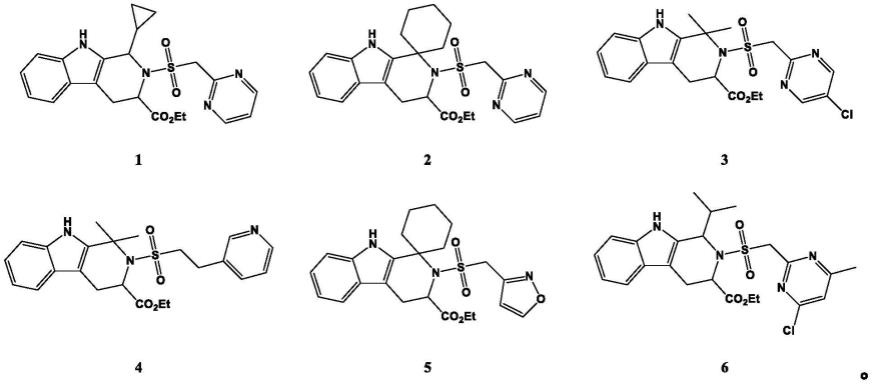
在一些优选的实施方案中,所述式(i)所示化合物选自:
[0039][0040]
本发明中,所述术语“卤素”是指氟、氯、溴和碘。术语“卤代”是指被氟、氯、溴或碘取代。
[0041]
本发明中,所述术语“杂芳基”是指含至少1个选自o、n和s的杂原子,任选含1-3个独立选自o、n和s的另外的杂原子的任何芳环结构。所述杂芳基可以是单环(例如5-6元单环杂芳基),或者双环(例如9-10元双环杂芳基),所述杂芳基可连接在环的任何n原子或c原子上,以便形成稳定的结构。适宜的杂芳基的实例包括,但不限于吡咯基、呋喃基、噻吩基、噁唑基、咪唑基、吡唑基、异噁唑基、噻唑基、异噻唑基、三唑基、噁二唑基、噻二唑基、吡啶基、嘧啶基、哒嗪基、吡嗪基、吡喃基、中氮茚基、吲哚基、异吲哚啉基、吲唑基、苯并呋喃基、苯并噻吩基、苯并咪唑基、苯并噻唑基、嘌呤基、喹嗪基、喹啉基、异喹啉基、噌啉基、酞嗪基、喹唑啉基、喹喔啉基、萘啶基、蝶啶基等。
[0042]
为了应用在药物中,本发明中,术语“药学上可接受的盐”包括酸加成盐,其例如,通过将所述化合物溶液与药学上可接受的酸诸如盐酸、硫酸、磷酸、反丁烯二酸、顺丁烯二酸、丁二酸、乙酸、苯甲酸、柠檬酸、酒石酸的溶液混合形成。代表性的药学上可接受的盐包
括如下:盐酸盐、二盐酸盐、氢溴酸盐、硝酸盐、硫酸氢盐、硫酸盐、磷酸盐、磷酸氢盐、磷酸二氢盐、碳酸盐、碳酸氢盐、硼酸盐、乙酸盐、苯磺酸盐、苯甲酸盐、酒石酸氢盐、樟脑磺酸盐、克拉维酸盐、柠檬酸盐、依地酸盐、乙磺酸盐、延胡索酸盐、葡庚糖酸盐、葡糖酸盐、谷氨酸盐、羟基萘甲酸盐、异硫代硫酸盐、乳酸盐、乳糖酸盐、月桂酸盐、苹果酸盐、顺丁烯二酸盐、反丁烯二酸盐、丁二酸盐、扁桃酸盐、甲磺酸盐、萘磺酸盐、油酸盐、棕榈酸盐、泛酸盐、聚半乳糖醛酸盐、水杨酸盐、硬脂酸盐、丹宁酸盐、甲苯磺酸盐和戊酸盐。
[0043]
当本发明化合物具有至少1个手性中心时,它们可相应地以对映体形式存在。当化合物具有2个或更多个手性中心时,它们可相应地以非对映异构体形式存在。应该理解的是,所有这样的立体异构体及其混合物均包括在本发明范围之内。
[0044]
本发明中,术语“互变异构体”是指经由低能垒互相转化的不同能量的结构异构体。本发明化合物可以以不同的互变异构体形式存在,所有这些形式均包括在本发明的范围内。
[0045]
在本发明中,术语“溶剂化物”是指一个或多个溶剂分子与本发明的化合物所形成的缔合物。形成溶剂化物的溶剂包括,但并不限于,水,异丙醇,乙醇,甲醇,二甲亚砜,乙酸乙酯,乙酸。
[0046]
本发明中,术语“前药”是指本发明化合物的功能性衍生物,其易于在体内转化为所需的化合物。选择和制备适宜的前药衍生物的常规程序,在例如,“design of prodrugs”,h.bundgaard,elsevier编著,1985中描述。
[0047]
本发明的另一个方面在于提供一种包括式(i)所示化合物、其药学上可接受的盐、立体异构体、互变异构体、溶剂化物和前药的药物组合物。
[0048]
在一些实施方案中,所述药物组合物包括药学上可接受的赋形剂。
[0049]
典型的药物组合物为:散剂、片剂、颗粒剂、胶囊剂、溶液剂、乳剂、混悬剂、注射剂、喷雾剂、气雾剂、粉雾剂、洗剂、搽剂、软膏剂、硬膏剂、糊剂、贴剂等。
[0050]
术语“赋形剂”指的是:抗黏着剂、抗氧化剂、黏合剂、包衣剂、压片助剂、崩解剂、润滑剂、乳化剂等。典型的赋形剂包括:淀粉、碳酸钙、磷酸钙、硬脂酸钙、交联羧甲基纤维素、交联聚乙烯吡咯烷酮、柠檬酸、交聚维酮、半胱氨酸、乙基纤维素、明胶、羟丙基纤维素、羟丙基甲基纤维素、乳糖、硬脂酸镁、麦芽糖醇、甘露醇、蛋氨酸、甲基纤维素、对羟基苯甲酸甲酯、聚乙二醇、柠檬酸钠、山梨醇、硬脂酸、蔗糖、滑石粉、二氧化钛等。
[0051]
本发明化合物的每日剂量可在很大范围内变化,例如每成人每天0.01-1000mg。对于口服给药,优选提供片剂形式的组合物,所述片剂含0.01、0.05、0.1、0.5、1.0、2.5、5.0、10.0、15.0、25.0、50.0、100、150、200、250和500毫克的活性成分,为待治疗的患者进行症状的剂量调整。一般在每天约0.01mg/kg-约300mg/kg体重的剂量水平提供药物的有效量。优选地,该范围在从每天约0.5-约5.0mg/kg体重,最优选地,从每天约1.0-约3.0mg/kg体重。按照给药方案,可以每天给予本化合物1-4次。
[0052]
给药的最佳剂量可由本领域专业人员易于确定并且将依具体使用的化合物、给药模式、制剂的强度、给药方式以及疾病状况的进展不同而异。另外,与具体被治疗的患者有关的因素,包括患者年龄、体重、饮食和给药次数,将会产生调整剂量的需求。
[0053]
本发明还提供了一种药物组合,其为药物产品,可包括本发明式(i)所示化合物、其药学上可接受的盐、立体异构体、互变异构体、溶剂化物和前药以及可用于治疗癌症或对
于癌症的治疗有帮助的其他药剂。
[0054]
本发明发现了本发明化合物对于肿瘤细胞特别是胃癌细胞,例如sgc-7901、nci-n87、ags等的增殖具有十分优异的抑制活性,其甚至强于阳性对照药。
[0055]
因此,本发明还提供了本发明式(i)所示化合物、其药学上可接受的盐、立体异构体、互变异构体、溶剂化物和前药在制备药物中的用途,所述药物用于抗肿瘤。
[0056]
优选的,所述药物用于治疗胃癌。
[0057]
本发明还提供了一种制备本发明式(i)所示化合物的方法,其包括以下步骤:
[0058][0059]
化合物a与化合物b在冰醋酸中缩合生成中间体c,中间体c与化合物d经酯化反应生成中间体e,中间体e与中间体f反应生成式(i)所示化合物;
[0060]
其中,r
0-r3、l、het、m的定义如本文所述。
[0061]
有益效果
[0062]
本发明提供了一种用于治疗胃癌的药物,本发明还提供了所述药物的制备方法。本发明所述药物为β-咔啉类生物碱衍生物,具有良好的胃癌细胞(sgc-7901、nci-n87、ags)增殖抑制活性,因此可作为治疗胃癌的潜在药物。
具体实施方式
[0063]
在下文中更详细地描述了本发明以有助于对本发明的理解。
[0064]
所属领域的技术人员将认识到:本发明所描述的化学反应可以用来合适地制备许多本发明的其他化合物,且用于制备本发明的化合物的其它方法都被认为是在本发明的范围之内。例如,根据本发明那些非例证的化合物的合成可以成功地被所属领域的技术人员通过修饰方法完成,如适当的保护干扰基团,通过利用其他已知的试剂除了本发明所描述的,或将反应条件做一些常规的修改。另外,本发明所公开的反应或已知的反应条件也公认地适用于本发明其他化合物的制备。
[0065]
下面实施例中的实验方法,如无特殊说明,均为常规方法。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。
[0066]
实施例1:化合物1的制备
[0067][0068]
向圆底烧瓶中加入化合物1-a(4.08g,20mmol),再加入30ml的冰醋酸,搅拌使溶解,加热至回流,然后搅拌下缓慢滴加化合物1-b(15ml),回流反应,直至反应完全(tlc监测)。减压浓缩至干,残余物用甲醇-环己烷(5:1)重结晶,得到中间体1-c(4.56g,89%)。
[0069]
向圆底烧瓶中加入中间体1-c(2.56g,10mmol),再加入100ml无水乙醇,搅拌使溶解,冰浴至0-5℃,在此温度下缓慢滴加socl2(1.43g,12mmol),滴加完毕后移除冰浴并剧烈搅拌反应4h,真空脱除溶剂和多余的socl2,得到的中间体1-e直接投入下一步。
[0070]
向中间体1-e中加入65ml无水二氯甲烷,再加入2ml三乙胺,搅拌下分批加入化合物1-f(1.93g,10mmol),将反应混合物在室温搅拌15h。用50ml二氯甲烷稀释并用120ml饱和碳酸氢钠水溶液洗涤。分离有机层,用无水硫酸镁干燥,真空脱除溶剂,将残余物在硅胶上进行色谱分离,以体积梯度为0:100至30:80的乙酸乙酯:石油醚洗脱,得到白色固体的化合物1(3.70g,84%)。
[0071]
hr-esi-ms m/z 441.1580[m+h]
+
(理论值441.1597)。
[0072]
元素分析:c
22h24
n4o4s实测值:c,59.92;h,5.47;n,12.70;o,14.43;s,7.38(理论值:c,59.98;h,5.49;n,12.72;o,14.53;s,7.28)。
[0073]1h nmr(400mhz,dmso-d6)δ9.61(s,1h),8.63(d,j=7.0hz,2h),7.51(d,j=7.1hz,1h),7.35(d,j=7.2hz,1h),7.19(t,j=7.0hz,1h),7.14
–
7.02(m,2h),5.19(d,j=6.8hz,1h),4.85
–
4.72(m,3h),4.12(q,j=6.4hz,2h),3.19
–
3.05(m,2h),2.22(dp,j=6.8,5.6hz,1h),1.23(t,j=6.4hz,3h),0.63
–
0.42(m,4h)。
[0074]
实施例2:化合物2的制备
[0075][0076]
向圆底烧瓶中加入化合物1-a(4.08g,20mmol),再加入30ml的冰醋酸,搅拌使溶解,加热至回流,然后搅拌下缓慢滴加化合物2-b(20ml),回流反应,直至反应完全(tlc监测)。减压浓缩至干,残余物用甲醇重结晶,得到中间体2-c(4.4g,77%)。
[0077]
向圆底烧瓶中加入中间体2-c(2.84g,10mmol),再加入120ml无水乙醇,搅拌使溶解,冰浴至0-5℃,在此温度下缓慢滴加socl2(1.43g,12mmol),滴加完毕后移除冰浴并剧烈搅拌反应4h,真空脱除溶剂和多余的socl2,得到的中间体2-e直接投入下一步。
[0078]
向中间体2-e中加入80ml无水二氯甲烷,再加入2ml三乙胺,搅拌下分批加入化合物1-f(1.93g,10mmol),将反应混合物在室温搅拌18h。用60ml二氯甲烷稀释并用120ml饱和碳酸氢钠水溶液洗涤。分离有机层,用无水硫酸镁干燥,真空脱除溶剂,将残余物在硅胶上进行色谱分离,以体积梯度为0:100至35:75的乙酸乙酯:石油醚洗脱,得到淡黄色固体的化合物2(3.75g,80%)。
[0079]
hr-esi-ms m/z 469.1922[m+h]
+
(理论值469.1910)。
[0080]
元素分析:c
24h28
n4o4s实测值:c,61.58;h,6.05;n,11.99;o,13.76;s,6.69(理论值:c,61.52;h,6.02;n,11.96;o,13.66;s,6.84)。
[0081]1h nmr(400mhz,dmso-d6)δ10.25(s,1h),8.63(d,j=7.0hz,2h),7.47
–
7.38(m,2h),7.19(t,j=7.1hz,1h),7.15
–
7.03(m,2h),4.76(s,2h),4.71(t,j=8.6hz,1h),4.12(q,j=6.4hz,2h),3.17
–
3.02(m,2h),2.20(m,2h),2.02
–
1.91(m,2h),1.88
–
1.74(m,4h),1.55
–
1.38(m,2h),1.23(t,j=6.4hz,3h)。
[0082]
实施例3:化合物3的制备
[0083][0084]
按照实施例1相同的方法,区别在于用3-b代替1-b以及用3-f代替1-f,得到化合物3。
[0085]
hr-esi-ms m/z 463.1225[m+h]
+
(理论值463.1207)。
[0086]
元素分析:c
21h23
cln4o4s实测值:c,54.39;h,5.05;cl,7.60;n,12.14;o,13.93;s,6.90(理论值:c,54.48;h,5.01;cl,7.66;n,12.10;o,13.82;s,6.93)。
[0087]1h nmr(400mhz,dmso-d6)δ10.47(s,1h),8.07(s,2h),7.49
–
7.40(m,2h),7.17
–
7.05(m,2h),4.80(s,2h),4.73(t,j=8.6hz,1h),4.12(q,j=6.4hz,2h),3.17
–
3.02(m,2h),1.78(s,3h),1.73(s,3h),1.23(t,j=6.4hz,3h)。
[0088]
实施例4:化合物4的制备
[0089][0090]
按照实施例1相同的方法,区别在于用3-b代替1-b以及用4-f代替1-f,得到化合物4。
[0091]
hr-esi-ms m/z 463.1225[m+h]
+
(理论值442.1801)。
[0092]
元素分析:c
23h27
n3o4s实测值:c,62.63;h,6.19;n,9.54;o,14.38;s,7.20(理论值:c,62.56;h,6.16;n,9.52;o,14.49;s,7.26)。
[0093]1h nmr(400mhz,dmso-d6)δ10.47(s,1h),8.43-8.41(m,2h),7.54(d,j=7.7,1h),7.49
–
7.40(m,2h),7.29
–
7.22(m,1h),7.17
–
7.05(m,2h),4.72(t,j=8.6hz,1h),4.12(q,j=6.4hz,2h),3.60
–
3.42(m,2h),3.16
–
2.94(m,4h),1.78(s,3h),1.73(s,3h),1.23(t,j=6.4hz,3h)。
[0094]
实施例5:化合物5的制备
[0095][0096]
按照实施例1相同的方法,区别在于用2-b代替1-b以及有5-f代替1-f,得到化合物5。
[0097]
hr-esi-ms m/z 458.1770[m+h]
+
(理论值458.1750)。
[0098]
元素分析:c
23h27
n3o5s实测值:c,60.35;h,5.96;n,9.23;o,17.44;s,7.06(理论值:c,60.38;h,5.95;n,9.18;o,17.48;s,7.01)。
[0099]1h nmr(400mhz,dmso-d6)δ10.25(s,1h),8.61(d,j=7.2hz,1h),7.47
–
7.38(m,2h),7.15
–
7.03(m,2h),6.53(d,j=7.2hz,1h),4.76(t,j=8.6hz,1h),4.65
–
4.56(m,2h),4.12(q,j=6.4hz,2h),3.17
–
3.02(m,2h),2.20(m,2h),2.02
–
1.91(m,2h),1.88
–
1.74(m,4h),1.56
–
1.37(m,2h),1.23(t,j=6.4hz,3h)。
[0100]
实施例6:化合物6的制备
[0101][0102]
按照实施例1相同的方法,区别在于用6-b代替1-b以及用6-f代替1-f,得到化合物6。
[0103]
hr-esi-ms m/z 491.1535[m+h]
+
(理论值491.1520)。
[0104]
元素分析:c
23h27
cln4o4s实测值:c,56.28;h,5.55;cl,7.17;n,11.40;o,13.09;s,6.43(理论值:c,56.26;h,5.54;cl,7.22;n,11.41;o,13.03;s,6.53)。
[0105]1h nmr(400mhz,dmso-d6)δ9.29(s,1h),7.48(d,j=7.2hz,1h),7.31(d,j=7.2hz,
1h),7.12
–
7.00(m,2h),6.84(s,1h),5.26(d,j=7.4hz,1h),4.79(s,2h),4.74(t,j=8.6hz,1h),4.12(q,j=6.4hz,2h),3.19
–
3.05(m,2h),2.38(s,3h),2.13(septet,j=6.6hz,1h),1.23(d,j=8.6hz,3h),0.97(d,j=6.6hz,6h)。
[0106]
药效实施例:mtt法测试抑制胃癌细胞的活性
[0107]
将sgc-7901、nci-n87、ags细胞(来自中国科学院上海生命科学研究院细胞库)按常规肿瘤细胞培养方法按时还液、传代,收集对数生长期细胞株,分别接种于96孔培养板,每孔细胞数为1.0
×
105/100μl,然后置于5%co2培养箱培养,次日去掉培养基,加入不同浓度药物100μl(药物浓度采用对倍稀释),每个药物设置3个平行样,阴性对照组不加药物,5-氟尿嘧啶(5-fu)作为阳性对照,48h后,每孔加入mtt 10μl,继续培养4h,再每孔加入dmso100μl终止反应,常温放置1h,用酶标仪检测各孔在570nm处的吸光度od值,计算细胞生长抑制率(生长抑制率(%)=[(od
对照-od
实验
)/(od
对照-od
空白
)]
×
100%)。将得到的细胞生长抑制率用spss 22.0拟合,得到不同药物对sgc-7901、nci-n87、ags细胞生长的半数抑制率ic
50
。结果如下表1所示:
[0108]
表1:胃癌细胞增殖抑制活性
[0109][0110]
如表1所示出的,本发明化合物对于胃癌细胞(sgc-7901、nci-n87、ags)的增殖具有良好抑制活性,特别是r1、r2共同形成环己烷的本发明化合物2和5具有更佳的抑制活性。
[0111]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1