一种瑞卢戈利中间体及其制备方法与流程
本发明涉及到药物合成领域,具体地,涉及一种瑞卢戈利中间体及其制备方法。
背景技术:
1、瑞卢戈利(relugolix)是一款口服的gnrh受体拮抗剂,可以结合并阻断垂体前叶中的gnrh受体,减少促黄体生成激素(lh)和卵泡刺激素(fsh)的释放,从而降低女性卵巢生成的雌激素水平和男性睾丸激素的产生。瑞卢戈利子宫肌瘤适应症已在日本获批,前列腺癌适应症已在美国获批,除此之外子宫内膜异位症也在iii期中。适应症人群较为广泛。与同类药物相比,瑞卢戈利采用了反向添加疗法(add-back therapy),与同类药物单药疗法相比相对减少了雌激素水平过低相关的副作用的出现;前列腺癌适应症中疗效则略优于占据gnrh靶点药物市场一半左右的戈舍瑞林。
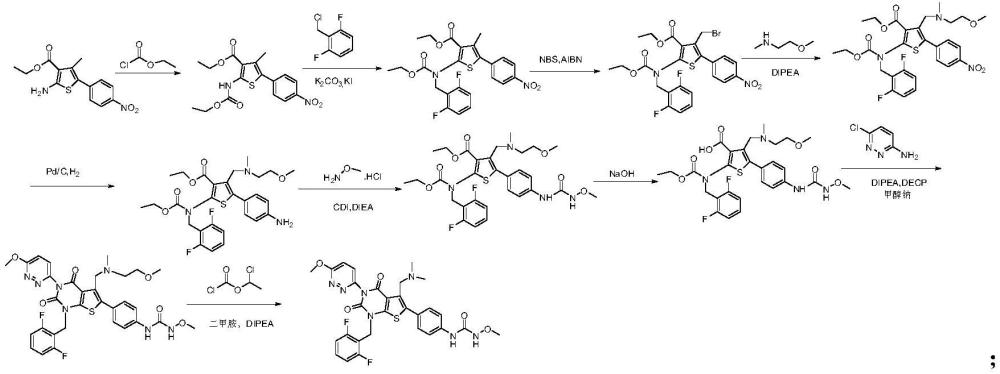
2、专利wo2004067535中公开了如下的瑞卢戈利及其中间体合成路线:
3、
4、专利wo2014051164中公开另一条瑞卢戈利及其中间体合成路线:
5、
6、以上两条合成路线中,硝基还原的步骤均为使用钯炭还原并且在氢化釜加压下进行,从而其大规模工业化生产受到限制。因此,本发明寻求一条更为简便、经济、安全、易实现规模放大的合成瑞卢戈利的新方法。
技术实现思路
1、本发明的目的提供一种简便、经济、安全、易实现规模放大的合成瑞卢戈利的新方法。
2、本发明的第一方面,提供了一种式i所示的化合物的制备方法,其特征在于,包括步骤:
3、(i)在第一溶剂中,化合物i-3与氨基保护剂反应,得到化合物i-4;
4、(ii)在第二溶剂中,缩合剂存在下,化合物i-4与3-氨基-6-甲氧基哒嗪或其盐酸盐反应,得到化合物i-5;
5、(iii)在第三溶剂中,碱存在下,化合物i-5发生关环反应,得到化合物i;
6、
7、式中,
8、r1为c1-c6烷基,优选地为甲基、乙基、正丙基、异丙基、正丁基或正戊基;
9、m为氨基保护基。
10、在另一优选例中,r1为正丙基。
11、在另一优选例中,步骤(i)中,所述的第一溶剂选自下组:甲醇、水、乙醇、正丙醇,异丙醇,正丁醇,叔丁醇、二氯甲烷、四氢呋喃、乙腈,或其组合。
12、在另一优选例中,步骤(i)中,所述的氨基保护剂与i-3摩尔比为0.8当量至5当量。
13、在另一优选例中,步骤(i)中,所述的溶剂使用量为2体积至20体积(以化合物i-3的摩尔体积比计算)。
14、在另一优选例中,步骤(i)中,所述的反应温度为20℃至100℃。
15、在另一优选例中,步骤(ii)中,所述的第二溶剂选自下组:n,n’-二甲基乙酰胺、n,n’-二甲基甲酰胺、二甲基亚砜、n-甲基吡咯烷酮。
16、在另一优选例中,步骤(ii)中,所述的缩合剂选自下组:丙基磷酸酐(t3p)、n,n’-羰基二咪唑(cdi)、2-(7-氮杂苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸盐(hatu)、苯并三氮唑-n,n,n',n'-四甲基脲六氟磷酸酯(hbtu)、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edci)、1-羟基苯并三唑(hobt)、二环己基碳二亚胺(dcc)。
17、在另一优选例中,所述的步骤(ii)中,优选3-氨基-6-甲氧基哒嗪或其盐酸盐与i-4摩尔比为1当量至3当量。
18、在另一优选例中,步骤(ii)中,缩合剂与i-4摩尔比为0.8当量至3当量。
19、在另一优选例中,步骤(ii)中,所述的第二溶剂使用量为3体积至10体积(以化合物i-4的摩尔体积比计算)。
20、在另一优选例中,步骤(ii)中,所述的反应温度为20℃至80℃。
21、在另一优选例中,步骤(iii)中,所述的第三溶剂选自下组:醇类(如甲醇、乙醇、异丙醇、丙醇、丁醇、乙二醇)、n,n’-二甲基甲酰胺、n,n’-二甲基乙酰胺、乙腈。
22、在另一优选例中,步骤(iii)中,所述的碱选自下组甲醇钠、乙醇钠、叔丁醇钠、叔丁醇钾、三乙胺、n,n-二异丙基乙基胺、氢氧化钠、氢氧化钾、氢氧化锂、碳酸钾、碳酸钠。
23、在另一优选例中,步骤(iii)中,所述的醇钠与i-5摩尔比为0.2当量至3当量。
24、在另一优选例中,步骤(iii)中,所述的第三溶剂使用量为5体积至30体积(以化合物i-4的摩尔体积比计算)。
25、在另一优选例中,步骤(iii)中,所述的反应温度为20℃至80℃。
26、在另一优选例中,所述方法还包括步骤:
27、s1)在第四溶剂中,碱存在下,化合物i-1发生水解反应,得到化合物i-2;
28、s2)在第五溶剂中,还原剂存在下,化合物i-2发生反应,得到化合物i-3;
29、
30、式中,
31、r1和r2各自独立地为c1-c6烷基。
32、在另一优选例中,步骤(s1)中,所述的第四溶剂选自下组:醇类(如甲醇、乙醇、异丙醇、丙醇、正丁醇、叔丁醇、乙二醇)、水,或其组合。
33、在另一优选例中,步骤(s1)中,所述的碱选自:氢氧化锂、氢氧化钾、氢氧化钠。
34、在另一优选例中,步骤(s2)中,所述的第五溶剂选自下组:醇类(如甲醇、乙醇、异丙醇、丙醇、丁醇、乙二醇)、四氢呋喃。
35、在另一优选例中,步骤(s2)中,还原剂为锌粉、铁粉和盐酸、硫酸、乙酸、氯化铵。
36、在另一优选例中,m选自:苄氧羰基、叔丁氧羰基、邻苯二甲酰基、苄基、对甲苯磺酰基、三氟乙酰基、芴甲氧羰基、烯丙氧羰基、邻(对)硝基苯磺酰基、三苯甲基;优选地,m为叔丁氧羰基。
37、在另一优选例中,所述氨基保护试剂选自:氯甲酸苄酯、二碳酸二叔丁酯、邻苯二甲酰氯、氯苄、三苯基氯甲烷、氯甲酸-9-芴基甲酯、氯甲酸烯丙酯;优选地,氨基保护试剂为二碳酸二叔丁酯。
38、在另一优选例中,r1为甲基、乙基、正丙基、异丙基、正丁基或正戊基,优选地为正丙基。
39、在另一优选例中,r1和r2各自独立地为甲基、乙基、正丙基、异丙基、正丁基或正戊基。
40、在另一优选例中,r2为甲基、乙基、正丙基、异丙基、正丁基或正戊基,优选地为乙基。
41、本发明的第二方面,提供了一种选自下组的中间体:
42、
43、式中,r1和m的定义如本发明第一方面所述,优选地,r1为正丙基;m为叔丁氧羰基。
44、本发明的第三方面,提供了一种式i-5化合物的制备方法,包括步骤:
45、(i)在第一溶剂中,化合物i-3与氨基保护剂反应,得到化合物i-4;
46、(ii)在第二溶剂中,缩合剂存在下,化合物i-4与3-氨基-6-甲氧基哒嗪或其盐酸盐反应,得到化合物i-5;
47、
48、式中,
49、r1和r2各自独立地为c1-c6烷基。
50、本发明的第四方面,提供了一种瑞卢戈利的制备方法,所述方法包括步骤:
51、(iii)在第三溶剂中,碱存在下,化合物i-5发生关环反应,得到化合物i;
52、(iv)在第六溶剂中,酸存在下,化合物i脱保护基,得到化合物i';
53、(v)在第七溶剂中,缩合剂和碱存在下,化合物i'与甲氧基胺或其盐(优选地,甲氧基胺盐酸盐)反应,得到瑞卢戈利;
54、
55、式中,r1和m的定义如本发明第一方面所述。
56、在另一优选例中,步骤(iv)中,所述的第六溶剂选自:乙酸乙酯、二氯甲烷乙腈、四氢呋喃、甲醇、乙醇,正丙醇,异丙醇,或其组合。
57、在另一优选例中,步骤(iv)中,所述的酸选自下组:盐酸硫酸、三氟乙酸。
58、在另一优选例中,步骤(v)中,所述的缩合剂为氯甲酸苯酯。
59、在另一优选例中,步骤(v)中,所述的碱选自下组:三乙胺、n,n-二异丙基乙基胺、或吡啶。
60、在另一优选例中,步骤(v)中,所述的第七溶剂选自下组:乙腈、二甲基亚砜、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺,或其组合。
61、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!