新型含有金刚烷骨架席夫碱衍生物的合成及抗肿瘤活性研究
1.本发明涉及一种新型含有金刚烷骨架的席夫碱衍生物的合成及抗肿瘤的活性的研究。
背景技术:
2.随着发病率和死亡率的增加,癌症是人们的主要死因,也是一个重大的公共卫生问题。肿瘤是由于身体内的局部组织细胞肿块异常,细胞增生所形成的新生物。根据2020年统计,全世界约有1930万新的癌症病例,此外,近1000万人死于癌症。其中,最常见的癌症是女性乳腺癌(226万例)、其次是肺癌(2.21万例)和前列腺癌(1.41万例);最常见的癌症死亡原因是肺癌(179万人死亡)、肝癌(83万人)和胃癌(76.9万人)。目前,癌症的主要治疗方法包括手术治疗,放疗,化疗,靶向药物治疗,中药治疗。在早期,患者常采用的方法是手术切除,但是由于副作用比较大,有复发和转移的可能,所以在手术后可以采用化疗和放疗的方法。许多癌症和死亡病例可以通过降低风险因素的流行率来预防,同时提高临床护理服务的有效性,特别是对生活在农村地区和弱势群体的患者。
3.金刚烷是一种脂环烃,具有很好的脂溶性,最主要的性质在于金刚烷的骨架是无毒性的,所以可以利用这一性质来改变它的药理活性。早在1964年人们就发现,低浓度的金刚烷胺能够抑制甲型流感病毒,高浓度时抑制乙型流感病毒及其它病毒,具有抗病毒的作用。缩氨基硫脲是由氨基硫脲与适当的酮或醛通过缩合反应,研究发现缩氨基硫脲化合物不但具有抗病毒活性,还具有抗菌、抗肿瘤、抗麻风病、抗结核和抗疟疾等多种生物活性。总之,席夫碱衍生物可诱导溶酶体损伤,增加细胞内活性氧,导致细胞凋亡,这有助于其抗肿瘤氧化机制。
技术实现要素:
4.1.本发明公开了一种含有金刚烷骨架席夫碱衍生物及其制备方法,使用cck8法对细胞进行毒性试验,评价化合物对a549、hela、mcf-7抗增殖效果。
5.2.本发明采用如下技术方案,含有金刚烷骨架席夫碱衍生物,结构为:。
6.2.本发明中r为,r1,r2,r3是各自单独的h,f,och3或ch3。
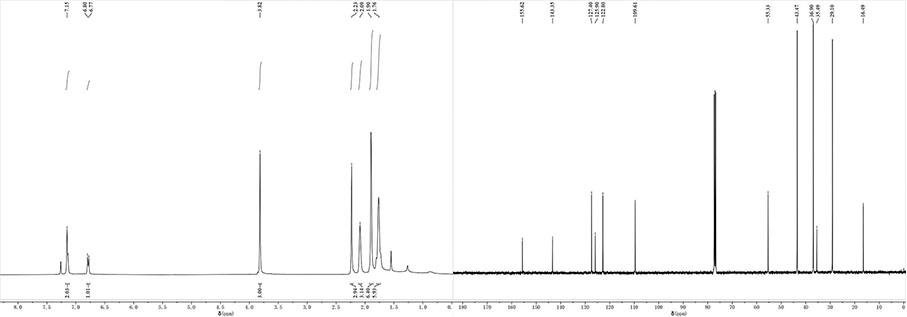
7.3.在本发明中,以1-溴金刚烷为起始原料,在钯碳的催化下进行了付克烷基化反应,生成了1-(4-甲氧基-3-甲基苯基)金刚烷,随后,经过自由基取代、氧化反应和去甲基化反应得到5-(金刚烷-1-基)-2-羟基苯甲醛,结构式为:
4.58 (s, 2h), 3.88 (s, 3h), 2.09 (s, 3h), 1.89 (s, 6h), 1.76 (d, j = 8.4 hz, 6h).
13
c nmr (101 mhz, chloroform-d) δ 154.61, 143.83, 126.54, 125.41, 110.68, 36.78,29.78,28.99。
18.(3)5-(金刚烷-1-基)-2-甲氧基苯甲醛的合成(化合物4)取100ml单口瓶,在常温下依次加入1-(3-(溴甲基)-4-甲氧基苯基)金刚烷0.899g,n-甲基吗啉-n-氧化物1.9g,最后加入无水四氢呋喃为溶剂。将整个反应体系转移到66摄氏度油浴锅中,通入氮气隔绝空气,连接直行冷凝管,当开始滴定时,计时,反应4h。反应结束后,冷却至室温,加入10ml蒸馏水,用无水乙醚萃取多次,用无水硫酸镁干燥40min,干燥结束后抽滤,将滤液浓缩,使用洗脱剂(v石油醚:v二氯甲烷=1:1)经柱层析洗脱,洗脱后,去除其溶剂,其残留物真空干燥一夜,得到白色固体。收率:46%.1h nmr (400 mhz, chloroform-d) δ 10.47 (s,1h), 7.82 (s,1h), 7.55 (s, 1h), 6.94 (d, j = 8.7 hz, 1h), 3.91 (s, 3h), 2.10 (s, 3h), 1.89 (s, 6h), 1.76 (d, j = 10.2 hz, 6h).
13
c nmr (101 mhz, chloroform-d) δ 190.07,159.94,143.87,132.63,124.83,124.37,111.43,55.69,43.16,36.67,35.70,28.89。
19.(4)5-(金刚烷-1-基)-2-羟基苯甲醛的合成(化合物5)取100ml单口瓶,在常温下依次加入(金刚烷-1-基)-2-甲氧基苯甲醛0.1g,加入定量二氯甲烷将其溶解,最后加入1ml三溴化硼。将整个反应体系转移到-10摄氏度低温反应器中,计时,反应6h。反应结束后,加入10ml蒸馏水,用无水乙醚萃取多次,用无水硫酸镁干燥40min,干燥结束后抽滤,将滤液浓缩,使用洗脱剂(v石油醚:v二氯甲烷=1:1)经柱层析洗脱,洗脱后,去除其溶剂,其残留物真空干燥一夜得到淡黄色固体。收率:47%..1h nmr (400 mhz, chloroform-d) δ 10.84 (s, 1h), 9.89 (s, 1h), 7.57 (d, j = 8.7 hz, 1h), 7.47 (s, 1h), 6.94 (d, j = 8.9 hz, 1h), 2.12 (s, 3h), 1.89 (s, 6h), 1.78 (d, j = 12.7 hz, 6h).
13
c nmr (101 mhz, chloroform-d) δ 196.82, 159.56, 143.12, 129.65, 120.23, 117.20, 43.19,36.64,35.58。
20.实施例2:目标化合物6(a-h)的合成(1)2-(5-(金刚烷-1-基)-2-羟基亚苄基)-n-(对甲苯基)肼-1-硫代氨基的合成(化合物6)取100ml单口瓶,依次加入5-(-金刚烷-1-基)-2-羟基苯甲醛50mg,n-(对甲苯基)肼基硫代酰胺42mg,加入10ml无水乙醇为溶剂,最后加入5滴冰醋酸。将整个反应体系转移到80摄氏度油浴锅中,计时,反应6h。反应结束后,冷却至室温,会析出白色固体。用无水乙醇过滤,多次冲洗,再用二氯甲烷多次冲洗,将滤饼干燥过夜。得到白色固体。收率:77%。1h nmr (400 mhz, dmso-d6) δ 11.87 (s, 1h), 9.83 (s, 1h), 9.75 (s, 1h), 8.52 (s, 1h), 7.74 (d, j = 20.2 hz, 2h), 7.29 (d, j = 8.3 hz, 4h), 6.84 (d, j = 8.6 hz, 1h), 2.03 (s, 3h), 1.84 (s, 6h), 1.71 (s, 6h).
13
c nmr (101 mhz, dmso-d6) δ 177.00, 158.55, 156.10, 155.19, 142.48, 129.64,128.79,128.04,124.47,122.98,119.57,116.43,116.16,43.15,36.66,35.64,28.83。
21.(2)2-(5-(金刚烷-1-基)-2-羟基亚苄基)-n-(3-甲氧基苯基)肼-1-硫代氨基的合成(化合物7)取100ml单口瓶,依次加入5-(-金刚烷-1-基)-2-羟基苯甲醛50mg,n-(3-甲氧基苯
(s, 1h), 6.84 (d, j = 8.6 hz, 1h), 2.04 (s, 3h), 1.85 (s, 6h), 1.71 (s, 6h).
13
c nmr (101 mhz, dmso-d6) δ 176.31, 155.11, 142.47, 139.80, 128.59, 126.18, 125.67, 123.52, 119.63, 116.40, 43.15, 36.67, 35.66, 28.84。
25.(6)2-(5-(金刚烷-1-基)-2-羟基亚苄基)-n-(3-氟苯基)肼-1-硫代氨基的合成(化合物11)取100ml单口瓶,依次加入5-(-金刚烷-1-基)-2-羟基苯甲醛103mg,n-(3-氟苯基)肼基硫代酰胺89mg,加入10ml无水乙醇为溶剂,最后加入5滴冰醋酸。将整个反应体系转移到80摄氏度油浴锅中,计时,反应6h。反应结束后,冷却至室温,会析出白色固体。用无水乙醇过滤,多次冲洗,再用二氯甲烷多次冲洗,将滤饼干燥过夜。得到白色固体。收率50%。.1h nmr (400 mhz, dmso-d6) δ 11.82 (s, 1h), 10.07 (s, 1h), 9.76 (s, 1h), 8.52 (s, 1h), 7.75 (s, 1h), 7.62 (s, 1h), 7.42 (s, 2h), 7.26 (s, 1h), 7.01 (s, 1h), 6.83 (s, 1h), 2.04 (s, 3h), 1.85 (s, 6h), 1.71 (s, 6h).
13
c nmr (101 mhz, dmso-d6) δ 176.04, 163.26, 160.85, 155.20, 142.90, 142.48, 141.51, 129.98, 128.80, 123.57, 121.53, 119.52, 116.43, 112.58,112.33,112.13,111.92,43.15,36.68,35.67,28.85。
26.(7)2-(5-(金刚烷-1-基)-2-羟基亚苄基)-n-(2-氟苯基)肼-1-硫代氨基的合成(化合物12)取100ml单口瓶,依次加入5-(-金刚烷-1-基)-2-羟基苯甲醛100mg,n-(4-氟苯基)肼基硫代酰胺86mg,加入10ml无水乙醇为溶剂,最后加入5滴冰醋酸。将整个反应体系转移到80摄氏度油浴锅中,计时,反应6h。反应结束后,冷却至室温,会析出白色固体。用无水乙醇过滤,多次冲洗,再用二氯甲烷多次冲洗,将滤饼干燥过夜。得到白色固体。收率75%。1h nmr (400 mhz, dmso-d6) δ 11.72 (s, 1h), 9.96 (s, 1h), 9.75 (s, 1h), 8.49 (s, 1h), 7.75 (s, 1h), 7.28 (d, j = 8.1 hz, 3h), 7.17 (d, j = 7.9 hz, 1h), 6.83 (d, j = 8.6 hz, 1h), 6.77 (d, j = 8.3 hz, 1h), 3.76 (s, 3h), 2.04 (s, 3h), 1.86 (s, 6h), 1.72 (s, 6h).
13
c nmr (101 mhz, dmso-d6) δ 176.01, 159.58, 155.12, 142.46, 140.88, 129.31, 128.65, 123.57, 119.61, 117.82, 116.42, 111.41,111.12,55.60,43.16,36.68,35.66,28.86。
27.(8)2-(5-(金刚烷-1-基)-2-羟基亚苄基)-n-(4-氟苯基)肼-1-硫代氨基的合成(化合物13)取100ml单口瓶,依次加入5-(-金刚烷-1-基)-2-羟基苯甲醛85mg,n-(4-氟苯基)肼基硫代酰胺80mg,加入10ml无水乙醇为溶剂,最后加入5滴冰醋酸。将整个反应体系转移到80摄氏度油浴锅中,计时,反应6h。反应结束后,冷却至室温,会析出白色固体。用无水乙醇过滤,多次冲洗,再用二氯甲烷多次冲洗,将滤饼干燥过夜。得到白色固体。收率79%1h nmr (400 mhz, dmso-d6) δ 11.71 (s, 1h), 9.98 (s, 1h), 9.73 (s, 1h), 8.51 (s, 1h), 7.75 (s, 1h), 7.54 (s, 2h), 7.23 (d, j = 25.5 hz, 3h), 6.85 (s, 1h), 2.03 (s, 3h), 1.85 (s, 6h), 1.71 (s, 6h).
13
c nmr (101 mhz, dmso-d6) δ 176.68, 161.34, 158.93, 155.12, 142.48, 136.15, 128.69, 123.51, 119.60,116.40,115.30,115.08,43.15,36.67,35.66,28.84。
28.实施例3:体外细胞毒性评价结果
1.本发明对目标化合物6a-h进行了cck-8实验测试,对hela,a549,mcf-7,和hek-293进行表达,目标化合物6a-h和5-氟尿嘧啶在20μm浓度下测试。由图可以看出,化合物6g对hela抑制效果最好,抑制率为91.18%,而5-氟尿嘧啶对hela细胞的抑制率为25.56%;化合物6g对mcf-7抑制效果最好,抑制率为76.48%,5-氟尿嘧啶对mcf-7细胞的抑制率为48.69%;化合物6f对a549抑制效果最好,但是其它化合物对a549抑制效果均不好,抑制率为61.36%,而5-氟尿嘧啶对hela细胞的抑制率为0%。
29.2.本发明计算出对化合物6a-h在320μm、160μm、80μm、40μm、20μm、10μm、5μm、2.5μm浓度下对a549、hela、mcf
‑ꢀ
7细胞的ic50值,其中,化合物6a、6f、6g对hela细胞、mcf-7的ic50值较低。
30.表1目标化合物6a-h对不同细胞的ic50值 ic(μm)ic(μm) helamcf-76a28.2520.606b》30》306c》30》306d》30》306e》30》306f19.8228.426g12.7117.076h》30》30
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1