猴痘病毒检测靶标的应用及猴痘病毒检测组合物、试剂盒的制作方法
1.本发明提供一种猴痘病毒检测靶标的应用及猴痘病毒检测组合物、试剂盒,属于临床体外检测技术领域。
背景技术:
2.猴痘病毒(monkeypox virus,mpxv)是一种dna病毒,属于痘病毒科(poxviridae),正痘病毒属(orthopoxvirus)。感染猴痘病毒可引发人兽共患传染性疾病。猴痘病毒不但可以同物种间传播,也可以跨物种传播,如可由动物传给人,也能够人际传播。普遍易感人群和患者中以儿童居多。人际之间的传播方式有1接触感染者的呼吸道分泌物、2皮肤损伤部位或3被污染的物品(如患者皮疹破裂后流出液体沾染的衣物、床单)等方式传播,此外还包括长时间面对面的呼吸道飞沫传播、母婴传播以及性传播等。
3.猴痘病毒的潜伏期为5~21d,病程一般持续2~5周,轻症患者4~6周就可自行痊愈,但发病严重时可发生虚脱、甚至衰竭而死亡。人感染猴痘病毒后的病死率为0%至11%,其中儿童感染者的病死率最高。猴痘病毒感染时的潜伏期长,易形成隐匿感染,给临床诊断带来困难,同时需警惕将猴痘临床症状同其它出疹疾病(如水痘、麻疹、疥疮、梅毒、细菌性皮肤感染和药物皮肤过敏等)相混淆,造成诊断和治疗的复杂性。因此,建立早期、快速、准确的检测猴痘病毒感染的方法具有重要意义。
4.实时荧光定量聚合酶链式反应pcr(quantitative real-time pcr,qpcr)技术因具有高准确度、高特异性和高灵敏度的特点,已广泛应用于体外分子诊断领域,如中国专利cn11475271公开了一个基于qpcr检测技术的猴痘体外分子诊断检测方法,但该方法覆盖样本种类偏少,仅检测了全血、囊泡和脓疱三种样本,并未覆盖《猴痘防控技术指南(2022版)》要求采集的其他样本类型(如呼吸道分泌物,血清等),不利于猴痘的早期诊断。
技术实现要素:
5.本发明选择猴痘病毒序列中高度保守的f3l基因(genbank:af380138)dna片段上第104-131位作为猴痘病毒的检测靶标,公开了该检测靶标的应用,以及利用该检测靶标对猴痘病毒进行检测的组合物和试剂盒。
6.猴痘病毒f3l基因全长462bp,编码由153个氨基酸构成的结合蛋白,利用该靶标设计的引物探针,对猴痘病毒进行检测,不但灵敏度高,而且荧光信号强度较高。中国专利cn 115161414a公开了一种猴痘病毒特异性检测靶标及其寡核苷酸和试剂盒,其检测靶标也是选择猴痘病毒f3l基因组种的保守性dna片段,也公开了检测靶标的碱基序列。但该专利选取的检测靶标虽然能达到检测灵敏度的要求,但荧光强度较弱,会增加假阴性的几率。而本技术选择猴痘病毒f3l基因组上dna片段第104-131位作为检测靶标,不但灵敏度高,而且荧光强度可以提高2-3倍,大大降低了假阴性的出现。
7.作为本发明的一个目的,提供一种猴痘病毒特异性检测靶标在制备猴痘病毒检测试剂上的应用。检测靶标可以为f3l基因上保守性dna片段中第104-131位核酸序列。该猴痘
病毒检测试剂可以用来确定机体是否感染猴痘病毒,还可以用来检测病患感染猴痘病毒的严重程度。该应用包括将来自机体的生物样品与检测试剂接触,所述检测试剂与上述核酸序列、其表达产物、或其表达产物的片段结合,检测所结合检测试剂的量,由此确定该核酸序列在机体内是否表达,存在表达,即诊断为感染猴痘病毒,不表达即诊断为未感染猴痘病毒。在一些实施例方案中,检测试剂为特异性结合检测靶标的抗体或其抗原结合片段。在另一个实施方案中,检测试剂可以为实时荧光pcr试剂,针对该靶标序列设计探针,同时设计上游引物和下游引物。
8.作为本发明的另一个目的,提供一种猴痘病毒特异性检测靶标在制备猴痘病毒检测试剂盒上的应用。检测靶标可以为f3l基因上保守性dna片段中第104-131位核酸序列。该猴痘病毒检测试剂盒可以用来确定机体是否感染猴痘病毒,还可以用来检测病患感染猴痘病毒的严重程度。该应用包括将来自机体的生物样品与检测试剂盒接触,所述检测试剂盒与上述核酸序列、其表达产物、或其表达产物的片段结合,试剂盒显示相应的结果,由此确定该核酸序列在机体内是否表达,存在表达,即诊断为感染猴痘病毒,不表达即诊断为未感染猴痘病毒。在一些实施例方案中,检测试剂盒为免疫学检测平台,如免疫层吸检测平台、酶联免疫检测平台、化学发光免疫检测平台等。在另一个实施方案中,检测试剂可以为实时荧光pcr检测试剂盒,利用上游引物和下游引物对检测样本中的dna序列进行扩增,由探针特异性结合检测靶标,由荧光情况判定待测样本中是否含有猴痘病毒。
9.作为本发明的另一个目的,提供一种筛选减少猴痘病毒感染的治疗试剂的方法,该方法,由检测靶标在机体内表达情况来表征。具体过程如下:a)在不存在治疗试剂的条件下,测定机体内检测标靶的第一种表达水平,b)在存在治疗试剂的条件下,测定机体内检测靶标的第二种表达水平,将第一种表达水平和第二种表达水平相比较,其中,与第一种表达水平相比,第二种表达水平的降低表明该治疗试剂可以用于猴痘病毒感染的治疗。
10.作为本发明的另一个目的,提供一种确定患者感染猴痘病毒的组合物,至少包括用于检测猴痘病毒f3l基因保守性dna片段第104-131位的第一引物、第二引物、以及探针。具体地,第一引物的位置为f3l基因中保守性dna片段上第39-60位,第二引物的位置为f3l基因中保守性dna片段上第140-161位,探针结合的靶标位置为f3l基因中保守性dna片段上第104-131位。
11.所述第一引物为seq id no:1:5
’‑
cagccaatttagctgcattatt-3’;
12.所述第二引物为seq id no:2:5
’‑
aatcagtggggcctagtaactc-3’;
13.所述探针为seq id no:3:5
’‑
cttccgtcaatgtctacacaggca-3’;
14.所述探针的5’端标记有荧光报告基团一,所述探针的3’端标记有荧光淬灭基团一;其中所述荧光报告基团一选自fam、vic、hex、cy5、cy3、joe和rox中的任何一种;所述荧光淬灭基团一选自bhq和tamra中的任何一种。
15.进一步,所述组合物还包括内标引物对和内标探针。可有效避免临床检测过程中遇到的假阴性。作为一个实施方案,所述内标引物对包括:
16.第一内标引物seq id no:4:5
’‑
ccatcttccaggagcgaga-3’;
17.第二内标引物seq id no:5:5
’‑
atgatgacccttttggctcc-3’;
18.内标探针seq id no:6:5
’‑
tcgtggagtccactggcgtctt-3’;
19.所述内标探针的5’端标记有荧光报告基团二,所述内标探针的3’端标记有荧光淬
灭基团二,所述荧光报告基团二选自fam、vic、hex、cy5、cy3、joe和rox中的任何一种,所述荧光淬灭基团二选自bhq和tamra中的任何一种。需要说明的是,荧光报告基团一和荧光报告基团二不相同
20.作为本发明的一个目的,提供一种用于检测猴痘病毒的试剂盒,包括上述的组合物。
21.进一步地,上述试剂盒还包括pcr反应mix,阳性质控和阴性质控。
22.其中,pcr反应mix包括pcr缓冲液、dntp溶液、taqdna聚合酶、udg酶;
23.其中,pcr缓冲液包括tris-hcl、mgcl2、kcl和triton x-100,在pcr缓冲液中tris-hcl的浓度为10~50mm、mgcl2的浓度为3~6mm,kcl的浓度为10~50mm,triton x-100的浓度为1%~10%;
24.dntp溶液包括datp、dttp、dctp、dgtp和dutp,在dntp溶液中datp的浓度为0.1~0.3mm、dttp的浓度为0.1~0.3mm、dctp的浓度为0.1~0.3mm、dgtp的浓度为0.1~0.3mm,dutp的浓度为0.1~0.3mm;
25.单次检测反应液中包含1.5u~3u的taqdna聚合酶和0.5u~2u的udg酶;
26.阳性质控包括含有人工合成猴痘f3l基因序列的puc57质粒,浓度约为1
×
103~1
×
106copies/ml,以及含有人工合成gapdh基因序列的puc57质粒,浓度约为1
×
103~1
×
105copies/ml;
27.阴性质控为含有人工合成gapdh基因序列的puc57质粒,浓度约为1
×
103~1
×
105copies/ml。
28.本发明所达到的有益技术效果:本发明以猴痘病毒f3l基因中保守性dna片段上第104-131位作为检测靶标,设计引物和探针,制备猴痘病毒检测组合物和试剂盒,适合各种检测样本,不但灵敏度高、特异性好,而且荧光信号强,为临床针对猴痘病毒感染的检测提供可靠的诊断保障。
附图说明
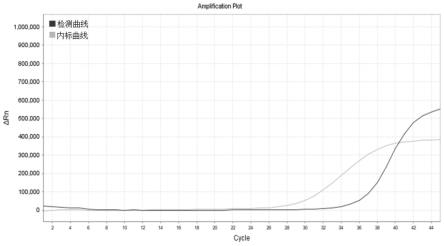
29.图1本发明示例性的实施例检测猴痘参考品的结果曲线图;
30.图2本发明示例性的实施例检测阴性样本的结果曲线图;
31.图3本发明示例性的备选组合一检测1000copies/ml猴痘参考品的结果曲线图;
32.图4本发明示例性的备选组合二检测1000copies/ml猴痘参考品的结果曲线图;
33.图5本发明检测1000copies/ml猴痘参考品的结果曲线图;
34.图6本发明示例性的引物探针组合与市售试剂盒检测25000copies/ml猴痘参考品的对比曲线图;
35.图7本发明示例性的引物探针组合与市售试剂盒检测2500copies/ml猴痘参考品的对比曲线图;
36.图8本发明示例性的引物探针组合与市售试剂盒检测1000copies/ml猴痘参考品的对比曲线图;
37.图9本发明示例性的引物探针组合与市售试剂盒检测500copies/ml猴痘参考品的对比曲线图。
具体实施方式
38.下面结合具体实施例对本发明作进一步描述。以下实施例仅用于更加清楚地说明本发明的技术方案,而不能以此来限制本发明的保护范围。
39.下面结合附图和实施例对本发明专利进一步说明。
40.实施例1猴痘病毒检测的引物及探针、组合物及试剂盒
41.申请人对早期出现的猴痘病毒毒株以及2020年在全球爆发的猴痘病毒毒株的深入研究及临床验证,发现,猴痘病毒基因组种f3l基因序列中保守性dna片段的第104-131位可以作为检测猴痘病毒的特别性检测靶标。根据这个靶标序列设计引物和探针,引物和探针的碱基序列如表1所示。
42.表1引物和探针碱基序列表
43.seq no引物探针名称序列(5
′
to 3
′
)1mpv-fcagccaatttagctgcattatt2mpv-raatcagtggggcctagtaactc3mpv-pcttccgtcaatgtctacacaggca4内标-fccatcttccaggagcgaga5内标-ratgatgacccttttggctcc6内标-ptcgtggagtccactggcgtctt
44.其中,作为示例性的一个具体实施例,mpv-p的5’端标记fam荧光基团,3’端标记bhq1淬灭基团;内标-p的5’端标记vic荧光基团,3’端标记bhq1淬灭基团。
45.一种猴痘病毒检测试剂盒:包括上述引物和探针的混合液。
46.一种猴痘病毒检测试剂盒:包括上述引物和探针混合液、pcr反应mix,阳性质控和阴性质控。
47.其中,pcr反应mix包含:pcr缓冲液、dntp、taq dna聚合酶、udg酶等混合液。
48.其中,pcr缓冲液由tris-hcl(10~50mm)、mgcl2(3~6mm)、kcl(10~50mm)和triton x-100(1%~10%)等构成的缓冲体系。
49.其中,dntp为datp(0.1~0.3mm)、dttp(0.1~0.3mm)、dctp(0.1~0.3mm)和dgtp(0.1~0.3mm)的混合物,混合溶液中还包含0.1~0.3mm的dutp。
50.其中,单次检测mix中包含1.5u~3u的taq dna聚合酶和0.5u~2u的udg酶。
51.其中,阳性质控包括含有人工合成猴痘f3l基因序列的puc57质粒,浓度约为1
×
103~1
×
106copies/ml,以及含有人工合成gapdh基因序列的puc57质粒,浓度约为1
×
103~1
×
105copies/ml;
52.阴性质控为带有人工合成gapdh基因序列的puc57质粒,浓度约为1
×
103~1
×
105copies/ml。
53.实施例2猴痘病毒检测过程
54.1.本技术可检测不同来源的样本,包括但不限于血浆样本、血清样本、痘疱液样本、咽拭子样本。为了更好的说明本技术的检测效果,现选用上述四种样本进行举例说明。
55.2.不同样本处理过程如下:
56.a)血浆样本:使用含edta抗凝剂的真空采血管采集血液样本5ml,室温静置30分钟,1500~2000rpm离心10min,吸取上清血浆于无菌离心管中;
57.b)血清样本:使用真空负压采血管采集血液样本5ml,室温静置30分钟,1500~2000rpm离心10min,吸取上清血浆于无菌离心管中;
58.c)痘疱液样本:用无菌聚酯或涤纶拭子用力涂抹病变部位,以确保收集足够的病毒dna,将拭子放入无菌收集管中;
59.d)咽拭子样本:用2根聚丙烯纤维头的塑料杆无菌拭子同时擦拭双侧咽扁桃体及咽后壁,将拭子放入无菌采样液管中,尾部弃去,旋紧管盖。
60.3.核酸提取:取不超过200ul(根据试剂盒说明调整)待测样本,使用天根病毒基因组dna/rna提取试剂盒(货号dp315)或qiagen-qiaamp dna mini kit(货号51304),按说明书提取待测样本中dna。
61.4.试剂配置:计算总测试数n,n=待测样本数(n)+质控品(2)+1。计算加到反应混合液中的各个试剂的量,计算如下表2所示:
62.表2各个试剂的计算量统计
63.试剂pcr反应mix引物探针混合液体积(μl)15
×
n5
×n64.取1.5ml离心管(灭菌)配制反应体系,pcr反应mix、引物探针混合液全部加入后,涡旋振荡10秒,离心待用,20μl/管分装至pcr反应管中(无菌和rnase-free),用毕pcr反应mix和引物探针混合液立即放入-18℃以下冻存。
65.5.加样:将待测样本、阳性质控品、阴性质控品提取的核酸分别转移5μl/管到每个pcr反应管中,盖紧管盖、离心、转移至pcr检测区。
66.6.pcr扩增:将pcr反应管放入荧光定量pcr的样品槽中。按顺序设置阳性质控品、阴性质控品和待测样本,并设置样本名称/编号;定义荧光检测通道:fam通道为猴痘病毒核酸检测通道,vic通道内标通道;推荐pcr参数设置如下表3所示:
67.表3 pcr扩增程序
[0068][0069]
7.质量控制:
[0070]
阳性质控品:fam和vic(内标)通道:ct≤35;
[0071]
阴性质控品:fam通道无ct值或ct》40,vic(内标)通道ct《35;
[0072]
以上要求必须在一个实验中同时满足。否则,该实验被视为无效,需要重新测试。
[0073]
8.结果判定:
[0074]
fam通道检测有明显扩增曲线,且检测ct值≤40,判定为mpv病毒阳性;
[0075]
fam通道检测检测40《ct值《45,vic(内标)通道检测有明显扩增曲线且检测ct值≤40,建议重复测试,如复测结果与先前结果一致,则判定mpv病毒阳性;
[0076]
fam通道检测无明显扩增曲线或检测ct值>40,vic(内标)通道检测有明显扩增曲线且检测ct值≤40,判定mpv病毒阴性或浓度低于试剂盒检出下限;
[0077]
fam通道检测无明显扩增曲线或检测ct值>40,vic(内标)通道检测无明显扩增曲线或检测ct值>40,测试无效,建议临床重新采样并重复测试。具体结果判定标准如表4所示:
[0078]
表4检测结果判断标准
[0079][0080]
试验例1猴痘病毒检测试剂盒对猴痘参考品的检测
[0081]
将实施例1所示的引物和探针,按照实施例2中的方法对中国食品药品检定研究院的猴痘病毒核酸试剂国家参考品(后文简称猴痘参考品,标准物质编号:nim-rm4060,批次编号:2201)进行验证检测,猴痘参考品浓度为2.7e+06copies/ml,同时,将未含猴痘参考品的阴性质控品作为阴性待测样本,阴性质控品的浓度约为1
×
103~1
×
105copies/ml,检测结果如图1和图2所示。从图1结果可以看出,采用本发明设计的引物、探针对猴痘参考品进行检测,其ct值为,可以判定该待测样本为阳性,这一结果与实际结果一致,表明本发明组合物能够准确的鉴别诊断猴痘病毒;从图2可以看出,未含猴痘参考品的待测样本,结果显示为阴性。
[0082]
试验例2猴痘病毒检测试剂盒的检测灵敏度
[0083]
将猴痘参考品分别使用咽拭子、血清、血浆和痘疱液阴性样本梯度稀释至2500copies/ml、1000copies/ml、500copies/ml、250copies/ml作为待测样本,每个梯度重复测试20次,使用三批组合物分别进行检测,以95%检出水平作为最低检测限,结果如下表5-8所示:
[0084]
表5、咽拭子样本三批试剂检测限检测结果
[0085]
[0086]
[0087][0088]
表6、血清样本三批试剂检测限检测结果
[0089]
[0090][0091]
表7、血浆样本三批试剂检测限检测结果
[0092]
[0093]
[0094][0095]
表8、痘疱液样本三批试剂检测限检测结果
[0096]
[0097][0098]
从表5-8所示结果可以看出,针对四种待测样本(四种样本:咽拭子、血清、血浆、痘疱液)经三批引物和探针组合各进行20次检测,阳性样本浓度为500copies/ml时阳性检出率均在95%以上,灵敏度高。其中如表9所示,对于咽拭子样本,在阳性样本浓度为500copies/ml时,三个批次的检出率均超过95%,第二批和第三批检出率为100%;对于血清样本,在阳性样本浓度为500copies/ml时,三个批次的检出率均为95%;对于血浆样本,在阳性样本浓度为500copies/ml时,三个批次的检出率均为95%;对于痘疱液样本,在阳性样本浓度为500copies/ml时,三个批次的检出率均为100%。由此可以看出,本技术的引物探针组合试剂,对于猴痘病毒的检测灵敏度较高,可以用作猴痘病毒核酸检测的试剂盒。
[0099]
表9四种待测样本的检测结果统计
[0100]
[0101][0102]
试验例3猴痘病毒检测试剂盒的特异性及抗干扰性
[0103]
1.内源性干扰物:针对与猴痘病毒具有同源性、易引起相同或相似临床症状的16种病原体样本作为干扰物样本,样本信息及检测结果如表10-11所示。
[0104]
表10近似病原体及其浓度
[0105][0106]
表11干扰物样本检测结果
[0107]
[0108][0109]
将上述16种干扰物与浓度为1
×
lod猴痘参考品混合作为待测样本,使用不同批次试剂盒进行检测,检测结果如表12所示。
[0110]
表12三批试剂竞争性干扰检测结果
[0111]
近似病原体第一批第二批第三批牛痘假病毒36.5535.8936.27天花假病毒37.4335.9737.65eb病毒36.4637.0135.14腺病毒36.8335.7136.36肠病毒36.1935.3037.69巨细胞病毒37.0536.2035.98人细小病毒35.6737.5635.73单纯疱疹病毒1型36.8635.4435.42单纯疱疹病毒2型35.7435.3737.99水痘带状疱疹病毒35.8936.2037.60人疱疹病毒36.0137.9637.10肺炎链球菌36.4235.1736.14无乳链球菌35.5536.3637.18李斯特氏菌37.3937.4735.76沙眼衣原体36.3337.3935.50淋病奈瑟菌35.0836.8437.47
[0112]
从表11的检测结果可以看出,针对16种病原体干扰物,经本发明的三批检测试剂检测后,均显示阴性,未出现假阳性的情况。从表12可以看出,16种病原体干扰物与lod浓度的猴痘参考品混合后,经本发明的三批检测试剂检测,均可成功检出lod浓度的猴痘病毒。因此,本发明可以排除不同病原体的干扰,精准的检测出猴痘病毒的携带情况。
[0113]
2.外源性干扰物:各干扰物及其浓度统计如表13所示,将各干扰物中加入1
×
lod的猴痘参考品作为待测样本,使用三批次试剂盒对上述待测样本进行检测,检测结果如表
14所示。
[0114]
表13加入的干扰物及浓度
[0115][0116]
表14外源性干扰物检测结果
[0117]
[0118]
[0119]
[0120][0121]
从表14可以看出,本发明在不同浓度的外源干扰物存在的条件下,仍然可以准确的检测出1xlod浓度的猴痘参考品,且ct值同对照无明显区别。
[0122]
综上所述,在不同干扰物存在的条件,本发明可以准确的检测出待测样本中猴痘病毒的存在情况。因此,本发明对各种干扰物的抗干扰能力强,对猴痘病毒的特异性好。
[0123]
对比例
[0124]
1.在采用核酸检测平台中,引物和探针的组合是影响检测能力的关键性因素。在不同的检测条件下,如多种病原体或不同干扰物存在下,要求所用引物和探针组合能保持较高的特异性和灵敏度,同时具有很好的扩增曲线和检测信号强度。对比申请人设计的备
选引物和探针组合(详见表15),分别为备选组合一和备选组合二,并以猴痘参考品作为待测样本进行检测,使用abi 7500平台进行检测,结果如图3-5所示。其中,待测样本中猴痘参考品浓度为1000copies/ml。
[0125]
表15备选引物和探针序列
[0126]
seq no引物探针名称序列(5'to 3')1备选引物1-fgctgcattatttttagcatctcg2备选引物1-rattgaatcagtggggcctagta3备选引物1-pctgccttatcgaatactcttccgtc4备选引物2-fagaatctgtaggccgtgtatca5备选引物2-ragctctgtatgatcttcaacgtagta6备选引物2-pcgaatactcttccgtcaatgtct
[0127]
从图3-5结果可以知,相比备选组合一ct值34.96和备选组合二ct值36.41,本技术引物和探针组合的不但ct更低,为33.87,而且荧光信号值提高达5倍。因此,本技术的引物和探针组合的扩增效率更高。
[0128]
2.将本技术引物和探针组合与市售产品进行检测对比,待测样本为不同浓度的猴痘参考品,使用abi 7500平台进行检测,检测结果如表15和图6-图9所示:
[0129]
表15待测样本浓度及检测ct值
[0130][0131]
从表14结果可知,本技术引物和探针组合的ct值与市售产品的ct值无明显差别,但从图6-9所示可以看出,本技术引物和探针组合对不同浓度的待测样本进行扩增后,其荧光信号强度均有所增强,特别地,待测样本浓度为500copies/ml时,荧光信号强度增强约3倍;待测样本浓度为250copies/ml时,荧光信号强度增强约2倍。因此,本技术的引物和探针组合可有效避免在检测低浓度样本时因荧光信号强度低带来的假阳性。
[0132]
上已以较佳实施例公布了本发明,然其并非用以限制本发明,凡采取等同替换或等效变换的方案所获得的技术方案,均落在本发明的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1