一种吡唑类衍生物、其制备方法及用途与流程
本发明涉及药物化学领域,具体涉及一种吡唑类衍生物作为赖氨酸特异性去甲基酶1(lsd1)抑制剂或其药学上可接受的盐、其制备方法及用途。
背景技术:
1、组蛋白赖氨酸特异性去甲基化酶1(lsd1)是首个被报道的组蛋白去甲基化酶,在黄素腺嘌呤二核苷酸(fad)的辅助下,可以特异性地识别h3k4和h3k9底物,并去除其单甲基或双甲基修饰。同时,lsd1可以与多种因子共同形成转录调控复合物,在转录因子的招募下到达指定基因的启动子区域,进而调控基因表达。
2、研究表明,lsd1与多种疾病相关,在多种肿瘤细胞中高表达,并与肿瘤不良预后密切相关,下调lsd1表达或抑制其活性可明显抑制肿瘤细胞生长。因此,开发一种高效、特异性的lsd1抑制剂,对于肿瘤等疾病的治疗具有非常重要的意义。
技术实现思路
1、本发明涉及一种吡唑类衍生物作为lsd1抑制剂,特别是涉及一种吡唑类衍生物及其制备方法和在医药上的应用,特别是如下式i所示的吡唑类衍生物及其在制备lsd1介导的疾病的药物中的用途,更具体而言,在制备适用于肿瘤药物中的用途。
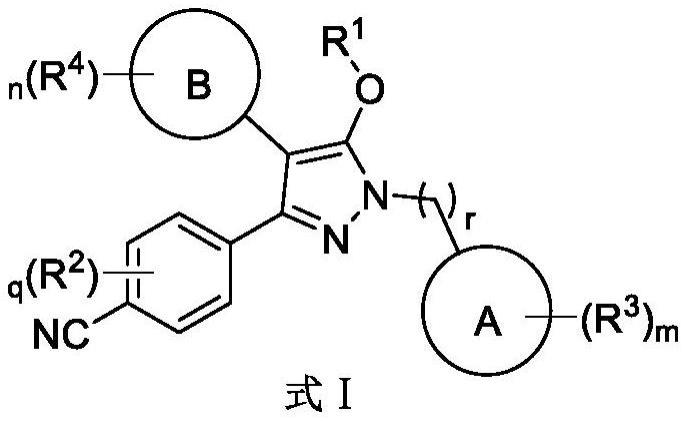
2、本发明的一个目的在于,提供了如下式i所示结构的吡唑类衍生物、其异构体或其药学上可接受的盐:
3、
4、其中,
5、环a选自饱和环烃基、饱和杂环烃基、不饱和环烃基或不饱和杂环烃基,其中所述环烃基、杂环烃基可选自单环、双环、桥环或螺环;
6、环b选自不饱和环烃基、不饱和杂环烃基,其中所述不饱和环烃基、不饱和杂环烃基可选自单环或双环;
7、r1选自:(c1-c6)烷基、(c3-c8)环烷基或杂环烷基,其中所述(c1-c6)烷基、(c3-c8)环烷基或杂环烷基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
8、r2选自:卤素、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
9、r3选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
10、r4选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
11、m选自:0、1、2、3、4或5;
12、n选自:0、1、2、3、4或5;
13、q选自:0、1、2、3或4;
14、r选自:0、1、2或3。
15、优选地,式i化合物、其异构体或其药学上可接受的盐,
16、其中,
17、环a选自5元至8元饱和单环烃基、4元至10元饱和杂环烃基,其中所述杂环烃基含有1-3个氮原子作为杂原子;
18、环b选自5元至8元不饱和单环烃基、5元至14元不饱和单环或双环杂环烃基,其中所述杂环烃基含有0-4个氮原子、0-2个氧原子作为杂原子且具有氮原子、氧原子数量不同时为0;
19、r1选自:(c1-c6)烷基、(c3-c8)环烷基或杂环烷基,其中所述(c1-c6)烷基、(c3-c8)环烷基或杂环烷基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
20、r2选自:卤素、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
21、r3选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
22、r4选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;
23、m选自:0、1、2、3、4或5;
24、n选自:0、1、2、3、4或5;
25、q选自:0、1、2、3或4;
26、r选自:0、1、2或3。
27、优选地,式i结构的化合物、其异构体或其药学上可接受的盐,
28、其中,
29、环a选自4元至10元饱和单环杂环烃基,其中所述杂环烃基含有1-3个氮原子作为杂原子,优选含有1-2个氮原子作为杂原子;
30、环b选自6元不饱和单环烃基、6元至10元不饱和双环杂环烃基,其中所述杂环烃基含有0-4个氮原子、0-2个氧原子作为杂原子且具有氮原子、氧原子不同时为0;优选地,b环选择6元至10元的芳基或杂环芳基,其中所述杂环芳基含有0-2个氮原子、0-2个氧原子作为杂原子且且氮原子、氧原子数量不同时为0;
31、r1选自:(c1-c6)烷基、(c3-c8)环烷基或杂环烷基,其中所述(c1-c6)烷基、(c3-c8)环烷基或杂环烷基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;优选地,r1选自:甲基、乙基、
32、r2选自:卤素、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;优选地,r2选自:氟、氯、溴、甲基、甲氧基、三氟甲基或三氟甲氧基;
33、r3选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;优选地,r3选自:氟、氯、氧代、羟基、氨基或
34、r4选自:卤素、氰基、氧代、羟基、取代或未被取代的氨基、(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基,其中所述(c1-c6)烷基、(c1-c6)烷氧基、(c3-c8)环烷基或(c3-c8)环烷基氧基是未取代的或被选自以下的一个或者多个取代基取代:卤素、氰基、羟基、氨基、(c1-c6)烷基或(c1-c6)烷氧基;优选地,r4选自:氟、氯、氧代、甲基、甲氧基、
35、m选自:0、1、2、3、4或5;优选地,m选自:0、1、2或3;
36、n选自:0、1、2、3、4或5;优选地,n选自:0、1、2、3或4;
37、q选自:0、1、2、3或4;优选地,q选自:1或2;
38、r选自:0、1、2或3;优选地,r选自:0或1。
39、优选地,式i结构的化合物、其异构体或其药学上可接受的盐,其进一步具有式ii所示的结构,
40、
41、其中,
42、环a选自环己烷基、哌啶基、哌嗪基、氮杂环庚基或高哌嗪基;优选地,所述哌啶基、哌嗪基、氮杂环庚基或高哌嗪基通过n原子连接到吡唑环上;
43、环b选自苯基、吡啶基、吲哚基、二氢吲哚基或吲唑基;
44、r1选自:甲基、乙基、
45、r3选自:氟、氯、氧代、羟基或氨基;
46、r4选自:氟、氯、氧代、甲基、甲氧基、
47、m选自:0、1、2或3;
48、n选自:0、1、2、3或4;
49、r选自:0或1。
50、更优选地,式i结构的化合物、其异构体或其药学上可接受的盐,所述化合物选自:
51、
52、
53、本发明的另一目的在于,提供了制备上述式i所示结构的化合物的制备方法,所述方法包括以下步骤:
54、
55、其中,r1、r2、r3、r4、环a、环b、m、n、q、r如上面对式i结构的化合物所定义;
56、(1)使化合物i-1与化合物i-2反应得到i-3
57、所述反应优选在合适的有机溶剂中进行。所述有机溶剂可选自四氢呋喃、、1,4-二氧六环、甲醇、乙醇、乙腈及其任意组合,优选乙醇。所述反应优选在适合的温度下进行,所述温度优选为50-80℃。所述反应优选进行合适的时间,例如8-12小时。
58、(2)使化合物i-3经取代反应得到i-4
59、所述反应优选在适合的有机溶剂中进行。所述有机溶剂可选自乙腈、甲苯、氯仿、四氢呋喃及其任意组合,优选乙腈。所述反应优选在适合的溴代试剂存在下进行。所述溴代试剂可选自n-溴代丁二酰亚胺、液溴、吡啶溴鎓盐,优选n-溴代丁二酰亚胺。所述反应优选在适合的温度下进行,所述温度优选为20-50℃。所述反应优选进行合适的时间,例如2-6小时。
60、(3)使化合物i-4与化合物i-5的硼酸或硼酸酯经偶联反应得到式i所示结构的衍生物
61、所述反应优选在适合的有机溶剂中进行。所述有机溶剂可选自四氢呋喃、1,4-二氧六环、甲苯、乙腈、乙醇、n,n-二甲基甲酰胺、水及其任意组合,优选n,n-二甲基甲酰胺。所述反应优选在适合的催化剂存在下进行。所述催化剂可选自pd(dppf)cl2、pd(oac)2、pd2(dba)3、pd(pph3)4,优选pd(dppf)cl2。所述碱可选自三乙胺、吡啶、4-二甲胺基吡啶、二异丙基乙胺、碳酸钾、碳酸铯、碳酸钠,优选碳酸钾。所述反应优选在适合的温度下进行,所述温度优选为80-120℃。所述反应优选进行合适的时间,例如4-12小时。
62、上述各反应步骤的具体条件为本领域公知,对此本发明不做具体限定。如本发明的教导结合本领域公知常识,本领域技术人员可以对通式中的各取代基进行选择替换以制备得到不同的化合物,这些选择和替换均在本发明的保护范围之内。
63、本发明还涉及上述式i化合物在制备预防或治疗与lsd1相关疾病的药物中的用途。
64、在一些实施例方案中,所述与lsd1相关疾病或病症选自肿瘤或癌症,例如急性髓系白血病(aml)、慢性髓系白血病(cml)、急性淋巴细胞白血病(all)、慢性淋巴细胞白血病(cll)、小细胞肺癌(sclc)、非小细胞肺癌(nsclc)、淋巴瘤、恶性肉瘤、乳腺癌、宫颈癌、结肠癌、肺癌、口腔癌、脑癌、胃癌、肝癌、结肠直肠癌、胰腺癌、皮肤癌、前列腺癌、骨癌、肾癌、卵巢癌、膀胱癌、输卵管肿瘤、腹膜肿瘤、黑色素瘤、神经胶质瘤、神经胶母细胞瘤、乳突状恶性瘤、头颈部肿瘤、或骨髓瘤。
65、本发明发现一类结构全新,具有如式i所示结构的lsd1抑制剂,其具有较好的lsd1酶抑制活性。
- 还没有人留言评论。精彩留言会获得点赞!