苯基脲类衍生物及其医药用途的制作方法
本发明属于医药,涉及一种苯基脲类衍生物及其医药用途,具体涉及该类化合物的游离碱、同分异构体、溶剂化物、及药学上可接受的盐型等结构形式;制备这类化合物的方法;包含该类化合物的组合物及其治疗用途。
背景技术:
1、人类基因组计划之后,组胺受体家族已经扩展到四种不同的g蛋白偶联受体(gpcr):h1、h2、h3和h4受体(nature review drug discovery,2005,4,107-120)。组胺h3受体较大程度上在中枢神经系统中表达并且较小程度上在周围神经系统中表达。
2、组胺h3受体(h3r)在脑中广泛表达,主要表达于大脑皮质,海马,杏仁核,纹状体等这些与记忆认知能力密切相关的区域。用选择性拮抗剂/反向激动剂阻断这些受体,可以增加神经递质如乙酰胆碱,多巴胺或5-羟色胺的释放,从而调节学习记忆、觉醒与睡眠等多种神经性行为(british journal of pharmacology,2008,154(6),1166-1181)。
3、文献表明组胺h3受体配体可用于治疗认知障碍(british journal ofpharmacology,2008,154(6),1166-1181)、痴呆(drug news perspective,2010,23(2),99-103)、注意缺陷多动障碍、肥胖症(indian journal of pharmacology,2001,(33),17-28)、精神分裂症(biochemical pharmacology,2007,73(8),1215-1224)和疼痛(journal ofpharmacology and experimental therapeutics,2011,336(1),30-37)。
4、目前组胺h3受体配体类化合物,主要分为4(5)位被取代的咪唑环类和非咪唑环类两大类。含有咪唑环的化合物具有低血脑屏障渗透、与细胞色素p-450蛋白相互作用以及肝脏和眼毒性的缺点。非咪唑环类的代表化合物专利:①us20020177589a1公开了可用于调节新型组胺h3受体配体,该发明专利中的化合物可用于治疗阿尔茨海默症、认知障碍。该化合物中代表化合物为abt-239,在临床实验中具有严重的心脏副作用,使得临床实验终止。②wo2012114348a1公开了作为组胺h3受体配体的新型化合物,该发明化合物可用于治疗多种病症,例如认知障碍、痴呆等。在进入临床的药物中,治疗认知障碍的h3r拮抗剂/反向激动剂samelisant(suvn-g3031)目前处于在研状态,目前临床二期适应症为发作性睡病。认知障碍适应症研究于2015-2017年开展临床试验一期,后续无进展。③wo2014030170a1公开了作为组胺h3抑制剂的哒嗪酮衍生物,以及他们作为h3抑制剂的用途,它们的制备方法及其药物组合物。该发明化合物可用于治疗多种病症,例如认知障碍、睡眠/觉醒障碍、饮食障碍等。但是在进行临床实验时,pk/pd数据不理想,使得临床实验终止。
5、综上所述,目前虽然已公开了一些组胺h3受体配体类化合物,但是迄今为止,在该研发领域就一个获批上市的药物—pitolisant(h3r拮抗剂/反向激动剂),上市的适应症是嗜睡症。suvn-g3031等在研药物处于临床2期研究的仍是嗜睡症,认知障碍等神经系统疾病的临床研究已经宣告失败。
6、因此,亟需寻找和发现结构新颖、安全性高、药效优于pitolisant、suvn-g3031等药物的新化学实体,用于预防或治疗与h3靶点相关的疾病,是本领域是技术人员尚未解决的技术难题。
技术实现思路
1、本发明旨在提供一种结构全新的苯基脲类衍生物,可作为组胺h3受体配体化合物,用于预防或治疗与组胺h3受体相关的疾病。
2、为实现上述发明目的,本发明提供的技术方案具体如下:
3、一种苯基脲类衍生物,为具有如下结构通式ⅰ的化合物或其药学上可接受的盐:
4、
5、式中:
6、x选自o或s;
7、m选自0、1、2、3、4、5或6;
8、a选自c1-6烷基、-nr’r”、取代或未取代的5-8元杂环基、取代或未取代的5-8元杂芳基中的一种;杂环基、杂芳基上至少有一个取代基,取代基选自如下基团中的一种或几种:c1-6烷基、c1-6烷氧基、c2-6烯基、c2-6炔基、卤素、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基、c1-6烷氧基酰胺基、c1-6烷氧基砜基、c1-6烷氧基亚砜基、3-6元环烷基、3-6元杂环基、芳基、杂芳基;
9、r’、r”各自独立的选自氢、c1-6烷基、c1-6烷氧基、卤素、氨基、羟基、羧基、羰基、酰胺基、氰基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基、c1-6烷氧基酰胺基中的一种或几种,且r’、r”不同时为氢;
10、r1、r2各自独立的选自氢、c1-6烷基、-c(o)-烷基或-s(o)2-烷基;
11、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、c2-6烯基、c2-6炔基、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基中的一种或几种;
12、或,r3、r4与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构,苯并双环结构包括但不限于苯并杂环;
13、或,r5、r6与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构;苯并双环结构包括但不限于苯并杂环;
14、杂环基、杂芳基、苯并杂环中含有至少一个杂原子,杂原子选自n、o或s。
15、优选的,为具有如下结构通式ⅱ的化合物或其药学上可接受的盐:
16、
17、式中:
18、x选自o或s;
19、m选自0、1、2、3、4、5或6;
20、a选自取代或未取代的5-8元杂环基、取代或未取代的5-8元杂芳基中的一种;杂环基、杂芳基上至少有一个取代基,取代基选自如下基团中的一种或几种:c1-6烷基、c1-6烷氧基、c2-6烯基、c2-6炔基、卤素、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基、c1-6烷氧基酰胺基、c1-6烷氧基砜基、c1-6烷氧基亚砜基、3-6元环烷基、3-6元杂环基、芳基、杂芳基;
21、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、c2-6烯基、c2-6炔基、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基中的一种或几种;
22、或,r3、r4与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构,苯并双环结构包括但不限于苯并杂环;
23、或,r5、r6与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构;苯并双环结构包括但不限于苯并杂环;
24、杂环基、杂芳基、苯并杂环中含有至少一个杂原子,杂原子选自n、o或s。
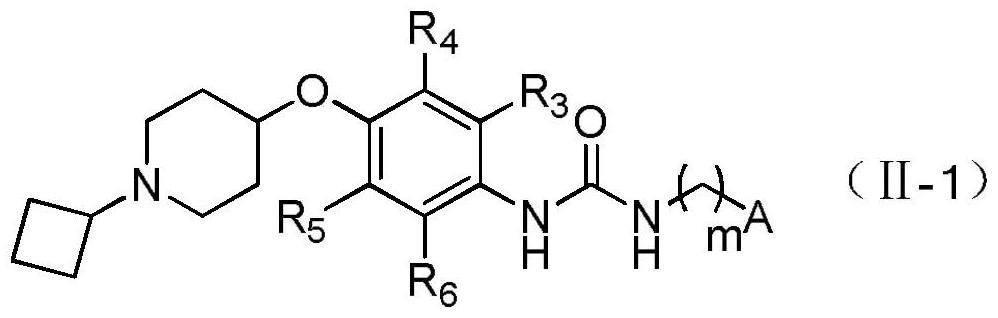
25、优选的,为具有如下结构通式ⅱ-1的化合物或其药学上可接受的盐:
26、
27、m选自1、2、3、4、5或6;
28、a选自取代或未取代的6元杂环基、取代或未取代的6元杂芳基中的一种;杂环基、杂芳基上至少有一个取代基,取代基选自如下基团中的一种或几种:c1-6烷基、c1-6烷氧基、卤素、氨基、羟基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基;
29、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、氨基、羟基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基中的一种或几种;
30、杂环基、杂芳基中含有至少一个杂原子,杂原子选自n、o或s。
31、优选的,为具有如下结构通式ⅲ的化合物或其药学上可接受的盐:
32、
33、式中:
34、m选自1、2、3、4、5或6;
35、r’、r”各自独立的选自氢、c1-6烷基、c1-6烷氧基、卤素、氨基、羟基、羧基、羰基、酰胺基、氰基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基、c1-6烷氧基酰胺基中的一种或几种,且r’、r”不同时为氢;
36、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、c2-6烯基、c2-6炔基、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基中的一种或几种;
37、或,r3、r4与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构,苯并双环结构包括但不限于苯并杂环;
38、或,r5、r6与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构;苯并双环结构包括但不限于苯并杂环;
39、苯并杂环中含有至少一个杂原子,杂原子选自n、o或s。
40、优选的,为具有如下结构通式iv的化合物或其药学上可接受的盐:
41、
42、a选自c1-6烷基;
43、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、c2-6烯基、c2-6炔基、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基中的一种或几种;
44、或,r3、r4与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构,苯并双环结构包括但不限于苯并杂环;
45、或,r5、r6与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构;苯并双环结构包括但不限于苯并杂环;
46、苯并杂环中含有至少一个杂原子,杂原子选自n、o或s。
47、本发明还提供了一种苯基脲类衍生物,包括编号为bios-a-1至bios-a-23的具有如下结构所示的化合物、同分异构体或其药学上可接受的盐:
48、bios-a-1:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-环戊基脲;
49、bios-a-2:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-环己基脲;
50、bios-a-3:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-吗啉基乙基)脲;
51、bios-a-4:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(哌啶-1-基)乙基)脲;
52、bios-a-5:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(吡咯烷-1-基)乙基)脲;
53、bios-a-6:(r)-1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(2-甲基吡咯烷-1-基)乙基)脲;
54、bios-a-7:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(4,4-二氟哌啶-1-基)乙基)脲;
55、bios-a-8:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(硫代吗啉基乙基)脲;
56、bios-a-9:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(4-羟基哌啶基-1-基)乙基)脲;
57、bios-a-10:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(4-甲基哌嗪-1-基)乙基)脲;
58、bios-a-11:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(4-异丙基哌嗪-1-基)乙基)脲;
59、bios-a-12:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(3-羟基哌啶-1-基)乙基)脲;
60、bios-a-13:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(n-甲基高哌嗪-1-基)乙基)脲;
61、bios-a-14:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(哌嗪-1-基)乙基)脲;
62、bios-a-15:1-(2-(4-环丁基哌嗪-1-基)乙基)-3-(4-((1-环丁基哌啶-4-基)氧基)苯基)脲;
63、bios-a-16:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-异丙基脲;
64、bios-a-17:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(二甲氨基)乙基)脲;
65、bios-a-18:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(二乙氨基)乙基)脲;
66、bios-a-19:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(乙氨基)乙基)脲;
67、bios-a-20:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-吗啉乙基)硫脲;
68、bios-a-21:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(哌啶-1-基)乙基)硫脲;
69、bios-a-22:1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(吡咯烷-1-基)乙基)硫脲;
70、bios-a-23:(r)-1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(2-甲基吡咯烷-1-基)乙基)硫脲。
71、前述编号为bios-a-1至bios-a-23的化合物或其药学上可接受的盐,具体结构式如下:
72、
73、进一步的,本发明还提供了一种苯基脲类衍生物,包括如下结构所示的手性化合物或其药学上可接受的盐:
74、(r)-1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(2-甲基吡咯烷-1-基)乙基)脲;
75、(r)-1-(4-((1-环丁基哌啶-4-基)氧基)苯基)-3-(2-(2-甲基吡咯烷-1-基)乙基)硫脲。
76、本发明所述的“化合物”,包括但不限于化合物的如下情形:游离碱、立体异构体、几何异构体、互变异构体、同位素、药学上可接受的盐、溶剂化物、水合物、前药(酯或磷酸酯)等形式。
77、本发明所述的“化合物”,可以是不对称的,例如,具有一个或多个立体异构体。除非另有说明,所有立体异构体都包括,如对映异构体和非对映异构体。本发明中含有不对称碳原子的化合物,可以光学活性纯的形式或外消旋形式被分离出来。光学活性纯的形式可以通过外消旋混合物拆分、使用手性原料或手性试剂合成的方法获得。
78、本发明所述的“药学上可接受的盐”是指本发明化合物的盐,由本发明发现的具有特定取代基的化合物与相对无毒的碱制备。当本发明的化合物中含有相对酸性的功能团时,可以通过在纯的溶液或合适的惰性溶剂中用足够量的碱与这类化合物的中性形式接触的方式,获得碱加成盐。药学上可接受的碱加成盐,包括但不限于钠、钾、钙、镁盐、铵或有机氨。例如:碱金属盐、碱土金属盐、其他金属盐、无机碱盐、有机碱盐、无机酸盐、低级烷磺酸盐、芳基磺酸盐、有机酸盐、氨基酸盐等。
79、除了盐的形式,本发明所提供的化合物还存在前药形式。本文所描述的化合物的前药容易地在生理条件下发生化学变化从而转化成本发明的化合物。此外,前体药物可以在体内环境中通过化学或生化方法被转换到本发明的化合物。
80、含有前述通式结构的化合物,本文中所用的术语具有如下含义:
81、术语“卤素”,指氟、氯、溴或碘,优选氟、氯或溴。
82、术语“烷基”,指由碳原子和氢原子组成的直链或支链的饱和烃基团,如c1-6烷基,包括但不限于甲基、乙基、丙基(含正丙基和异丙基)、丁基(含正丁基、异丁基、仲丁基或叔丁基)、戊基(含正戊基、异戊基、新戊基)、正己基、2-甲基己基。
83、术语“环烷基”,指由碳原子和氢原子组成单环或双环烷基,如c3-8环烷基,包括但不限于环丙基、环丁基、环戊基、环己基、环庚基和环辛基等。
84、术语“烷氧基”,指通过氧原子相连的直链或支链烷基,如c1-6烷氧基,包括但不限于甲氧基、乙氧基、正丙氧基(含正丙氧基和异丙氧基)、丁氧基(含正丁氧基、异丁氧基、仲丁氧基或叔丁氧基)、戊氧基(含正戊氧基、异戊氧基、新戊氧基)、正己氧基、2-甲基己氧基等。
85、术语“烷胺基”,指含有氮原子的开链烷基,如c1-6烷胺基,包括但不限于甲胺基、乙胺基、异丙胺基、二甲基胺基、甲基乙基胺基、二乙基胺基等。
86、术语“芳基”,是指5-12个(整数)碳原子的全碳单环或稠合多环基团,具有完全共轭的π-电子体系,包括但不限于苯环、萘环、蒽环。
87、术语“杂环基”、“杂芳基”,指具有3-12个(整数)环原子的单环或稠合环,其中有1、2、3个环原子或更多的环原子选自n、o、s中的一个或多个,其余环原子为c,且具有完全共轭或不共轭的π-电子体系。杂环基可以是饱和的、或非饱和的基团。杂环基的实例包括但不限于吡咯基、吲哚基、吡咯烷基、咪唑基、吡唑基、四唑基、吡啶基、喹啉基、异喹啉基、哌啶基、嘧啶基、吡嗪基、哌嗪基、呋喃基、吡喃基、吗啉基。
88、本发明提供的上述化合物的制备方法,通过以下步骤制备,但不仅限于以下方法:
89、
90、反应过程如下:
91、对位氟代的硝基苯类化合物(原料1)和哌啶醇、氢化钠溶于dmf中反应,然后在盐酸/乙酸乙酯溶液中反应得到中间体1,随后将其与邻环丁酮进行还原胺化反应得到中间体2,在pd/c氢气氛围中还原得到中间体3,中间体3与异氰酸酯在二氯甲烷中反应得到目标化合物;
92、或,中间体3与氯代异氰酸酯在二氯甲烷中反应得到中间体4,随后与胺反应得到中间体5或目标化合物;
93、或,中间体5与劳森试剂反应得到目标化合物。
94、前述合成方法中涉及的取代基r’、r”、r3、r4、r5、r6,定义如下:
95、r’、r”各自独立的选自氢、c1-6烷基、c1-6烷氧基、卤素、氨基、羟基、羧基、羰基、酰胺基、氰基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6卤代烷氧基、c1-6烷氧基羟基、c1-6烷氧基氨基、c1-6烷氧基酰胺基中的一种或几种,且r’、r”不同时为氢;
96、r3、r4、r5、r6各自独立的选自氢、卤素、c1-6烷基、c2-6烯基、c2-6炔基、氨基、羟基、氰基、酰胺基、砜基、亚砜基、c1-6卤代烷基、c1-6烷基羟基、c1-6烷基氨基、c1-6烷基酰胺基、c1-6烷基砜基、c1-6烷基亚砜基中的一种或几种;
97、或,r3、r4与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构,所述的苯并双环结构包括但不限于苯并杂环;
98、或,r5、r6与各自连接的苯环上碳原子共同形成取代或未取代的苯并双环结构;所述的苯并双环结构包括但不限于苯并杂环;
99、本发明还提供了一种药物组合物,包含至少一种如前所述的化合物或其药学上可接受的盐作为活性成份,以及至少一种或多种药学上可接受的载体。
100、本发明所述的“药物组合物”,指一种或多种本发明的化合物或其盐与在本领域中通常接受的用于将生物活性化合物输送至有机体(例如人)的载体的制剂。药物组合物的目的是有利于对有机体给药输送。
101、本发明所述的化合物或其药学上可接受的盐或其药物组合物的给药途径,包括但不限于口服、直肠、透黏膜、经肠给药,或者局部、经皮、吸入、肠胃外、舌下、阴道内、鼻内、眼内、腹膜内、肌内、皮下、静脉内给药。优选的给药途径是口服给药。
102、本发明还提供了一种制备如前所述的化合物或药物组合物在预防或治疗与组胺h3受体相关的疾病中的用途。
103、优选的,前述的药物用于预防或治疗认知障碍、痴呆、注意缺陷多动障碍、精神分裂症、癫痫、睡眠障碍、睡眠呼吸暂停、肥胖、进食障碍、疼痛和瘙痒。
104、优选的,前述的药物用于预防或治疗神经病理性疼痛,包括但不限于周围性神经病理性疼痛或中枢性神经病理性疼痛。
105、更优选的,周围性神经病理性疼痛为三叉神经痛、舌咽神经痛、急性或慢性炎性脱髓鞘性多发性神经根神经痛、酒精性多发神经痛、化疗引起的多发性神经痛、复杂性区域痛综合征、嵌压性神经痛(如腕管综合症)、hiv感觉神经痛、医源性神经痛(如乳腺切除术后疼痛)、肿瘤压迫或浸润神经痛、营养缺陷相关性神经痛、糖尿病性神经痛、幻肢痛、疱疹后神经痛、放疗后神经丛痛病、神经根病(颈、胸或腰骶)、毒物接触相关性神经痛或创伤后神经痛。
106、更优选的,中枢性神经病理性疼痛为卒中后疼痛、多发性硬化相关性疼痛、帕金森病相关性疼痛、创伤后脊髓损伤性疼痛、脊髓空洞症、缺血后脊髓病、压迫性脊髓病、hiv脊髓病或放射后脊髓病。
107、与现有技术相比,本发明有益效果如下:
108、本发明基于组胺h3受体配体出发,开发了一系列的结构新颖的苯基脲类衍生物,该系列化合物具有制备路线简单,原料易得的特点,并对化合物进行了一系列相关的生物学试验,试验结果均表明该类化合物具有显著的h3受体拮抗活性,可作为先导分子用于预防或治疗与h3受体相关的疾病。
- 还没有人留言评论。精彩留言会获得点赞!