一种用于检测结核分枝杆菌利福平耐药基因型的方法及检测产品与流程
本发明属于医学分子生物学诊断,涉及一种用于检测结核分枝杆菌利福平耐药基因型的方法及检测产品。
背景技术:
1、结核病是全球最大的传染病杀手之一,尤其是在发展中国家。据《2022年全球结核病报告》估算,2021年,全球新发结核病患者1060万名,比2020年增加4.5%。此外,全球有160万人死于结核病,结核病死亡人数也较2020年有所增加。中国2021年估算的结核病新发患者人数为78.0万,在30个结核病高负担国家中估算结核病发病人数排第3位,占全球结核病患者总数的7.4%,低于印度和印度尼西亚。结核病耐药是目前临床上面临的主要难题之一,2021年新患者中利福平耐药结核病(rr-tb)为45万例,耐药结核病负担增加了3%。利福平是最有效的结核病一线抗结核药物,rr-tb的治疗较困难,需联合较多的抗结核药物尤其是二线抗结核药物组成化疗方案,而且疗程较长。由此可见,结核病仍然是严重的公共卫生问题,利福平耐药的快速检测是有效治疗结核病的关键。
2、目前,临床上开展的传统的结核分枝杆菌(m.tuberculosis,mtb)利福平表型药敏试验方法是建立在细菌培养基础上的,一般先在固体或液体培养基上培养细菌,细菌生长后菌种鉴定为mtb后再进一步进行药敏实验,一般需要1-2个月时间,繁琐费时,严重延误结核病的早期诊断和有效化疗,导致耐药结核病的传播。
3、随着分子生物学技术的发展,以及mtb对部分一线和二线抗结核药物耐药分子机制的部分阐明,如目前研究已经证实mtb利福平耐药与rna多聚合酶的β亚单位编码基因rpob突变有关,其中90%~96%的突变都发生在rpob 507~533位密码子(为利福平耐药决定区域,rrdr)一个81bp的片段上,最常见的突变位点是531和526位氨基酸密码子,大多数呈现高水平耐药;而511、513~516和521、522、529、533位密码子突变一般导致中、低水平耐药;507~509、517、523、532位氨基酸置换可能与mtb利福平耐药无关。通过检测耐药相关位点的基因突变部位和突变性质,可了解患者的耐药情况,目前已建立了一系列快速检测mtb耐药基因型的方法,这些分子药敏试验方法是建立在基因扩增基础上的,可快速(2~48h)、灵敏地从mtb分离株或预处理的临床标本中检出mtb耐药基因突变,但目前临床应用的分子药敏试验方法各有优缺点,如反向杂交法和基因芯片方法均可了解耐药基因常见的突变位点和性质,但杂交、检测过程较繁琐费时,通常需1-2天时间,而且开放性检测,可能会污染扩增产物而导致假耐药的报告;实时荧光定量pcr和探针熔解曲线法均采用闭管检测,不会交叉污染或造成实验室污染,检测过程简便、快速,只需2~3h,但它们只能了解耐药基因是否存在突变,不报告具体的突变位点和突变类型,鉴于有些基因位点突变可能与耐药无关,而导致假阳性;耐药基因测序方法是分子药敏试验的金标准,但目前尚未在临床实验室开展,只是基因测序公司在做测序服务。
4、基质辅助激光解吸电离飞行时间质谱(matrix-assisted laser desorption/ionization time-of-flight mass spectrometry,简称maldi-tof ms)技术,是20世纪80年代末建立并迅速发展起来的一种质谱分析技术,是一种新型的软电离生物质谱。其基本原理是样品与芯片基质结合形成结晶后,样品以单分子状态分散在基质中。干燥后在质谱仪中经高能激光激发,样品解吸附;基质-样品之间发生电荷转移使得样品分子电离,电离的样品在电场作用下飞过真空的飞行管,根据到达检测器的飞行时间不同而被检测,即通过离子的质量电荷之比(m/z)与离子的飞行时间成正比来分析离子,并测得样品分子的分子量,进而得到分析物的基因型信息。根据这一原理,可以把不同质量的离子按质荷比大小进行分离,准确检测多肽、蛋白质、核酸、多糖等生物大分子的分子质量和纯度,具有准确性高、灵活性强、通量大、检测周期短和性价比高的优点。
5、目前应用质谱法检测mtb利福平耐药基因的方法已有报道。其中,中国专利“检测结核分枝杆菌(tb)的耐药基因突变型的方法和试剂盒”(申请号201110448201.4)公开报道对katg、inha regulatory、inha、kasa、rpob、rrs、rpsl、embb和gyra基因进行突变检测的引物设计、实验过程和检测方法等,但其检测的mtb利福平耐药基因rpob的突变位点和突变类型均比较少,只涉及4个密码子位点(531、526、516和513密码子位点)和6种突变基因型(ser531leu、his526tyr、his526asn、his526asp、asp516val和asp516gly),会影响检测的灵敏度。中国专利“结核分枝杆菌rpob基因的核酸指纹特征图谱库及其用途”(申请号201210196931.4)公开报道应用核酸指纹特征图谱库对mtb rpob基因进行检测,虾碱性磷酸酶(shrimp alkaline phosphatase,sap)消化后要对产物进行酶切反应,质谱仪检测后得到的各种mtb的核酸指纹特征图谱,通过计算机软件进行汇总和整理,得到所述的mtbrpob基因rrdr的核酸指纹特征图谱库。根据实验产生的质谱峰图,与数据库进行比对,以检测mtb rpob基因rrdr是否突变及突变型,从而判断mt对利福平的耐药性。其采用转录和核酸酶切步骤,较繁琐费时,对工作人员技术要求比较高。中国专利“结核杆菌耐药基因位点、引物组及其基于massarray核酸质谱平台的检测方法”(申请号202210106388.8)公开报道设计覆盖如rpob、inha、katg、eis、rrs、gyrb及gyra突变位点的扩增引物和应用质谱法进行耐药基因的检测,其检测的mtb利福平耐药基因rpob的突变位点和突变类型均比较多,涉及8个密码子位点(482、513、516、522、526、531、533和572位密码子位点)和30种突变基因型,但是该方法针对每个基因的每个位点设计pcr扩增引物和延伸引物,繁琐费时,增加了工作难度,容易出错,推广难度比较大。
6、综上所述,目前应用质谱方法检测mtb耐药基因型的方法还需要进一步的研究、改进,以满足临床简单、快速、灵敏、特异的检测方法,为临床医生合理制定治疗方案提供实验依据。
技术实现思路
1、本发明的目的是提供一种用于检测结核分枝杆菌利福平耐药基因型的方法及检测产品。
2、第一方面,本发明提供了成套引物,包括特异pcr扩增引物组、单碱基延伸引物组1和单碱基延伸引物组2;
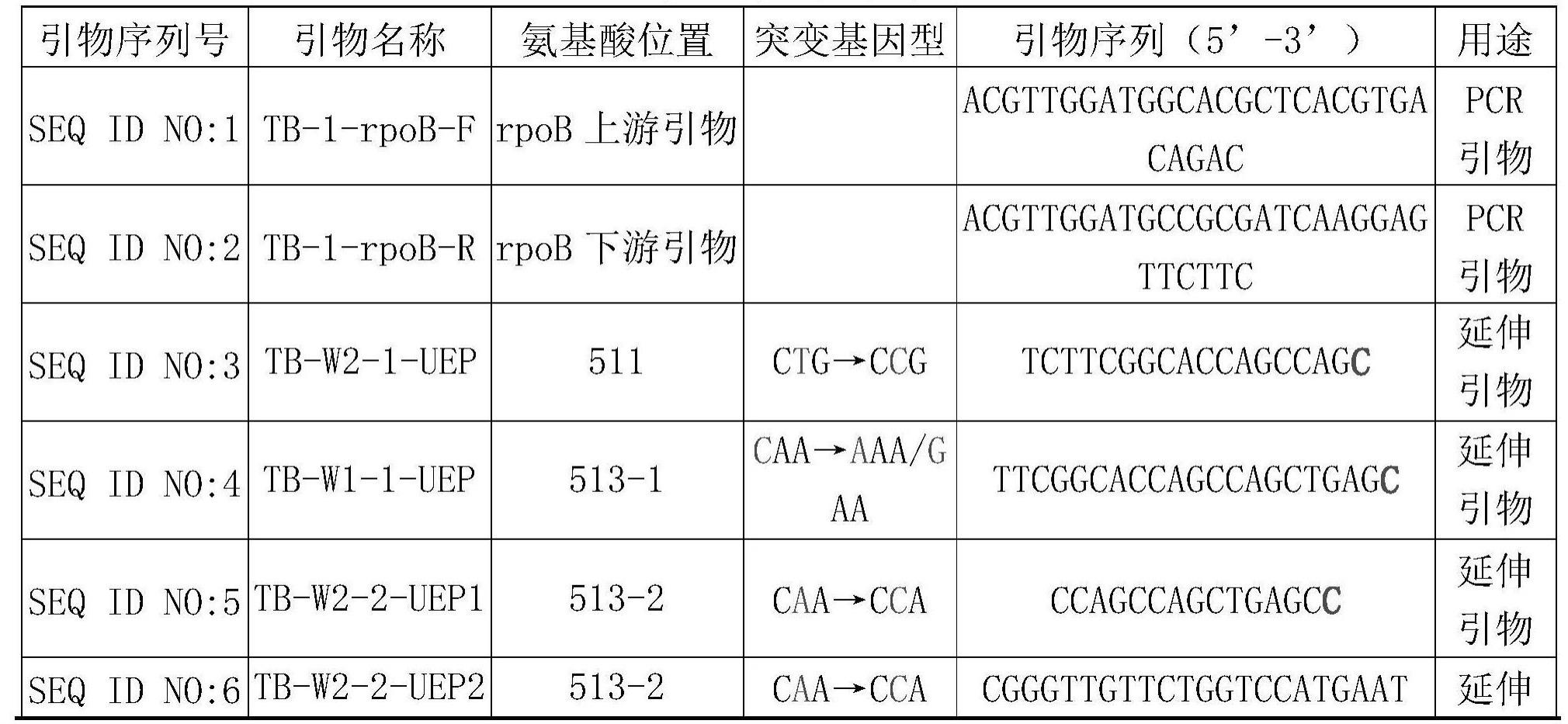
3、所述特异pcr扩增引物组由具有seq id no:1第11-29位核苷酸所示引物(seq idno:1第11-29位为pcr引物核心序列)和具有seq id no:2第11-30位核苷酸所示引物(seqid no:2第11-30位为pcr引物核心序列)组成;
4、所述单碱基延伸引物组1由seq id no:4、seq id no:7、seq id no:8、seq id no:10、seq id no:11、seq id no:12、seq id no:14和具有seq id no:16第3-18位核苷酸所示的引物组成;
5、所述单碱基延伸引物组2由seq id no:3、seq id no:5、seq id no:6、seq id no:9、seq id no:13、seq id no:15和seq id no:17所示的引物组成。
6、上文所述成套引物中,所述特异pcr扩增引物组中各引物末端添加保护碱基;
7、所述特异pcr扩增引物组中各引物为在对应引物末端添加保护碱基;具体为在5’端添加包括5-15个碱基的保护碱基序列,优选为加入10bp的tag:acgttggatg。
8、上述特异pcr扩增引物组的pcr扩增引物可扩增区域是包含突变位点在内的一段dna序列。所述扩增引物在3’端具有与目的基因序列完全匹配的15个或以上碱基;为了避免pcr引物进入质谱仪检测窗口而干扰检测效果,在5’端增加一定数目的碱基,常见如10bp的tag(acgttggatg),以使pcr引物的分子量增大,从而超出质谱仪检测窗口。
9、所述单碱基延伸引物组中各引物末端添加接头序列;进一步地,所述接头序列优选为1-15个碱基,更优选1-3个碱基。
10、上文所述的成套引物中,在一个具体实施方案中,
11、所述特异pcr扩增引物组由seq id no:1所示引物和seq id no:2所示引物组成;
12、所述单碱基延伸引物组1由seq id no:4、seq id no:7、seq id no:8、seq id no:10、seq id no:11、seq id no:12、seq id no:14和seq id no:16所示的引物组成。
13、所述单碱基延伸引物组2由seq id no:3、seq id no:5、seq id no:6、seq id no:9、seq id no:13、seq id no:15和seq id no:17所示的引物组成。
14、第二方面,本发明提供了pcr试剂,包括含有第一方面中所述特异pcr扩增引物组的pcr试剂、含有第一方面中所述单碱基延伸引物组1的pcr试剂和含有第一方面中单碱基延伸引物组2的pcr试剂。
15、第三方面,本发明提供了第一方面所述成套引物或第二方面所述pcr试剂在制备具有如下任一功能产品中的应用;
16、1)检测mtb中利福平耐药基因rpob的突变位点;
17、2)检测mtb中利福平耐药基因rpob的突变位点的基因型;
18、3)鉴定或辅助鉴定mtb对利福平的耐药性。
19、上文应用中,所述产品为试剂盒。
20、第四方面,本发明提供了一个试剂盒,包括第一方面所述成套引物或第二方面所述pcr试剂。
21、上文所述试剂盒还包括碱性磷酸酶和质谱仪检测所需试剂或仪器。
22、所述mtb中的利福平耐药基因rpob的突变位点及其对应的基因型分别如下:
23、利福平耐药基因rpob编码蛋白第511位密码子,突变前后该位点基因型为ctg→ccg;
24、利福平耐药基因rpob编码蛋白第513位密码子,突变前后该位点的基因型为caa→aaa或gaa;
25、利福平耐药基因rpob编码蛋白第513位密码子,突变前后该位点的基因型为caa→cca;
26、利福平耐药基因rpob编码蛋白第513位密码子,突变前后该位点的基因型为caa→cat;
27、利福平耐药基因rpob编码蛋白第516位密码子,突变前后该位点的基因型为gac→tac;
28、利福平耐药基因rpob编码蛋白第516位密码子,突变前后该位点的基因型为gac→gtc或ggc;
29、利福平耐药基因rpob编码蛋白第516位密码子,突变前后该位点的基因型为gac→gag;
30、利福平耐药基因rpob编码蛋白第526位密码子,突变前后该位点的基因型为cac→gac或tac或aac;
31、利福平耐药基因rpob编码蛋白第526位密码子,突变前后该位点的基因型为cac→ctc或cgc;
32、利福平耐药基因rpob编码蛋白第526位密码子,突变前后该位点的基因型为cac→caa;
33、利福平耐药基因rpob编码蛋白第531位密码子,突变前后该位点的基因型为tcg→ttg或tgg;
34、利福平耐药基因rpob编码蛋白第531位密码子,突变前后该位点的基因型为tcg→tcc
35、利福平耐药基因rpob编码蛋白第533位密码子,突变前后该位点的基因型为ctg→ccg。
36、上述突变位点为rpob基因编码蛋白中突变氨基酸密码子的位置;
37、上述基因型用突变位点的氨基酸密码子表示,且有下划线的核苷酸为突变核苷酸;箭头前为野生基因型,箭头后面为突变基因型。
38、上文所述试剂盒还包括记载如下检测结核分枝杆菌利福平耐药基因型方法的可读载体:
39、所述检测方法包括如下步骤:
40、(1)提取待测样本的基因组dna;
41、(2)以所述待测样本的基因组dna为模板,用第一方面中所述特异pcr扩增引物组进行pcr扩增,扩增分为2个体系,分别记作tb-w1和tb-w2,得到tb-w1pcr扩增产物和tb-w2pcr扩增产物;
42、(3)将所述tb-w1pcr扩增产物和tb-w2pcr扩增产物分别用碱性磷酸酶消化,得到tb-w1消化产物和tb-w2消化产物;
43、(4)将所述tb-w1消化产物和所述tb-w2消化产物分别用所述单碱基延伸引物组1和所述单碱基延伸引物组2进行多重单碱基延伸,得到tb-w1延伸产物和tb-w2延伸产物;tb-w1消化产物对应用单碱基延伸引物组1,tb-w2消化产物对应用单碱基延伸引物组2。
44、(5)使用树脂对所述tb-w1延伸产物和tb-w2延伸产物进行纯化,得到tb-w1纯化产物和tb-w2纯化产物;
45、(6)将所述tb-w1纯化产物和所述tb-w2纯化产物用质谱仪进行检测,得到mtb利福平耐药基因rpob的突变位点及其基因型。
46、上文用质谱仪进行检测具体为分别点到微阵列芯片的基质上,放入massarray核酸质谱分析系统(massarray analyzer 4system)进行检测。
47、上述可读载体可以为说明书、cd等可以记载检测方法的读取载体。
48、在一个实施方案中,上述试剂盒具体包括如下:
49、(1)pcr扩增试剂,包括:反应液ⅰ(dntps、tris-hcl、mgcl2,)、酶ⅰ(扩增酶、ung酶)和特异pcr扩增引物组;
50、(2)sap酶的消化:包括:反应液ⅱ(tris-hcl、mgcl2)和酶ⅱ(sap酶);
51、(3)单碱基延伸反应的试剂,包括:反应液ⅲ(ddntps、tris-hcl、mgcl2)、酶ⅲ(延伸酶)和单碱基延伸引物组1或2。
52、在一个具体实施方案中,该试剂盒还可包括:
53、(4)纯化用树脂;
54、(5)点样及质谱检测用芯片等试剂。
55、在另一个具体实施方案中,用于pcr产物纯化的试剂:碱性磷酸酶,或碱性磷酸酶和外切酶exoi,或电泳凝胶回收试剂,或pcr产物纯化柱。其中当包括碱性磷酸酶和外切酶exoi的纯化试剂时,所使用的pcr引物无需包括保护碱基。
56、第五方面,本发明提供了第四方面所述试剂盒在制备具有如下任一功能产品中的应用;
57、1)检测mtb中利福平耐药基因rpob的突变位点;
58、2)检测mtb中利福平耐药基因rpob的突变位点的基因型;
59、3)鉴定或辅助鉴定mtb对利福平的耐药性。
60、第六方面,本发明提供了一种检测mtb利福平耐药基因rpob的突变位点的基因型的方法,包括如下步骤:
61、(1)提取待测样本的基因组dna;
62、(2)以所述待测样本的基因组dna为模板,用第一方面中的特异pcr扩增引物组进行pcr扩增,扩增分为2个体系,分别记作tb-w1和tb-w2,得到tb-w1pcr扩增产物和tb-w2pcr扩增产物;
63、(3)将所述tb-w1pcr扩增产物和tb-w2pcr扩增产物分别用碱性磷酸酶消化,得到tb-w1消化产物和tb-w2消化产物;
64、(4)将tb-w1消化产物和tb-w2消化产物分别用所述单碱基延伸引物组1和所述单碱基延伸引物组2进行多重单碱基延伸,得到tb-w1延伸产物和tb-w2延伸产物;
65、(5)使用树脂对所述tb-w1延伸产物和tb-w2延伸产物进行纯化,得到tb-w1纯化产物和tb-w2纯化产物;
66、(6)将所述tb-w1纯化产物和所述tb-w2纯化产物用质谱仪进行检测,得到mtb利福平耐药基因rpob的突变位点及其基因型。
67、上文用质谱仪进行检测具体为将(5)得到的纯化产物分别点到微阵列芯片的基质上,放入massarray核酸质谱分析系统(massarray analyzer 4system)进行检测。
68、上文中,当待测样本是提取的dna时,省略步骤(1)直接从步骤(2)开始。
69、步骤(2)中pcr扩增所采用的程序为:50℃预变性2min;95℃预变性2min;40~50个循环95℃变性30sec,56℃退火30sec,72℃延伸30sec;72℃延伸5min。
70、步骤(3)中用碱性磷酸酶消化具体为sap消化,所采用的程序为:37℃30min;65℃5min。
71、步骤(4)中单碱基延伸反应所采用的程序为:94℃预变性30sec;40~50个循环94℃变性5sec,56℃退火5sec和80℃延伸5sec 5个循环;72℃延伸3min。
72、在一个实施方案中,步骤(5)的纯化过程可以选自碱性磷酸酶消化、碱性磷酸酶和外切酶exoi消化、切胶纯化、pcr纯化柱过柱等。在一个具体实施方案中,当使用碱性磷酸酶消化、或碱性磷酸酶和外切酶exoi消化进行纯化后,进行高温酶失活处理。
73、本发明的原理之一在于:本发明提供了一种联合pcr扩增、单碱基延伸反应和质谱检测的技术,检测mtb利福平rpob基因的耐药基因型的方法及检测产品。针对mtb利福平耐药热点位点设计1对pcr引物进行扩增含有特定靶序列的dna片段产物;在单碱基延伸过程中,对pcr的消化产物进行多重单碱基延伸,延伸引物在对应的位点处延伸一个核苷酸,使得所延伸的核苷酸与该位点处的基因型互补配对。单碱基延伸产生由延伸引物和延伸产物组成的待检混合物。通过maldi-tof ms对纯化后的待检混合物进行检测,通过质谱峰确定待检混合物中各物质分子量,并与预先计算的各延伸引物和延伸产物的理论分子量进行比较,确定延伸产物中的待检测样品的基因型,从而确定该样品对利福平是敏感还是耐药。
74、本发明原理之二在于,为了解决多重延伸产物的相互干扰,以及排除不适宜的待检位点,本发明进行了优化筛选,从而确定了优化的延伸引物组合。
75、本发明原理之三在于,在pcr体系进一步优化过程中,为了使得延伸引物和延伸产物的分子量尽量分布在理想的质谱检测窗口,本发明在扩增引物中引入不影响pcr扩增的tag序列,使得最终的延伸产物既落入检测窗口,同时各自区分,避免了分子量的叠合,从而提高了检测准确率和灵敏度。
76、本发明的实验证明,本发明的引物及方法具有如下技术效果:
77、1.敏感:本发明联合了pcr扩增、单碱基延伸反应和质谱检测等技术为一体,既可通过pcr技术放大检测模板,又可通过质谱技术检测微量样本,综合了两种技术的优点,远远优于单独使用pcr检测耐药基因型的方法,因此它的检测灵敏度很高。
78、2.特异:单碱基延伸又称为“微测序”,使用特异性单碱基延伸引物对dna分子进行识别,具有测序技术的高准确性,特异性好、假阳性低等特点;尤其是,不同于测序技术延伸数百个碱基,该技术仅延伸单个碱基,出错概率更低;
79、3.简便安全:操作简单、安全、自动化程度高、防污染;
80、4.快速:速度快、高通量,可在5-6小时内完成数百个样本的检测。
81、5、本发明可对多个待检个体进行检测,分别得到具有不同基因位点的检测结果,其中受检者可以是单个位点发生突变,也可以是多个位点发生突变。这表示受检者可以携带一个或多个基因突变。
82、6、本发明克服了以往技术一次检测基因位点过少的缺陷,成本低廉。
83、本发明的原理与定义:
84、本发明提供了一种联合pcr扩增、单碱基延伸和质谱检测等技术,判别mtb利福平耐药基因型的方法及检测产品。其原理在于:在pcr步骤中,通过设计并使用特异的引物,从而能扩增mtb利福平耐药基因突变热点位点所在dna片段。在单碱基延伸步骤中,对上一步消化后的pcr的产物进行多重单碱基延伸。其中,延伸引物共15条,分2个体系进行单碱基延伸,分别在2个反应体系中与6个耐药基因位点对应,并在对应的特定位点处延伸一个核苷酸,该核苷酸与特定位点处的基因型互补配对(如某基因位点处是a基因型,将在对应的延伸引物上延伸t核苷酸)。在单碱基延伸步骤中,采用ddntp代替dntp,因此,在延伸一个碱基后,延伸引物将终止延伸。在质谱检测过程中,单碱基延伸产物在纯化后,点到微阵列芯片的基质上,并在真空环境中被激光激发,通过飞行管至检测器。不同物质通过飞行管的时间与它们的分子量呈负相关,即分子量越大,飞行速度越慢,到达检测器的时间越晚。
85、本发明所述的“结核分枝杆菌利福平耐药基因型的检测”,包括对mtb突变位点和利福平耐药性的判断。例如,对临床样品或mtb分离株进行分析,检测其mtb rpob基因rrdr是否发生突变及突变类型,从而判断mtb是对利福平敏感或耐药,从而帮助临床医生合理制定患者的化疗方案。
86、本发明针对结核分枝杆菌rpob基因的常见耐药突变区段设计pcr引物,该引物的扩增片段包含结核分枝杆菌利福平耐药决定区(rrdr,81bp)。利福平耐药菌株的基因突变大多数集中在507~533位的27个氨基酸(81bp)组成的区域,96%利福平耐药株是由该序列(511、513、516、526、531和533等位点)突变所致。
87、目前应用于利福平耐药性检测的技术路线是在用pcr方法对rpob基因突变集中区域扩增基础上,对扩增产物进行突变检测定,已有方法有直接测序法、聚合酶链反应-单链构象多态性分析法(pcr-sscp)、双脱氧指纹图法、反向系列探针杂交法(lipa)、基因芯片法、探针熔解曲线法等。质谱技术用于利福平耐药性检测是一种新的技术手段,较现有的分子生物学检测方法,该方法兼具快速、准确、高通量和价格低廉等优势。
88、在单碱基延伸步骤中,对上一步pcr的产物依次进行消化和多重单碱基延伸。其中延伸引物共15条,分别与反应孔1中8个和反应孔2中7个特定位点对应,并在对应的特定位点处延伸一个核苷酸,该核苷酸与特定位点处的基因型互补配对(如某特定位点处是a基因型,将在对应的延伸引物上延伸t核苷酸)。在单碱基延伸步骤中,采用ddntp代替dntp,因此,在延伸一个碱基后,延伸引物将终止延伸。
89、在质谱检测过程中,单碱基延伸产物在纯化后,点到微阵列芯片的基质上,并在真空环境中被激光激发,通过飞行管至检测器。不同物质通过飞行管的时间与它们的分子量呈负相关,即分子量越大,飞行速度越慢,到达检测器的时间越晚。
90、术语“保护碱基”,指在pcr引物的5’端额外增加的碱基。由于保护碱基的序列使得pcr引物的分子量增大,可以避免反应剩余的pcr引物进入质谱检测窗口,以避免干扰检测效果。此外,延伸引物的5’端也可以适量增加碱基序列,但其作用并非如同pcr引物的保护碱基,使其超出检测窗口,而是适当调整延伸引物的分子量,使延伸引物及其产物在检测窗口内处于一个合理的位置。例如,当两个基因位点对应的延伸引物及产物的分子量接近时,通过给其中一个延伸引物增加碱基,改变引物及其产物的分子量,与其他延伸引物及产物的分子量之间拉大差距,以避免局部区域质谱峰过于集中而产生干扰和分辨不清,从而提高检测效果。因此,增加碱基后的延伸引物及产物的分子量,一定不会超出检测窗口。上述延伸引物的额外碱基可称为引物接头。
91、术语“碱性磷酸酶消化”,其作用是降解pcr反应后体系中残余dntp,其原理是使dntp的5’-p末端转换成5’-0h末端,从而失去与引物结合使引物延伸的能力,避免了对下一步单碱基延伸的影响。
92、术语“单碱基延伸”,又被称之为微测序(mini sequence),指在体系中加入延伸引物和ddntp,ddntp与延伸引物的3’端连接形成延伸产物(即引物延伸了一个碱基),根据碱基互补配对原则,由特定位点处基因型决定具体连接何种ddntp,这个过程类似于pcr过程中dntp根据互补链的碱基组成,逐个添加到pcr引物上。由于“ddntp”与普通dntp不同的是,在特定位点处连接一个ddntp,而不能像pcr那样,不断的往下延伸,因此称之为单碱基延伸。单碱基延伸与测序过程非常相似,测序体系中加入的是dntp和ddntp的混合物,测序引物连接dntp后将继续延伸,只有连接ddntp后,方终止延伸,因此测序产生的是长短不一的核苷酸片段的混合物;单碱基延伸体系中加入只有ddntp,延伸引物只能连接一个ddntp,并终止延伸,因此单碱基延伸产生的是延伸引物仅延伸一个碱基的核苷酸片段。
93、术语“检测产品”,指用于检测耐药基因位点基因型的任何常规产品,包括:检测试剂、检测芯片(如微阵列芯片、基因芯片、液体芯片等)、检测载体,以及检测试剂盒等。
94、术语“ddntp”是一种特殊的核苷酸,本技术方案共采用四种,它们之间存在分子量差异,如ddatp、ddctp、ddgtp、ddttp的分子量分别是271.2da、247.2da、287.2da、327.1da(其中ddttp是修饰后的分子量)。当延伸引物根据特定位点的基因型而延伸不同的核苷酸,将形成分子量差异。通过质谱检测,可分辨出这种差异。例如,某特定位点若是a→t突变时,对应的延伸引物长度为17个碱基(分子量5257.4da),当该位点处没有突变时是a基因型,延伸引物将延伸一个t核苷酸并终止延伸,形成18个碱基长、分子量5584.5da的延伸产物,当该位点处突变时是t基因型,延伸引物将延伸一个a核苷酸并终止延伸,形成18个碱基长、分子量5528.6da的延伸产物,两种产物之间存在55.9da的分子量差异。即对该位点而言,若使用此5257.4da的延伸引物,没有突变时a基因型将对应5584.5da的质谱峰,突变时t基因型将对应5528.6da的质谱峰。
95、术语“纯化”,指用于减少待检体系内其他物质对后续反应的影响的处理步骤。本发明的pcr产物纯化有两种方式:一是分离杂质并丢弃,二是使杂质失去活性。其中,切胶纯化、过纯化柱等都是通过电泳、纯化柱等分离杂质,并回收相对较纯的pcr产物,可以认为是第一种纯化方式,该方式一般耗时,操作复杂,特别是样本量大时;碱性磷酸酶的作用是降解(亦称“消化”)dntp,使之不能继续作为dna聚合酶或单碱基延伸酶的底物参与pcr或单碱基延伸反应,从而不干扰后续反应,可以认为是第二种纯化方式。应当指出的是,单独的外切酶exoi不起纯化作用,当它与碱性磷酸酶混合使用时,其作用是预先将单链dna(在反应完成后的pcr产物体系中,主要是剩余的pcr引物)降解成dntp,再由碱性磷酸酶使dntp继续降解。由于pcr引物被降解,不会进入最后的质谱检测步骤,因此,如果计划纯化步骤中增加exoi外切酶处理,那么无需使用具有保护碱基的pcr引物。此外,在单碱基延伸步骤之前,由于外切酶和碱性磷酸酶都通过高温失活,其不会降解在单碱基延伸步骤中加入的单链的延伸引物、ddntp等,因此避免对后续实验产生影响。
96、术语“检测窗口”,指可用于质谱检测核苷酸分子量的范围,通常涉及引物的设计参考范围。其中,在设计延伸引物时,对于不同的特定位点,根据这些位点所在dna区域的序列特点,以及特定位点的基因型,可以设计出分子量不同的延伸引物和延伸产物,避免不同延伸引物及产物之间由于分子量接近而存在干扰,从而可在一个相对宽阔的检测窗口,如4000~9000da,实现对多个特定位点的检测。
- 还没有人留言评论。精彩留言会获得点赞!