一种内皮诱导培养基、诱导多能干细胞向血管内皮细胞分化的方法与流程
本技术涉及细胞培养,具体涉及一种诱导多能干细胞向血管内皮细胞分化的方法。
背景技术:
1、干细胞是一种能够自我更新、分裂以及分化成其它细胞类群的细胞。从干细胞在发育中所处的阶段来看,干细胞可以分为胚胎干细胞和成体干细胞。胚胎干细胞是一种多能干细胞,可以无限增殖并分化成人体两百多种类型细胞、形成机体的组织和器官,即能分化成多种细胞和组织的潜能的干细胞。人工诱导的多能干细胞具有与胚胎干细胞相似的分化能力、表观遗传修饰和细胞形态等其他特征,为干细胞的研究提供了新的思路。
2、目前,利用多能干细胞的诱导培养血管内皮细胞的内皮诱导培养基中往往含有动物源成分,如使用小鼠胚胎成纤维细胞、动物血清等。虽然上述培养基可以保证干细胞及其诱导分化的细胞具有优异的自我更新能力,但是由于内皮诱导培养基中引入大量动物源性物质,给干细胞及其诱导分化的细胞自我更新及分化过程带来了不确定因素,增加了误差;此外,目前已有的内皮诱导培养基的诱导效率偏低,导致血管内皮细胞的转化率低等。
3、因此,需要提供一种不含有动物源成分的内皮诱导培养基,并且该培养基能够为培养细胞提供足够的营养物质和稳定的生存环境,从而能够高效地将多能干细胞诱导分化形成血管内皮细胞。
技术实现思路
1、为了提高多能干细胞诱导分化成血管内皮细胞的转化率,本技术提供一种内皮诱导培养基。
2、第一方面,本技术提供一种内皮诱导培养基,采用如下的技术方案:
3、一种内皮诱导培养基,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:a组分:100-400ng/ml vegf165;
4、b组分:0-300ng/ml bfgf、0-1.5mm 8-溴腺苷-3,5-环单磷酸、0-60μm melatonin;
5、c组分:0-20μm dapt和0-4μm forskolin;
6、所述b组分与c组分的含量不同时为0。
7、本技术以e6培养基作为基础培养基,并通过添加必要组分:人血管内皮生长因子vegf165,以及其他组分:bfgf、8-溴腺苷-3,5-环单磷酸、melatonin、dapt等,获得了一种内皮诱导培养基,该培养基一方面不含有动物源成分,能够有效避免由于动物源性物质对培养细胞的自我更新及分化过程带来了不确定因素以及对培养细胞造成污染的情况的发生;另一方面,上述培养基有效地将多能干细胞诱导分化为血管内皮细胞,细胞转化率能到达到85%以上,使得血管内皮细胞能够实现大规模的工业应用。
8、本技术中,vegf165为人血管内皮生长因子,vegf165能够诱导血管生成及内皮细胞生长,刺激内皮细胞进行有丝分裂与细胞迁移。bfgf为碱性成纤维细胞生长因子,是一个传递发育信号、能促进中胚层和神经外胚层细胞分裂的多肽,具有强烈的血管生成作用,bfgf在体外,能刺激细胞增殖、迁移,诱导纤溶酶原激活物及胶原酶活性,是与肝素有高亲和力的细胞促分裂原,同时具有维持多能干细胞分化潜能的作用。8-溴腺苷-3,5-环单磷酸是一种细胞渗透性环amp类似物。melatonin是一种mt receptor激动剂激素,melatonin与vegf信号通路相互作用,并显示出调节新生血管形成的活性。本技术通过实验探究发现,8-溴腺苷-3,5-环单磷酸与melatonin的添加量能够显著影响多能干细胞诱导分化为血管内皮细胞的转化率。dapt是一种γ-secretase抑制剂,并间接抑制γ-分泌酶底物notch的活性,进而影响细胞信号传导,维持高水平kdr启动子活性,提高细胞与vegfa165结合,促进向血管内皮分化能力。forskolin是从毛喉鞘蕊花中提取的一种天然产物,是腺苷酸环化酶激活剂,forskolin能够增加vegfa165的受体neuropilin1和kdr的表达,进而提高vegfa165的效果,对多能干细胞向血管内皮细胞的诱导分化有明显的促进作用,forskolin还可以增加细胞的camp水平,从而提高诱导分化的效率。
9、本技术中,多能干细胞可以为胚胎干细胞或诱导多能干细胞。
10、可选地,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:100-400ng/ml vegf165、100-300ng/ml bfgf、0.5-1.5mm 8-溴腺苷-3,5-环单磷酸和40-60μmmelatonin。
11、在一个具体的实施方案中,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:300ng/ml vegf165、200ng/ml bfgf、1mm 8-溴腺苷-3,5-环单磷酸和50μmmelatonin。
12、在一个具体的实施方案中,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:200ng/ml vegf165、300ng/ml bfgf、1.5mm 8-溴腺苷-3,5-环单磷酸和50μmmelatonin。
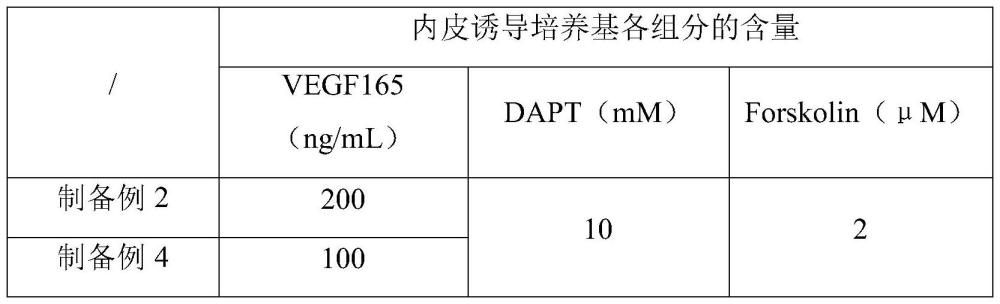
13、可选地,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:100-400ng/ml vegf165、5-20μm dapt和1-4μm forskolin。
14、在一个具体的实施方案中,所述vegf165的含量可以为100ng/ml、200ng/ml或400ng/ml。
15、在一个具体的实施方案中,所述dapt的含量可以为5μm、10μm、15μm或20μm。
16、在一个具体的实施方案中,所述forskolin的含量可以为1μm、2μm、3μm或4μm。
17、可选地,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:100-400ng/ml vegf165、100-300ng/ml bfgf、0.5-1.5mm 8-溴腺苷-3,5-环单磷酸、40-60μmmelatonin、5-20μm dapt和1-4μm forskolin。
18、在一个具体的实施方案中,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:300ng/ml vegf165、200ng/ml bfgf、1mm 8-溴腺苷-3,5-环单磷酸、50μmmelatonin、15μm dapt和3μm forskolin。
19、在一个具体的实施方案中,所述内皮诱导培养基包括e6培养基,还包括以下含量的组分:300ng/ml vegf165、300ng/ml bfgf、1mm 8-溴腺苷-3,5-环单磷酸、40μmmelatonin、10μm dapt和3μm forskolin。
20、第二方面,本技术提供一种诱导多能干细胞向血管内皮细胞分化的方法,该方法采用了前述内皮诱导培养基。
21、可选地,所述诱导多能干细胞向血管内皮细胞分化的方法,包括以下步骤:
22、(1)将多能干细胞于培养基a中诱导培养24h;
23、(2)更换培养基为e6培养基,诱导培养24h;
24、(3)更换培养基为权利要求1-4中任一项所述的内皮诱导培养基,诱导培养48h;
25、(4)更换培养基为培养基b,培养48h;
26、(5)传代培养。
27、本技术提供一种诱导多能干细胞向血管内皮细胞分化的方法,该方法首先采用培养基a刺激wnt信号通路诱导多能干细胞进入中胚层祖细胞,然后采用内皮诱导培养基将中胚层祖细胞诱导分化为血管内皮细胞,最后采用培养基b进行培养,进一步培养分化筛选血管内皮细胞。通过采用上述方法,能够有效地将多能干细胞诱导分化为血管内皮细胞,并且诱导分化的转化率能够达到85%以上。
28、可选地,所述培养基a为含有4-8μm chir99021的e6培养基;培养基b为包含8-12ng/ml vegf165、8-12ng/ml bfgf和8-12μm氢化可的松的e6培养基。
29、在一个具体的实施方案中,所述培养基a为含有6μm chir99021的e6培养基;培养基b为包含10ng/ml vegf165、10ng/ml bfgf和10μm氢化可的松的e6培养基。
30、本技术中,chir99021是一种gsk3抑制剂,chir99021能激活wnt/β-catenin信号通路,诱导多能干细胞进入中胚层祖细胞。
31、可选地,所述步骤(1)进行之前,还需要对多能干细胞进行预处理,具体为:
32、将融合度为70-80%的多能干细胞进行消化、孵育,然后向细胞培养板中加入含有y-27632的e8培养基,并用移液枪上述吹打8-10次,获得单细胞悬液,经过滤、离心、重悬、培养40-50h,获得多能干细胞。
33、可选地,所述e8培养基中y-27632的含量为4-6μm。
34、在一个具体的实施方案中,e8培养基中y-27632的含量为5μm。
35、可选地,所述重悬、培养采用的培养基为含有4-6μm y-27632的e8培养基。
36、在一个具体的实施方案中,所述重悬、培养采用的培养基为含有5μm y-27632的e8培养基。
37、综上所述,本技术具有以下有益效果:
38、1.本技术以e6培养基作为基础培养基,并通过添加必要组分:人血管内皮生长因子vegf165,以及其他组分:bfgf、8-溴腺苷-3,5-环单磷酸、melatonin、dapt等,获得了一种内皮诱导培养基,培养基一方面不含有动物源成分,另一方面能够有效地将多能干细胞诱导分化为血管内皮细胞,使诱导分化转化率达到85%以上。
39、2.本技术进一步以e6培养基作为基础培养基,并添加以下重量份的组分:100-400ng/ml vegf165、5-20μm dapt和1-4μm forskolin,获得的培养基对多能干细胞诱导分化,获得的细胞表达内皮细胞标志蛋白cd31的比例能够达到91%以上。
40、3.本技术提供一种诱导多能干细胞向血管内皮细胞分化的方法,该方法依次采用培养基a(含有chir99021的e6培养基)、内皮诱导培养基及培养基b(包含vegf 165、bfgf和氢化可的松的e6培养基)对多能干细胞进行培养,能够有效将多能干细胞诱导分化为血管内皮细胞,使得血管内皮细胞能够实现大规模的工业应用。
- 还没有人留言评论。精彩留言会获得点赞!