基于毛细管电泳片段分析检测白血病融合基因的引物组合、试剂盒及方法与流程
本发明属于分子生物学领域,具体涉及基于毛细管电泳片段分析检测白血病融合基因的引物组合、试剂盒及方法。
背景技术:
1、白血病是一种骨髓造血干细胞恶性克隆性增生的疾病,尤其在儿童和青少年中较为常见。研究表明大部分的白血病患者中存在某种染色体机结构的畸变,包括染色体的缺失、插入、倒位、重复、易位等引起染色体重排,形成新的融合基因。融合基因是肿瘤发生发展的重要驱动因素,形成的融合基因可以通过激活原癌基因表达,使抑癌基因结构变异,失去活性或者形成新的融合蛋白导致转录调节因子异常,进而造成下游信号通路的激活或者增强,最终促进细胞生长增殖,抑制细胞分化,从而导致肿瘤的发生。迄今为止,白血病涉及至少数百种融合基因。白血病融合基因可以作为诊断不同类型白血病的分子生物学特异性标志和确诊依据。如慢性粒细胞白血病cml或者部分急性淋巴细胞白血病all中:bcr-abl1;急性t淋巴细胞白血病中(t-all):sil-tal1;急性早幼粒细胞白血病apl:pml-rara等。
2、who 2016版血液肿瘤分类标准中所提到的融合基因已有一百多种,融合基因的鉴定为血液肿瘤的诊断、分型、临床治疗方案的选择、疗效监测和靶向药物的研发提供了重要的分子指标。血液肿瘤中融合基因检测技术的开发具有极大的临床意义和市场价值。
3、当前,融合基因的检测方法主要包括染色体核型分析,荧光原位杂交(fish),以及多重巢式rt-pcr,实时荧光定量pcr和数字pcr定量检测,以及高通量测序检测。但这几种方法都有各自的缺陷或者弊端。染色体核型分析分辨率低,最小分辨率局限5mb,不能发现染色体“微缺失”或“微重复因为的融合基因。fish技术具有操作复杂,人力成本高,通量低,分辨率也不高的特点。与染色体核型分析和荧光原位杂交技术相比,pcr检测方法具快速,操作简单,灵敏度高等有点。然而实时荧光定量rt-pcr和数字rt-pcr虽然检测灵敏度高,但是通量很低,一管只能检测1-2种融合形式,不适合做血液病融合基因筛查试剂,仅仅合适做微小残留监测等。高通量测序技术虽然灵敏度较高,也可检测未知融合,但是较高的成本,且需要非常专业的生物信息分析人员,较长的检测周期等都限制了其在融合基因检测中的应用。
4、因此,目前市面上,用来进行血液病多种融合基因定性筛查的方法为多重巢式rt-pcr技术,但是该技术也存在如下缺陷:
5、(1)巢式rt-pcr,需要经过至少两轮pcr的扩增,利用第一次扩增产生的产物开盖稀释后,再作为扩增模板,进行第二轮扩增得到特异性的目的片段。pcr产物稀释返回模板处理间,进行再扩增这一实验过程的增加,不仅增加了实验的繁琐性,还很大程度增加了污染概率,也不符合pcr实验室常规操作流程的顺利开展。
6、(2)巢式pcr得到的最终产物,目前都是通过琼脂糖凝胶电泳进行产物的分析,根据是否有对应的目的片段及目的片段的长度,来确定是否有相应融合基因产生。由于琼脂糖凝胶电泳对于扩增片段的分辨率在50-100bp,这大大降低了每管多重可扩增的片段数,每管扩增至多进行5-10个扩增片段。
7、(3)同样由于琼脂糖凝胶电泳分辨率限制,该技术对于同种融合基因的不同融合形式也很难有具体区分,如pml-rara融合形式有s型,v性和l型。其中s型和v型之间断裂点相隔较近,有的融合形式之间片段相差不足100bp,通过琼脂糖凝胶电泳很难确定具体是什么融合形式。
8、(4)对于基因融合导致基因表达量增加,如hox11,hox11l2,evi基因的表达增强,通过该类方法也很难实现检测。
9、随着对白血病研究的不断深入,越来越多的白血病融合基因已被发现,当前检测白血病融合病基因的方法已经远远不能满足市场对于同时对绝大部分融合基因进行一次性筛查的需求,亟待开发一种快速,方便,有效,准确且易于标准化的血液病融合基因检测方法和试剂。
技术实现思路
1、为了解决上述问题中的一种,本发明提供了一种基于毛细管电泳片段分析检测白血病融合基因的引物组合、试剂盒及方法,本发明的检测方法操作简单、特异性强、快速高效,通量高、成本低,可一次性实现对白血病121种融合基因共291种融合亚型的定性检测。
2、为了达到上述目的,本发明采用了如下技术手段:
3、本发明的第一方面提供了一种基于毛细管电泳片段分析检测白血病融合基因的引物组合,所述引物组合由四个引物大组组成:第一引物大组包括seq id no.1-seq idno.48所示的引物序列;第二引物大组包括seq id no.47-seq id no.84所示的引物序列;第三引物大组包括seq id no.85-seq id no.134所示的引物序列;第四引物大组包括seqid no.47-seq id no.48以及seq id no.135-seq id no.189所示的引物序列,所述引物组合可检测白血病的121种融合基因的291种融合亚型,所述融合基因还包括监测表达量的融合基因类型。
4、在本发明的一些实施方案中,所述引物组合中的各引物大组分别由两个引物小组组成:第一引物大组包括由seq id no.1-seq id no.24所示的引物序列组成的第一引物小组和seq id no.25-seq id no.48所示的引物序列组成的第二引物小组;第二引物大组包括由seq id no.47-seq id no.64所示的引物序列组成的第一引物小组和seq id no.65-seq id no.84所示的引物序列组成的第二引物小组;第三引物大组包括由seq id no.85-seq id no.116所示的引物序列组成的第一引物小组和seq id no.117-seq id no.134所示的引物序列组成的第二引物小组;第四引物大组包括由seq id no.135-seq id no.164所示的引物序列组成的第一引物小组和seq id no.165-seq id no.189以及seq idno.47-seq id no.48所示的引物序列组成的第二引物小组,其中seq id no.47-seq idno.48为第一引物大组、第二引物大组和第四引物大组的质控引物,seq id no.133-seq idno.134为第三引物大组的质控引物。
5、在本发明的一些实施方案中,所述第一引物大组、第二引物大组、第三引物大组、第四引物大组的不同引物小组中的引物序列,分别采用不同的荧光标记;所述荧光标记的荧光基团选自fam、hex、vic、tamra、rox、texred中的任意一种。优选地,荧光基团尽量标记在多种融合基因扩增通用最多的引物上,减少引物合成成本和减少扩增中太多荧光引物造成的荧光干扰。
6、在本发明的一些实施方案中,所述第一引物大组中seq id no.5、seq id no.15、seq id no.22、seq id no.27、seq id no.43、seq id no.46、seq id no.47所示的引物序列5’端进行荧光标记;所述第二引物大组中seq id no.49、seq id no.59、seq id no.62、seq id no.64、seq id no.65、seq id no.67、seq id no.70、seq id no.72、seq idno.74、seq id no.77、seq id no.79、seq id no.80、seq id no.83所示的引物序列5’端进行荧光标记;所述第三引物大组中seq id no.85、seq id no.115、seq id no.116、seq idno.117、seq id no.124、seq id no.125、seq id no.128、seq id no.132、seq id no.133所示的引物序列5’端进行荧光标记;所述第四引物大组中seq id no.135、seq id no.137、seq id no.147、seq id no.154、seq id no.156、seq id no.163、seq id no.165、seq idno.168、seq id no.175、seq id no.181、seq id no.182、seq id no.183、seq id no.184、seq id no.47、seq id no.186、seq id no.188所示的引物序列5’端进行荧光标记,位于同一小组的引物序列荧光标记相同。
7、其中,seq id no.5、seq id no.15、seq id no.22、seq id no.27、seq id no.49、seq id no.64、seq id no.65、seq id no.67、seq id no.70、seq id no.72、seq idno.74、seq id no.80、seq id no.83、seq id no.132、seq id no.135、seq id no.137、seqid no.147、seq id no.154、seq id no.156、seq id no.163、seq id no.165、seq idno.168所示的引物为通用引物。
8、本发明的第二方面提供了一种基于毛细管电泳片段分析检测白血病融合基因的试剂盒,包括本发明第一方面所述的引物组合。
9、在本发明的一些实施方案中,试剂盒还包括扩增酶混合液、阳性分型参考标准物质、阴性对照,毛细管电泳内标试剂。
10、在本发明的一些实施方案中,所述阳性分型参考标准物质由白血病121种融合基因291种融合亚型的阳性质粒用引物组合:seq id no.1至seq id no.189的引物分别进行pcr扩增得到阳性片段,并按照四个引物大组分别进行混合后制备而成。
11、在本发明的一些实施方案中,所述扩增酶混合液为pcr扩增缓冲液,mg+,热启动酶混合液,所述阴性对照为正常人血液rna反转录得到的cdna。
12、本发明的第三方面提供了一种基于毛细管电泳片段分析检测白血病融合基因的方法,包括如下步骤:
13、(1)获取待测样本的cdna模板;
14、(2)本发明第一方面所述的引物组合按照四个引物大组分别混合得到四个检测引物组,分四组进行多重pcr扩增,得到扩增产物;
15、(3)采用毛细管电泳对扩增产物进行检测;
16、数据分析中利用阳性分型参考标准物质对目标bin进行准确位置调整;当除质控和监测表达量的融合类型位置以外的目的bin上出现了高于100rfu的目的峰,则判定该样本对应bin上的融合基因阳性;对于监测表达量的融合类型,bin位置出现目的峰,则需要进行峰高比,目的基因位置的峰比质控位置的峰大于1/4,则表明对应的基因表达阳性。
17、在本发明的一些实施方案中,四组pcr扩增的扩增体系为:5×pcr master mix 2μl,检测引物组(primer mix)1μl,待测cdna 2μl,去离子纯净水2μl,体系总体积10μl。其中seq id no.1-seq id no.48所示的引物组成第一组检测引物组;seq id no.47-seq idno.84所示的引物组成第二组检测引物组;seq id no.85-seq id no.134所示的引物组成的第三组检测引物组;seq id no.135-seq id no.189和seq id no.47,seq id no.48所示的引物组成第四组检测引物组。
18、在本发明的一些具体实施方案中,为了最大限度的减少多重pcr扩增过程中,非特异性片段的产生,采用降落pcr(touchdown pcr)扩增程序进行pcr扩增,扩增程序为:预变性95℃10min 1个循环;变性到延伸5个循环:变性95℃10s,退火66℃30s,每个循环降低1℃,延伸70℃40s;变性到延伸25个循环:变性95℃10s,退火60℃30s,延伸70℃40s;扩增后延伸60℃30min 1个循环;扩增产物4℃或16℃保存。
19、在本发明的一些实施方案中,所述引物组合在扩增体系中,seq id no.1-seq idno.24的引物浓度均为1pmol/μl,seq id no.25-seq id no.48的引物浓度均为1.5pmol/μl;seq id no.47-seq id no.64的引物浓度均为1.5pmol/μl,seq id no.64-seq id no.84的引物浓度均为1pmol/μl;seq id no.85-seq id no.116的引物浓度为1pmol/μl,seq idno.117-seq id no.134的引物浓度为1.5pmol/μl;seq id no.135-seq id no.164的引物浓度为1pmol/μl,seq id no.165-seq id no.189的引物浓度为1.5pmol/μl。
20、在本发明的一些具体实施方案中,pcr扩增产物毛细管电泳检测方法如下:
21、配置混有分子量内标和甲酰胺的上样混合液(分子量内标和甲酰胺混合比例为1:500),然后根据检测样本pcr扩增产物数(每检测样本-含阴性对照*4管pcr产物)+4个阳性分型参考标准物质计算管数,用移液器给每个检测孔分装9μl的分子量内标和甲酰胺的混合液,取1μl的pcr扩增产物或者1μl阳性分型参考标准物质加入混合液中,盖上封板膜,瞬时离心,去除样品加样管中的气泡。把加样板95℃变性5分钟,迅速冰浴2分钟,是pcr产物彻底变性为单链核酸。按照遗传分析仪用户使用手册步骤进行毛细管电泳检测上机。参数设置为进样时间设置为15s,进样电压为3kv、运行时间为2000s。
22、在本发明的一些具体实施方案中,结果判读方案如下:
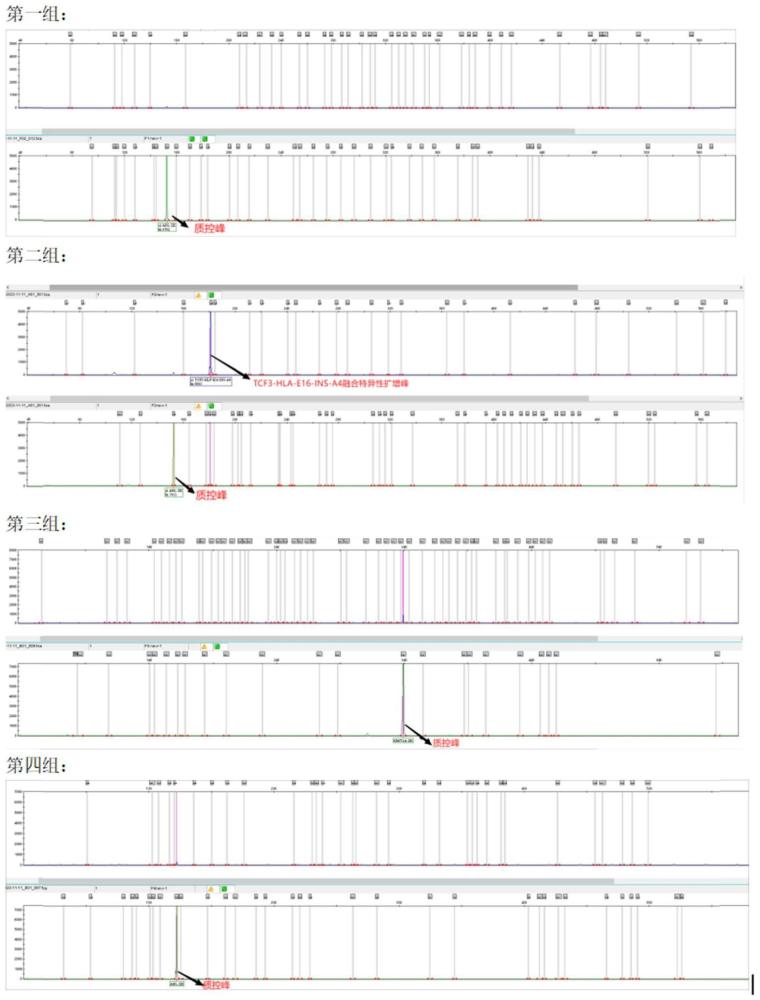
23、(1)实验有效性判读:阴性对照检测结果,其中第一组、第二组,第三组扩增结果,只有质控位置出现目的峰,且峰高值大于300rfu,其他位置bin上无明显的非特异性峰(峰高>100ruf);第四组扩增结果,质控位置出现目的峰,且峰高大于300rfu,测量基因表达的目的片段位置hox11、hox11l2、evi位置可能也有目的片段峰,但是其峰高和质控峰高的比值不高于1/4。
24、(2)样本有效性的判读:待测样本检测结果,其中第1-4四组扩增,质控bin位置必须出现目的峰,且峰高不低于300rfu。表明样本cdna模板正常。
25、(3)结果判读:在实验操作和样本有效的前提下,对样本4组扩增结果进行分析,在除质控和监测表达量的融合类型:hox11、hox11l2、evi位置以外的目的bin上出现了高于100rfu的目的峰,则判定该样本对应bin上的融合基因阳性;对于监测表达量的融合类型:hox11、hox11l2、evi的bin位置出现目的峰,则需要进行峰高比,目的基因位置的峰比质控位置的峰大于1/4,则表明对应的基因表达阳性。
26、本发明的有益效果
27、相对于现有技术,本发明具有以下有益效果:
28、(1)通过1个超多重复合pcr扩增体系能够同时扩增多重融合基因的融合类型:
29、本发明专利利用4个多重复合pcr扩增体系,实现了白血病121种融合基因291种融合亚型的检测,其优势在于:
30、①位点涵盖全面:本试剂盒检测的融合基因基本涵盖了who 2016版血液肿瘤分类标准中所包含的可以在转录cdna检测到的融合类型,包含了慢性/急性髓系细胞白血病(cml/aml)、急性b淋巴细胞和t淋巴细胞细胞白血病(b-/t-all),髓系/淋巴系伴嗜酸性粒细胞增多性白血病,急性早幼粒细胞白血病(apl)等各类型白血病中的常见的融合类型。可以一次性对白血病患者是否存在融合基因进行定性筛查,为临床医生提供更多的信息。
31、②极大降低操作强度和检测成本,一管pcr多重扩增平均可以检测70多种融合亚型,相比传统的琼脂糖电泳,一管最多只能检测5-10种融合亚型,一管可检测融合亚型数比常规多了10-15倍。
32、(2)使用遗传分析仪通过毛细管电泳检测扩增产物:
33、本发明采用的检测平台是广泛使用的检测平台,通过毛细管电泳对扩增产物进行检测,主要优势在于:
34、①检测灵敏度高
35、用qf-pcr结合毛细管电泳大幅提高了检测灵敏度,比琼脂糖电泳检测灵敏度提高了100倍以上,能够灵敏的检测到扩增产物,并且可以明确区分具体的融合亚型。另外一方面,由于检测灵敏度高,降低了对pcr扩增产物量的要求,不需要进行巢式pcr也可以达到检测限,可以进一步降低检测成本,简化操作流程,避免污染等。
36、②检测分辨率高
37、通常在70-600bp检测范围内可清晰。有效地区分1bp的差异,如此高的片段长度分辨率,使得相隔2-3bp的产物大小也可以清晰分辨而防止阳性不同融合类型误判的发生,同时高分辨率还使得同一荧光通道可检测更多为融合亚型成为可能。
38、③检测结果可定量
39、检测结果有特异峰高会有具体数值显示,且峰高和模板起始量在一定范围内有线性对应关系,可以在一定程度上与内参(质控基因)比较,实现对融合基因导致的基因过表达这种融合类型的检测。
40、④可以同时对6种荧光信号进行检测
41、遗传分析仪器可以实现对6种荧光信号进行同时接受,不同荧光信号之间不会有很大的相互干扰,其中一个通道需要用来进行分子内标的检测,还有5个通道可以对样本不同融合亚型进行检测,本专利中只示出了采用2个通道对样本进行检测,实际可以利用此方法一管检测更多的基因融合。
42、⑤检测速度快速
43、可自动化大批量检测:毛细管电泳流程40分钟完成检测,根据一次性检测样本量,可以一次性检测16孔,或者32孔,或者96孔的一次性检测。
44、⑥检测结果可以利用分析软件进行自动分析和判读。
- 还没有人留言评论。精彩留言会获得点赞!