一种利用噬菌体简单分离纯化芽孢的方法
本发明属于生物,具体涉及一种利用噬菌体简单分离纯化芽孢的方法。
背景技术:
1、某些产芽孢细菌在营养条件缺乏或不利于细菌生长的情况下会产生一种细菌休眠体,叫做芽孢。芽孢的含水量极低,膜壁结构较厚,抗逆性极强,因此吸引了大量的研究学者对芽孢的性质进行探索。其中,研究芽孢最关键的一步就是分离纯化芽孢。
2、目前已有分离纯化芽孢的方法,大都需要将芽孢培养至固体培养基后,用无菌水将菌苔进行洗脱后收集芽孢,导致芽孢有一定残留;同时,通过若干次重悬后反复离心纯化芽孢,耗时较长且步骤繁多、操作复杂。某些学者利用溶菌酶除去芽孢外层母细胞以分离纯化芽孢,而溶菌酶在一定低浓度下会使芽孢萌发,一定高浓度下使芽孢破裂,使芽孢品质受损。专利申请cn 108485977 a公开了一种简单快速的芽孢分离纯化方法,cn 111424000 a公开了一种快速分离嗜热脂肪地芽孢杆菌芽孢和营养菌体的方法,但其原理均是在分别形成细菌悬浮层和芽孢沉淀层后利用离心将芽孢分离出来,且悬浮介质的选择及离心处理的条件对芽孢分离效果影响大,操作繁琐。
技术实现思路
1、本发明的目的在于提供一种利用噬菌体简单分离纯化芽孢的方法,利用裂解性噬菌体对母细胞的裂解作用,且噬菌体无法裂解未萌发芽孢,经离心热处理除去噬菌体而达到纯化芽孢的目的;操作简单,避免了芽孢提前萌发;对裂解性噬菌体来源要求不高,成本经济,芽孢纯化率可达85%-96%,且能控制芽孢的萌发,解决了现有技术中存在的问题。
2、本发明提供了如下技术方案:
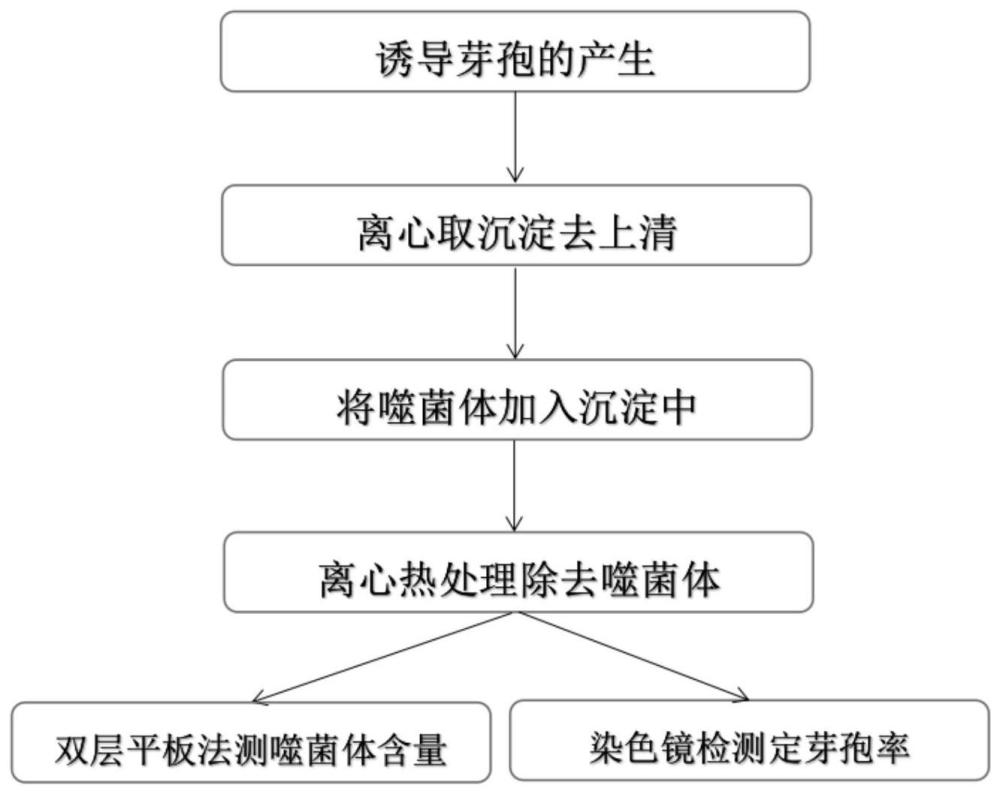
3、一种利用噬菌体简单分离纯化芽孢的方法,包括如下操作步骤:
4、s1将含芽孢杆菌芽孢的菌体混悬液收集至无菌离心容器中离心,得芽孢沉淀;
5、s2将适量裂解性噬菌体液加入步骤s1的芽孢沉淀中,培养一定时间;
6、s3待已产芽孢的母细胞裂解后,离心去除上清液,得裂解性噬菌体与芽孢的混悬液;
7、s4加热步骤s3的混悬液,继续除去残留噬菌体;
8、s5利用双层平板法验证芽孢液中的裂解性噬菌体是否除净,以验证芽孢的纯度。
9、进一步地,步骤s1芽孢杆菌为枯草芽孢杆菌(bacillus subtilis)、产气荚膜梭菌(clostridium perfringens)、蜡样芽胞杆菌(bacillus cereus)或地衣芽孢杆菌(bacillus licheniformis);步骤s1含芽孢杆菌芽孢的菌体混悬液的制备采用诱导芽孢杆菌产芽孢的液体培养基;
10、步骤s1、步骤s3离心转速为5000-12000r/min。
11、进一步地,步骤s1芽孢杆菌为枯草芽孢杆菌,含枯草芽孢杆菌芽孢的菌体混悬液的制备采用诱导枯草芽孢杆菌产芽孢的液体培养基,培养基组分如下:lb肉汤、mgso4·7h2o、na2hpo4和nah2po4。
12、进一步地,步骤s2培养时间为6-24h后,去除噬菌体。
13、进一步地,步骤s3离心时间为10-30min。
14、进一步地,步骤s3采用染色镜检观察母细胞裂解情况。可以看到大部分母细胞已经被裂解,只观察到芽孢存在时,表明裂解完成。
15、进一步地,以枯草芽孢杆菌配置100ml液体培养基为例,其中需要lb肉汤3g,mgso4·7h2o 0.3g,na2hpo4和nah2po4各为0.2g。
16、进一步地,上述枯草芽孢杆菌为枯草芽孢杆菌wb800。对其进行16s rrna测序,经ncbi比对,其为枯草芽孢杆菌ctxw 7-6-2。
17、进一步地,步骤s2中的裂解性噬菌体液是经增殖处理获得的高效价增殖噬菌体液,其制备如下:
18、s201、将宿主芽孢杆菌菌液转接至液体培养基中培养;
19、s202、将裂解性噬菌体稀释至10-5梯度,按与芽孢杆菌1:1-7的浓度比等体积转接至上述液体培养基中增殖6-24h;
20、s203、4℃、10 000×g离心15min后,取上清液过滤,得到噬菌体增殖液;重复以上步骤3-5次,获得高效价噬菌体增殖噬菌体液。
21、进一步地,宿主芽孢杆菌为枯草芽孢杆菌时,进行步骤s2裂解性噬菌体液的制备步骤如下:
22、s201、将枯草芽孢杆菌菌液转接至lb肉汤液体培养基中培养2-3d;
23、s202、将分离纯化的噬菌体稀释至10-5梯度,按与枯草芽孢杆菌1:1-7的浓度比等体积转接至上述液体培养基中增殖6-24h;
24、s203、4℃、10 000×g离心15min后,取上清液过滤,得到噬菌体增殖液;重复以上步骤3-5次,获得高效价噬菌体增殖噬菌体液。
25、进一步地,步骤s202中的裂解性噬菌体为具备在6-24h使宿主芽孢杆菌降低至少2个lg值的噬菌体。
26、进一步地,上述高效价噬菌体增殖噬菌体液的制备具体实施如下:
27、1)取0.5ml裂解性噬菌体稀释(10-5)制得的噬菌体液与0.5ml均质枯草芽孢杆菌菌液混合于装有25ml lb肉汤液体培养基的50ml离心管中,37℃静置1h,随后置于振荡培养箱中培养24h。其中,噬菌体液与均质枯草芽孢杆菌菌液的浓度比为1:1-7。
28、2)4℃、10 000×g离心15min后,取上清液过0.22μm滤器,得到噬菌体增殖液;重复以上步骤3-5次,获得高效价噬菌体增殖液。
29、进一步地,用双层平板法测定噬菌体效价。
30、噬菌体效价(pfu/ml)=平均噬菌斑数×稀释倍数×10ml。
31、进一步地,获得的高效价的噬菌体增殖液可采用以下两种方法保存:
32、(1)置于4℃用于短期保存;(2)将噬菌体液与无菌甘油混合至终浓度为40%,并在-80℃长期保存。
33、进一步地,对于效价较高的裂解性噬菌体,可进一步测定其在6-24h对宿主菌降低的lg值。并选择具备在6-24h使宿主芽孢杆菌降低至少2个lg值的噬菌体用于后续纯化分离。
34、进一步地,步骤s4加热温度90℃-100℃,加热时间0.5-1h。
35、进一步地,步骤s4加热采用二次加热:首先于90℃加热处理30min,然后置于室温一段时间,再于90℃继续二次加热处理。该方式方便芽孢对自身的不耐热而造成的破坏进行修复。
36、进一步地,步骤s5判定噬菌体是否除净采用如下方法:
37、s501、先向培养皿中倒入琼脂固体培养基;
38、s502、固体培养基凝固后,再倒入含有宿主枯草芽孢杆菌和s4处理后的混悬液的半固体培养基,二者体积比为1:1;
39、s503、培养一段时间后,计算噬菌斑的数量;若无噬菌斑,表明噬菌体除净。
40、进一步地,s502是将s4处理后的混悬液12000r/min离心2min,取上清液,然后上清液与宿主芽孢杆菌菌液各500μl混合,倒入半固体培养基。
41、进一步地,宿主菌为枯草芽孢杆菌时,s503培养时间为12h。
42、进一步地,步骤s5芽孢纯度为85%-96%,或更高。
43、本发明的有益效果:
44、1、本发明芽孢分离纯化方法区别于现有技术的思路和原理,采用裂解性噬菌体对母细胞进行裂解,而对未萌发芽孢则不具有裂解作用,从而再经过离心热处理后达到纯化芽孢的目的,操作简单,还能防止芽孢提前萌发。
45、2、本发明方法所用裂解性噬菌体可采用市售噬菌体或由污水水样或其他样品经分离筛选纯化获得的噬菌体。经芽孢纯化效果分析,筛得的符合条件的裂解性噬菌体(使宿主芽孢杆菌降低至少2个lg值)均能实现较好的芽孢纯化率,尤其采用自行分离的裂解性噬菌体,经济实用,成本低。采用以上裂解性噬菌体在进行本发明芽孢分离纯化中,能保证芽孢纯化率高,具备有益的应用推广价值。
- 还没有人留言评论。精彩留言会获得点赞!