碳氢化合物吸附剂及其制备方法
碳氢化合物吸附剂及其制备方法
1.相关申请的交叉引用
2.本技术要求于2020年11月16日向韩国知识产权局提交的韩国专利申请号10-2020-0152736的优先权和权益,并通过引用将其全文并入本文。
技术领域
3.本技术涉及具有核-壳结构的碳氢化合物吸附剂及其制备方法。
背景技术:
4.汽油车辆的尾气通过三元催化剂进行净化,并且当催化剂的温度大于或等于400℃时,可以获得接近100%的净化性能。然而,在紧接着发动机启动之后的冷启动阶段,三元催化剂不能正常工作,因此尾气没有得到净化,并被排放到大气中。特别地,已知碳氢化合物(hc)总排放(em)的约70%在冷启动阶段排放。
5.作为解决这些问题的方法,向排气系统中引入沸石基碳氢化合物吸附剂(hc捕获剂),所述碳氢化合物吸附剂暂时吸附冷启动阶段排放的碳氢化合物,直到三元催化剂预热完成,并且碳氢化合物在三元催化剂预热结束时从碳氢化合物吸附剂解吸,并通过三元催化剂进行净化。
6.在目前报道的大多数研究中,沸石基碳氢化合物吸附剂的耐高温加热性不足,并且其结构在850℃以上会发生塌陷。因此,只研究了在底盘上安装和使用沸石基碳氢化合物吸附剂的方法。然而,在底盘上,三元催化剂的预热速度较慢,因此难以应用碳氢化合物吸附剂技术,因为在三元催化剂活化之前,碳氢化合物吸附剂发生碳氢化合物逃逸。
技术实现要素:
7.本技术的目的为提供一种碳氢化合物吸附剂,所述碳氢化合物吸附剂具有改进的水热稳定性,同时具有较高的不饱和碳氢化合物吸附量,从而解决在高温潮湿环境下由于结构塌陷和活性位点损失导致的耐久性降低的问题。
8.本技术的另一个目的为提供一种制备碳氢化合物吸附剂的方法。
9.根据本技术的实施方案,碳氢化合物吸附剂包含核-壳颗粒,所述核-壳颗粒包含内核和包覆所述内核的外壳,其中,所述内核包含与除了硅(si)和铝(al)之外的金属进行离子交换的经离子交换的沸石,所述外壳包含介孔金属氧化物。
10.沸石的si/al摩尔比可以为约10至约200。
11.沸石可以与金属进行离子交换,所述金属包括cr、fe、co、ti、w、ir、pt、rd、pd、ru、th、ni、cu、v、au、re、zr、mo或其组合。
12.介孔金属氧化物的孔径可以为约2nm至约10nm。
13.介孔金属氧化物可以包括ceo2、zro2、al2o3或其组合。
14.基于核-壳颗粒的总重量,介孔金属氧化物的金属的量可以为约0.1重量%至约7重量%。
15.根据本技术的另一个实施方案,制备碳氢化合物吸附剂的方法包括制备包含沸石的内核,和形成包含介孔金属氧化物的外壳,从而制备核-壳颗粒,其中所述方法还包括使沸石与除了硅(si)和铝(al)之外的金属进行离子交换。
16.可以通过以下步骤进行核-壳颗粒的制备:混合包含内核的溶液和包含金属氧化物前体的溶液,并在约100℃至约200℃下使其反应约12小时至约24小时。
17.核-壳颗粒的制备还可以包括在约70℃至约150℃下干燥反应产物约10小时至约24小时,然后在约400℃至约700℃下煅烧约1小时至约24小时。
18.包含内核的溶液还可以包含葡萄糖、果糖、半乳糖、蔗糖、麦芽糖或其组合。
19.包含金属氧化物前体的溶液还可以包含尿素、氨、碳酸钠、碳酸氢钠、碳酸钾、碳酸氢钾、乙酸钠、乙酸钾、二乙醇胺、三甲基胺、六亚甲基二胺、四甲基氢氧化铵或其组合。
20.在沸石与金属的离子交换中,可以使用湿浸渍法,其中将内核或核-壳颗粒加入到包含金属的溶液中,从而将金属浸渍到沸石中。
21.所述方法还可以包括在约70℃至约150℃下干燥浸渍金属的内核或核-壳颗粒约10小时至约24小时,然后在约400℃至约700℃下煅烧生成物约1小时至约24小时。
22.本技术的碳氢化合物吸附剂改善了水热稳定性,同时具有较高的不饱和碳氢化合物吸附量,从而解决了在高温潮湿环境下由于结构塌陷和活性位点损失导致的耐久性降低的问题。
附图说明
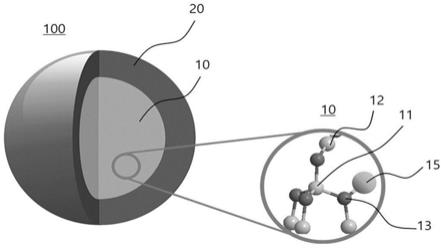
23.图1为显示根据本技术的实施方案的碳氢化合物吸附剂的示意图。
24.图2为在实施例1中制备的碳氢化合物吸附剂的电子显微镜照片。
25.图3为在实施例1中使用的h型沸石的电子显微镜照片。
26.图4为显示在实施例1和对比实施例1至3中制备的碳氢化合物吸附剂的吸附/解吸评估结果的图表。
27.图5为显示在实施例1、实施例2和对比实施例1中制备的碳氢化合物吸附剂的吸附/解吸评估结果的图表。
28.图6为显示在实施例1、3和4以及对比实施例1中制备的碳氢化合物吸附剂的吸附/解吸评估结果的图表。
具体实施方式
29.通过后文参考附图描述的实施方案,本技术的优点和特征以及实现本技术的方法将变得明显。然而,实施形式不限于下文描述的示例性实施方案。除非另有定义,否则本文使用的所有术语(包括技术术语和科学术语)均具有与本领域技术人员通常理解的含义相同的含义。此外,除非明确定义,否则不应理想地或过度地解释常用词典中定义的术语。
30.此外,除非明确地相反描述,否则术语“包括”和变化形式例如“包含”或“含有”应理解为意指包含所述元件,但是不排除任何其它元件。
31.此外,除非另有说明,否则单数包括复数。
32.根据本技术的实施方案的碳氢化合物吸附剂包含核-壳颗粒,所述核-壳颗粒包含内核和包覆所述内核的外壳。碳氢化合物吸附剂可以包含多种核-壳颗粒。
33.图1为显示碳氢化合物吸附剂的示意图。下文将参考图1描述碳氢化合物吸附剂。
34.参考图1,碳氢化合物吸附剂包含核-壳颗粒100,所述核-壳颗粒100包含内核10和包覆所述内核10的外壳20。
35.内核10可以包括合成或天然的沸石颗粒,例如可以使用y型沸石(fau)、mfi型沸石、丝光型沸石、β型沸石(bea)、a型沸石、x型沸石、l型沸石、cha沸石和zsm-5。在图1中,作为内核10的示例,显示了由铝原子11、硅原子12和氧原子13组成的沸石,但是本技术不限于此。沸石的si/al摩尔比可以为约10至约200,例如,约10至约70。当沸石的si/al摩尔比超过约200时,不饱和碳氢化合物的吸附效率可能降低。
36.沸石可以与除了硅(si)和铝(al)之外的金属进行离子交换,并且可以与例如包括以下元素的金属进行离子交换:cr、fe、co、ti、w、ir、pt、rd、pd、ru、th、ni、cu、v、au、re、zr、mo或其组合。基于核-壳颗粒100的总重量,金属的量可以为约1重量%至约10重量%。当金属的含量小于约1重量%时,不饱和碳氢化合物的吸附性能可能下降,并且当其超过约10重量%时,水热稳定性可能降低。
37.另一方面,含有大量铝(al)的沸石比铝含量较低或不含铝的沸石具有更高的不饱和碳氢化合物吸附量,但是其存在在高温含水(h2o)环境中塌陷的问题。由于实际尾气中含有水(h2o),因此需要防止水与含铝沸石接触,以便在这种环境中使用沸石。
38.因此,碳氢化合物吸附剂包含外壳20,所述外壳20包含介孔金属氧化物。外壳20以介孔金属氧化物的形式包覆内核10,从而改善水热稳定性,并因此可以解决在高温潮湿环境下由于结构塌陷和活性位点损失导致的耐久性降低的问题。
39.当金属氧化物为具有介孔尺寸的孔的介孔金属氧化物时,水热稳定性可以得到显著改善。孔径可以为约2nm至约10nm,例如,约2nm至约6nm。
40.介孔金属氧化物可以包括ceo2、zro2、al2o3或其组合,并且可以例如为ceo2。当介孔金属氧化物包括ceo2时,水热稳定性可以得到进一步改善。
41.基于核-壳颗粒100的总重量,介孔金属氧化物的金属的量可以为约0.1重量%至约7重量%,例如,约0.1重量%至约4重量%。当介孔金属氧化物的金属的含量小于约0.1重量%时,水热稳定性可能降低,并且当其超过约7重量%时,水热变质后性能可能下降。
42.根据本技术的另一个实施方案的制备碳氢化合物吸附剂的方法包括制备包含沸石的内核,和形成包含介孔金属氧化物的外壳,从而制备核-壳颗粒。
43.沸石可以商业购买或者以已知的方法制备。例如,沸石可以如下制备:进行原材料混合物的水热合成以制备碱金属型沸石,所述原材料混合物包含二氧化硅源(例如二氧化硅、二氧化硅溶胶和硅酸钠)、氧化铝源(例如氧化铝凝胶、氧化铝溶胶和铝酸钠)、碱源(例如氢氧化钠和硅酸钠)、水和有机碱(例如胺)(如果需要),然后对碱金属型沸石进行离子交换,以制备质子(h)型沸石。此外,质子型沸石可以通过以下步骤制备:用氯化铵水溶液或硝酸铵水溶液等对在水热合成法中制备的碱金属型沸石进行处理,以制备铵型沸石,然后在约400℃至约700℃下煅烧铵型沸石。
44.在包含沸石的内核的表面上形成包含介孔金属氧化物的外壳,从而制备核-壳颗粒。
45.具体地,可以通过混合包含内核的溶液和包含金属氧化物前体的溶液并使其反应来制备核-壳颗粒。
46.可以通过将所获得的沸石加入到溶剂中来制备包含内核的溶液,此时,可以进一步加入包含大量羟基(oh)的易溶于水的环状烃,例如,葡萄糖、果糖、半乳糖、蔗糖、麦芽糖或其组合。葡萄糖等有助于形成外壳的介孔,并可有助于均匀地合成外壳。
47.此外,包含金属氧化物前体的溶液可以包含易溶于水的弱碱性物质,例如,尿素、氨、碳酸钠、碳酸氢钠、碳酸钾、碳酸氢钾、乙酸钠、乙酸钾、二乙醇胺、三甲基胺、六亚甲基二胺、四甲基氢氧化铵或其组合。
48.可以通过将金属氧化物前体加入到溶剂中来制备包含金属氧化物前体的溶液。金属氧化物的前体可以为包含ce、zr、al或其组合的硝酸盐、水合物、氯化物或硫酸盐。例如,当金属氧化物为ceo2时,金属氧化物前体可以为硝酸铈(iii)(ce(no3)3)。此时,还可以加入尿素等。尿素可以使包含金属氧化物前体的溶液呈碱性,从而有助于葡萄糖的去质子化,使得能够均匀地合成外壳。
49.溶剂可以包括蒸馏水、去离子水、乙醇、甲醇、乙二醇、丙二醇、异丙醇或其组合。
50.反应可以在约100℃至约200℃下进行约12小时至约24小时,例如,在约140℃至约170℃下进行约18小时至约24小时。
51.核-壳颗粒的制备还可以包括在约70℃至约150℃下干燥反应产物约10小时至约24小时,然后在约400℃至约700℃下煅烧约1小时至约24小时。
52.另一方面,制备碳氢化合物吸附剂的方法还可以包括使沸石与除了硅(si)和铝(al)之外的金属进行离子交换。离子交换可以在形成外壳之前和之后进行。然而,当在形成外壳之前进行离子交换时,介孔金属氧化物外壳可以抑制金属离子的烧结,因此可以显著改善碳氢化合物吸附剂的水热稳定性。
53.具体地,沸石与金属的离子交换可以使用湿浸渍法,其中将内核或核-壳颗粒加入到包含金属的溶液中,从而将金属浸渍到沸石中。
54.可以通过将金属前体加入到溶剂中来制备包含金属的溶液。金属氧化物的前体可以为包括cr、fe、co、ti、w、ir、pt、rd、pd、ru、th、ni、cu、v、au、re、zr、mo或其组合的硝酸盐、水合物、氯化物、硫酸盐等。例如,当金属为cu时,金属氧化物前体可以为硝酸铜(ii)(cu(no3)2)。
55.溶剂可以包括蒸馏水、去离子水、乙醇、甲醇、乙二醇、丙二醇、异丙醇或其组合。
56.与金属的离子交换还可以包括在约70℃至约150℃下干燥与金属进行离子交换的沸石约10小时至约24小时,然后在约400℃至约700℃下煅烧约1小时至约24小时。
57.碳氢化合物吸附剂可用于吸附汽车排气系统中的碳氢化合物,并且特别地,可用于吸附冷启动阶段排放的碳氢化合物,直到三元催化剂的预热完成。
58.碳氢化合物可以包括丙烯、甲苯、乙烷、乙烯、丙烷、苯、二甲苯、乙烯、2-甲基丁烷、甲醛、苯乙烯、乙醛或其组合。
59.下文描述了本技术的具体实施例。然而,下文描述的实施例仅用于说明目的,并且不限制本技术的范围。
60.制备实施例:碳氢化合物吸附剂的制备
61.实施例1
62.1)金属离子交换步骤
63.将三水合硝酸铜(cu(no3)2·
3h2o,98%,sigma-aldrich co.,ltd.)溶解在去离子
水中,以制备硝酸铜ii(cu(no3)2)溶液。将h型沸石颗粒加入到硝酸铜溶液中,最终在其中浸渍5重量%的铜。将混合物放置在旋转蒸发仪中,以除去其中的水分,回收浸渍cu的沸石,在100℃下干燥3小时,并在200ml/min的气流下以1℃/min的温升在550℃下煅烧6小时。
64.2)核-壳颗粒的制备
65.加入使用湿浸渍法浸渍cu的h型zsm-5沸石,然后与溶解有葡萄糖的去离子水混合(烧杯a)。随后,将硝酸铈iii(ce(no3)3)溶解在溶解有尿素的去离子水中(烧杯b)。将烧杯b中的溶液倒入烧杯a中,然后与其中的溶液混合。将最终混合物放置在内衬有特氟龙(四氟乙烯)的高压釜中,并在160℃的烘箱中反应20小时。然后,从高压釜中回收获得的材料,在100℃下干燥12小时,并在200ml/min至300ml/min的气流下以1℃/min的温升在550℃下煅烧12小时。
66.此处,核-壳颗粒包含5重量%的cu和4重量%的ce。所制备的核-壳颗粒的介孔ceo2外壳包含孔径为约2nm至约10nm的介孔金属氧化物。
67.实施例2
68.1)核-壳颗粒的制备
69.将h型zsm-5沸石加入到溶解有葡萄糖的去离子水中,然后与其混合(烧杯a)。将硝酸铈iii(ce(no3)3)溶解在溶解有尿素的去离子水中(烧杯b)。将烧杯b中的溶液加入到烧杯a的溶液中并与其混合。将最终混合物放置在内衬有特氟龙(四氟乙烯)的高压釜中,并在160℃的烘箱中反应20小时。随后,回收获得的材料,在100℃下干燥12小时,并在200ml/min至300ml/min的气流下以1℃/min的温升在550℃下煅烧12小时。
70.此处,核-壳颗粒包含4重量%的ce。所制备的核-壳颗粒的介孔ceo2外壳包含孔径为约2nm至约10nm的介孔金属氧化物。
71.2)金属离子交换步骤
72.使用湿浸渍法将cu浸渍到核-壳颗粒中。具体地,将三水合硝酸铜(cu(no3)2·
3h2o,98%,sigma-aldrich co.,ltd.)溶解在去离子水中,以制备硝酸铜ii(cu(no3)2)溶液。将核-壳颗粒加入到硝酸铜溶液中,最终在其中浸渍5重量%的铜。将混合物放置在旋转蒸发仪中,以除去其中的水分并回收浸渍cu的核-壳颗粒,在100℃下干燥浸渍cu的核-壳颗粒3小时,并在200ml/min的气流下以1℃/min的温升在550℃下煅烧6小时。
73.实施例3
74.根据与实施例1相同的方法制备碳氢化合物吸附剂,除了将铈含量调节为1重量%。
75.实施例4
76.与根据实施例1相同的方法制备碳氢化合物吸附剂,除了将铈含量调节为7重量%。
77.对比实施例1
78.使用实施例1的浸渍cu的沸石内核作为碳氢化合物吸附剂。
79.对比实施例2
80.使用物理混合ceo2的方法制备包含作为添加剂的ceo2的碳氢化合物吸附剂。将碳氢化合物吸附剂中ceo2颗粒的铈含量调节为4重量%。
81.对比实施例3
82.通过使用除了能够产生介孔的葡萄糖之外的前体合成ceo2外壳的方法,制备包含不具有介孔的ceo2外壳的碳氢化合物吸附剂。将碳氢化合物吸附剂中不具有介孔的ceo2外壳的铈含量调节为4重量%。
83.实验实施例1:碳氢化合物吸附剂的电子显微镜观察
84.用电子显微镜观察根据实施例1的碳氢化合物吸附剂,结果显示在图2中。此外,用电子显微镜观察实施例1中使用的h型沸石,结果显示在图3中。
85.参考图2和图3,根据实施例1的碳氢化合物吸附剂具有核-壳结构,其中zsm-5沸石内核被介孔ceo2外壳包覆。
86.实验实施例2:碳氢化合物吸附剂的吸附性能和水热稳定性的评估
87.在将60mg粉末状核-壳颗粒样品装入反应管中并在he气流下在600℃下预处理30分钟之后,在70℃下在c3h6、c7h8、co、h2、o2、co2、h2o和ar/he混合气体的载气(在λ1的条件下)的气流下吸附碳氢化合物5分钟,然后以约53℃/min的速度将温度升高至约300℃,评估碳氢化合物吸附剂的碳氢化合物吸附/解吸性能。
88.图4显示了根据实施例1和对比实施例1至3的碳氢化合物吸附剂的吸附/解吸评估结果。
89.在图4中,效率可以通过等式1计算。
90.[等式1]
[0091]
效率(%)=(1-q
out
/q
in
)*100
[0092]
在等式1中,q
in
表示供给至碳氢化合物吸附剂的碳氢化合物的量,q
out
表示通过碳氢化合物吸附剂排出的碳氢化合物的量。
[0093]
等式1通过将碳氢化合物供给至用于吸附碳氢化合物的碳氢化合物吸附剂并测量碳氢化合物的供给量和用于吸附碳氢化合物的碳氢化合物吸附剂排出的碳氢化合物的量,然后使用在300℃之前供给至用于吸附碳氢化合物的碳氢化合物吸附剂的碳氢化合物的量与通过用于吸附碳氢化合物的碳氢化合物吸附剂排出的碳氢化合物的量的比值来计算用于吸附碳氢化合物的碳氢化合物吸附剂的效率。
[0094]
ht表示经水热处理的碳氢化合物吸附剂的结果,“新鲜”表示未经水热处理的新鲜碳氢化合物吸附剂的结果。碳氢化合物吸附剂的水热处理可以例如在包含约10重量%水的空气中在约800℃下进行约24小时。总hc表示包括丙烯和甲苯的总碳氢化合物的结果。
[0095]
参考图4,当核-壳颗粒的外壳包含介孔ceo2时,获得了最优异的水热稳定性。
[0096]
此外,图5显示了根据实施例1和2以及对比实施例1的碳氢化合物吸附剂的吸附/解吸评估结果。
[0097]
参考图5,当沸石在形成外壳之前与金属进行离子交换(如图1所示)时,介孔金属氧化物外壳可以抑制金属离子的烧结,因此显著改善碳氢化合物吸附剂的水热稳定性。
[0098]
此外,图6显示了根据实施例1、3和4以及对比实施例1的碳氢化合物吸附剂的吸附/解吸评估结果。
[0099]
参考图6,当介孔ceo2外壳的金属为0.1重量%至4重量%时,碳氢化合物吸附性能和水热稳定性变得更加优异。
[0100]
虽然结合目前被视为是实际的示例性实施方案描述本技术,应理解本公开并不限于所公开的实施方案,但是,相反地,本公开旨在覆盖包括在所附权利要求的精神和范围之
内的各种修改形式和等效形式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1