一种自驱动Mn/Fe复合植物纤维管状微马达催化剂的制备方法及其应用
一种自驱动mn/fe复合植物纤维管状微马达催化剂的制备方法及其应用
技术领域
1.本发明属于无机微纳米材料及环境领域,具体涉及一种自驱动mn/fe复合植物纤维管状微马达催化剂的制备方法及其应用。
背景技术:
2.随着社会经济的发展,全球生态系统污染问题日益突出,尤其是人类活动和集约化农业造成的水污染以及土壤污染,在破坏水资源和土壤资源的同时,更是对人类健康构成严重威胁。由于在环境中持久存在,难以生物降解和通过食物链生物累积等特点,有机污染物已经成为世界各国关注的热点。
3.在原位水土修复的实际应用中,多相催化剂容易发生团聚现象,导致其在水体和土壤中的迁移和扩散率低,从而严重影响过硫酸盐活化效果和氧化降解效率。如何提高修复剂在环境中的迁移效果一直以来都是水土原位修复中的关键问题之一。尤其是在土壤原位修复中,氧化药剂通常以溶液的形式,通过搅拌、高压旋喷、建井注射以及直推注射等工艺注入土壤中。搅拌工艺需要破碎地面,且由于作业设备的限制,处理深度有限。在没有外部机械搅拌的情况下,氧化药剂在土壤中扩散作用的强弱直接影响到修复的效果。低渗透性的土壤及地下非均性会对注入氧化剂的运移产生很大的影响。近年来,作为一种具有独特自驱动特性的微纳米功能材料,微纳马达的迅速发展为水体污染和土壤污染治理提供了新的途径。相对于传统的环境修复用微纳米材料,微纳马达可以从外部环境获得驱动力,深入土壤缝隙等狭小空间进行长距离大范围作业,同时可以利用其自主运动和伴随产生的微纳米气泡增强修复剂在水体和土壤中的迁移和扩散,提高修复效率。此外,在携带大量修复材料的同时不影响其自身驱动,并且可以通过外场精确控制其方位,从而进行针对性分布和高效回收。在原位水土修复中,微纳马达的这些特点为增强修复剂迁移、提高污染物降解效率提供了新的策略。
4.专利申请cn111825241a,一种基于微纳米马达材料的污染物的治理方法及处理装置,提供了一种基于微纳米马达材料的微塑料污染物的治理方法,其包括:将微纳米马达材料加入到待处理的污水中,然后再在污水中加入双氧水开始处理过程,所述微纳米马达材料在待处理的水中发生催化反应,持续产生微纳米气泡,驱动水中的污染物上浮到水面并富集在气泡泡沫相中,然后将泡沫相与污水进行分离。所述微纳米马达材料为能催化双氧水分解的材料。对于水土修复的针对性不高,同时其微马达的来源也完全依赖于化工合成。
技术实现要素:
5.本发明的第一个目的是提供一种基于植物纤维的自驱动mn/fe复合催化管状微马达的制备方法,操作简便,经济可靠,环境友好,具有独特的自驱动和自主扩散特性。在含有低浓度双氧水的环境中,该自驱动材料可以高效自主运动。本制备方法适用于各种具有中空管状结构的植物纤维,具有普适性。
6.本发明的第二个目的是提供上述方法制得的基于植物纤维的自驱动mn/fe复合催化管状微马达催化剂在原位水土修复中增强修复剂迁移和扩散的应用,通过在环境修复剂中添加制备的自驱动微马达修复材料,可以有效增强修复剂在水土中的横向和纵向迁移扩散,扩大处理范围。
7.本发明的第三个目的是提供上述方法制得的基于植物纤维的自驱动mn/fe复合催化管状微马达催化剂在高级氧化降解水土中有机污染物的应用,绿色环保,可以在含有双氧水的高级氧化体系中通过自驱动和所产生的微纳米气泡增强传质作用,提高有机污染物降解效率。本方法适用于各种可以通过高级氧化法降解的污染物,具有普适性。
8.为达到上述目的,本发明主要提供如下技术方案:
9.一种自驱动mn/fe复合植物纤维管状微马达催化剂的制备方法,包括以下步骤:
10.(1)将具有中空管状结构的天然植物纤维处理为适合长度;
11.(2)通过浸渍法和共沉积法在具有管状结构的植物纤维上修饰mnfe2o4@mno2;或者,通过水热法在具有管状结构的植物纤维上修饰fe3o4@mno2;
12.进一步而言,一种用于原位修复污染水土的自驱动mn/fe复合植物纤维管状微马达催化剂的制备和使用方法,具体的步骤包括以下内容:
13.(1)将具有中空管状结构的天然植物纤维(木棉纤维、梧桐纤维等)进行切割,使其长度控制在管径至1毫米的范围内,得到管状植物纤维模板;
14.(2)在具有管状结构的植物纤维上修饰mnfe2o4@mno2:将管状植物纤维模板分散在高锰酸钾溶液中,磁力搅拌后,在室温下浸泡3~72小时,然后过滤收集产物后用大量去离子水和乙醇清洗,产物置于冷冻干燥机中,保持一段时间,直至产物干燥,得到mno2管状微马达,再将mno2管状微马达分散在mnfe2o4纳米颗粒的水溶液中,其中,mno2管状微马达和mnfe2o4纳米颗粒的质量比为5:1,在室温下振荡1天以上,离心收集产物并用大量去离子水和乙醇清洗,产物置于冷冻干燥机中,保持一段时间,直至产物干燥,得到mnfe2o4@mno2管状微马达;
15.或者,通过水热法在具有管状结构的植物纤维上修饰fe3o4@mno2:将管状植物纤维模板分散在含有氯化铁、柠檬酸钠、乙酸钠的乙二醇溶液中,混合均匀后置于水热釜中,在200℃下保持12小时,自然降温后,过滤收集产物并用大量去离子水和乙醇清洗,产物置于冷冻干燥机中,保持一段时间,直至产物干燥,得到fe3o4管状纤维,再将0.075g fe3o4管状纤维分散在含有盐酸的高锰酸钾溶液中,振荡30分钟,所得混合溶液置于水热釜中,在100℃下保持6小时,自然降温后,过滤收集产物并用大量去离子水和乙醇清洗,产物置于冷冻干燥机中,保持一段时间,直至产物干燥,得到fe3o4@mno2管状微马达。
16.本发明制得的自驱动mn/fe复合催化管状微马达可以增强修复剂在土壤中的纵向和横向迁移扩散作用。方法如下:在原位修复水土时,在修复剂中添加双氧水和所制得的自驱动管状微马达,微马达可以通过其无缆自驱动和所产生的微纳米气泡增强修复剂的迁移和扩散,扩大作用范围。
17.本发明还提供了上述方法制得的自驱动mn/fe复合催化管状微马达通过类fenton反应氧化降解水土中四环素、诺氟沙星和荧蒽等有机污染物的应用。方法如下:将所制得的自驱动mn/fe复合催化管状微马达作为双氧水/过硫酸盐复配体系的催化剂,通过活化双氧水和过硫酸盐产生的具有强氧化性的自由基降解水土中的有机污染物。
18.其中,降解土壤中四环素的具体步骤如下:配制含有四环素浓度为400mg kg-1
的污染土壤。将5g四环素污染的土壤加入50ml浓度为1%的双氧水溶液配制成悬浮液,加入过硫酸盐(5mm),然后加入50mg上述制得的自驱动mn/fe复合催化管状微马达,在室温下反应30分钟。在相同的反应条件下,含有过硫酸盐、双氧水和自驱动mn/fe复合催化管状微马达的催化体系对四环素的降解效率最高。所用自驱动管状纤维微马达均可磁控,回收再利用。
19.降解土壤中诺氟沙星的具体步骤如下:配制含有诺氟沙星浓度为40mg kg-1
的污染土壤。将5g诺氟沙星污染的土壤加入10ml浓度为1%的双氧水溶液配制成悬浮液,加入过硫酸盐(1mm),然后加入50mg上述制得的mn/fe复合催化管状微马达,在室温下反应15分钟。在相同的反应条件下,含有过硫酸盐、双氧水和自驱动mn/fe复合催化管状微马达的催化体系对诺氟沙星的降解效率最高。所用自驱动管状纤维微马达均可磁控,回收再利用。
20.降解土壤中荧蒽的具体步骤如下:配制含有荧蒽浓度为40mg kg-1
的污染土壤。将5g荧蒽污染的土壤加入10ml浓度为1%的双氧水溶液配制成悬浮液,加入过硫酸盐(1mm),然后加入50mg上述制得的mn/fe复合催化管状微马达,在室温下反应180分钟。在相同的反应条件下,含有过硫酸盐、双氧水和自驱动mn/fe复合催化管状微马达的催化体系对荧蒽的降解效率最高。所用自驱动管状纤维微马达均可磁控,回收再利用。
21.上述方法所采用的天然管状植物纤维模板可用但不限于梧桐纤维、木棉纤维,利用任何具有中空管状结构的植物纤维均可通过此方法制备得到管状微马达催化剂。在降解有机污染物的高级氧化的复配体系中所采用的过硫酸盐不限于过一硫酸盐pms,也可以使用过二硫酸盐pds等。所氧化降解的污染物也不限于四环素、诺氟沙星和荧蒽等抗生素和多环芳烃,任何能够通过fenton反应和类fenton反应氧化降解的易/难溶于水的有机污染物均可通过此方法高效降解。
22.与现有技术相比,本发明的有益之处在于:
23.1、本发明制备的用于类fenton反应的催化剂为基于植物纤维模板的管状微马达,所采用的植物纤维具有天然环保、产量丰富、价格低廉、结构均一等优点,适用于环境功能材料的批量制备。通过简单的水热法、浸渍法和共沉积法在具有中空管状结构的天然植物纤维上原位修饰所需的催化剂,便可获得能够进行自主运动的管状微马达,避免了传统管状微马达制备中所用到的昂贵的仪器材料和复杂的操作步骤符合绿色环保的要求;
24.2、本发明制备的用于类fenton反应的催化剂为自驱动催化剂,能够在水土中实现自驱动,可利用植物纤维自身特殊的管状结构,通过催化双氧水分解,从微管中喷射微纳米气泡获得驱动力,实现自主运动,从而深入到传统手段无法触及的狭小空间执行任务,还可以进行长距离、大范围、原位作业;
25.5、本发明制备的用于类fenton反应的催化剂为具有自驱动能力的非均相催化剂,可以在反应结束后通过简单的磁控实现分离、回收、处理并重复使用,不会造成二次污染,符合绿色环保的要求,克服了催化剂团聚问题和传统fenton试剂的缺点;
26.6、本发明制备的用于类fenton反应的催化剂可以通过自主运动和所产生微纳米气泡的作用,增强修复剂在污染水土中横向和纵向的迁移效率,扩大修复剂在污染区域中的范围,提高催化剂利用效率;
27.7、本发明制备的自驱动类fenton反应催化剂可以通过自主运动和所产生微纳米气泡的增强传质作用,有效提高降解有机污染物的反应效率提高水土中有机污染物的处理
效果。
附图说明
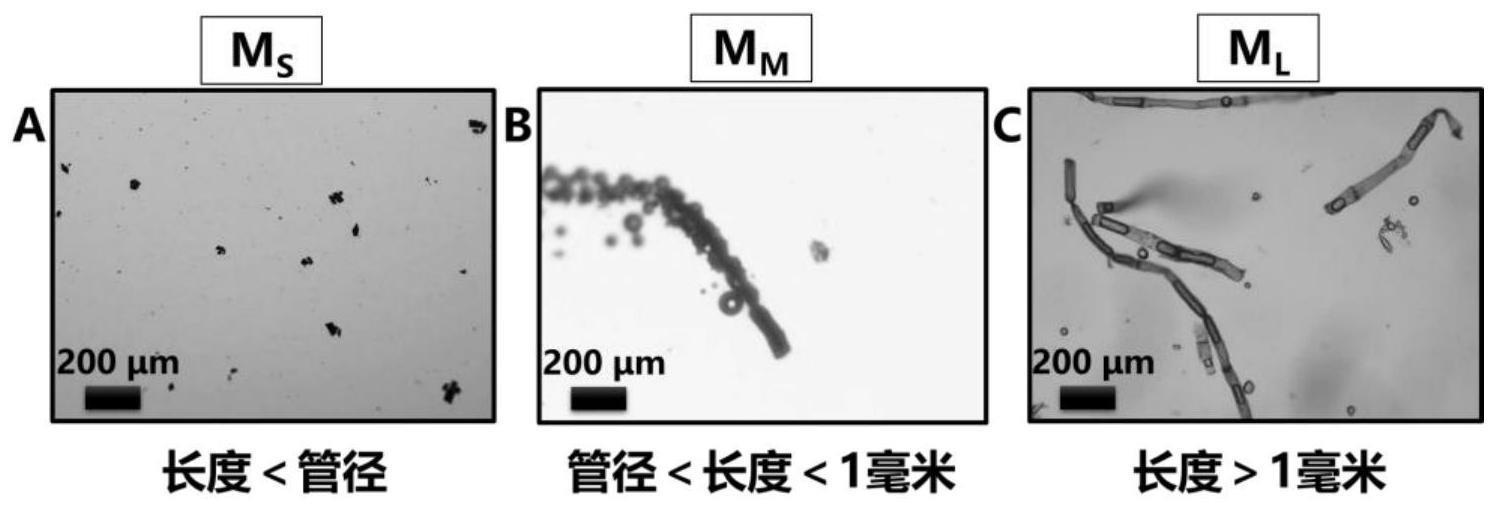
28.图1为本发明实施例1所制备的不同长度的管状微马达的普通光学显微镜图像,其中a为长度小于管径的管状微马达(ms),b为长度处于管径至1毫米的管状微马达(mm),c为长度大于1毫米的管状微马达(m
l
)。
29.图2为本发明实施例2所制备的自驱动mnfe2o4@mno2管状微马达和自驱动fe3o4@mno2管状微马达的制备示意图。
30.图3为本发明实施例2所制备的mno2管状微马达和mnfe2o4@mno2管状微马达的扫描电子显微镜(sem)图像,其中a为mno2管状微马达,b为mnfe2o4@mno2管状微马达。
31.图4为本发明实施例2所制备的mnfe2o4@mno2管状微马达的x射线能量色散(edx)图像。
32.图5为本发明实施例2所制备的fe3o4管状纤维和fe3o4@mno2管状微马达的扫描电子显微镜(sem)图像,其中a为fe3o4管状纤维,b为fe3o4@mno2管状微马达。
33.图6为本发明实施例2所制备的fe3o4@mno2管状微马达的x射线能量色散(edx)图像。
34.图7为本发明实施例3所设置的mn/fe复合催化管状微马达的土壤填充柱迁移实验的装置示意图。
35.图8为本发明实施例3的静态fe3o4@mno2管状微马达和自驱动fe3o4@mno2管状微马达的土壤填充柱迁移实验,其中a为静态fe3o4@mno2管状微马达在土柱中的纵向迁移效果,b为自驱动fe3o4@mno2管状微马达在土柱中的纵向迁移效果。
36.图9为本发明实施例3的静态fe3o4@mno2管状微马达和自驱动fe3o4@mno2管状微马达的土壤填充柱迁移实验,其中a为静态fe3o4@mno2管状微马达在土柱中的局部迁移效果(注水端和出水端),b为自驱动fe3o4@mno2管状微马达在土柱中的局部(注水端和出水端)迁移效果。
37.图10为本发明实施例4的不同过氧化氢浓度体系对自驱动mn/fe复合催化管状微马达的土壤填充柱迁移回收实验。
38.图11为本发明实施例4的不同过氧化氢浓度体系对自驱动mn/fe复合催化管状微马达的土壤填充柱迁移回收比率。
39.图12为本发明实施例5所制备的cn-fe3o4@mno2管状微马达的制备示意图。
40.图13为本发明实施例5所设置的cn-fe3o4@mno2管状微马达在土壤层中的横向迁移实验的装置图。
41.图14为本发明实施例5的静态cn-fe3o4@mno2管状微马达和自驱动cn-fe3o4@mno2管状微马达在土壤层中的横向迁移实验,其中a为静态cn-fe3o4@mno2管状微马达在土壤层中的横向迁移效果,b为自驱动cn-fe3o4@mno2管状微马达在土壤层中的横向迁移效果;
42.图15为实施例6所设置的cn-fe3o4@mno2管状微马达在土壤填充柱中迁移率计算实验的装置示意图。
43.图16为实施例6的静态cn-fe3o4@mno2管状微马达和自驱动cn-fe3o4@mno2管状微马达在土壤填充柱中迁移率计算实验,其中a为静态cn-fe3o4@mno2管状微马达在土壤填充柱
中不同时间和取样点的荧光比率,b为自驱动cn-fe3o4@mno2管状微马达在土壤填充柱中不同时间和取样点的荧光比率。
44.图17为实施例7的不同催化反应体系对四环素污染土壤的降解效率。
45.图18为实施例8的不同催化反应体系对诺氟沙星污染土壤的降解效率。
46.图19为实施例9的不同催化反应体系对荧蒽污染土壤的降解效率。
具体实施方式
47.下面结合附图和具体实施例对本发明作进一步详细说明。
48.实施例1
49.为了探究机械切割后纤维模板的长度对管状微马达制备的影响。将未处理的管状植物纤维切割成长度小于管径、长度处于管径至1毫米、长度大于1毫米,所得纤维模板分别分散于1m高锰酸钾溶液(60ml)中,磁力搅拌1小时后,在室温下浸泡72小时,然后过滤收集产物后用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到管状微马达,分别记为ms、mm、m
l
。将所得的管状微马达分散在含有1.0%双氧水和0.1%sds溶液中观察其运动,使用装备有olympus cellsens dimension系统的光学显微镜拍摄微马达的运动行为。
50.如图1所示,实施例1所制备的管状微马达的普通光学显微镜图像。由图1a可以看出:当管状植物纤维被切割成长度小于管径,图像显示所得管状微马达ms管状结构破碎且静止不动,这证明:管状植物纤维被切割成长度小于管径时,将无法维持微马达运动所需的管状结构且在燃料溶液中不产生气泡和驱动力。由图1b可以看出:当管状植物纤维被切割成长度处于管径至1毫米,图像显示所得管状微马达mm管状结构完整且展现优异的运动行为,这证明:管状植物纤维被切割成长度处于管径至1毫米时,可以维持微马达运动所需的管状结构且在燃料溶液中产生气泡和驱动力。由图1c可以看出:当管状植物纤维被切割成长度大于1毫米,图像显示所得管状微马达m
l
管状结构完整但静止不动,这证明:管状植物纤维被切割成长度大于1毫米时,可以维持微马达运动所需的管状结构,但是由于纤维马达质量较大,管状微马达m
l
在燃料溶液中仅产生气泡但不产生运动行为。
51.实施例2
52.以最优实验条件制备自驱动mn/fe复合植物纤维管状微马达。
53.如图2所示,通过在具有中空管状结构的天然植物纤维模板上负载mnfe2o4@mno2或者fe3o4@mno2,得到mnfe2o4@mno2管状微马达和fe3o4@mno2管状微马达。具体步骤如下:
54.(1)利用机械加工的方法对木棉纤维和梧桐纤维进行切割,使其长度控制在管径至1毫米的范围内,得到木棉纤维模板和梧桐纤维模板。
55.(2)在木棉纤维模板负载mnfe2o4@mno2,具体步骤:将fecl3·
6h2o(2g)、mncl2·
4h2o(0.752g)、naac(5g)和peg(3g)分散在70ml eg中,超声并磁力搅拌1小时以上,充分溶解后,将混合溶液转移至水热釜中,在200℃下保持10小时。反应结束后冷却至室温,离心收集产物后用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到mnfe2o4纳米颗粒。将1.2g木棉纤维模板分散在1m高锰酸钾溶液(60ml)中,磁力搅拌1小时后,在室温下浸泡3~72小时,然后过滤收集产物后用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到mno2管状微马达。将mno2管状微马达分散在
mnfe2o4纳米颗粒的水溶液中,其中,mno2管状微马达和mnfe2o4纳米颗粒的质量比为5:1,在室温下振荡1天以上,离心收集产物并用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到mnfe2o4@mno2管状微马达。
56.或者,在梧桐纤维模板负载fe3o4@mno2,具体步骤:将0.2g梧桐纤维模板分散在含有氯化铁(2.2g)、柠檬酸钠(0.8g)、乙酸钠(6.64g)的乙二醇溶液(68ml)中,混合均匀后置于水热釜中,在200℃下保持12小时,自然降温后,过滤收集产物并用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到fe3o4管状纤维。将0.075g fe3o4管状纤维分散在0.055m高锰酸钾溶液(20ml)中,加入0.25ml浓盐酸后振荡30分钟,所得混合溶液置于水热釜中,在100℃下保持6小时,自然降温后,过滤收集产物并用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到fe3o4@mno2管状微马达。
57.对实施例2所制备的mno2管状微马达和mnfe2o4@mno2管状微马达进行扫描电子显微镜(sem)测试。
58.如图3所示,实施例2所制备的mno2管状微马达和mnfe2o4@mno2管状微马达的sem图谱。由图3a可以看出:mno2管状微马达是开口直径约为10微米的管状纤维,mno2随机分布在天然木棉管状纤维的表面,mno2的修饰没有破坏天然木棉管状纤维的结构。由图3b可以看出:mnfe2o4@mno2管状微马达是开口直径约为10微米的管状纤维,磁性mnfe2o4纳米颗粒随机分布在mno2管状微马达的表面,磁性mnfe2o4纳米颗粒的修饰没有破坏mno2管状微马达的结构。
59.对实施例2所制备的mnfe2o4@mno2管状微马达进行x射线能量色散光谱(edx)分析。
60.如图4所示,实施例2所制备的mnfe2o4@mno2管状微马达的edx元素分布。在图4可以看出:mnfe2o4@mno2管状微马达上均匀分布有c、o、mn和fe元素。这证明天然木棉管状纤维上成功修饰有mno2和磁性mnfe2o4纳米颗粒。
61.对实施例2所制备的fe3o4管状纤维和fe3o4@mno2管状微马达进行扫描电子显微镜(sem)测试。
62.如图5所示,实施例2所制备的fe3o4管状纤维和fe3o4@mno2管状微马达的sem图谱。由图5a可以看出:fe3o4管状纤维是开口直径约为20微米的管状纤维,磁性fe3o4纳米颗粒随机分布在天然梧桐管状纤维的表面,fe3o4的修饰没有破坏天然梧桐管状纤维的结构。由图5b可以看出:fe3o4@mno2管状微马达是开口直径约为20微米的管状纤维,mno2随机分布在fe3o4管状纤维的表面,mno2的修饰没有破坏fe3o4管状纤维的结构。
63.对实施例2所制备的fe3o4@mno2管状微马达进行x射线能量色散光谱(edx)分析。
64.如图6所示,实施例2所制备的fe3o4@mno2管状微马达的edx元素分布。在图6可以看出:fe3o4@mno2管状微马达上均匀分布有c、o、mn和fe元素。这证明天然梧桐管状纤维上成功修饰有mno2和磁性fe3o4纳米颗粒。
65.实施例3
66.为了探究mn/fe复合催化管状微马达在土壤中的纵向扩散迁移效果,搭建模拟催化剂迁移实验的土壤填充柱装置。
67.如图7所示,实施例3的管状微马达催化剂纵向迁移实验的土壤填充柱装置,具体包括:在下端带有出水口的玻璃柱中填充石英砂(填充高度30厘米),加入100mg实施例1制得的fe3o4@mno2管状微马达催化剂,然后向上端的加液球中加入100ml去离子水或者浓度为
c3n4纳米片;然后,将20mg fe3o4@mno2管状微马达分散在含有5mg g-c3n4纳米片的水溶液(4ml)中,在室温下振荡12小时,离心收集产物并用大量去离子水和乙醇清洗,产物置于零下60℃冷冻干燥机中,保持12小时,得到cn-fe3o4@mno2管状微马达。
77.如图13所示,实施例5的催化剂横向扩散迁移实验的土壤层装置,具体包括:在表面皿中平铺一层土壤(土壤厚度0.5厘米),在土壤圆心点处加入100mg上述制得的cn-fe3o4@mno2管状微马达催化剂,然后加入10ml去离子水或者浓度为3%的双氧水溶液作为冲洗液,于波长为365nm的紫外灯照射下,在室温中反应3分钟,裸眼观察并拍照记录cn-fe3o4@mno2管状微马达催化剂在土壤层的自主迁移效果。
78.如图14所示,实施例5的静态cn-fe3o4@mno2管状微马达和自驱动cn-fe3o4@mno2管状微马达在土壤层中的横向扩散作用迁移实验。从图14a可以看出:静态cn-fe3o4@mno2管状微马达在平面土壤层中的被动扩散迁移行为微乎其微,催化剂仍处于加样点。从图14b可以看出:明显的自驱动cn-fe3o4@mno2管状微马达在平面土壤层中的主动扩散迁移增强,充分证明通过自主运动、主动扩散和所产生气泡的作用,自驱动cn-fe3o4@mno2管状微马达催化剂在土壤中的横向迁移效率增强。特别是,裸眼直接观察到微马达基催化剂在土壤中的迁移效果,无需样品前处理,无需大型元素分析仪器,即可明确催化剂的迁移效果。
79.实施例6
80.为了探究实施例5所制备的自驱动cn-fe3o4@mno2管状微马达催化剂在增强催化剂于土壤填充柱中的纵向扩散作用和催化剂迁移率光学计算方法,设置模拟土壤填充柱(包含有3个取样点)的催化剂迁移实验装置。
81.如图15所示,实施例6的土壤填充柱(包含有3个取样点)的催化剂迁移实验装置,具体包括:在下端带有出水口的玻璃柱中填充石英砂(填充高度20厘米),加入100mg实施例5所制得的cn-fe3o4@mno2管状微马达催化剂,然后加入20ml去离子水或者浓度为1%的双氧水溶液,在室温下反应30分钟,在一定时间间隔下,分别在三个取样点处吸取0.5ml流出液,在带有紫外灯配置的显微镜下观察拍照流出液中的固体沉淀,并用显微镜系统统计画面荧光强度,对比静态催化剂和动态催化剂在土壤填充柱的迁移效果并计算催化剂迁移率。
82.如图16所示,实施例6的静态cn-fe3o4@mno2管状微马达和自驱动cn-fe3o4@mno2管状微马达在土壤填充柱中迁移率计算结果。按照f/f0*100%计算催化剂荧光强度比率,其中,f为采集液中固体沉淀的荧光强度,f0为取样点在0分钟时采集液中固体沉淀的荧光强度。从图16a可以看出:30分钟内,取样点的荧光强度比率几乎没有降低,取样点的荧光强度比率表现为略微上升后降低,取样点的荧光强度比率上升幅度可以忽略不计。这表明,30分钟内,静态cn-fe3o4@mno2管状微马达在土壤填充柱中的被动扩散迁移行为微乎其微,催化剂始终处于初始加样点。从图16b可以看出:30分钟内,取样点
①
的荧光强度比率有明显的降低,取样点
②
的荧光强度比率表现为大幅度上升后骤降,取样点
③
的荧光强度比率急剧上升。这表明,30分钟内,自驱动cn-fe3o4@mno2管状微马达在土壤填充柱中的主动扩散迁移增强,充分证明通过自主运动、主动扩散和所产生气泡的作用,自驱动cn-fe3o4@mno2管状微马达催化剂在土壤中的迁移效率增强。特别是,利用催化剂的荧光特性,该方法仅需分析所取微量样品的荧光比率即可考察微马达基催化剂在土壤中的迁移效果,无需样品前处理,无需大型元素分析仪器,完全可以实现评估荧光催化剂在土壤中的自主迁移效率。所提出的土壤环境中催化剂迁移效率的可视化统计策略是完全可行的。
83.实施例7
84.为了探究不同催化体系对四环素污染土壤的降解效率,在室温下,将5g四环素污染土壤(400mg kg-1
)与不同催化剂添加到烧杯中反应,以对比不同催化体系的催化降解性能。其中,mnfe2o4@mno2管状微马达催化剂的浓度为1mg ml-1
,双氧水的浓度为1%,pms的浓度为5mm。在规定的时间间隔内,吸取2ml溶液与3ml提取液,超声处理5分钟,离心收集上清液,并用0.22μm过滤头过滤上清液。所得溶液立即使用紫外-可见分光光度计测定四环素的浓度。
85.如图17所示,实施例7的不同催化体系对四环素污染土壤的降解效率的对比图。首先,对比折线a和b发现,当溶液中存在1%双氧水时,30分钟后,四环素的降解效率仅有20%;相对地,当溶液中只存在5mm pms时,30分钟后,四环素的降解效率仅达到40%。另外,折线c证明,当催化体系同时包含双氧水(1%)和pms(5mm)时,四环素的降解效率达到30%。再者,对比折线b、c和e发现,当溶液中同时存在pms和mno2管状微马达时,5分钟后,四环素的降解效率可达到约60%,30分钟后,四环素的降解效率缓慢增加至65%,因此,可以证明mno2管状微马达可以有效活化pms,进而有效促进四环素的降解。该过程的降解现象归功于微马达对pms的活化产生的强氧化性so4·-对四环素的氧化分解。同样地,对比折线a、c和d发现,当溶液中同时存在双氧水和mno2管状微马达时,5分钟后,四环素的降解效率仅达到约40%,30分钟后,四环素的降解效率达到约60%,因此,可以证明微马达可以和双氧水反应,进而有效降解四环素。该过程的降解现象归功于微马达分解双氧水产生的
·
oh对四环素的类fenton氧化反应,并且微马达存在自搅拌和自扩散,增强催化剂与污染物的接触传质过程和催化剂在土壤修复区域的自主扩散效果,提高污染物降解效率。折线c和g证明了mnfe2o4可以活化pms和双氧水增强四环素的降解效率。最后,从折线h看出,当溶液中同时存在pms、双氧水和mnfe2o4@mno2管状微马达催化剂时,30分钟后,四环素的降解效率可达到90%以上。特别是,折线f、g和h证明了mnfe2o4@mno2异质结对四环素降解的可行性。之所以mnfe2o4@mno2管状微马达催化剂对四环素的降解效率是大于mno2管状微马达催化剂的降解效率,是因为mnfe2o4和mno2可以共同强化活化双氧水和pms氧化反应。总之,由于实施例2中所得的mnfe2o4@mno2管状微马达催化剂可以利用基于双氧水/过硫酸盐复配体系活化的类fenton氧化反应,使得其可以高效降解四环素。并且,催化剂的自主运动及产生的气泡能够在土壤中引起自搅拌,自主扩散迁移增强,加速污染物、氧化剂与催化剂三者的混合,显著提高降解效率。
86.实施例8
87.为了探究不同催化体系对诺氟沙星污染土壤的降解效率,在室温下,将5g诺氟沙星污染土壤(40mg kg-1
)与不同催化剂添加到烧杯中反应,以对比不同催化体系的催化降解性能。其中,fe3o4@mno2管状微马达催化剂的浓度为5mg ml-1
,双氧水的浓度为1%,pms的浓度为1mm。在规定的时间间隔内,吸取2ml溶液与3ml提取液,超声处理5分钟,离心收集上清液,并用0.22μm过滤头过滤上清液。所得溶液立即使用紫外-可见分光光度计测定诺氟沙星的浓度。
88.如图18所示,实施例8的不同催化体系对诺氟沙星污染土壤的降解效率的对比图。首先,对比折线a和b发现,当溶液中只存在1%双氧水时,15分钟后,诺氟沙星的降解效率可以忽略不计;同样地,当溶液中只存在1mm pms时,15分钟后,诺氟沙星的降解效率仅达到
5%左右。其次,折线c证明,当溶液中只存在fe3o4@mno2管状微马达催化剂时,15分钟后,诺氟沙星的降解效率微乎其微,因此,可以排除微马达基催化剂对诺氟沙星的吸附作用。再者,对比折线b、c和d发现,当溶液中同时存在pms和fe3o4@mno2管状微马达时,15分钟后,诺氟沙星的降解效率可达到约40%,因此,可以证明fe3o4@mno2管状微马达可以有效活化pms,进而有效促进诺氟沙星的降解。该过程的降解现象归功于微马达上修饰的fe3o4@mno2异质结对pms活化产生的so4·-对诺氟沙星的类fenton氧化分解。同样地,对比折线a、c和e发现,当溶液中同时存在双氧水和微马达时,15分钟后,诺氟沙星的降解效率可达到约80%,因此,可以证明微马达可以和双氧水反应,进而有效降解诺氟沙星。该过程的降解现象归功于微马达分解双氧水产生的强氧化性
·
oh对诺氟沙星的类fenton氧化反应。最后,从折线f看出,当溶液中同时存在pms、双氧水和fe3o4@mno2管状微马达时,15分钟后,诺氟沙星的降解效率可达到约90%。总之,由于实施例2中所得的fe3o4@mno2管状微马达催化剂可以利用基于双氧水/过硫酸盐复配体系活化的类fenton氧化反应,使得其可以高效降解诺氟沙星。并且,催化剂的自主运动及产生的气泡能够在土壤中引起自搅拌,自主扩散迁移增强,加速污染物、氧化剂与催化剂三者的混合,显著提高降解效率。
89.实施例9
90.为了探究不同催化体系对荧蒽污染土壤的降解效率,在室温下,将5g荧蒽污染土壤(40mg kg-1
)与不同催化剂添加到烧杯中反应,以对比不同催化体系的催化降解性能。其中,fe3o4@mno2管状微马达催化剂的浓度为5mg ml-1
,双氧水的浓度为1%,pms的浓度为1mm。在规定的时间间隔内,吸取1ml溶液与4ml乙醇,超声处理15分钟,离心收集上清液,并用0.22μm过滤头过滤上清液。所得溶液立即使用荧光分光光度计测定荧蒽的浓度。
91.如图19所示,实施例9的不同催化体系对荧蒽污染土壤的降解效率的对比图。首先,对比折线a和b发现,当溶液中只存在1%双氧水时,180分钟后,荧蒽的降解效率可以忽略不计;同样地,当溶液中只存在1mm pms时,180分钟后,荧蒽的降解效率仅达到10%左右。其次,折线c证明,当溶液中只存在fe3o4@mno2管状微马达催化剂时,180分钟后,荧蒽的降解效率微乎其微,因此,可以排除微马达基催化剂对荧蒽的吸附作用。再者,对比折线b、c和e发现,当溶液中同时存在pms和fe3o4@mno2管状微马达时,180分钟后,荧蒽的降解效率可达到约50%,因此,可以证明fe3o4@mno2管状微马达可以有效活化pms,进而有效促进荧蒽的降解。该过程的降解现象归功于微马达上修饰的fe3o4@mno2异质结对pms活化产生的so4·-对荧蒽的类fenton氧化分解。同样地,对比折线a、c和d发现,当溶液中同时存在双氧水和微马达时,180分钟后,荧蒽的降解效率可达到约70%,因此,可以证明微马达可以和双氧水反应,进而有效降解荧蒽。该过程的降解现象归功于微马达分解双氧水产生的强氧化性
·
oh对荧蒽的类fenton氧化反应。最后,从折线f看出,当溶液中同时存在pms、双氧水和fe3o4@mno2管状微马达时,180分钟后,荧蒽的降解效率可达到约80%。总之,由于实施例2中所得的fe3o4@mno2管状微马达催化剂可以利用基于双氧水/过硫酸盐复配体系活化的类fenton氧化反应,使得其可以高效降解荧蒽。并且,催化剂的自主运动及产生的气泡能够在土壤中引起自搅拌,自主扩散迁移增强,加速污染物、氧化剂与催化剂三者的混合,显著提高降解效率。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1