具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物及其制备与应用
1.本发明涉及纳米材料、生物催化及分析化学领域,具体地,本发明涉及一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物及其制备与应用。
背景技术:
2.世界范围内糖尿病的发病率在不断增加,糖尿病已经成为威胁现代人类健康和生命的重大慢性疾病。检测人体内血糖浓度是糖尿病患者护理的基本措施。而葡萄糖传感器常用来检测人体内血糖浓度。其中葡萄糖传感器可分为有酶和无酶传感器,目前的酶基生物传感器主要是利用葡萄糖氧化酶(god),其在氧气环境下能将葡萄糖氧化。然而,葡萄糖氧化酶很容易受到外界环境(如ph值、温度、有机溶剂等)的影响而失活或变性,大大阻碍了其实际应用。因此,迫切需要开发一种准确、响应速度快、灵敏度高的无酶葡萄糖检测体系。
3.纳米和亚纳米材料因其成本低、稳定性高、易于批量生产等优点,已成为酶促反应中天然酶的替代品。特别是具有原子金属-氮(mnx)位点的单原子催化剂(sacs),由于其具有精确的配位结构及均匀分散的金属活性位点而受到越来越多的关注。然而,这些仿酶催化剂只能用来模仿一种酶。因此,将不同种类的仿酶催化剂进行整合形成复合物以完成多步级联反应是必要的。例如,将葡萄糖氧化酶(gox)和辣根过氧化物酶(hrp)的仿酶催化剂结合在一起,得到具有级联酶催化活性的复合物,用于级联催化葡萄糖的检测。然而,目前报道的具有级联酶催化活性的复合物大多是基于简单的将不同种类的仿酶催化剂堆叠在一起,该方法导致催化剂的催化位点堆叠,使得化合物之间相互干扰,进一步大大降低了级联反应效率。因此,如何提高催化剂的级联酶催化活性,是实现高催化活性和高选择性级联催化葡萄糖的检测中亟待突破的重大技术问题。
技术实现要素:
4.针对上述问题,本发明的主要目的在于提供一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物及其制备与应用,实现催化活性位点隔离,提高级联酶催化剂的催化活性,进而实现高催化活性和高选择性级联催化葡萄糖的检测。
5.为实现上述目的,本发明的技术方案如下:
6.作为本发明的第一个方面,提供一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物,包括:氮掺杂碳壳(简称为n-c壳)、负载于n-c壳外层的金属纳米颗粒,以及修饰于n-c壳内层的金属单原子;其中,金属纳米颗粒具有葡萄糖氧化酶活性,金属单原子具有过氧化物酶活性。
7.作为本发明的第二个方面,提供一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物的方法,包括如下步骤:
8.1)提供具有颗粒直径为100~900nm的金属氧化物作为前驱体;
9.2)以步骤1)中所得的金属氧化物为模板,通过原位聚合方法在金属氧化物的外层
修饰含n的高分子聚合物,得到核壳结构的纳米材料;
10.3)将步骤2)中所得的纳米材料在惰性气体氛围下加热以进行碳化处理,得到n-c壳内层修饰金属单原子的材料;
11.4)以步骤3)中所得的材料为模板,通过原位还原金属盐前驱体的方式,在n-c壳外层修饰金属纳米颗粒,得到纳米复合物。
12.作为本发明的第三个方面,提供一种级联催化的无酶葡萄糖检测体系,包括:具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物、有机显色剂、ph缓冲液和待测葡萄糖溶液。
13.作为本发明的第四个方面,提供一种具有级联酶催化活性的金属单原子/金属纳米颗粒的纳米复合物在无酶检测葡萄糖中的应用。
14.基于上述技术方案,本发明提供的具有级联催化作用的金属单原子/金属纳米颗粒的纳米复合物及其制备与应用至少具有以下有益效果其中之一或其中一部分:
15.1、本发明提供的具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物,其中金属单原子具有仿过氧化物酶活性,金属纳米颗粒具有仿葡萄糖氧化酶的活性,首次将不同的酶催化活性位点在空间上隔开,其中金属单原子活性位点锚定到n-c壳的内层,而金属纳米颗粒负载到n-c壳的外层,通过该特定结构避免了仿酶催化剂在参与级联反应时的相互干扰,提高了催化活性和选择性。该纳米复合物稳定性高、易于量产、制备成本低,有望广泛用于生物传感、医药、食品工程和催化等领域。
16.2、本发明提供的金属单原子/金属纳米颗粒的纳米复合物在应用于级联催化葡萄糖的检测中时,在金属纳米颗粒提供的氧化酶活性下将葡萄糖氧化成葡萄糖酸和过氧化氢,进一步过氧化氢在内层金属单原子的过氧化物酶活性下分解产生活性自由基来将有机显色剂氧化,如此使得金属单原子和金属纳米颗粒之问独立工作且串联催化。因此,当将金属单原子/金属纳米颗粒的纳米复合物应用于葡萄糖的无酶检测时,基于有机显色剂氧化产物的显色值与过氧化氢浓度之间以及过氧化氢浓度与葡萄糖浓度之间的线性关系来对葡萄糖进行定性或定量检测,实现了一步无酶检测葡萄糖。与传统简单堆叠式仿酶催化剂相比,其催化活性提高了9.8倍。
附图说明
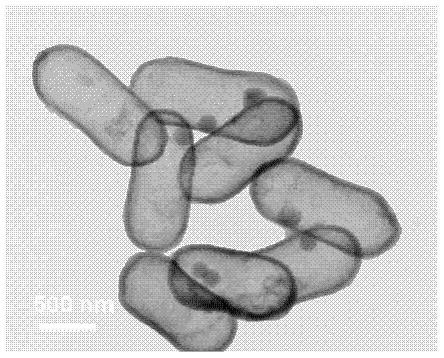
17.图1是本发明实施例1中fe1/nc的透射电子显微镜(tem)图;
18.图2是本发明实施例1由fe1/nc负载au nps后的fe1@au nps的透射电子显微镜(tem)图;
19.图3是本发明实施例1中fe1@au nps的扫描电子显微镜(sem)图;
20.图4是本发明实施例1中fe1@au nps的球差矫正高角度环形暗场扫描透射电子显微镜(ac haadf-stem)图;
21.图5是本发明实施例5、对比例1和对比例2的fe1@au nps纳米复合物仿过氧化物酶活性的效果图;
22.图6是本发明实施例6、对比例3和对比例4的fe1@au nps纳米复合物仿葡萄糖氧化酶活性的效果图;
23.图7是本发明实施例7、对比例5和对比例6的fe1@au nps、fe1/au nps和fe1&au nps
纳米复合物的级联催化反应的活性图;
24.图8是本发明实施例8的基于fe1@au nps催化体系的葡萄糖比色传感的定性检测图;
25.图9是本发明实施例9基于fe1@au nps催化体系的葡萄糖比色传感的定量检测图;
26.图10是本发明实施例10的fe1@au nps催化剂检测葡萄糖的选择性对比图。
具体实施方式
27.为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,对本发明作进一步的详细说明。
28.通过调研文献发现,在将具有级联酶催化活性的催化剂应用于级联催化葡萄糖检测过程中,如何有效隔离催化活性位点,防止化合物的相互干扰,是提升级联催化剂催化效率的技术难点。本发明基于金属纳米颗粒具有葡萄糖氧化酶活性及金属单原子具有过氧化物酶活性,通将金属纳米颗粒负载于n-c壳外层,将金属单原子修饰于n-c壳内层,实现催化活性位点的隔离,提升其催化活性,实现高催化活性和高选择性级联催化葡萄糖的检测。
29.需要说明的是,本发明中金属单原子修饰于n-c壳内层是指在n-c壳上,金属原子(fe、co、ni等)以单原子分散的形式掺杂于n-c壳。
30.具体而言,根据本发明的实施例,提供了一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物,包括:n-c壳、负载于n-c壳外层的金属纳米颗粒,以及修饰于n-c壳内层的金属单原子;其中,金属纳米颗粒具有葡萄糖氧化酶活性,金属单原子具有过氧化物酶活性。
31.由于氮掺杂可有效地在碳结构中诱导大量分散的缺陷,金属单原子锚定于n-c壳内层缺陷中形成具有mnx位点的单原子催化剂,用于模仿过氧化物酶,而金属纳米颗粒负载于n-c壳外层,用于模仿葡萄糖氧化酶。n-c壳的存在不影响金属纳米颗粒的葡萄糖氧化酶活性以及金属单原子的过氧化物酶活性;不干扰金属纳米颗粒、金属单原子各自的催化反应。因此,n-c壳能够有效实现将金属单原子和金属纳米颗粒分隔开,使其各自发挥催化作用并协同完成多步的级联催化反应。
32.根据本发明的实施例,金属单原子为选自mn、fe、co、ni、cu或zn中的至少一种,即,这些金属单原子修饰n-c壳可为单种、两种或多种单原子修饰,例如可以是fe单原子修饰n-c壳,co和fe双单原子修饰n-c壳,co、fe和zn三单原子修饰n-c壳等。
33.根据本发明的实施例,金属纳米颗粒为选自au、ag、pt、rh或ir的单金属纳米颗粒或选自feco、ptco、或fecopt的多金属纳米颗粒。
34.根据本发明的实施例,多金属纳米颗粒并非多种仿酶的简单堆叠,而是作为纳米合金来模拟一种酶,存在单一的催化活性位点。
35.根据本发明的实施例,金属单原子占纳米复合物总质量的0.1~10.0wt%,金属纳米颗粒占纳米复合物总质量的0.5~25.0wt%,金属纳米颗粒的平均直径范围为0.5~20nm,以适应于n-c壳结构,利于金属单原子和金属纳米颗粒负载其内外层。
36.根据本发明的实施例,还提供了一种制备上述的具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物的方法,包括如下步骤:
37.1)提供具有颗粒直径为100~900nm的金属氧化物作为前驱体。
38.2)以步骤1)中所得的金属氧化物为模板,通过原位聚合方法在金属氧化物的外层修饰含n的高分子聚合物,得到核壳结构的纳米材料。
39.3)将步骤2)中所得的纳米材料在惰性气体氛围下加热以进行碳化处理,得到n-c壳内层修饰金属单原子的材料。
40.4)以步骤3)中所得的材料为模板,通过原位还原金属盐前驱体的方式,在n-c壳外层修饰金属纳米颗粒,得到纳米复合物。
41.根据本发明的实施例,步骤1)中,金属氧化物为mno2、fe2o3、coo、nio、cuo或zno;作为优选,金属氧化物通过水热法提供,水热反应的温度为50~300℃,反应时间为1~5天,以成功制备在纳米尺寸范围内的金属氧化物。
42.根据本发明的实施例,步骤2)具体包括:将步骤1)所得的金属氧化物加入到tris缓冲溶液或h2so4溶液中;以及向所得的溶液中加入聚合单体进行聚合反应,得到核壳结构的纳米材料;其中,聚合单体选自多巴胺、吡咯或吡啶。
43.根据本发明的实施例,步骤3)中惰性气体可以为氮气或氩气。
44.根据本发明的实施例,步骤3)中加热温度为200~900℃的温度,优选为300~800℃,更优选为400~600℃,保温时间为0.5~5h,升温速率为1~10℃
·
min-1
。
45.根据本发明的实施例,因氮掺杂碳的中空核壳结构不稳定,所以加热温度不宜过高,保温时间不宜过长。当加热温度过高(如高于900℃)且加热时间过长(如大于5h)时,氮掺杂碳的中空核壳结构会因为不稳定而被破坏。当加热温度过低(如低于200℃)且加热时间过短(如小于0.5h),将无法实现金属单原子扩散并锚定于n-c壳内层。因此,只有在适宜的加热温度(200~900℃)以及保温时间(0.5~5h)的条件下才能实现金属单原子修饰在n-c壳内层。
46.根据本发明的实施例,步骤4)具体包括:将步骤3)所得的材料分散于水中后,向所得分散液中缓慢加入金属盐溶液,得到混合液;以及向混合液中加入还原剂以使金属盐发生还原反应,得到纳米复合物。
47.根据本发明的实施例,金属盐例如可以是haucl4、ptcl4、agno3、co(no3)3、fecl3、rhcl3、ircl3等;还原剂例如可以是nabh4、lialh4等;还原反应在低温下进行,例如采用冰浴溶剂法进行,反应时间为10~180s。
48.根据本发明的实施例,还提供了一种具有级联酶催化活性的金属单原子/金属纳米颗粒的纳米复合物在无酶检测葡萄糖中的应用。
49.根据本发明的实施例,该应用包括以下步骤:
50.(1)将不同浓度的葡萄糖溶液、金属单原子/金属纳米颗粒的纳米复合物、有机显色剂分别加到ph缓冲液中,对得到的含不同浓度葡萄糖的混合溶液进行孵育;
51.(2)通过观察步骤(1)所得的混合溶液颜色来实现定性检测,混合溶液的颜色越深说明葡萄糖浓度越大;或者检测混合溶液的吸光度值,绘制关于葡萄糖浓度和吸光度值的线性方程来实现定量检测。
52.根据本发明的实施例,ph缓冲液为1-10mm、纳米复合物为200-4000μg/ml、葡萄糖溶液0-100mm、有机显色剂为1-20mm。
53.根据本发明的实施例,ph缓冲液的ph优选为7.2~7.4。
54.根据本发明的实施例,有机显色剂为3,3’,5,5
’‑
四甲基联苯胺(tmb)、邻苯二胺
(opd)或2,2
’‑
联氮-双(3-乙基苯并噻唑啉-6-磺酸)二胺盐(abts)。更优选地,有机显色剂为tmb。
55.根据本发明的实施例,在含有不同浓度葡萄糖的混合溶液孵育过程中,金属纳米颗粒具有葡萄糖氧化酶活性,可将葡萄糖氧化成葡萄糖酸和过氧化氢,过氧化氢被内层具有过氧化物酶活性的金属单原子分解产生活性自由基,活性自由基与显色剂发生氧化反应,使得不同浓度葡萄糖的混合溶液产生梯度显色。可见,本发明的金属单原子和金属纳米颗粒在无酶检测葡萄糖中的应用中,金属单原子和金属纳米颗粒之间独立工作且串联催化,并实现了对葡萄糖的一步无酶检测葡萄糖。
56.根据本发明的实施例,金属单原子/金属纳米颗粒的纳米复合物相比于简单堆叠的仿酶催化剂,在用于级联催化葡萄糖时具有更高的催化活性,因此,将级联酶催化剂的活性位点隔离开,利于提高其催化活性,进而实现高催化活性和高选择性级联催化葡萄糖的检测。在无酶葡萄糖检测应用中,葡萄糖检测范围为0-10mm,检测限为10μm。
57.根据本发明的实施例,还提供了一种级联催化的无酶葡萄糖检测体系,包括:具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物、有机显色剂、ph缓冲液和待测葡萄糖溶液。
58.以下列举多个具体实施例来对本发明的技术方案作详细说明。需要说明的是,下文中的具体实施例仅用于示例,并不用于限制本发明。下列实施例中具体实验条件或方法如未注明,均按本领域的常规条件或方法进行。
59.实施例1:金属单原子/金属纳米颗粒的纳米复合物的制备
60.1)制备fe2o3:将fecl3·
6h2o溶液(50ml,2m)在75℃的油浴锅中加热搅拌5分钟,然后逐滴加入naoh溶液(50ml,5.4m),加热15分钟后,将na2so4溶液(50ml,0.6m)加入到上述混合溶液中。最后,将得到的fe(oh)3凝胶转移到100ml不锈钢高压釜内衬中,在100℃下反应5天。得到的红色产物fe2o3离心收集,用乙醇和去离子水洗涤3次,在80℃中真空干燥。
61.2)将步骤1)所得粉末样品fe2o3(350mg)分散到400ml新鲜制备的tris缓冲溶液中(10mm,ph 8.5)。然后在上述缓冲液中加入160mg多巴胺,以在fe2o3外层修饰聚多巴胺。让混合溶液在室温下搅拌2小时。用去离子水和乙醇洗涤三次,离心收集。将所得产物在80℃中进行真空干燥,即可得到fe2o3@pda。
62.3)将步骤2)中所得30mg粉末材料,置于管式炉中,用体积分数为99.999%的氩气通入炉管,气体的流速为50ml/min。再将管式炉以5℃/min的升温速率升温到500℃,保温2h,再以5℃/min的升温速率升温到700℃,保温2h后,冷却至室温,即可得到n-c壳内层修饰fe单原子的fe1/nc粉末材料。
63.4)将步骤3)中所得2mg粉末材料溶解在20ml的水溶液中,超声分散,逐滴加入haucl4溶液(200μl,10mm),搅拌1分钟后,加入新鲜制备的冰浴的nabh4水溶液(50μl,0.1m),立即用离心机离心收集,离心转速为11000rpm,离心时间为10min。最后,将得到的产物进行冷冻干燥,即可得到n-c壳内层修饰fe单原子,外层修饰au nps的fei@au nps纳米复合物。
64.结构性能表征:
65.图1是本发明实施例1中fe1/nc的透射电子显微镜(tem)图,如图1所示,得到的fe1/nc呈现出空心花生状的结构且没有发现fe颗粒的聚集,其平均直径为600nm左右。图2和图3是本发明实施例1由fe1/nc负载au nps后的fe1@au nps的透射电子显微镜(tem)和扫描电子
显微镜(sem)图,如图2和图3所示,平均直径为5-10nm的au nps是均匀的分布在n-c壳的外层。图4是本发明实施例1中fe1@au nps的球差矫正高角度环形暗场扫描透射电子显微镜(ac haadf-stem)图,其中a图和b图分别为n-c壳内层和外层,可见圈示绝大部分单原子在内层呈均匀分布,仅有极少量单原子分布在外层。
66.通过电感耦合等离子体质谱方法对所得到的fe1@au nps纳米复合物中的组成进行测定,fe单原子的含量占整体纳米复合物的质量比是2.1wt%,au nps的含量占整体纳米复合物的质量比是1.3wt%,被稳定的金纳米颗粒平均直径范围为15nm。
67.实施例2:金属单原子/金属纳米颗粒的纳米复合物的制备
68.1)制备mno2:将0.38g kmno4和0.8ml hcl加入到35ml去离子水中,在磁搅拌下形成透明溶液。然后转移到容量为50ml的不锈钢高压釜内衬中,在140℃加热2天,得到的产物mno2离心收集,用去离子水和乙醇洗涤,然后在80℃中真空干燥。
69.2)将步骤1)所得粉末样品mno2(350mg)分散到400ml新鲜制备的tris缓冲溶液中(10mm,ph 8.5)。然后在上述缓冲液中加入160mg多巴胺,以在mno2外层修饰聚多巴胺。让混合溶液在室温下搅拌2小时。用去离子水和乙醇洗涤三次,离心收集。将所得产物在80℃中进行真空干燥,即可得到mno2@pda。
70.3)将步骤2)中所得30mg粉末材料,置于管式炉中,用体积分数为99.999%的氩气通入炉管,气体的流速为50ml/min。再将管式炉以5℃/min的升温速率升温到300℃,保温1h,再以5℃/min的升温速率升温到500℃,保温3h后,冷却至室温,即可得到n-c壳内层修饰mn单原子的mn1/nc粉末材料。
71.4)将步骤3)中所得2mg粉末材料溶解在20m1的水溶液中,超声分散,逐滴加入ptcl4溶液(300μl,30mm),搅拌1分钟后,加入新鲜制备的冰浴的nabh4水溶液(100μl,0.1m),立即用离心机离心收集,离心转速为11000rpm,离心时间为10min。最后,将得到的产物进行冷冻干燥,即可得到n-c壳内层修饰mn单原子,外层修饰pt nps的mn1@pt nps纳米复合物。
72.通过电感耦合等离子体质谱方法对所得到的mn1@pt nps复合催化剂中的组成进行测定,mn单原子的含量占整体纳米复合物的质量比范围是2.8wt%,pt nps的含量占整体纳米复合物的质量比范围是4.1wt%,被稳定的铂纳米颗粒平均直径范围为8.3nm。
73.实施例3:金属单原子/金属纳米颗粒的纳米复合物的制备
74.1)制备coo:将600mg c
15h21
coo6和2.2g ctab加入到60ml去离子水中,在磁搅拌下形成透明溶液。然后转移到容量为100ml的不锈钢高压釜内衬中,在180℃加热3天,得到的产物coo离心收集,用去离子水和乙醇洗涤,然后在80℃中真空干燥。
75.2)将步骤1)所得粉末样品coo(350mg)分散到400ml新鲜制备的tris缓冲溶液中(10mm,ph 8.5)。然后在上述缓冲液中加入320mg多巴胺,以在fe2o3外层修饰聚多巴胺。让混合溶液在室温下搅拌2小时。用去离子水和乙醇洗涤三次,离心收集。将所得产物在80℃中进行真空干燥,即可得到coo@pda。
76.3)将步骤2)中所得30mg粉末材料,置于管式炉中,用体积分数为99.999%的氮气通入炉管,气体的流速为50ml/min。再将管式炉以5℃/min的升温速率升温到200℃,保温1h,再以10℃/min的升温速率升温到300℃,保温0.5h后,冷却至室温,即可得到n-c壳内层修饰co单原子的co1/nc粉末材料。
77.4)将步骤3)中所得2mg粉末材料溶解在20ml的水溶液中,超声分散,逐滴加入
agno3溶液(500μl,20mm),搅拌1分钟后,加入新鲜制备的冰浴的nabh4水溶液(500μl,0.1m),立即用离心机离心收集,离心转速为11000rpm,离心时间为10min。最后,将得到的产物进行冷冻干燥,即可得到n-c壳内层修饰co单原子,外层修饰ag nps的co1@agnps纳米复合物。
78.通过电感耦合等离子体质谱方法对所得到的co1@agnps复合催化剂中的组成进行测定,co单原子的含量占整体纳米复合物的质量比范围是2.2wt%,ag nps的含量占整体纳米复合物的质量比范围是1.4wt%,被稳定的银纳米颗粒平均直径范围为6.5nm。
79.实施例4:金属单原子/金属纳米颗粒的纳米复合物的制备
80.1)制备mno2:将0.38g kmno4和0.8ml hcl加入到35ml去离子水中,在磁搅拌下形成透明溶液。然后转移到容量为50ml的不锈钢高压釜内衬中,在140℃加热2天,得到的产物mno2离心收集,用去离子水和乙醇洗涤,然后在80℃中真空干燥。
81.2)将步骤1)所得粉末样品mno2(300mg)分散到新鲜制备的h2so4中溶液中(24ml,1m)。然后在0℃搅拌下滴加300ul吡咯。将悬浮液在0℃下进一步搅拌6小时。以在mno2外层修饰聚吡咯。用去离子水和乙醇洗涤三次,离心收集。将所得产物在80℃中进行真空干燥,即可得到mno2@ppy。
82.3)将步骤2)中所得30mg粉末材料,置于管式炉中,用体积分数为99.999%的氩气通入炉管,气体的流速为50ml/min。再将管式炉以5℃/min的升温速率升温到500℃,保温1h,再以5℃/min的升温速率升温到900℃,保温3h后,冷却至室温,即可得到n-c壳内层修饰mn单原子的mn1/nc粉末材料。
83.4)将步骤3)中所得5mg粉末材料溶解在30ml的水溶液中,超声分散,逐滴加入ptcl4溶液(300μl,30mm)和co(no3)3溶液(200μl,20mm),搅拌1分钟后,加入新鲜制备的冰浴的nabh4水溶液(100μl,0.1m),立即用离心机离心收集,离心转速为11000rpm,离心时间为10min。最后,将得到的产物进行冷冻干燥,即可得到n-c壳内层修饰mn单原子,外层修饰ptco nps的mn1@ptco nps纳米复合物。
84.通过电感耦合等离子体质谱方法对所得到的mn1@ptco nps复合催化剂中的组成进行测定,mn单原子的含量占整体纳米复合物的质量比范围是2.8wt%,pt元素的含量占整体纳米复合物的质量比范围是4.1wt%,co元素的含量占整体纳米复合物的质量比范围是2.6wt%,被稳定的ptco纳米颗粒平均直径范围为12nm。
85.实施例5:金属单原子/金属纳米颗粒的纳米复合物的仿过氧化物酶活性验证
86.催化反应体系包含h2o2(20μl,10mm)、实施例1获得的fe1@au nps纳米复合物(20μl,200μg/ml)、有机显色剂tmb(20μl,6mm)和ph 7.2缓冲液(140μl,10mm)。在室温(25℃)下反应10分钟。
87.对比例1:金属单原子/金属纳米颗粒的纳米复合物的仿过氧化物酶活性验证
88.与实施例5的催化反应体系及操作类似,区别在于催化反应体系中不含fe1@au nps纳米复合物。
89.对比例2:金属单原子/金属纳米颗粒的纳米复合物的仿过氧化物酶活性验证
90.与实施例5的催化反应体系及操作类似,区别在于催化反应体系中不含h2o2。
91.将实施例5(fe1@au nps+h2o2+tmb)、对比例1(h2o2+tmb)和对比例2(fe1@au nps+tmb)反应后得到的溶液,在同样的条件下利用酶标仪检测其在500~800nm内的吸光值。
92.图5是本发明实施例5、对比例1和对比例2的fe1@au nps纳米复合物仿过氧化物酶
活性的效果图。
93.如图5所示,实施例5得到的溶液样品在652nm附近显示出明显的显色剂氧化产物的吸收峰,说明fe1@au nps在ph 7.2处具有明显的仿过氧化物酶的活性;对比例1在652nm附近无吸收峰,说明若没有fe1@au nps纳米复合物作催化剂将不会发生显色反应;对比例2在652nm附近无明显的吸收峰,说明实施例5中溶液样品的吸收峰不是fe1@au nps自身的响应峰。
94.实施例6:金属单原子/金属纳米颗粒的纳米复合物仿葡萄糖氧化酶活性验证
95.催化反应体系包含葡萄糖(20μl,10mm)、上述实施例1获得的fe1@au nps级联催化剂(20μl,200μg/ml)和ph 7.2缓冲液(160μl,10mm)。在室温(25℃)下反应30分钟后,离心取上清液。向上清液(60μl)中加入显色剂tmb(20μl,6mm)、hr(20μl,200μg/ml)和ph4.0醋酸盐缓冲液(100μl,100mm)。继续在室温(25℃)下反应10分钟后,利用酶标仪检测其500~800nm内的显色剂氧化产物的吸光值;
96.对比例3:金属单原子/金属纳米颗粒的纳米复合物仿葡萄糖氧化酶活性验证
97.与实施例6的催化反应体系及操作类似,区别在于催化反应体系中不含fe1@au nps纳米复合物。
98.对比例4:金属单原子/金属纳米颗粒的纳米复合物仿葡萄糖氧化酶活性验证
99.与实施例6的催化反应体系及操作类似,区别在于催化反应体系中不含葡萄糖。
100.将实施例6(fe1@au nps+葡萄糖+tmb)、对比例3(葡萄糖+tmb)和对比例4(fe1@au nps+tmb)反应后得到的溶液,在同样的条件下利用酶标仪检测其500~800nm内的显色剂氧化产物的吸光值。
101.图6是本发明实施例6、对比例3和对比例4的fe1@au nps纳米复合物的级联催化反应的活性图。
102.如图6所示,实施例6得到的溶液样品在652nm附近显示出明显的显色剂氧化产物的吸收峰,即基于hrp-tmb比色法验证了葡萄糖第一步催化反应中生成的中间产物h2o2,进而说明fe1@au nps在ph 7.2处具有明显的仿葡萄糖氧化酶的活性;对比例3在652nm附近无吸收峰,说明若没有fe1@au nps作催化剂将不会发生显色反应;对比例4在652nm附近无明显的吸收峰,说明实施例6中溶液样品的吸收峰不是fe1@au nps自身的响应峰。
103.实施例7:金属单原子/金属纳米颗粒的纳米复合物级联催化反应的性能研究
104.催化反应体系包含葡萄糖(20μl,10mm)、显色剂tmb(20μl,6mm)、上述实施例1获得的fe1@au nps级联催化剂(20μl,200μg/ml)和ph 7.2缓冲液(140μl,10mm)。在室温(25℃)下反应30分钟后,利用酶标仪检测其652nm显色剂氧化产物的吸光值,;
105.对比例5:金属单原子/金属纳米颗粒的纳米复合物反应动力学的研究
106.与实施例7的催化反应体系及操作类似,区别在于催化反应体系中的fe1@au nps纳米复合物替代为传统简单堆叠的fe1/au nps纳米复合物。
107.对比例6:金属单原子/金属纳米颗粒的纳米复合物反应动力学的研究
108.与实施例7的催化反应体系及操作类似,区别在于催化反应体系中的fe1@au nps纳米复合物替代为共平面构建的fe1&au nps纳米复合物。
109.图7是本发明实施例7、对比例5和对比例6的fe1@au nps、fe1/au nps和fe1&au nps纳米复合物的级联催化反应的活性图。
110.如图7所示,在葡萄糖级联催化的反应中,实施例7得到的fe1@au nps纳米复合物展现出了最高的级联催化活性,其催化葡萄糖的级联活性分别是传统简单堆叠的fe1/au nps和共平面构建的fe1&au nps纳米复合物的9.8和2倍。
111.实施例8:葡萄糖的定性检测
112.催化反应体系为包含不同浓度的葡萄糖(20μl,0mm、0.5mm、1mm、2mm、4mm、5mm、6mm、8mm、9mm、12mm、14mm、16mm)、fe1@au nps(20μl,200μg/ml)、显色剂tmb(20μl,6mm)和ph 7.2缓冲液(140μl,10mm)。在25℃下反应30分钟。
113.图8是本发明实施例8的基于fe1@au nps催化体系的葡萄糖比色传感的定性检测图,如图8所示,观察离心管1-12溶液颜色变化,对照管1中无颜色变化,2-12管蓝色依次加深,证明fe1@au nps具有仿葡萄糖氧化酶活性,可以用于葡萄糖定性检测。
114.实施例9:葡萄糖的定量检测
115.催化反应体系为包含不同浓度的葡萄糖(20μl,0mm、0.5mm、1mm、2mm、4mm、5mm、6mm、8mm、9mm、12mm、14mm、16mm)、fe1@au nps(20μl,200μg/ml)、显色剂tmb(20μl,6mm)和ph 7.2缓冲液(140μl,10mm).在25℃下反应30分钟,利用酶标仪检测其652nm处的吸光值并绘制出葡萄糖标准工作曲线。
116.图9是本发明实施例9基于fe1@au nps催化体系的葡萄糖比色传感的定量检测图,如图9所示,线性范围0-1.6mm,abs.=0.6523c+0.0015(r2=0.995)。
117.实施例10:金属单原子/金属纳米颗粒的纳米复合物在无酶检测葡萄糖中的应用
118.选择性实验:分别取20μl,5mm的葡萄糖及50mm多巴胺、l-半胱氨酸、蔗糖、果糖、抗坏血酸、尿酸和麦芽糖加入到催化反应体系,其中反应体系包含fe1@au nps(20μl,200μg/ml)、显色剂tmb(20μl,6mm)和ph 7.2缓冲液(140μl,10mm)。在25℃下反应30分钟,利用酶标仪检测其652nm处的吸光值。
119.图10是本发明实施例10的fe1@au nps催化剂检测葡萄糖的选择性对比图。如图10所示,从左到右依次为葡萄糖、多巴胺、l-半胱氨酸、蔗糖、果糖、抗坏血酸、尿酸和麦芽糖。在对照组的浓度比葡萄糖浓度高10倍的情况下,葡萄糖的吸光度还远远高于对照组,说明所构建的fe1@au nps检测系统对葡萄糖的具有较高的选择性。
120.综上所述,本发明提供了一种具有级联催化活性的金属单原子/金属纳米颗粒的纳米复合物及其制备与应用,基于金属单原子/金属纳米颗粒的复合物体系的葡萄糖比色传感展现出了较宽的线性范围、低的检测限、较高的催化活性及优异的选择性。这些结果表明,金属单原子/金属纳米颗粒的复合物仿酶催化剂在无酶葡萄糖检测中具有很大的应用前景。
121.以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1