碳纳米管/钴铁类水滑石纳米片复合物的制备方法及其电催化应用与流程
本发明属于新能源材料技术及电催化技术领域,具体涉及碳纳米管/钴铁类水滑石纳米片复合物的制备方法,还包括催化剂在碱性电解水阳极析氧反应中的电催化应用
背景技术:
随着由化石燃料引发的全球气候变暖等环境问题突出,研究人员将大量的精力投入到新能源的开发,以及高效存储与转换当中。而在新能源存储与转换过程中涉及到的析氧反应(oer)进程缓慢,是阻碍燃料电池,水裂解储能系统(oer)、太氧能燃料合成(oer)应用推广中的主要问题之一。在这些能源存储与转换装置中,用于oer的催化剂有贵金属ru、ir及其氧化物。贵金属催化剂因其地球储量小,价格昂贵等因素,限制了其在新能源方面的应用。并且这些贵金属催化剂稳定性差,不能长期使用。因此,研究开发一种便与生产、非贵金属、可循环使用的oer的催化剂成为研究热点。
铁钴镍基的材料包括铁钴镍的氢氧化物、氧化物,具有良好的oer催化活性。其中,钴铁双金属氢氧化物又称为钴铁类水滑石,记为cofe-ldh,是一种二维层状材料,其组成通式可表示为[co1-x2+fex3+(oh)2]x+(an-)x/n·mh2o,由带正电荷的氢氧化物层和与之电荷相平衡的层间阴离子组成。由于钴铁在地球中的储量非常丰富,因此钴铁基的纳米材料,特别是cofe-ldh在能源转换和存储领域呈现出了良好的应用前景。然而实际应用过程中,cofe-ldh催化剂材料还存在比表面积小、导电性差、易聚集和稳定性差等缺点。为了克服以上缺点,研究者将ldh进行剥离成单层或多层的薄片(ldhns),以提高其比表面积和活性位点,同时将一些碳材料如石墨烯(gr)和碳纳米管(cnt)等材料与ldh纳米片复合,提高复合材料的导电性,阻止ldh聚集,改善其性能。碳纳米管,又名巴基管,是一种具有特殊结构(径向尺寸为纳米量级,轴向尺寸为微米量级,管子两端基本上都封口)的一维量子材料。碳纳米管主要由呈六边形排列的碳原子构成数层到数十层的同轴圆管。层与层之间保持固定的距离,约0.34nm,直径一般为2~20nm。碳纳米管具超高的比表面积(~1315m2/g)和优良的导电性,能够大大提高电催化反应中的电荷传递和传质效率。而且羧基化以后的碳纳米管(hcnts)带负电,能与带正电荷的ldh纳米片进行分子级别的静电堆积,可使ldhns中的过渡金属催化中心与导电的sp2杂化碳原子紧密接触,大大缩短电解质的扩散距离。虽然通过静电组装将ldh和hcnts进行复合可以解决ldh材料导电性差和聚集等问题,但其制备方法涉及ldh的剥离、静电组装等问题。
为了简化催化剂的制备方法,提高工业化生产的可执行性,本发明将二价钴和三价铁溶于hcnts的甲酰胺和水的混合溶液中,以稀碱直接滴定,在hcnts基底上原位生长超薄的cofe-ldhns,制得碳纳米管/钴铁类水滑石纳米片复合物(ldhns/hcnts)氧催化剂。目前采用此一步法制备ldhns/hcnts氧催化剂以及该催化剂用于碱性电解水阳极oer的研究还未见报道。
本发明采用的以羧基化的碳纳米管为基底,在甲酰胺和水的混合溶液中原位生长超薄的cofe-ldhns,避免了ldh的剥离步骤,阻止了ldhns的聚集,增加了催化剂的活性位点,降低了oer的过电位,从而提高了其oer电催化性能。该方法所得电催化剂充分发挥了ldhns和hcnts在电催化方面的协同作用,对开发新型析氧反应催化剂具有重要意义。
技术实现要素:
针对目前制备ldh复合物存在的聚集、粒径大、粒径分布范围宽、比表面积小等现有技术的不足以及本领域研究和应用的需求,本发明的目的之一是提供一种碳纳米管/钴铁类水滑石纳米片复合物的制备方法,其特征在于在羧基化的碳纳米管的甲酰胺-水混合溶液中经共沉淀一步法制得,包括以下具体步骤:
取一定量羧基化的碳纳米管,记为hcnts,超声分散于50ml甲酰胺和水的混合溶剂中,使其浓度为0.4~0.8mg/ml,按一定摩尔比加入九水合硝酸铁和六水合硝酸钴,使总金属离子浓度为6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌的条件下,用浓度为0.14mol/l的氢氧化钠的甲酰胺和水混合溶液缓慢滴定至反应液ph为8.5~9.5,将反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts。
其中九水合硝酸铁和六水合硝酸钴的摩尔比为1:2;甲酰胺和水的混合溶剂或溶液中甲酰胺的体积百分比为40~100%;所得钴铁类水滑石/碳纳米管纳米复合物中钴铁类水滑石纳米片的尺寸小于100nm,厚度小于2nm,且垂直生长于碳纳米管上。
本发明的目的之二是提供一种一步法制备得到的碳纳米管/钴铁类水滑石纳米片复合物对碱性电解水阳极析氧反应的催化应用。
本发明以羧基化的碳纳米管为基底,在甲酰胺和水的混合溶液中原位生长超薄的cofe-ldhns,避免了ldh的剥离步骤,增加了催化剂的活性位点,降低了oer的过电位,从而提高了其电催化性能。
与现有技术相比,本发明具有以下主要优点和有益效果:
1)本发明所述的一步当制备碳纳米管/钴铁类水滑石纳米片复合物的方法,不但解决了ldhns聚集、导电性差的问题,而且避免了ldh的剥离步骤,增加了ldhns与cnt的紧密接触,从而提高了催化剂的导电性和活性催化位点,充分发挥了ldhns和cnt在电催化方面的优异性能;
2)本发明所述制备方法所得的催化剂为非贵金属复合材料,所用原料易于购买和制备,资源丰富且价格较低,易于操作,便于大规模生产;具有较好的oer活性,良好的稳定性,在0.1mol/lkoh电解液中施以恒电压,经历9h催化剂的电流密度依然保持91%,较目前研究报道的非贵金属/非金属催化剂的催化活性具有显著优势。
附图说明:
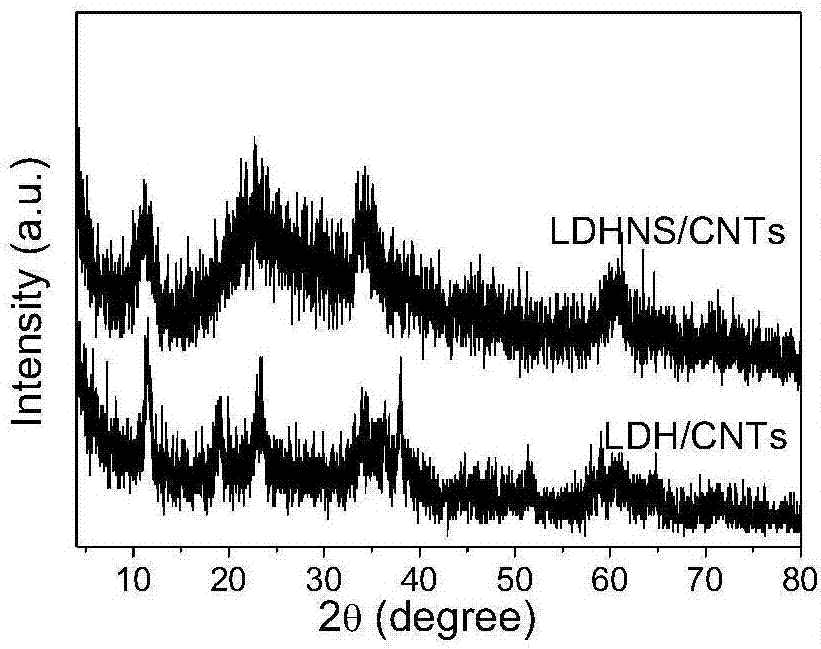
图1为实施例2所得ldhns/hcnts复合物和对比例2所得ldh/hcnts的xrd图谱。
图2为实施例2所得ldhns/hcnts复合物的tem图。
图3为实施例2所得ldhns/hcnts复合物、对比例1所得ldh、对比例2所得ldh/hcnts复合物以及ruo2修饰玻碳电极的oer线性伏安曲线图。
图4为实图2中所得的各条线性伏安扫描曲线对应的tafel曲线。
图5为实施例2所得ldhns/hcnts复合物在10ma/cm2对应的电位下电流衰减曲线图。
图6为实施例2所得ldhns/hcnts复合物和对比例2所得ldh/hcnts通过不同扫速得出的双电层电容cdl。
具体实施方式:
为进一步理解本发明,下面结合附图和实施例对本发明作进一步说明,但并不以任何方式限制本发明。
实施例1:
取一定量的羧基化的碳纳米管超声分散于50ml含50%甲酰胺的水溶液中,使其浓度为0.4mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts-0.4。
实施例2:
取一定量的羧基化的碳纳米管超声分散于50ml含50%甲酰胺的水溶液中,使其浓度为0.6mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts-0.6。
实施例3:
取一定量的羧基化的碳纳米管超声分散于50ml含50%甲酰胺的水溶液中,使其浓度为0.8mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts-0.8。
实施例4:
取一定量的羧基化的碳纳米管超声分散于50ml含60%甲酰胺的水溶液中,使其浓度为0.6mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts-60。
实施例5:
取一定量的羧基化的碳纳米管超声分散于50ml含80%甲酰胺的水溶液中,使其浓度为0.6mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldhns/hcnts-80。
对比例1:
向50ml含50%甲酰胺的水溶液中按2:1的摩尔比加入六水合硝酸钴和九水合硝酸铁,使其浓度为6mmol/l,搅拌1h使其完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的含50%甲酰胺的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石纳米片,记为ldhns。
对比例2:
取一定量的羧基化的碳纳米管超声分散于50ml水中,使其浓度为0.6mg/ml,按2:1的摩尔比向其中加入六水合硝酸钴和九水合硝酸铁,使总金属离子浓度6mmol/l,搅拌1h使金属盐完全溶解,在剧烈搅拌条件下,用0.14mol/l的氢氧化钠的水溶液缓慢滴定至反应液的ph为8.5~9.5,反应液4000rpm离心分离后,分别用去离子水和乙醇洗涤3次,即得钴铁类水滑石/碳纳米管纳米复合物,记为ldh/hcnts。
图1为实施例2所得ldhns/hcnts复合物和对比例2所得ldh/hcnts的xrd图谱。如图所示,ldhns/hcnts和ldh/hcnts都出现了ldh-no3的特征峰,分别为003(11.5°),006(18.8°),012(34.2o),说明了在两种复合物中都生成了nife-ldh层状材料,另外xrd图谱中都在24°左右出现了cnt的衍射峰。但两者之间又有明显的区别,由于在混合溶液中,含有的甲酰胺发挥了其溶涨和抑制作用,复合物ldhns/hcnts中的ldhns呈现为超薄纳米片,而且不能平行堆积,而是以垂直的方式原位生长在碳纳米管表面,因而导致了水滑石纳米片的各特征衍射峰明显变宽,表明其超薄的特性,这一特性有利于其发挥oer催化活性。
图2为实施例2所得ldhns/hcnts纳米复合物的透射电镜图。从图中可以看出,由于反应介质中甲酰胺的存在,原位生长在羧基化碳纳米管上ldhns呈现出了超薄特性,纳米片的尺寸小于100nm,其厚度小于2mn,而且垂直生长于碳纳米管表面。我们推断:羧基化的碳纳米管为基底,其表面的羧基官能团将金属种类co2+和fe3+吸附固定后,随着碱液的缓慢滴定加入,在碳纳米管表面原位生长了超薄的ldhns。由于甲酰胺的溶涨和抑制作用,超薄的ldhns无法平行堆积,从而以垂直的方式在碳纳米管表面形成了超薄的纳米片,最终导致形成了ldhns/hcnts复合物。
实施例6:
分别将20mg实施例2、对比例1和对比例2所得的催化剂分散于200μl乙醇以及20μl0.5%的nafion溶液中,超声混匀溶液后,取3μl浆液滴涂于玻碳电极上,待其完全干燥后压片在chi660d电化学工作站上测定其oer电催化性能;
上述电催化性能测试均以饱和hg/hgo电极为参比电极,pt电极为对电极,扫速为10mv/s,电解液为0.1mkoh。tafel斜率可由e=a+blogj计算出。
其中e为超电势,j为电流密度,a和b分别为常数,其中b为tafel斜率。
实施例7:
将20mg实施例2所得ldhns/hcnts和对比例2所得ldh/hcnts催化剂分别分散于200μl乙醇以及20μl0.5%的nafion溶液中,超声混匀溶液后,取3μl浆液滴涂于玻碳电极上,待其完全干燥后在chi660d电化学工作站上测定其cv曲线。以扫速为横坐标,0.25v对应的cv电位差的绝对值为纵坐标,通过斜率得出双电层电容cdl;
上述电催化性能测试均以饱和hg/hgo电极为参比电极,pt电极为对电极,扫面方向为由负电位向正电位扫描,电解液为0.1mkoh。
图3为实施例2所得ldhns/hcnts复合物、对比例1所得ldh、对比例2所得ldh/hcnts以及ruo2修饰玻碳电极的oer线性伏安曲线图。如图所示,ldhns/hcnts修饰电极的oer起始过电位为180mv,明显低于ldh的340mv和ruo2的330mv,而ldh/hcnts催化剂对应的起始过电位相比于ldh降至330mv。同时,当电流密度为10ma/cm2时,ldhns/hcnts、ldh/hcnts、ruo2和ldh对应的过电位分别约为250、420、420和520mv。明显可以看出,在羧基化的碳纳米管基底上原位生成cofe-ldhns后,有效地降低了其过电位,这是主要是由于复合hcnts与超薄ldhns复合后,ldhns并未发生聚集,充分暴露了其催化活性位点,提高了催化剂的通透性和导电能力,有利于氧分子的逸出和电子的传递,大大改善了催化剂的oer催化性能。
图4为图3中各条曲线通过计算得出的tafel斜率。如图所示,在各自的极化区间,ldh、ldh/hcnts、ruo2和ldhns/hcnts的tafel斜率分别为105mv/dec、79mv/dec、73mv/dec和46mv/dec。低的tafel斜率表明高的电子迁移速率。ldh具有较大tafel斜率,在复合羧基化碳纳米管以后,ldh/hcnts的tafel斜率均有所降低,在含有甲酰胺的介质中,ldhns原位生长在hcnts表面,因此ldhns/hcnts呈现出了最低的tafel斜率,甚至低于贵金属ruo2的tafel斜率,表明ldhns/hcnts具有最快的电子转移速率。
图5为实施例2所得ldhns/hcnts复合物修饰玻碳电极于10ma/cm2下的恒电压测试图。如图所示,经过9h的连续oer测试过程,ldhns/hcnts的oer电流密度仅发生了小于8%的衰减,这主要是由于氧气气泡的持续析出,不断冲击电极表面ldhns/hcnts催化剂而造成的微量脱落,由此可见ldhns/hcnts修电极在碱性溶液中表现出了良好oer催化稳定性,具有较长的使用寿命。
图6为实施例2所得ldhns/hcnts复合物、对比例2所得ldh/hcnts的双电层电容cdl。如图所示,与在水介质中合成的ldh/hcnts相比,ldhns/hcnts催化剂的cdl增大了0.4mf/cm2,说明在含有甲酰胺的介质中合成的ldhns/hcnts相比于水中合成的ldh/hcnts具有更大的有效活性表面积,此结果与透射电镜和lsv结果相一致。高的有效电活性面积进一步阐明了ldhns/hcnts良好oer的原因。
- 还没有人留言评论。精彩留言会获得点赞!