一种高效定量检测C反应蛋白的免疫学试剂盒的制作方法
本发明涉及生物检测
技术领域:
,具体涉及一种高效定量检测C反应蛋白的免疫学试剂盒。
背景技术:
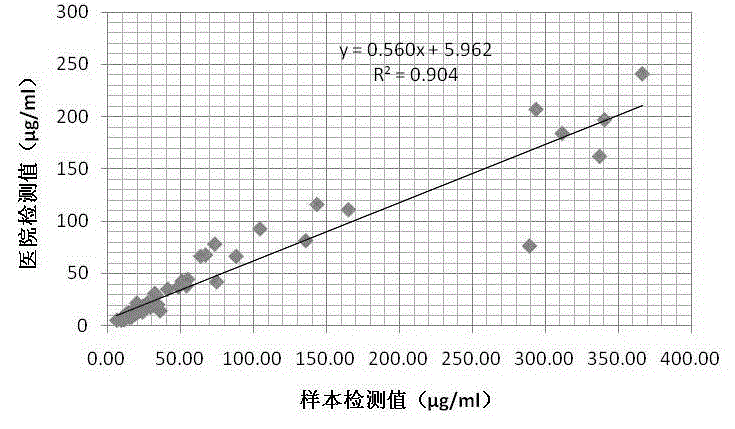
:C反应蛋白(C-reactiveprotein)是一种能与肺炎链球菌C多糖体反应形成复合物的急性时相反应蛋白,半衰期19小时;血清CRP由肝脏合成,白细胞介素1β、6以及肿瘤坏死因子是其合成的最重要的调节因子;CRP的分子量为105500,由含有五个相同的未糖基化的多肽亚单位组成,每个亚单位含有187个氨基酸,这些亚单位间通过非共价键连结成环状的五聚体,并有一个链间二硫键。1930年,Tillett和Francis首次在急性大叶性肺炎患者的血清中发现一种能在Ca2+存在时与肺炎球菌细胞壁中的C-多糖发生特异性沉淀反应的物质。1941年,Avery等测知它是一种蛋白质,故称为C反应蛋白(CRP)。1944年,Jones将其作为临床风湿热诊断标准的次要指标之一。后来,人们在非感染性疾病和感染性疾病患者的急性期血清中都测到了CRP,于是人们认为,CRP是组织损伤的一种非特异性反应。进一步研究发现:病毒或细菌感染、梗塞、免疫复合物沉积等因素都可导致组织损伤。在组织损伤的急性期,肝脏合成的一些血浆蛋白显著增加,这些蛋白质通称为急性时相蛋白,其中CRP是急性时相蛋白中变化最显著的一种。CRP在正常人血清中其含量极微;在组织受到损伤、炎症、感染或肿瘤破坏时CRP可以在数小时内急剧上升,可增高数倍或数百倍,2~3天达峰值,待病情改善时逐渐下降,恢复正常。CRP被广泛应用于临床疾病的早期诊断及鉴别诊断,其升高可见于:1、组织损伤、感染、肿瘤、心肌梗塞及一系列急慢性炎症性疾病,如风湿性关节炎、全身性血管炎、多肌痛风湿病;2、术后感染及并发症的指标:手术后病人CRP升高,术后7~10天CRP水平应下降,如CRP不降低或再次升高,提示可能并发感染或血栓栓塞;3、可作为细菌性感染和病毒性感染的鉴别诊断:大多数细菌性感染会引起患者血清CRP升高,而病毒性感染则多数不升高。CRP的检测在八十年代以前作为炎症和组织损伤的非特异性标志物大量应用于临床。但由于过去CRP的检测方法较为落后,假阳性和假阴性很高,影响了它在临床上的价值,而逐渐被临床所忽视。近年来,由于检测技术的更新,测定CRP的快速、简便和可靠的方法已迅速建立。使CRP在临床应用领域大大增加。其在医学上的价值正得到广泛验正和承认。目前临床上用于检测CRP的方法包括普通ELISA、免疫比浊法和胶体金法。普通ELISA法具有较高的灵敏度,但操作繁琐,易出现假阳性和假阴性。免疫比浊法有较高的灵敏度,操作简易,但线性较差。胶体金法灵敏度高,操作简易,但对定量检测的要求高,不适合用于精确定量。目前的普通ELISA试剂盒的检测范围在3~350mg/L,有必要继续优化检测灵敏度,开发能检测到更低含量CRP的免疫学方法和相应试剂盒。技术实现要素:本发明为了克服现有技术检测C反应蛋白存在灵敏性低、易出现假阳性的缺陷,提供一种高效定量检测C反应蛋白的免疫学试剂盒。该试剂盒与传统的试剂盒相比具有特异性强、灵敏度高、检测范围更低、线性条件好等优点。为了实现上述目的,本发明是通过以下方案予以实现的。一种高效定量检测CRP的免疫学试剂盒,该试剂盒以抗CRP的多克隆抗体和抗CRP的单克隆抗体混合在一起作为联合捕获抗体,以抗CRP的单克隆抗体或抗CRP的多克隆抗体作为检测抗体,通过抗原抗体反应检测CRP。现有技术中的免疫学试剂盒在检测CRP时,捕获抗体都是仅使用一种类型的抗体,要么是单克隆抗体,要么是多克隆抗体;而本发明的试剂盒将抗CRP的单克隆抗体与抗CRP的多克隆抗体混合制备成捕获抗体,以抗CRP的单克隆抗体作为检测抗体,这种免疫学试剂盒的检测敏感性和特异性显著提高。敏感性和特异性显著提高的原因在于,联合捕获抗体在不同的溶液环境下增加了抗原抗体的结合表位,减少了假阴性,但有可能增加假阳性,所以我们在选择检测抗体时采用芯片法来作交叉实验,筛选到的检测抗体特异性十分强,该检测抗体与39种抗原蛋白无交叉反应。从而弥补了联合捕获抗体可能导致的假阳性。本发明用作检测抗体的单克隆抗体和用作联合捕获抗体的单克隆抗体均来自于美国瑞博奥生物科技有限公司。美国瑞博奥生物科技有限公司将小鼠脾脏与骨髓瘤细胞SP2/0融合后得到2株杂交瘤细胞株,分别命名为H16740(该杂交瘤细胞分泌的抗CRP单克隆抗体的货号119-16740)和H14815(该杂交瘤细胞分泌的抗CRP单克隆抗体的货号为119-14815)。作为检测抗体的抗CRP的单克隆抗体为货号为119-16740的抗体;作为联合捕获抗体的单克隆抗体为货号为119-14815的抗体。本发明在前期筛选检测抗体时,也用到了其他类型的抗体,如美国瑞博奥生物科技有限公司,货号为119-16718的抗CRP单克隆抗体,但是该抗体采用芯片法来作交叉实验时,其特异性并不好。优选地,本发明所述抗CRP的多克隆抗体是根据以下方法制备的:将SEQIDNO:1所示基因通过原核表达系统获得的蛋白作为CRP抗原标准品免疫SPF级新西兰兔,得到含有抗CRP多抗的兔血清,先用硫酸铵沉淀法从兔血清中初步纯化免疫球蛋白IgG,再用ProteinG/A亲和柱进一步纯化,得到抗CRP多抗。所述的CRP抗原标准品是采用原核表达系统表达的蛋白,该蛋白可溶性程度高,空间构象更接近天然抗原。优选地,所述试剂盒为检测CRP的酶联免疫试剂盒,该试剂盒包括包被联合捕获抗体的微孔板,浓缩洗涤液,重组人CRP蛋白的标准品抗原,待测样本浓缩稀释液,稀释抗体和标记酶的浓缩稀释液,生物素标记的检测抗体,标记酶溶液,TMB底物,终止液;所述捕获抗体是抗CRP多克隆抗体和抗CRP单克隆抗体混合在一起的联合捕获抗体;检测抗体为抗CRP的单克隆抗体或抗CRP的多克隆抗体。优选地,检测CRP的酶联免疫试剂盒中,所述联合捕获抗体的包被浓度是每种抗体0.3~0.5ug/孔,所述待测血清的稀释倍数是1:10,所述检测抗体的浓度为0.1mg/L,所述生物素标记的检测抗体的稀释浓度是1:5000。优选地,所述试剂盒为检测CRP的胶体金试剂盒,试剂盒包括至少一个试纸条,试纸条包括样品垫,标记垫,硝酸纤维素膜,吸水纸,标记垫上包被胶体金标记的抗CRP检测抗体,硝酸纤维素膜包括包被有抗鼠IgG二抗的质控区和包被有联合捕获抗体的检测区。更优选地,所述联合捕获抗体的包被浓度分别为0.5~1mg/ml,用量按膜包被液量为20~25ug/30cm2;所述检测抗体的包被浓度为0.2~1mg/ml,用量按膜包被液量为0.8ug/cm2。优选地,所述试剂盒为检测CRP的时间分辨荧光免疫层析试剂盒,试剂盒包括多个检测试纸条,所述试纸条包括样品垫、结合物释放垫、硝酸纤维素膜和吸水纸;所述结合物释放垫中含过量的抗CRP检测抗体和荧光微球的复合物;硝酸纤维素膜上有检测线(又称T线)和对照线(又称C线),检测线含定量的联合捕获抗体,对照线含定量的抗鼠IgG二抗。本发明所述时间分辨荧光免疫层析试剂盒的检测原理是双抗夹心法,将直径范围0.01~1um的胶乳微球与抗CRP单抗和各类不同的荧光素共价结合,利用荧光素在激光发作用下可以发射荧光,当此荧光胶乳标记的CRP单抗与样本中的抗原结合形成复合物,在层析作用下移至包被膜的检测区,在包被膜的检测区包被有能与CRP抗原结合的联合捕获抗体。复合物聚积在包被膜的T线区,受到光源激发释发出相应波长的发射光,通过荧光检测系统捕捉的光信号转化为数字信号,从而可用于准确定量的快速免疫检测中与现有技术相比,本发明具有以下有益效果:本发明所述的高效定量检测C反应蛋白(CRP)的酶联免疫试剂盒,采用抗CRP的多克隆抗体和抗CRP的单克隆抗体两种抗体联合作为捕获抗体,以特殊的抗CRP的单克隆抗体作为检测抗体,这种试剂盒具有特异性强、检测范围更低、灵敏度高,灵敏度可达200pg/ml(对照组检测值<效价检测值的一半),而常规CRP检测试剂盒检测范围的最低检测值是3ug/ml。附图说明图1.抗CRP检测单抗交叉反应测试;A.蛋白芯片检测结果显示该单抗和其它39个靶标无交叉反应;B.交叉反应测试40个靶标列表。图2.本发明所述的试剂盒的样本检测值与医院检测值的比较图。图3.时间分辨荧光侧向层析试纸条的结构。具体实施方式下面通过说明书附图和具体实施例对本发明进一步具体描述,下述所使用的实验方法若无特殊说明,均为本
技术领域:
现有常规的方法,所使用的配料或材料,如无特殊说明,均为通过商业途径可得到的配料或材料。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以作出若干改进,这些改进也应视为本发明的保护范围。实施例1S1.CRP基因的分泌表达:将如SEQIDNO:1所示的CRP基因序列插入pET28a载体,经测序成功后转入大肠杆菌,表达产物经SDS-PADG验证得到单一条带,经WesternBlotting验证分泌表达产物与抗CRP单抗特异结合。S2.抗CRP多抗的制备、纯化及鉴定:用S1所述的大肠杆菌表达的CRP蛋白免疫SPF级新西兰兔(广东省实验动物中心),免疫三次,每次间隔半个月。最后一次加强免疫三天后,通过心脏采血,血清析出后,先用硫酸铵沉淀法从兔血清中初步纯化免疫球蛋白IgG,再用ProteinG/A亲和柱进一步纯化抗CRP多抗,SDS-PAGE和WesternBlotting鉴定纯化的抗体。S3.抗CRP单抗:本发明用作检测抗体的单克隆抗体和用作联合捕获抗体的单克隆抗体均来自于美国瑞博奥生物科技有限公司。美国瑞博奥生物科技有限公司将小鼠脾脏细胞与骨髓瘤细胞SP2/0融合后得到2株杂交瘤细胞株,分别命名为H16740(该杂交瘤细胞分泌的抗CRP单克隆抗体的货号119-16740)和H14815(该杂交瘤细胞分泌的抗CRP单克隆抗体的货号为119-14815)。作为检测抗体的抗CRP的单克隆抗体为货号为119-16740的抗体;作为联合捕获抗体的单克隆抗体为货号为119-14815的抗体。本发明在前期筛选检测抗体时,也用到了其他类型的抗体,如美国瑞博奥生物科技有限公司,货号为119-16718的抗CRP单克隆抗体,但是该抗体采用芯片法来作交叉实验时,其特异性并不好,会出现交叉反应。实施例2一、以实施例1所述的联合捕获抗体和检测抗体建立一种检测CRP的酶联免疫试剂盒(ELISA),试剂盒的组成如下:1.ELISA酶标板:采用吸附性能好,空白值低,批次稳定的聚苯乙烯板包被捕获抗体,预先用封闭液处理。2.联合捕获抗体:采用实施例1制备的多克隆抗体和筛选的单克隆抗体作为联合捕获抗体,每个抗体的包被浓度每孔在0.3~0.5ug之间。3.检测抗体:将实施例1筛选的检测抗体进行生物素化,检测抗体的最佳稀释浓度为0.1mg/L。4.洗涤液:含0.1%Tween-20的20X浓缩洗涤液。5.标准品:含重组人类CRP蛋白的标准品抗原干粉。6.稀释液:2瓶用于稀释样本的15ml5X浓缩稀释液D,1瓶用于稀释抗体和HRP-链亲和素的15ml5X浓缩稀释液B。其中,1X浓缩稀释液D的组成为:加入0.5%BSA,0.1~1%的还原剂的PBS缓冲液;1X浓缩稀释液B的组成为:加入0.5%BSA,0.05%的吐温-20的PBS缓冲液。7.200µl300X浓缩HRP-链亲和素溶液。8.底物:12mlTMB溶液。9.终止液:8ml浓度为0.2M的硫酸溶液。二、所述ELISA试剂盒的操作步骤1.将所有试剂放置室温条件(18~25℃)下平衡30分钟,标准品和样本都设置至少一个重复。2.加入100μl稀释好的标准品及样品,盖上封板膜室温条件下孵育2.5个小时或者4℃过夜,放置于洗板机洗涤并倒转微孔板在纸巾上吸干净。3.加入100μl稀释好的生物素化的检测抗体,室温条件下孵育1个小时。4.放置于洗板机洗涤并倒转微孔板在纸巾上吸干净。5.加入100μl稀释好的HRP-链亲和素,孵育45分钟。6.重复4的步骤。7.加入100μlTMB反应30分钟,再加入50μl终止液终止反应,于酶标仪450nm读数。8.根据检测结果得出折线图公式,计算待测血清的CRP含量。三、所述ELISA试剂盒的质量分析1.ELISA试剂盒的灵敏度:参照实施例1中的操作步骤,分别用联合抗体及单抗包被,在微孔板中依次加入1800、1200、900、600、200、66.67、22.22、7.41pg/ml的CRP抗原蛋白,设两个重复求平均值,所得检测结果如下,可知采用联合抗体包被其检测灵敏度可达200pg/ml(对照组检测值<效价检测值的一半),而采用单抗包被的灵敏度只有600pg/ml,见表1。常规CRP检测试剂盒检测范围的最低检测值是3ug/ml。表1抗原(pg/ml)联合抗体包被单抗包被18001.0470.91512000.7640.4789000.6440.3436000.4610.2142000.1930.09866.670.0870.08122.220.0670.06600.0680.0672.ELISA试剂盒检测抗体的特异性:采用RayBiotech公司出品的人类蛋白芯片,加入抗CRP检测单抗,所得结果如图1所示,可知抗体与其它抗原蛋白无交叉反应。四、所述ELISA试剂盒的应用与改良CRP定量检测试剂盒针对同一批临床样本(59例病人血清)共做了两次检测,其中第一次只采用抗CRP单克隆抗体作为捕获抗体包板,检测结果如下表2所示。表2OD450值样本检测值(ug/ml)医院检测值(ug/ml)1.0148.398.842.3121.351111.23310.5812.42.11519.466.31.0548.7910.22.43222.571621.17910.0411.21.48613.1114.12.25920.841161.19410.197.942.22420.4981.30.8176.425.11.54313.6813.41.69315.1819.32.45522.82072.32321.481841.80316.28202.1820.0541.90.988.057.292.60724.322411.76315.88221.25510.88.262.64424.691970.9798.048.181.17610.0110.20.9798.048.841.44612.7117.41.54913.7415.21.1439.688.71.56213.8714.11.37912.04131.3751221.61.44112.6614.61.9617.8534.81.21810.4311.21.97317.9844.31.2210.4512.81.0738.9812.21.63514.629.21.23510.6131.71315.3818.22.22220.4766.52.22520.592.60.6975.225.142.23620.61781.79416.1917.71.9617.8542.51.80416.29381.37712.0210.91.82416.4918.31.83716.6230.82.28121.0667.50.8266.517.371.0098.347.230.7035.285.591.62514.511.31.39312.1812.32.26620.9176.22.00318.2836.9从上表2中可以看出:大多数检测值与医院检测值没有相关性。于是针对第一次的结果对实验进行了调整,采用联合抗体(即实施例1筛选的抗CRP的多克隆抗体和抗CRP的单克隆抗体混合在一起作为联合捕获抗体)的方式进行包板,这种试剂盒对59例病人血清的检测结果如下表3和图2所示。表3OD450值样本检测值(ug/ml)医院检测值(ug/ml)0.58516.368.841.135164.741110.57215.912.40.90487.7166.30.51213.8310.21.151336.971620.64818.6511.21.03435.6214.11.037143.111160.53414.587.941135.4981.30.368.955.10.70820.9313.40.95431.619.31.0542932071.095311.281841.00233.97201.06374.3241.90.43811.47.291.053366.232410.85827.16220.5715.838.261.158340.291970.46112.148.180.5816.1810.20.4712.448.840.7422.217.40.64618.5715.20.48512.938.70.76423.1714.10.77623.66130.67319.5921.60.72321.5214.61.12840.7834.80.53314.5511.20.8654.4944.30.61417.412.80.51513.9412.20.97832.7729.20.69120.27130.78924.218.20.71363.3866.50.832104.0992.60.260.5965.140.63873.11780.929.0517.70.81550.5842.50.85153.7380.53914.7510.90.77523.6218.30.96131.9430.70.74166.7167.50.3779.487.3743211.217.230.42510.985.590.47312.5411.30.63618.212.31.757288.8976.20.78748.2336.9由表3和图2的结果可以看出,经调整后大部分检测值都在标准曲线范围内,相关系数是0.904,匹配度高。图2采用样本检测值作为X轴,医院检测值作为Y轴绘制散点图,生成趋势线和公式,并得R平方值为0.904,结果表明,用联合抗体的方式,检测的准确度更高。实施例3以实施例1筛选的联合捕获抗体和检测抗体建立一种检测CRP的胶体金免疫层析试剂盒:试剂盒包括多个检测试纸条,所述试纸条由样品垫,胶体金标记垫,硝酸纤维素膜(NC膜)和吸水纸组成(见图3),所述NC膜包被有检测区和质控区,检测区包被联合捕获抗体,质控区包被抗鼠IgG二抗;所述胶体金标记垫包被检测抗体;所述胶体金标记垫的制备过程为,以氯金酸-柠檬酸三钠还原法制备活化的胶体金溶液,将检测抗体按照100~500ug检测抗体蛋白每100ul胶体金溶液的比例加入到胶体金溶液中,搅拌室温反应2小时,离心洗涤2次,沉淀用胶体金溶液复溶至50ml,按0.8ug/cm2的用量涂覆在胶体金标记垫上,室温干燥备用。硝酸纤维素膜的制备过程为:将联合捕获抗体(抗CRP的单抗和多抗)和抗鼠IgG用包被液调整至浓度为0.5至1mg/ml,将抗鼠IgG用包被缓冲液PBS调整至浓度为0.8mg/ml,按膜包被液量为20ug/30cm2至25ug/30cm2的用量将联合捕获抗体喷到NC膜的检测区,分别按膜包被液量为25ug/30cm2至30ug/27cm2的用量将抗鼠IgG喷到质控区,过夜冷冻干燥,加入干燥剂封存备用。在底板上依次相互搭接地粘贴样品垫,胶体金标记垫,NC膜和吸水纸,按照要求切割成适当宽度的试纸条形成试剂盒。实施例4以实施例1所述的联合捕获抗体和检测抗体建立一种检测CRP的时间分辨荧光免疫层析试剂盒,所述试剂盒包括多个检测试纸条,所述试纸条由样品垫,荧光微球包被的释放垫,硝酸纤维素膜(NC膜)和吸水纸组成(见图3)。其中,样品垫用于加样(血清或全血);释放垫中含过量的抗CRP检测抗体和荧光微球的复合物;NC膜上有两道线:检测线,又称T线,含定量的联合捕获抗体;对照线,又称C线,含定量的抗鼠IgG二抗。本试剂盒采用时间分辨荧光微球作为标记载体,将检测抗体标记于荧光微球上,利用侧向层析技术,将标记抗体的微球干燥于释放垫上,同时在NC膜上喷制相应的联合捕获抗体,利用双抗体夹心法检测血清或全血中的CRP。当将含有待测抗原(CRP)的样品滴在加样区,待测样品中的CRP与结合垫中的荧光纳米微球标记的抗CRP检测抗体结合并通过毛细作用向前层析,当达到检测区后,与检测线上固定的联合捕获抗体结合,形成微粒-抗体-抗原的抗体夹心复合物并被固定在检测线上,而多余的荧光微球标记物继续向前层析,与固定在质控线二抗结合。反应结束后,用紫外光源(365nm)对检测区扫描检测,检测线和质控线上荧光纳米微球发出高强度的荧光(615nm),且衰变时间也较长。利用延缓测量时间,待样品基质中自然发生的短寿命荧光(1~10ns)全部衰变后,再测量微球的特异性激发荧光,这样就可以完全排除特异本底荧光的干扰。通过检测线和质控线荧光强度的强弱及其比值,即可分析出样品中待测物的浓度。SEQUENCELISTING<110>广州瑞博奥生物科技有限公司<120>一种高效定量检测C反应蛋白的免疫学试剂盒<130><160>1<170>PatentInversion3.3<210>1<211>675<212>DNA<213>CRP基因序列<400>1atggagaagctgttgtgtttcttggtcttgaccagcctctctcatgcttttggccagaca60gacatgtcgaggaaggcttttgtgtttcccaaagagtcggatacttcctatgtatccctc120aaagcaccgttaacgaagcctctcaaagccttcactgtgtgcctccacttctacacggaa180ctgtcctcgacccgtgggtacagtattttctcgtatgccaccaagagacaagacaatgag240attctcatattttggtctaaggatataggatacagttttacagtgggtgggtctgaaata300ttattcgaggttcctgaagtcacagtagctccagtacacatttgtacaagctgggagtcc360gcctcagggatcgtggagttctgggtagatgggaagcccagggtgaggaagagtctgaag420aagggatacactgtgggggcagaagcaagcatcatcttggggcaggagcaggattccttc480ggtgggaactttgaaggaagccagtccctggtgggagacattggaaatgtgaacatgtgg540gactttgtgctgtcaccagatgagattaacaccatctatcttggcgggcccttcagtcct600aatgtcctgaactggcgggcactgaagtatgaagtgcaaggcgaagtgttcaccaaaccc660cagctgtggccctga675当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1