检测宫颈中的癌变的方法与流程
描述
发明领域
本发明涉及检测宫颈中的癌变的方法。更具体地说,本发明涉及诊断宫颈癌的一些程序,其整合或替代细胞学的作用领域与分子生物学的作用领域,并且提供用于hpv诱导的宫颈病变的诊断、预后和管理的系统,其采用非常灵敏且特异的分析方法,如蛋白印迹和三明治elisa,以便检测朝肿瘤性病变的转化已变得不可逆的那些情况。
发明背景
人乳头瘤病毒(hpv)的感染和癌症之间的联系激发了研究者的持续兴趣。hpv感染了鳞状上皮的基底细胞并且诱导良性病变的形成和/或在某些情况下诱导侵略性恶性肿瘤的形成。hpv病毒颗粒由蛋白外壳(衣壳)围绕编码区和非编码区中有组织的环状双链dna组成。在编码区中,已鉴定了八个早期开放阅读框(orf)(e1-e8)和两个晚期orf(l1、l2)。早期orf编码参与以下的蛋白:增殖期间病毒dna的复制、病毒基因表达的调控(e2)、病毒的组装(e4)、病毒的永生化和转化(e6和e7-只有处于高风险的hpv时)。只有在细胞分化之后,晚期orf才被激活并编码病毒衣壳蛋白(l1和l2)。启动子、增强子和其它调控元件位于非编码区的上游调控区(urr)。
所有的hpv类型仅在角质形成细胞(或产生角蛋白的上皮细胞)中发育并繁殖,所述角质形成细胞的分化对于病毒的发育是关键的。当通过上皮层的损伤时,hpv到达并感染位于上皮基底层的角质形成细胞干细胞。在这里,病毒利用细胞的复制机构开始它的复制:其将其自身基因组繁殖若干次,同时保持低病毒负荷(多至50-300拷贝)。当基底的细胞增殖并朝上皮的外层移动时,病毒也同时移动,并持续繁殖,而不进一步扩增其基因组,以便逃脱免疫系统的检测。当宿主的角质形成细胞到达其分化的s期(角质化)时,hpv将其基因组复制多至约1000个拷贝。事实上,在该阶段,病毒释放e6和e7蛋白,这刺激细胞传代至s期(kadajam等人,papillomavirusdnareplication-frominitiationtogenomicinstability.virology.2009feb.20;384(2):360-8)。最后,当角质形成细胞到达表面上皮并死亡时,重新包装为衣壳的病毒基因组离开细胞。
在工业化国家,多亏了pap试验的宣传以及特别是有组织的筛选程序,宫颈癌是一种被警惕控制的疾病。事实上,这是可以通过对侵袭前病变(宫颈上皮内瘤变,cin)进行早期检测和处理而进行预防的几种肿瘤疾病之一。通过对取自宫颈的少量细胞进行细胞学检查,确定鳞状上皮中异常(sil,鳞状上皮内病变)的存在是可能的,将鳞状上皮中的异常分为asc-us(未明确意义的不典型鳞状细胞)、asc-h(不典型鳞状细胞-不排除hsil)、lsil(低度鳞状上皮内病变)、hsil(高度鳞状上皮内病变)以及最后是″恶性上皮肿瘤″(这时癌性细胞已经存在)。预计,在35-65岁的年龄组中每三年进行pap试验筛选可以将侵略性癌症的风险降低90%(iarcworkinggroupontheevaluationofcancerpreventivestrategies.iarchandbooksofcancerpreventionvol.10.cervixcancerscreeninglyon:iarcpress,2005)。
在过去几十年,hpv已被公认为宫颈癌的必要不充分原因(iarcworkinggroup2005,loc.cit)。只有被高风险类型的hpv持续感染才可以引起癌症(schiffmanm等人lancet.2007;370∶890-907)。国际癌症研究署(i.a.r.c.)最近确认了关于一些类型的hpv的致癌性的声明(straifka,等人,onbehalfofthewhointernationalagencyforresearchoncancermonographworkinggroup.lancetoncol.2009;10:321-322),并且鉴定了12种高风险类型加一种可疑类型,而12种其它类型与肿瘤具有不确定的关系。这种疾病自然史的知识的重要进步迅速导致引入两种新的预防工具:预防感染本身的疫苗以及检测高致癌风险的hpv菌株的dna测试(hr-hpvdna检测),以鉴定具有侵袭前病变或侵略性病变的女性或者处于发展侵袭前病变或侵略性病变的风险的女性。在宫颈的筛选中,已证明hr-hpvdna检测比细胞学更灵敏(arbynj.等人,vaccine.2006;24suppl3:s3-78-89;cuzickj.等人.intjcancer.2006;119:1095-1101)。
然而,致瘤性转化是高风险hpv感染的罕见并发症,在大多数情况下,其为瞬时事件。而且,已显示,也与hpv感染有关的低度病变(cin1,其与pap试验中的lsil相对应)不能被认为是真实的侵袭前病变,因为在大多数情况下,它们自发地消退(schiffmanm.等人,lancet.2007;370∶890-907)。因为该原因,因此,hr-hpvdna检测具有低特异性(cuzickj.等人,2006,loc.cit.)。
可随机控制的试验显示hr-hpvdna检测在降低宫颈癌的死亡率和发生率中的功效(sankarana-rayananr.等人,nengljmed.2009;360∶1385-94;bulkmansnw.等人.lancet.2007;370:1764-7)。这些研究的结果激发在意大利构建大型可论证试验,使用hr-hpvdna检测作为初步的筛选分析,随后对阳性情况进行细胞学检查(confortinim.等人,jmedscreen.2010;17:79-86)。应注意到,不仅cin1病变可消退,而且cin2和cin3(其与pap试验中的hsil对应)通常消退,尤其是在年轻女性中(schiffmanm.等人,2007,loc.cit;roncog.等人,jnatlcancerinst,2008;100:492-501)。
被引用的筛选程序的特征意味着一定百分比的过度诊断可能是由于筛选测试本身;然而,由在三年间隔下的细胞学筛选引起的过度诊断被认为是可接受的。在2004年开始的意大利ntcc研究(用于宫颈癌的新技术)显示,在年龄小于35岁的女性中,hr-hpvdna检测相比于细胞学增加了过度诊断和过度处理,即使细胞学″分类″(即,阳性hr-hpvdna检测结果的″诊断研究″)是通过pap试验来实施的(roncog.etg.等人,2008,loc.cit;roncog.等人,lancetoncoi2010jan18)。另一方面,在年龄超过35岁的女性中,显示,如果过度诊断存在的话,即使不采用分类细胞学,它也是低的。
以上发现还突出对高度gin和癌症的特异性生物标志物的需求,所述特异性生物标志物旨在密切地检测与转化相关的分子变化,而不是简单检测hr-hpvdna感染。当接种hpv疫苗的女性组群进入筛选时,特异性甚至更相关(francoel.等人,vaccine.2006;24suppl3:s171-7)。
目前,准备使用的生物标志物仅仅是与e6和el病毒基因的表达直接或间接相关的生物标志物,所述e6和el病毒基因调控hpv的复制。来自高风险表型的e6和el基因被称为癌基因,并且它们改变的转录调控似乎是细胞朝恶性肿瘤转化的必要步骤,所述改变的转录调控影响几乎全部的细胞通路(fehrmannf,laiminsla.oncogene.2003;22∶5201-7)并且促进dna的不稳定性。hpv癌基因的表达及其对宿主细胞的影响可以通过鉴定病毒e6-e7mrna转录本被直接地追踪(lieak,kristenseng.,expertrevmoldiagn.2008;8:405-15),或者通过检测p16细胞蛋白被间接地追踪(ca-rozzif.等人,lancetoncoi.2008,9∶937-945;benevolom.等人,amjclinpathol.2008;129:606-12)。据所知,后者是参与细胞周期控制的蛋白,其在被hpv转化的宫颈细胞中过表达。事实上,如广泛地报道,p16的表达被hr-hpve7蛋白影响,并且其在宫颈中的上调与病变严重性的增加显著相关(benevolom.等人,modpathol.2006mar;19(3):384-9)。
然而,由于缺乏解释免疫染色的标准准则,对p16的免疫组化评价当前显示有限的再现性(tsoumpoui,等人,p16(ink4a)immunostainingincytologicalandhistologicalspecimensfromtheuterinecervix:asystematicreviewandmeta-analysis,cancertreatrev.2009;35:210-20)。关于hpv的e6-e7mrna可以是在体外完全测试的用于鉴定临床相关的hr-hpvdna感染的有希望的生物标志物。事实上,可以看出,e6-e7mrna增加宫颈疾病的严重性(sotlark.等人,jmedvirol.2004;74:107-16;castlepe.等人,clincancerres.2007;13∶2599-605)。已报道,p16和e6-e7mrna两项分析比hr-hpvdnal的灵敏性小少许,但是更特异(carozzif.等人,lancetoncol.2008,9:937-945;szarewskia.等人,cancerepidemiolbiomarkersprev.2008;17:3033-4;monsonegoj.等人,eurogin2010,monaco.es4-4)。
以上提及的研究路线(病毒mrna转录本e6-e7的检测)包括例如欧洲专利ep1463839、ep1718774和ep2267155(norchipa/s)以及美国专利us7524631(patterson)。
迄今为止,然而,不存在指示癌前病变向宫颈癌不可逆转化的生物标志物(kooyj.等人,dualimmunostainingofcervicalcytologyspecimenswithatypicalsquamouscellsforp16/ki-67doesnotexcludetheexistenceofahigh-gradesquamousintraepitheliallesion.virchowsarch.2013oct1;pac-chiarottia.等人,prognosticvalueofp16-ink4aproteininwomenwithnegativeorcin1histologyresult:afollow-upstudy.intjcancer.2014,134,897-904)。
发明概述
在与本发明相关的研究框架中,已考虑了两个病毒癌基因e6和e7与宿主细胞的抑癌基因p53和prb的相互作用。事实上,已知,致癌蛋白e6与宿主细胞的抑癌蛋白p53结合,诱导所述抑癌蛋白p53的降解,以及破坏停止生长的活动并激活该抑癌蛋白特有的细胞凋亡。类似地,致癌蛋白e7复合宿主细胞的prb蛋白,并使其失活,从而使其抑癌活性失效(ishijit.,molecularmechanismofcarcinogenesisbyhumanpapillomavirus-16.jdermatol2000,feb;27(2):73-86l;buitrago-pereza.等人,molecularsignatureofhpv-inducedcarcinogenesis:prb,p53andgeneexpressionprofiling.currgenomics.2009mar;10(1):26-34;shaikhf.等人,molecularscreeningofcom-poundstothepredictedprotein-proteininteractionsiteofrb1-e7withp53-e6inhpv.bioinformation.2012;8(13):607-12)。
具体地,e6和e7基因的表达以及相关蛋白的随后产生是引起hpv诱导癌发生的必要原因,其特征是e6和p53蛋白以及e7和prb蛋白分别的相互作用。e6在细胞质中结合p53并且还招募e6ap泛素连接酶,这使得p53成为蛋白酶体降解的靶标。类似地,e7在细胞质中结合prb并且招募cullin2泛素连接酶,其继而促进被蛋白酶体降解。
根据本发明,已发现,通过相对简单的检测鉴定癌变的瞬间,通过鉴定来源于病毒癌基因e6和e7与宿主细胞的肿瘤抑制基因p53和prb相互作用的那些蛋白的存在是可能的,所述蛋白代表不可逆瘤转化的指数。为了能够实现其在致瘤性转化已发生的选择性情况中的功能,与尽管病变的发生也是高度的,但癌变过程仍可逆的情况相比,本发明提出的检查应当在hr-hpvdna检测的阳性结果之后和/或在不典型鳞状细胞(asc)或更差的细胞学诊断之后,插入宫颈癌的筛选或早期诊断的程序的诊断程序中。优选地,提出的测试应当在执行hr-hpvdna和pap试验均具有阳性结果之后进行。
本发明所提出的程序创新了对已确诊具有与hpv感染相关的宫颈高度发育异常病变的女性的临床管理。本质上,其相当于用特定的技术分析由病毒癌基因所编码的蛋白(e6和e7)以及由宿主细胞的肿瘤抑制基因所编码的蛋白(p53和prb),根据宿主中病毒基因组的整合期和/或相互作用期对它们进行分类和测量。如所注意,所提出程序的特异性是定义由于病毒蛋白与人蛋白的相互作用导致恶性转化的不可逆性的状态。
在本发明所提出的方法的实施中,可以通过任何分析技术探寻来源于e6与p53相互作用的蛋白(具体地,蛋白复合物e6/p53)和来源于e7与prb相互作用的蛋白(具体地,蛋白复合物e7/prb),其允许以简单而可靠的方式鉴定细胞样本中的以上提及的蛋白复合物之一或两者的形成,所述细胞样本取自所检查的患者的宫颈的鳞状-柱状接合处。更具体地说,所采用的分析技术应当能够在样本中检测蛋白e6或蛋白e7的存在,以及检测分别含有结合p53蛋白或prb蛋白的蛋白e6或蛋白e7的较大蛋白复合物的存在。在实践中,适合于以最佳的方式实现此类目标的两种技术是:a)蛋白印迹分析方法和b)三明治酶联免疫吸附分析(三明治elisa)。
a)蛋白印迹:进行新的宫颈取样,并且将样本在生理盐水中于4-8℃储存。然后使后者经历被称为蛋白印迹(免疫印迹)的生化方法的分析。该方法用于鉴定在指定的组织匀浆或细胞提取物样本中的蛋白。设想对样本进行离心,分离上清液,以及从而基于之前热变性的蛋白的分子量,在十二烷基硫酸钠的存在下通过聚丙烯酰胺凝胶电泳(sds-page),对之前热变性的蛋白进行分离。然后将蛋白从凝胶转移至通常为硝酸纤维的膜上,在这里它们被特异性抗体识别并结合。
b)三明治elisa:如果之前的测试还没有进行取样,则在液相中实施新的宫颈取样(thinprep-hologic,inc.,marlborough,ma,orsurepath-bddiagnostics,burlington,nc),否则在该情况下使用剩余的样本。通过酶免疫分析三明治elisa的手段分析样本。这是在生化中使用的免疫学分析方法以通过一种或多种抗体的手段检测物质的存在,酶与所述抗体之一结合:其取决于检测的目的蛋白,所述方法意味着宫颈样本在反应板中的直接转移,所述反应板适当地准备有特异性抗体抗蛋白e6和抗蛋白e7,以及随后通过其它特异性抗p53蛋白和抗prb蛋白抗体进行测试,用于检测目的蛋白复合物的相互作用。
根据本发明,使用特异性单克隆抗体-来自高致癌风险的hpv株的抗体抗蛋白e6和抗蛋白e7、商购的抗体抗p53蛋白、抗体抗prb蛋白机进行蛋白印迹和三明治elisa方法。这些方法导致不仅能够鉴定四种目的蛋白的存在,而且能够检测e6和p53(e6/p53)之间以及e7和prb(e7/prb)之间可能的相互作用状态,这代表了癌前病变向宫颈癌转化的不可逆性点。
根据本发明所提出的,探寻已具有细胞学不典型鳞状细胞(asc)或更差的诊断的女性中的这些蛋白允许增加hr-hpvdna检测和分类pap试验的诊断准确性,其增加筛选的整体灵敏性和特异性。具体而言,该探寻的引入将增加筛选的ppv(阳性预测值,其是真阳性对象和总共所有阳性对象(真和假)的比值),并且然后减少过度诊断和过度处理。
发明详述
根据其最广义的实施方案,因此,本发明具体地提供用于在经受宫颈癌筛选的女性中检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,所述方法包括在取自所检查的患者的宫颈上皮的鳞状-柱状结合处的细胞样本中检测由蛋白e6与蛋白p53组成的蛋白复合物e6/p53的存在和/或由蛋白e7与蛋白prb组成的蛋白复合物e7/prb的存在,其中检出所述两种蛋白复合物中的至少一种表明,在所检查的患者中,癌变已变得不可逆,优选在蛋白印迹或三明治elisa的分析技术中,通过抗体抗蛋白e6和抗体抗蛋白e7的组合使用以及优选抗体抗蛋白p53和抗体抗蛋白prb的组合使用进行所述检测。
根据常规技术,利用蛋白印迹检测e6/e7和p53/prb的相互作用的程序a)由以下步骤组成:(a)样本的制备(例如,匀浆/抽提、离心并煮沸用于变性样本缓冲液中的蛋白);(b)凝胶电泳;(c)转膜;(d)通常用牛血清白蛋白(bsa)或牛奶封闭膜的非特异性位点;(e)鉴定通过与抗体(一种初级抗体和一种识别二抗所连接的抗原的抗体,其与检测系统缀合,识别初级抗体)孵育探寻的蛋白;(f)通常通过比色反应或化学发光检测结合的抗体-抗原。
因此,本发明还具体地提供用于在经历宫颈癌筛选的女性中检测由人乳头瘤病毒(hpv)诱导的瘤细胞转化的方法,根据蛋白印迹技术其包括以下操作:
a)制备细胞样本,并且将其置于生理溶液中,所述细胞样本取自所检查的患者的宫颈上皮的鳞状-柱状结合处;
b)从所述样本提取蛋白,以及使获得的蛋白变性;
c)使所获得的变性蛋白经历聚丙烯酰胺凝胶电泳;
d)将从之前操作获得的蛋白转移至膜上,并且中和所述膜的空位点;
e)通过以下步骤鉴定所述蛋白:将所述蛋白与至少以下的抗体孵育:
第一单克隆抗体抗蛋白e6;
第一单克隆抗体抗蛋白e7;
然后,与缀合有生物素或信使酶如碱性磷酸酶的二级抗igg抗体孵育;
f)使来自之前操作的产物经历比色检测或化学发光检测;
其中显示蛋白e6(分子量18kda)和e7(分子量16kda)中的至少一种的双反应条带的所述检测结果表明,在所检查的患者中,癌变已变得不可逆,所述双条带包含第一条带和第二条带,所述第一条带与所探寻的蛋白即e6或e7对应,所述第二条带对应的分子量不同于且高于第一条带的各自蛋白的分子量,所述第二条带的分子量基本上等于71kd(蛋白复合物e6/p53)以及等于115,5kd(蛋白复合物e7/prb)。事实上,与在这些情况下明显的第二条带对应的分子量基本上等于p53和e6或者e7和prb的分子量的总和,从而指示真实的且其在结合的两个蛋白之间的相互作用。
优选地,根据本发明,显示如上所述的蛋白e6和蛋白e7的双反应条带的步骤f)被认为具有较高的安全性,其指示癌变已经建立。
根据本发明的优选实施方案,在e)阶段中,还将之前所述的蛋白与下述抗体孵育:
第一单克隆抗体抗蛋白p53;
第一单克隆抗体抗蛋白prb;
与所述第一单克隆抗体抗蛋白e6和抗蛋白e7孵育的情况所进行的操作类似的其它操作表明在所检查的患者中,癌变已变得不可逆,其中所述检测结果显示出蛋白p53和prb中的至少一种的双反应条带,所述双条带包含第一条带和第二条带,所述第一条带与所探寻的蛋白p53或prb的分子量对应,所述第二条带对应的分子量不同于且高于第一条带的各自蛋白的分子量。与第二条带(在这些情况下是明显的)对应的分子量在该情况下也大约等于p53和e6或者e7和prb的分子量的总和,从而指示配对的两种蛋白之间的真实相互作用。
如所注意的,蛋白e6和p53之间以及蛋白e7和prb之间的相互作用事实上引起p53的降解和prb的降解。考虑到p53引起细胞周期在g1期停滞,或者其引起细胞凋亡的机制,其允许肿瘤细胞克隆的抑制并确保基因组的稳定性,以及prb是具有细胞生长抑制活性的蛋白,这解释了e6和p53之间以及e7和prb之间的相互作用以及随后的降解如何产生两个基因的正常调控功能的废除,其很可能作为细胞致瘤性转化的引发物。
根据本发明的方法,显示蛋白e6和e7的单反应条带(其中所述单条带与所探寻的蛋白e6或e7的分子量对应)的所述检测结果表明,在所检查的患者中,癌变尚未开始或者尚未不可逆。根据相同准则,如果检测结果不显示蛋白e6和e7的任何反应条带,则结果表明在所检查的患者中,未发生病毒dna与细胞dna的整合。
优选地,根据本发明,所述步骤e)的二抗抗igg与碱性磷酸酶缀合,以及步骤f)的检测是比色检测或化学发光检测。而且,根据本发明的优选实施方案,以上提及的第一单克隆抗体抗蛋白e6和抗蛋白e7是针对病毒型hpv16和hpv18的蛋白e6或蛋白e7的小鼠单克隆抗体。
还根据本发明的优选实施方案,第一单克隆抗体抗p53蛋白是小鼠单克隆抗体抗人p53蛋白,以及第一单克隆抗体抗prb蛋白是小鼠单克隆抗体抗人prb蛋白。
如之前所提到的,在hr-hpvdna检测的阳性结果之后和/或在不典型鳞状细胞(asc)或更差的细胞学诊断之后,将本发明所述的诊断方法优选插入作为用于宫颈癌的女性群体的筛选的部分。
根据本发明的方法的具体实施方案,所提出的分析提供移出宫颈的鳞状-柱状结合处的上皮细胞的方法,优选通过被称为″细胞刷″(一次性刷尖,用于取出宫颈内的细胞进行细胞学检查,具有围绕其各自的轴放射性螺旋排列的刚毛以及朝向末端倾斜的长度,以便具有圆锥形的整体形状)的工具的手段进行移出。将由此获得的样本于4℃下在生理盐水(1ml)中储存;以及进行目的蛋白的提取和蛋白印迹技术的分析。
将通过离心样本所获得的细胞沉积物用0.9重量%的氯化钠洗涤两次。在于5,000rpm下离心5分钟之后,将细胞收集在裂解缓冲液中并且在添加蛋白酶抑制剂之后,让其于4℃搅拌30分钟。然后将裂解物于4℃,14,000rpm下离心20分钟以从上清液提取蛋白。在特定的缓冲液中热变性(95℃,5分钟)之后,在十二烷基磺酸钠的存在下通过聚丙烯酰胺凝胶电泳(sds-page)分析由此获得的蛋白。将蛋白转移至polyscreen膜(dupontnen)上。
将回收的凝胶和膜在含有转移缓冲液的两个单独的托盘中浸没15分钟,通过将组件顺序放置来制备三明治。为了该目的,可以使用aicos-denmark的semi-dry-electroblotter系统。作为确认转移,将膜在振动叠上的盘中优选用红色的丽春红染色5分钟,将其用去离子水洗涤。
此外根据上述具体的实施方案,进行膜的空位点的中和和目的蛋白的随后分析。对于存在的蛋白,利用下述单克隆初级抗体通过持续搅拌90分钟来分析用含有2%牛奶的洗涤缓冲液制备的膜:
■对于蛋白e6,小鼠第一单克隆抗体抗蛋白e6(hpv16e6+hpv18e6抗体[c1p5],abeam);
■对于蛋白e7,小鼠第一单克隆抗体抗蛋白e7(hpv16-e7抗体[编号28-0006],invitrogencorporation);
■对于蛋白p53,小鼠第一单克隆抗体抗蛋白p53(抗p53抗体[编号aho0112],invitrogencorporation);
■对于蛋白prb,小鼠第一单克隆抗体抗蛋白rb(抗人rb抗体[编号554162],bdbiosciences)。
进行与第二小鼠抗体抗igg的孵育;然后进行洗涤以及通过磷酸酶发生反应,以便检测病毒癌蛋白e6和e7的存在以及它们分别与蛋白p53和prb的可能相互作用的存在,这解释了如上所描述的结果。
根据常规技术,程序b)按照与本发明已经建立的蛋白印迹的方法a)有关的科学概念,使用三明治elisa检测e6/e7和p53/prb的相互作用,所述程序b)由以下阶段组成:(a)鉴定使用中的根据液相法(lbc)得到的储存样本;(b)将蛋白e6或e7的捕获抗体吸附在微量滴定板的不同孔中;(c)通过封闭缓冲液封闭结合蛋白的孔的剩余位点;(d)将来自lbc转运的样本直接加入各孔中;(e)通过与稀释的抗体抗p53蛋白在吸附有抗体抗蛋白e6的孔中以及与稀释的抗体抗prb蛋白在吸附有抗体抗e7蛋白的孔中孵育来鉴定目的蛋白;(f)用0.3%h2o2在甲醇中的溶液封闭内源底物;(g)在它们各自的孔中孵育缀合辣根过氧化物酶(hrp)的抗体;(h)将发色溶液tmb(3,3',5,5'-四甲联苯胺)加入到各孔中;(i)用分光光度计在450nm的波长下,通过量化有点蓝的颜色进行结果的读取。
为了验证测试,以上操作在两种单独的孔中进行,所述两种不同的孔的不同之处在于最初引入的初级抗体的类型不同:一种孔填充有必须被鉴定的蛋白(e6或e7)的特异性抗体,而另一种孔被非特异性抗体饱和。为了验证所考虑的测试,首先,测试在后者的孔中必须是阴性结果以及在所测试的生物样本实际含有目的抗体的情况下,测试在另一种孔(被目的蛋白特异的初级抗体饱和的孔)中应当是阳性的。
因此,本发明还具体地涉及在经受宫颈癌筛选的女性中检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,所述方法包括根据三明治elisa技术所述的以下操作:
a)鉴定使用中的根据液相细胞学方法(lbc)得到的以溶液形式储存的取自所检查的女性的宫颈的鳞状-柱状接合处的细胞样本;
b)将蛋白e6和e7的捕获抗体通过于4℃过夜孵育以及随后用pbs(磷酸缓冲盐水)洗涤而吸附在pvc的微板的不同孔中;
c)通过在pbs中的含脱脂牛奶的封闭缓冲液来封闭结合蛋白的孔的剩余位点,于室温下孵育至少1-2小时或者于4℃过夜孵育;
d)将来自液相细胞学瓶的100微升样本直接地加入各孔中,于37℃孵育90分钟并且通过在pbs中进一步洗涤进行移除;
e)通过与100微升稀释的抗体抗蛋白p53在吸附有抗体抗蛋白e6的孔中以及与100微升稀释的抗体抗蛋白prb在吸附有抗体抗蛋白e7的孔中于室温孵育1-2小时并且在pbs中进一步反复的洗涤进行移除来鉴定目的蛋白;
f)通过与h2o2在甲醇中的0,3%溶液在室温下孵育20分钟来封闭内源底物;
g)将100微升的含有缀合辣根过氧化物酶(hrp)的抗体溶液孵育进各孔中;
h)在各孔中加入发色团溶液tmb,持续20分钟(酶促反应:h2o2+还原底物→2h2o+被氧化的底物)并且通过添加2mh2o2溶液封闭反应;
i)使步骤h)的反应产物通过分光光度计读取在450nm波长下检测的光强度,
其中显示发生染色的由阳性吸光度记录的结果表明,在所检查的患者中,蛋白复合物e6/p53和/或e7/prb是存在的,这证实了病毒蛋白和那些人之间的相互作用,并且因此存在不可逆的致癌作用。
在最初引入的初级抗体类型不同的两种不同的孔中验证测试的对照:一种孔填充有想要探寻的蛋白(e6或e7)的特异性抗体,最少三个其它的孔用非特异性抗体饱和。如果测试在最后的孔中是阴性的以及在用目的蛋白特异的初级抗体饱和的孔中是阳性的,则其被认为是有效的。
根据本发明的方法,对于步骤e)、f)、g)和h),可以使用允许放大发色信号的在市场上可获得的其它系统(例如,使用生物素化的抗体抗p53或prb蛋白并且用缀合过氧化物酶或另外酶的链霉亲和素进行证实)。
优选地,根据本发明,具有较高安全性的被认为指示已经确立癌变的结果是根据步骤i)所述检测的那些结果,所述步骤i)的所述检测结果显示对于复合物e6/p53和复合物e7/prb而言检测的吸收值。
根据本发明的方法,显示对于两种蛋白复合物(e6/p53和e7/prb)而言阳性反应的该检测结果表明,在所检查的患者中,癌变已经开始并且变得不可逆。根据相同的标准,在不显示对于两种蛋白复合物(e6/p53和e7/prb)而言任何阳性反应(即缺乏吸收信号)的检测结果的情况下,所述结果表明,在所检查的患者中,尚未发生病毒dna与细胞dna的相互作用;不排除存在病毒dna与细胞dna整合的可能性,所述整合用该程序不可诊断。
优选地,根据本发明,通过与缀合辣根过氧化物酶的特异性抗体反应来证实所述步骤e)的抗体,以及阶段f)、g)和h)的检测是比色类型的检测。而且,根据本发明的优选实施方案,以上提及的第一单克隆抗体抗e6蛋白和抗e7蛋白是针对病毒型hpv16和hpv18的蛋白e6或e7蛋白的小鼠单克隆抗体。
还根据优选的实施方案,第一单克隆抗体抗p53是小鼠单克隆抗体抗人p53蛋白,第一单克隆抗体抗prb蛋白是小鼠单克隆抗体抗人prb蛋白。
如之前所注意到的,在阳性测试结果的hr-hpvdna之后和/或在不典型鳞状细胞(asc)或更差的细胞学诊断之后,将本发明所述的诊断方法优选插入作为用于宫颈癌的女性群体的筛选的部分。
根据本发明的方法的具体实施方案,所提出的分析提供移出宫颈的鳞状-柱状结合处的上皮细胞的方法,优选通过被称为″细胞刷″的工具的手段进行移出。将由此获得的样本在溶液中保藏用于液相细胞学诊断,然后用三明治elisa技术进行目的蛋白的分析。
仍根据上述具体的实施方案,通过三明治抗体反应:在板上吸附的病毒抗体抗蛋白(e6或e7)、在样本中存在的目的复合物蛋白(e6/e7或p53/prb)、抗人(p53或prb)蛋白,直接地测试用于液相细胞学的样本中包含的细胞,而不进行蛋白的抽提。所述方法确保完全的结合特异性并且通过使用下述第一单克隆抗体证明蛋白复合物e6/p53和e7/prb的存在:
■对于蛋白e6,小鼠第一单克隆抗体抗蛋白e6(hpv16e6+hpv18e6抗体[c1p5],abeam);
■对于蛋白e7,小鼠第一单克隆抗体抗蛋白e7(hpv16-e7抗体[编号28-0006],invitrogencorporation);
·对于蛋白p53,小鼠第一单克隆抗体抗蛋白p53(抗p53抗体[编号aho0112],invitrogencorporation);
·对于蛋白prb,小鼠第一单克隆抗体抗蛋白rb(抗人rb抗体[编号554162],bdbiosciences)。
随后与缀合有过氧化物酶的小鼠抗体抗lgg孵育并且发生通过分光光度计读取记录的比色反应,证实研究的目的复合物蛋白的阳性,其解释了如上已经描述的结果。
更通常,本发明还具体地提供用于检测由具有致癌作用的任何蛋白(例如:braf、kras、nras、her2等)与参与身体的各种器官和系统的与细胞肿瘤抑制作用有关的其它蛋白(例如p53、prb、pten、brca、cd95等)的相互作用引起的任何瘤细胞转化的诊断方法模型。
具体而言,用特异性单克隆抗体鉴定具有致癌作用或肿瘤抑制活性的这些蛋白,并且通过蛋白印迹和/或elisa三明治技术证明它们的相互作用。优选地,根据所提出的方法,还用特异性单克隆抗体直接地鉴定已相互作用的蛋白复合物(致癌蛋白/肿瘤抑制蛋白)。
总体来说,因此,根据如以上所描述的,本发明允许提出有效检测由具有致癌活性的任何蛋白和与细胞肿瘤抑制活性有关的另外蛋白的相互作用引起的任何瘤细胞转化的方法,其中还将所述方法插入作为癌症患者或疑似患者的诊断程序和/或治疗处理的一部分,所述方法使用抑制所述蛋白相互作用的靶向治疗。
附图简述
仅出于示例的目的参照下述中报道的实验工作的描述以及参照相关的附图,本发明的具体特征以及其优势将变得更明显,其中:
图1显示从经历pap试验筛选的2500名女性群体中选择为阳性的78例女性的细胞学诊断的柱状图。
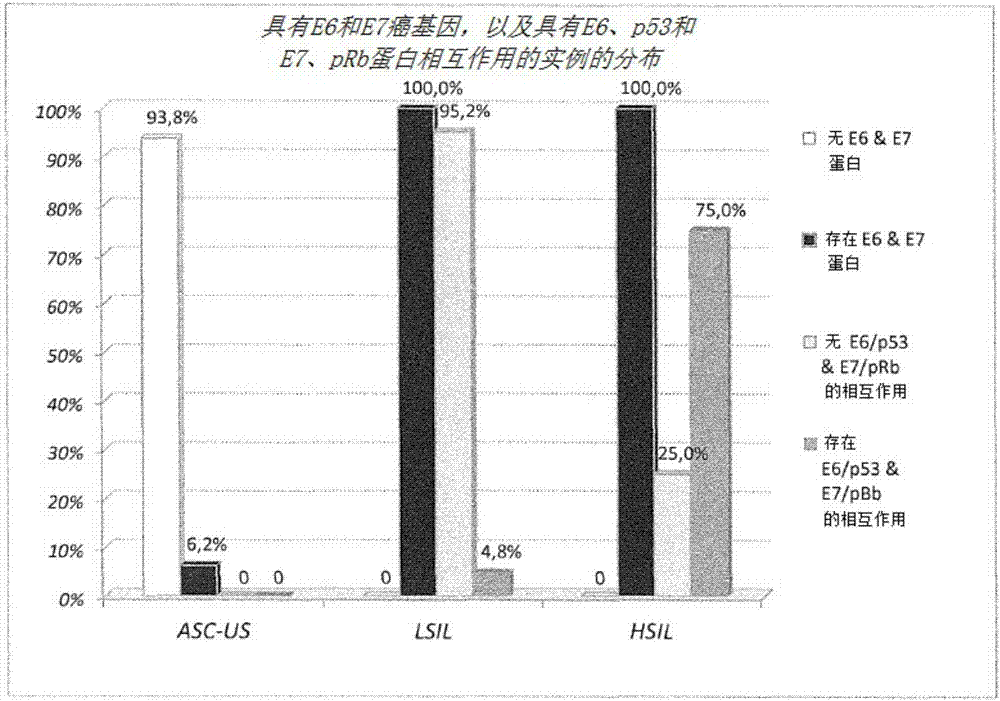
图2显示将根据本发明的诊断方法应用至针对图1的pap试验选择为阳性的78例女性的结果的直方图;
图3-6显示选自根据本发明的诊断方法的结果的一种情况,其中e6和e7蛋白存在,以及其中e6/p53和e7/prb的相互作用也存在;
图7是图示说明应用本发明的诊断方法的阳性pap试验和阳性hr-hpvdna检测的女性管理的指示的流程图;以及
图8是图示说明将三明治elisa方法应用至本发明的诊断方法的的流程图。
使未经选择的女性群体经历pap试验作为初步检查的筛选测试
在本发明的背景下,进行研究旨在鉴定已发展高度发育异常病变或宫颈癌的具有临床相关病变的女性。对未经选择的2,500名女性的宫颈试样进行所述研究,其在卡塞塔当地卫生局asl的卫生咨询门诊部中心自发地发生。所述研究在2012年6月至9月进行并且包括通知女性并获得知情同意书。在该群体中,进行常规的pap试验,并且在卡塞塔asl的细胞病理学实验室分析所述试验。
在所调查的2,500名女性中,总共78名(即为3.12%)被诊断为非阴性的,即针对pap试验为asc+(鳞状细胞非典型或更差)。如还在附图1的图表中所示的,细胞学诊断的asc+被分为下述:32例具有asc-us细胞学特征(41%)、42例为lsil(54%)以及4例为hsil(5%)。
96.88%的实例为鳞状上皮内病变或恶性阴性的,其属于正常变化或良性炎性变化的分类中,有时由于微生物(细菌、真菌或阴道毛滴虫)的存在而被标记。
召回具有阳性诊断的78名女性以根据本发明的方法经历进一步的检查,通过第二样本研究e6/p53和e7/prb蛋白的整合/相互作用。
在马尔恰尼塞医院的分子生物学实验室,根据如上所述的本发明所述方法的具体实施方案的程序获取并测试样本。
在本文的附图2中示出通过蛋白印迹分析pap试验阳性的78个样本获得的数据。柱状图首先显示,在具有asc-us细胞学诊断的32个样本中,只有2个样本(6.3%)对于e6和e7蛋白的存在而言是阳性的,而在其它30个样本(93.7%)中,未发现e6和e7蛋白。
另一方面,在lsil(42)和hsil(4)细胞学诊断的所有样本中,已证明了e6和e7蛋白的存在。因此,根据本发明所述的诊断方法,在pap试验具有非阴性诊断的总共78个样本中,只有48个样本对于e6和e7蛋白的存在而言是阳性的。
从观察到的数据,清楚的是,在大多数的asc-us(93.7%)中,不发生病毒基因组的整合,以及根据结果其可以意味着:
1)hpv不存在:发现的细胞学异常本质上仅仅是炎症性的;
2)存在低风险hpv:通常不能够整合进基因组但是限于游离形式;
3)存在高风险hpv:仍然处于早期阶段,具有非常新近的感染且缺乏整合。
对于具有lsil和hsil细胞学诊断的所有情况,鉴定e6和e7蛋白,并且因此可以阐明这些样本具有高风险hpv,以及确定感染不是新近的,如已经具有病毒基因组的整合。
考虑到也如图2中所示的存在蛋白e6和e7的48个阳性实例,本发明的诊断方法允许观察到e6/p53和e7/prb的相互作用在4,8%的lsil实例和75,0%的hsil实例中存在,其在显示存在蛋白e6和e7的asc-us中不存在。
图2的柱状图中所示的结果还总结在下表中。
表1
用蛋白印迹测试的蛋白e6/p53和e7/prb的整合/相互作用的实例的细胞学和组织学诊断的关联
以上所示的数据表明,48.8%的lsil和75.0%的hsil具有e6/p53和e7/prb的相互作用,认为癌变过程已处于晚期;对于剩下的无相互作用的lsil和hsil实例,可以认为癌变过程仍处于早期,消退仍然是可能的。
在所报道的本文的研究中通过蛋白印迹获得的结果类型的最有意义的实例显示于附图3、4、5和6,其显示获自样本的蛋白印迹分析的结果,在这里,除e6和e7之外,还发现p53和prb的相互作用。
分别涉及用第一单克隆抗体抗e6和抗e7蛋白进行的蛋白印迹的结果的图3和图4的观察表明各样本的双反应条带,18kd和71kd(抗e6蛋白)、16kd和115.5kd(抗e7蛋白)。根据本发明,分子量高于e6和e7的另外条带的存在表明e6和p53之间以及e7和prb之间的相互作用存在。
已通过分别用第一单克隆抗体抗p53和抗prb蛋白进行的两个另外的蛋白印迹分析确认所述假设。在图5和图6中,显示确认此假设获得的结果,因为反应条带精确地匹配之前所观察到的两个另外条带。
对于具有e6和e7蛋白而无e6/p53和e7/prb的相互作用的样本,用第一单克隆抗体抗e6蛋白和抗e7蛋白进行的蛋白印迹显示对于各样本而言分别为18kd(抗体抗e6蛋白)和16kd(抗e7蛋白)的单一反应条带。
然而,对于e6和e7蛋白的存在而言为阴性的样本,用第一单克隆抗体抗e6蛋白与抗e7蛋白进行的蛋白印迹均显示无反应条带,证明在这些样本中,不存在病毒dna向细胞的整合。
根据获得的结果,清楚的是,所研究的所有hsil和大部分lsil存在病毒基因组与e6和e7蛋白的整合的产生。然而,75.0%的高度病变和只有很少低度病变(4.8%)显示蛋白e6/p53和e7/prb的相互作用。这些数据确认了相互作用是癌变的标志物。
因此,用于评价e6和e7蛋白的存在以及它们的可能相互作用(e6/p53和e7/prb)的蛋白印迹技术表明hpvdna检测和细胞学二者的较高特异性,其允许鉴定具有临床相关病变(cin2+)的患者。lsil和hsil的组织学随访证实了该假设。具体而言(参见,表1),在具有e6/p53和e7/prb蛋白相互作用的四例hsil中,两例为cin3(重度发育异常-原位癌)(50.0%),以及一例为侵略性鳞状细胞癌(25.0%),无相互作用的第四例被诊断为cin3。同样,具有e6/p53和e7/prb蛋白相互作用的两例lsil(4.8%)中,发现一例为cin2(中度发育异常)(50.0%),以及另一例为cin3(50.0%)。无相互作用的40例lsil(95.2%)中,37例为cin1(轻度发育异常)(88.1%),以及3例为cin2(7.1%)。
这些信息证实了蛋白相互作用和癌变之间的联系,甚至仍要理解什么是来自这些相互作用整合的并从而癌性转化的生物学基础步骤。基本上只有少数表达e6和e7蛋白的整合病变过表达向完全癌变的进展。这暗示了这样的假设:存在病毒蛋白的定量阈值,在所述阈值之上,它们的相互作用发展。根据最代表性实例的研究,进一步的研究将能够证实该假设。
考虑到将上文报道的评价作为基本原则,根据本发明的方法,我们提出,特别是根据图7图表中的示意指示,在诊断路径中,在hr-hpvdna阳性测试和pap试验阳性asc+病变之后,进行蛋白e6/p53和e7/prb的整合/相互作用测试的蛋白印迹或三明治elisa。
利用该诊断策略,可以增加细胞学(asc+)诊断和分子(hr-hpvdna阳性测试)诊断在宫颈筛选中的特异性,仅对具有病毒基因组的整合/相互作用的情况,预约另外召回的女性进行第二级调查。相同的策略还可以应用于子宫外区域(肛门-生殖区域、口咽区域等)中hpv引起的肿瘤性病变。
与有组织的筛选以及充足灵敏性和增加特异性的所用测试(如在这里作为实例报道的测试)联合的有效疫苗策略将通过减少宫颈癌的影响导致乳头瘤病毒感染流行率的降低,还通过靶向疗法导致卫生和社会经济优势,大大降低死亡率。
本发明所述的方法的另外可能有利用途在于在疾病进展的不同阶段使用与假酸浆烯酮(shaikhf.等人,2012,loc.cit.)相同的方法进行实关于抗癌症药物的活性和相互作用的e6/p53和e7/prb的抑制活性的实验,用于所述药物在靶向疗法中的开发和实验。
相同的方法还意图在细胞样本中鉴定由致癌基因编码的蛋白(也是非病毒的)和在细胞的检查中由肿瘤抑制基因编码的蛋白,以及通过蛋白印迹和/或elisa三明治鉴定它们之间可能的相互作用,所述细胞样本取自除所检查的任何患者的宫颈之外的任何解剖学位点。
具体参照本发明的某些具体实施方案来公开本发明,但是应当理解,在不脱离所附权利要求中所限定的发明的范围的情况下,由本领域技术人员可以做出改变和变化。
权利要求书(按照条约第19条的修改)
1.在经受宫颈癌筛选的女性中,检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,所述方法包括,在取自被检查的患者的宫颈上皮的鳞状-柱状结合处的细胞样本中,检测由蛋白e6与蛋白p53组成的蛋白复合物e6/p53和由蛋白e7与蛋白prb组成的蛋白复合物e7/prb的存在,其中所述两种蛋白复合物的检出表明,在所检查的患者中,癌变已变得不可逆,通过抗体抗蛋白e6和抗体抗蛋白e7的组合使用进行所述检测。
2.如权利要求1所述的方法,其包括蛋白印迹技术所述的下述步骤:
a)制备取自被检测的患者的宫颈上皮的鳞状-柱状结合处的细胞样本,并将其置于生理溶液中;
b)从所述样本提取蛋白并且使获得的所述蛋白变性;
c)使由此获得的变性蛋白进行聚丙烯酰胺凝胶电泳;
d)将从前面步骤获得的所述蛋白转移在膜上并且中和所述膜的空位点;
e)通过以下步骤鉴定所述蛋白:将所述蛋白与至少下述抗体孵育:
第一单克隆抗体抗蛋白e6;
第一单克隆抗体抗蛋白e7;
然后与缀合有生物素或信使酶如碱性磷酸酶的第二抗igg抗体孵育;
f)使来自前面步骤的产物进行比色检测或化学发光检测;
其中显示蛋白e6和e7中的双反应条带的所述检测的结果表明,在检查的患者中,癌变已变得不可逆,所述双条带包含第一条带和第二条带,所述第一条带与所探寻的蛋白即e6或e7的分子量对应,以及所述第二条带对应的分子量不同于且高于第一条带的各蛋白的所述分子量,所述分子量基本上等于蛋白复合物e6/p53的71kd以及等于蛋白复合物e7/prb的115,5kd。
3.如权利要求2所述的方法,其中在所述步骤e)中,所述蛋白还与下述抗体孵育:
第一单克隆抗体抗蛋白p53;
第一单克隆抗体抗蛋白prb;
进一步的步骤类似于所述第一单克隆抗体抗蛋白e6和抗蛋白e7孵育的情况进行的步骤,并且显示蛋白p53和prb中的至少一种的双反应条带的所述检测的结果表明,在检查的患者中,癌变已变得不可逆,所述双条带包含第一条带和第二条带,所述第一条带与所探寻的蛋白p53或prb的分子量对应,所述第二条带对应的分子量不同于且高于所述第一条带的各蛋白的所述分子量。
4.如权利要求2或3所述的方法,其中显示蛋白e6和e7的单一反应条带的所述检测的结果表明,在所检查的患者中,癌变尚未开始或者尚未变得不可逆,所述单一条带与所探寻的蛋白e6或e7的分子量对应。
5.如权利要求4所述的方法,其中未显示蛋白e6和e7的任何反应条带的所述检测的结果表明,在所检查的患者中,没有发生病毒dna与细胞dna的整合。
6.如权利要求2或3中任一项所述的方法,其中所述步骤e)的第二抗igg抗体缀合有碱性磷酸酶,以及其中操作f)的所述检测是比色检测或化学发光检测。
7.如权利要求2所述的方法,其中所述第一单克隆抗体抗蛋白e6是病毒型hpv16和hpv18的小鼠抗蛋白e6抗体,以及所述第一单克隆抗体抗蛋白e7是病毒型hpv16和hpv18的小鼠抗蛋白e7抗体。
8.如权利要求3所述的方法,其中所述第一单克隆抗体抗蛋白p53是小鼠单克隆抗人蛋白p53抗体,以及所述第一单克隆抗体抗蛋白prb是小鼠单克隆抗人蛋白prb抗体。
9.如权利要求1所述的方法,其中所述检测通过抗体抗蛋白e6、抗体抗蛋白e7、抗体抗蛋白p53和抗体抗蛋白prb的组合使用进行,其包括三明治elisa技术所述的下述步骤:
a)鉴定根据液相细胞学(lbc)储存的待检查的样本;
b)将作为病毒蛋白e6或e7的捕获抗体的抗体抗蛋白e6和抗蛋白e7吸附在微孔板的不同孔中;
c)通过封闭缓冲液封闭结合所述蛋白的孔的剩余位点;
d)将待分析的所示细胞样本直接加入各孔;
e)通过与稀释的抗体抗蛋白p53在吸附有抗体抗蛋白e6的孔中以及通过与稀释的抗体抗蛋白prb在吸附有抗体抗蛋白e7的孔中孵育来鉴定所述目的蛋白;
f)封闭内源底物;
g)将缀合辣根过氧化物酶(hrp)的抗体孵育进各个孔中;
h)将发色团溶液加入各孔中;
i)使步骤h)的反应产物通过分光度计在450nm波长下读取检测的光强度,
其中显示由阳性吸收所记录的发生染色的结果表明,在所检查的患者中,蛋白复合物e6/p53和e7/prb是存在的,其证实了病毒蛋白和人蛋白之间的相互作用,并且因此指示,在所检查的患者中,癌变开始并且已变得不可逆。
10.如权利要求9的步骤e)、f)、g)和h)所述的方法,其中使用允许放大发色信号的可商购的系统,优选使用生物素化的抗蛋白p53和prb抗体并且用缀合过氧化物酶或另外酶的链霉亲和素进行证实。
11.如权利要求9所述的方法,其中在检测结果不显示蛋白复合物e6/p53和e7/prb的任何反应阳性,在450nm下缺乏信号吸收的情况下,所述结果表明,在所检查的患者中,没有发生病毒dna与细胞dna的整合;不排除存在病毒dna与细胞dna整合的可能性。
12.如权利要求9所述的方法,其中所述第一单克隆抗体抗蛋白e6是病毒型hpv16和hpv18的小鼠单克隆抗体抗蛋白e6,所述第一单克隆抗体抗蛋白e7是病毒型hpv16的小鼠单克隆抗体抗蛋白e7,所述第一单克隆抗体抗蛋白p53是小鼠单克隆抗体抗人p53蛋白,所述第一单克隆抗体抗prb蛋白是小鼠单克隆抗体抗人prb蛋白。
13.如权利要求2-5和9-12中任一项所述的检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,其中在不典型鳞状细胞(asc)或更差的细胞学诊断,以及随后hr-hpvdna测试的阳性结果之后,将所述方法插入在对女性群体的筛选程序的框架中,或者插入在宫颈癌的早期诊断、检测的程序中。
14.如权利要求2-5和9-12中任一项所述的检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,其中在hr-hpvdna测试的阳性结果,以及随后不典型鳞状细胞(asc)或更差的细胞学诊断之后,将所述方法插入在女性群体的筛选程序的框架中,或者插入在宫颈癌的早期诊断、检测的程序中。
15.如权利要求2-5和9-12中任一项所述的检测由人乳头瘤病毒(hpv)引起的瘤细胞转化的方法,其中将所述方法插入在对子宫外区域,如肛门-生殖区域、口咽区域等中具有hpv引起的肿瘤性病变,或疑似具有hpv引起的肿瘤性病变的患者的诊断活动、筛选或随访的框架中。
- 还没有人留言评论。精彩留言会获得点赞!