流式细胞术细胞分选系统及其使用方法与流程
相关申请的交叉引用
本申请要求于2014年12月4日提交的美国临时专利申请序列号62/087,662的优先权,所述申请的公开内容通过引用结合在此。
引言
流式细胞术是用于分析和分离如细胞和组成分子等生物颗粒的有价值的方法。如此,其具有宽范围的诊断应用和治疗应用。所述方法利用液流来线性地分隔颗粒,从而使得它们可以呈一列地穿过检测装置。可以根据个别细胞在液流中的位置以及可检测标记的存在来区分所述细胞。因此,可以使用流式细胞仪来产生生物颗粒群的诊断特征曲线。
已经通过将分选或收集能力添加到流式细胞仪中来实现了对生物颗粒的分离。通过机械移除或电移除来将分隔流中被检测为具有一个或多个期望特性的颗粒分别与样本流分离。常见的流式分选技术利用液滴(drop)分选,在液滴分选中,将包含线性分隔的颗粒的液流分解成液滴,并且使包含兴趣颗粒的液滴带电并通过穿过电场来将其偏转到收集管中。
流中的线性分隔颗粒可以随着它们穿过刚好位于喷嘴尖头下方的观察点而被表征。一旦认为颗粒满足一个或多个期望标准,就可以预测其将到达液滴分离点并在液滴中脱离所述流的时间。理想地,在包含所选颗粒的液滴刚好脱离所述流之前向液流施加短暂电荷,并且然后在液滴分离之后立即将所述电荷接地。待分选液滴在从脱离液流时保持电荷,并且所有其他液滴不带电。可以通过电场将带电液滴从其他液滴的向下轨迹偏转并且将其收集到适当容器中,而不带电液滴直接落入到排水管中。微滴(droplet)分选器通过向液滴施加电荷(通常为50至150伏特)来偏转包含兴趣细胞的液滴。液滴通过静电场偏转并且根据电荷而遵循不同的轨迹,从而使得它们到达收集容器。可以通过施加不同的电荷来将细胞分布于多个组中,每个离散电荷将液滴引导到容器中。
在一些应用中,期望将多井托盘(multi-welltray)用作存放分选液滴的容器,例如,从而使得每个分选液滴可以被分选到其自己的单独容器中。关于使用多井托盘的系统,所述系统被配置成用于相对于分选位置而移动托盘,从而使得分选微滴可以存放到多井托盘的个别井(例如,容器)中。托盘相对于分选位置的移动当前经由‘起停(stopandgo)’运动曲线来实施,其中,托盘移动到某个空间位置并停止,在这之后,分选开始。然后,托盘移动到下一个位置等等。
技术实现要素:
提供了用于分选细胞的系统。所述系统可以包括细胞分选器,所述细胞分选器包括偏转器,所述偏转器能够将被分析微滴偏转(即,被配置成用于偏转)到偏转微滴接收位置;以及支撑平台,所述支撑平台包括容器并且被配置成在两个维度上连续地移动。所述系统的方面可以进一步包括处理器,所述处理器可操作地耦合至具有指令的存储器,所述指令用于确定所述容器与所述偏转微滴接收位置的对准并且在所述容器被对准时向所述细胞分选器发送偏转信号。本发明的方面进一步包括计算机可读介质,所述计算机可读介质包括存储器,所述存储器具有用于在x-y平面中连续地移动支撑平台的指令,用于确定容器与偏转微滴接收位置的对准的算法,以及用于向细胞分选器发送偏转信号的指令。还提供了用于将细胞分选到容器中的方法。
附图说明
应当理解的是,以下描述的附图仅为了说明目的。附图不旨在以任何方式限制本发明教导的范围。
图1描绘了系统(100)的框图,所述系统包括分选器仪器(101);支撑平台(102),所述支撑平台支承容器并且能够相对于分选器而连续地移动;以及控制器(103),所述控制器协调分选器与平台之间的相互作用。
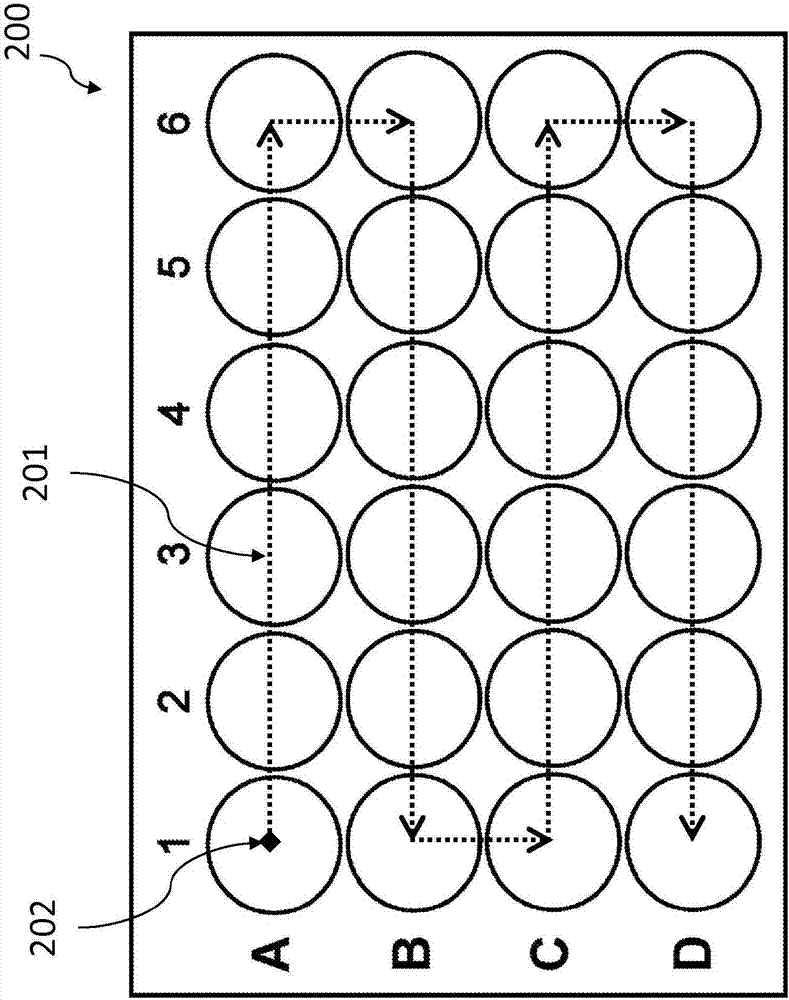
图2描绘了如从上方观察的24井托盘(200)的示意图。虚线(201)示出了起停(stop-and-go)设计中分选器喷嘴相对于托盘的轨迹。所述轨迹开始于井a1的中心202并且结束于d1。
图3描绘了24井托盘(300)的一部分以及与微滴接收位置相对应的分选器喷嘴的轨迹的一部分(虚线301)的示意图。此轨迹部分开始于井a1左方的点302并且延伸经过井a6。阴影区域303标记将液滴存放到井中是可能且可靠的区域。当分选器喷嘴被对准在这种区域之内时,分选器从控制器接收规定对液滴进行存放(例如,经由微滴偏转)的命令。
图4展示了平台沿着起停轨迹中的一条轴线的位移。在时间0处,喷嘴与第一井a1的中心对准。喷嘴在那里静止约0.75秒,然后在0.25秒内移动到a2的中心,再次静止0.75秒等等。耗费了将近6秒来处理6个井。
图5展示了平台随着时间沿着一条轴线的连续位移轨迹。分选器喷嘴开始在井a1的左边缘处对准并且以与其在现有起停实施方式中移动的速度相同的速度连续地移动到井a6的右边缘。现在,花费少于四倍的时间(1.5秒)来处理6个井。在两条虚线之间的垂直轴线上的区域501示出了将细胞存放到井a4中是可靠的位移范围。在两条虚线之间的水平轴线上的区域502示出了相应时间间隔(约0.5秒)。
定义
在更详细地描述示例性实施例之前,阐述了以下定义以便说明和限定本说明中所使用的术语的含义和范围。
除非另外限定,本文中所使用的所有技术性术语和科学性术语具有与本发明所属领域的技术人员通常理解的含义相同的含义。singleton(辛格尔顿)等人的dictionaryofmicrobiologyandmolecularbiology,2ded.(《微生物学与分子生物学词典第2版》)(纽约johnwileyandsons(约翰威利父子出版公司),1994年)以及hale&markham(哈勒和马卡姆)的theharpercollinsdictionaryofbiology(《哈普克林生物学词典》)(纽约harperperennial(哈珀永久出版社),1991年)为技术人员提供了本文中所使用的术语中的许多术语的一般含义。尽管如此,为了清晰和便于参考,以下定义了某些术语。
必须指出的是,除非上下文另外清楚地指明,如本文中所使用的以及在所附权利要求书中,单数形式“一个”、“一种”以及“所述”包括复数指代物。例如,术语“一种引物”指一个或多个引物,即,单个引物或多个引物。应当进一步指出的是,可以将权利要求书撰写成排除任何可选要素。如此,这种述旨在充当结合对权利要求要素的叙述使用如“仅仅”、“仅”等排他性术语或使用“负”限制的前提基础。
“处理器”指将执行其所需的功能的任何硬件和/或软件组合。例如,本文中的任何处理器可以是如以电子控制器、大型机、服务器或个人计算机(台式计算机或便携式计算机)的形式可用的可编程数字微处理器。在处理器是可编程的情况下,适当的编程可以从远程位置传达至处理器,或预先保存在计算机程序产品(比如,便携式或固定式计算机可读存储介质,无论基于磁性设备、光学设备或固态设备)中。例如,磁介质或光盘可以携带编程并且可以由与每个处理器通信的适当读取器在其相应站处进行读取。
“基于计算机的系统”指用于分析本发明的信息的硬件装置、软件装置和数据存储装置。基于计算机的系统的最小硬件包括中央处理单元(cpu)、输入装置、输出装置和数据存储装置。可以使用任何合宜的基于计算机的系统。数据存储装置可以包括任何产品(包括对如本文中所描述的本发明信息的记录)或可以访问这种产品的存储器访问装置。
如本文中所使用的,术语将数据、编程信息或其他信息“记录”到计算机可读介质上指用于使用任何合宜方法来存储信息的过程。可以基于用于访问所存储信息的装置来选择任何合宜的数据存储结构。各种数据处理器程序和格式(例如,文字处理文本文件、数据库格式等)可以用于进行存储。
如本文中所使用的,术语“样本”涉及包含一个或多个兴趣分析物的材料或材料混合物(在一些情况下,以液体形式)。在一些实施例中,以其最广泛的意义使用的所述术语指包含细胞或者产生细胞代谢物的任何植物、动物或细菌材料,如例如,与个体分离的组织或流体(包括但不限于,血浆、血清、脑脊液、淋巴、眼泪、唾液和组织切片)或者与体外细胞培养成分分离的组织或流体,以及来自环境的样本。术语“样本”还可以指“生物样本”。如本文中所使用的,术语“生物样本”指完整生物体或者其组织、细胞或组成部分的子集(例如,体液,包括但不限于血液、黏液、淋巴液、滑液、脑脊液、唾液、羊水、羊膜脐带血、尿液、阴道液和精液)。“生物样本”还可以指从完整生物体或其组织、细胞或组成部分的子集中制备的匀浆、裂解物或提取物或者其一小部分或一部分,包括但不限于:血浆;血清;脊髓液;淋巴液;皮肤、呼吸道、肠道和泌尿生殖道的外部部分;眼泪;唾液;乳汁;血细胞;肿瘤以及器官。在某些实施例中,已经将样本从动物或植物中移除。生物样本可以包括细胞。术语“细胞”在常规意义上用于指至少具有核和细胞膜的活生物体(真核和原核两者)的基本结构单元。在某些实施例中,细胞包括如来自细菌的原核细胞。在其他实施例中,细胞包括真核细胞,比如,从来自动物、植物或真菌的生物样本中获得的细胞。
如本文中所使用的,术语“确定”、“测量”以及“评估”和“测定”可被互换地使用并且包括定量确定和定性确定。
如本文中所使用的术语“分离”指至少60%地、至少75%地、至少90%地、至少95%地、至少98%地以及甚至至少99%地独立于其他组成部分的兴趣部分,在净化之前,所述兴趣部分与所述其他组成部分相关联。
“多个”至少包含2个构件。在某些情况下,多个可以具有10个或更多个,比如,100个或更多个、1000个或更多个、10,000个或更多个、100,000个或更多个、106个或更多个、107个或更多个、108个或更多个或者109个或更多个构件。
数值范围包括限定所述范围的数字。
如本文中所使用的术语“分隔”指对两个要素的物理分隔(例如,根据大小或亲和度等)以及对一个要素的降级,使另一个要素完好无损。
本文中所描述的方法包括多个步骤。如所期望的,可以在两个步骤之间已经经过预定量的时间之后执行每个步骤。如此,在执行每个步骤之间的时间可以是1秒或更多、10秒或更多、30秒或更多、60秒或更多、5分钟或更多、10分钟或更多、60分钟或更多并且包括5小时或更多。在某些实施例中,在完成之前步骤之后立即执行每个随后步骤。在其他实施例中,可以在完成之前步骤之后的潜伏时间或等待时间(例如,几分钟到整夜的等待时间)之后执行步骤。
其他术语定义可能在整个说明书中出现。
具体实施方式
如以上所概述的,提供了用于分选细胞的系统。所述系统可以包括细胞分选器,所述细胞分选器包括偏转器,所述偏转器能够将分析微滴偏转到偏转微滴接收位置;以及支撑平台,所述支撑平台包括容器并且被配置成在两个维度上连续地移动。所述系统的方面可以进一步包括处理器,所述处理器可操作地耦合至具有指令的存储器,所述指令用于确定所述容器与所述偏转微滴接收位置的对准并且在所述容器被对准时向所述细胞分选器发送偏转信号。还提供了一种包括存储器的计算机可读介质,所述存储器具有用于在x-y平面中连续地移动支撑平台的指令,用于确定容器与偏转微滴接收位置的对准的算法,以及用于向细胞分选器发送偏转信号的指令。还提供了用于将细胞分选到容器中的方法。
在更详细地描述各种实施例之前,应当理解的是,本公开的教导不限于所描述的特定实施例,并且如此当然可以变化。还应当理解的是,因为本发明教导的范围将仅由所附权利要求书限制,所以本文中所使用的术语仅出于描述特定实施例的目的,而不旨在是限制性的。
本文中所使用的章节标题仅出于组织性目的,而不应当被解释为以任何方式限制所描述的主题。虽然本发明教导是结合各种实施例而加以描述的,但是本发明教导并不旨在受限于这种实施例。相反,如本领域的技术人员将理解的,本发明教导包括各种替代型式、修改型式及等同型式。
除非另外限定,本文中所使用的所有技术性术语和科学性术语具有与本公开所属领域的技术人员通常理解的含义相同的含义。尽管类似于或等同于本文中所描述的方法和材料的任何方法和材料也可以用于实践或测试本发明教导,但是现在对一些示例性方法和材料进行描述。
对任何出版物的引用内容是针对其在申请日期之前的公开,并且不应当被解释为承认本权利要求书因为先前发明而不能获得比这种出版物更早的申请日期。另外,所提供的出版物的日期可以不同于可能独立地确认的实际出版日期。
如对本领域的技术人员将清楚的是,在阅读本公开时,本文中所描述和说明的单独实施例中的每个实施例具有离散的组成部分和特征,所述组成部分和特征可以在不偏离本发明教导的范围或精神的情况下易于与其他若干实施例中的任何实施例的特征分离或组合。可以按所叙述的事件的顺序或按逻辑上可能的任何其他顺序来执行所叙述的任何方法。
本文中所参考的所有专利和出版物(包括在这种专利和出版物内公开的所有顺序)通过引用而明确结合。
在进一步描述本发明时,首先更详细地描述系统。接下来,回顾在主题系统中使用的计算机可读介质。还描述了使用主题系统的兴趣方法。
细胞分选系统
本发明的方面包括用于分选细胞的系统及其使用方法。在一些实例中,所述系统是具有流道的流式细胞仪系统,所述流道装载有包括细胞混合物的样本,所述细胞基本上一次一个地穿过对所述细胞进行检测和/或标识(即,分析)的感测区域。然后,可以对此流动的被分析细胞流进行分选以便将期望被分析细胞群递送至细胞接收位置,而将流动流的其余部分丢弃或者单独收集。
如此,所述系统可以包括将令人期望的被分析细胞引导至细胞接收位置(即,细胞分选)的细胞分选器,在所述细胞接收位置处可能配置有连续移动的支撑平台,所述支撑平台被定位成用于将令人期望的被分析细胞收集到安装在支撑平台上的托盘的多个容器中。相比于以起停运动(例如,包括速度为0井/秒的周期的运动)移动的台,以连续运动移动的支撑平台由于连续移动的台发生的对支撑平台的移动机构的电动机和其他机械部分的减小的磨损而提供更长的机械零件寿命和/或更少的系统维护。所述系统可以包括控制器,所述控制器使多井托盘的连续运动与对来自细胞分选器的细胞的连续递送同步。控制器的逻辑在容器的轨迹中标识(多个)时隙,在所述时隙期间,当多井托盘沿着轨迹移动时,可以根据多井托盘的位置而将被分析细胞收集到(多个)特定容器中。当这种时隙开始时,将细胞收集到容器中是可能的,并且向细胞分选器的分选机构下发适当命令以便实际上将令人期望的细胞引导(例如,通过偏转包含细胞的液滴)至细胞接收位置。当时隙结束时,控制器可以下发阻止细胞分选的命令。在一些情况下,当已经将期望数量的微滴和/细胞收集到容器中时,不论特定时隙结束与否,控制器都可以下发阻止细胞分选的命令。
在一些实施例中,所述系统是用于分选细胞的系统,所述系统包括:细胞分选器,所述细胞分选器被配置成用于产生被分析微滴流并且包括偏转器,所述偏转器能够将被分析微滴从所述被分析微滴流偏转到偏转微滴接收位置;支撑平台,所述支撑平台包括容器并且被配置成在两个维度上连续地移动;以及处理器,所述处理器可操作地耦合至存储器,所述存储器包括存储于其上的指令,所述指令用于确定所述容器与所述偏转微滴接收位置的对准并且在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送偏转信号。
细胞分选器
主题系统可以包括能够将令人期望的细胞群与样本分隔和分离的细胞分选器。用于分析和/或分隔目标颗粒(例如,细胞)的任何合宜的细胞分选器可以用于主题系统,比如,能够进行机械分选、静电分选或磁分选的细胞分选器。在一些实例中,细胞分选器是流式细胞仪系统的一部分。在某些实例中,所述系统被配置成用于产生微滴流,其中,微滴包含被分析细胞。可由细胞分选器经由通过施加静电场来使微滴充以静电以及将带电微滴从流动流偏转,从而实现将兴趣微滴转移到接收位置。这种静电场可由被定位在流动流附近的偏转器板创建。如本文中所使用的,术语“偏转”或者“被偏转”指将兴趣微滴从流动的分析微滴流静电偏转,由此细胞分选器可以标识和跟踪流动流中的兴趣细胞并且仅转移流动流的包括要通过容器收集的那些兴趣细胞的那些微滴。在一些实例中,所述系统被配置成用于将单个微滴偏转到每个容器中。
在所述系统的一些实施例中,细胞分选器被配置成用于产生被分析微滴流并且将被分析微滴从被分析微滴流偏转到偏转微滴接收位置。如此,细胞分选器可以包括能够将被分析微滴从微滴流偏转到偏转微滴接收位置的偏转器。如本文中所使用的,术语“偏转微滴接收位置”指系统中可以在包含兴趣细胞的分选微滴已经被细胞分选器偏转之后收集所述分选微滴的位置。在一些情况下,细胞分选器可以经由可选喷嘴将兴趣微滴偏转至收集容器。喷嘴可以被配置在保持容器的支撑平台之上(即,正交地沿着z轴),其中,支撑平台被配置成连续地移动(即,在x-y平面中)。偏转微滴接收位置与x-y平面中由支撑平台限定的位置相对应,由流动的偏转微滴流限定的z轴在所述位置处相交。随着支撑平台连续地移动,偏转微滴接收位置也在x-y平面中移动。
仅由细胞分选器对兴趣微滴进行的偏转导致在偏转微滴接收位置处收集样本材料。如果单个容器被定位在偏转微滴接收位置处,则所述容器将被定位成用于从细胞分选器收集浓缩的兴趣被分析细胞群。在一些情况下,非偏转微滴跟随细胞分选器的不受电场影响的流动流或者受施加电场的影响的流动流,所述电场具有阻止偏转到微滴接收位置的极性和/或强度。可以丢弃或单独收集非偏转微滴。
可以将兴趣细胞作为根据各种参数(比如,经由将特定荧光标签附接到兴趣细胞上来标识的表型特性)而与细胞分选器的流动流分隔的目标。可以将任何合宜的细胞作为在主体系统的细胞分选器中进行的偏转的目标。在一些实施例中,所述系统被配置成用于偏转被确定为包括目标细胞的被分析微滴。
支撑平台
所述系统可以包括用于安装(多个)容器的支撑平台。支撑平台可以是被配置成用于将(多个)容器保持在位以及用于相对于细胞分选器的流动流而移动(多个)容器的任何合宜的安装设备。除了其他类型的支撑结构之外,支撑平台可以包括平面基板、带有轮廓的安装设备、圆柱形或管状支撑结构、或者激光器或led固持器。在一些实例中,支撑平台可以是多井托盘的底座。如本文中所使用的术语“多井托盘”和“多井板”可互换地用于指可以以任何合宜的格式来配置的收集容器(例如,井、小瓶、管等)的二维阵列。兴趣多井托盘包括但不限于:包括井构型的构造、在x-y平面按一系列行和列来安排的管和/或小瓶(例如,2x3、2x6、3x4、8x12、16x24),比如,12井、24井、96井和384井容器板或托盘。如本文中所使用的,术语“容器”指可以是许多容器(例如,多井托盘中的井、小瓶、管等)之一的离散容器。如所期望的,支撑平台的数量可以根据主题系统中的容器的数量而变化,比如,两个或更多个、三个或更多个或者四个或更多台并且包括五个或更多个支撑平台。在某些实施例中,兴趣系统包括一个支撑平台,比如,具有安装容器的支撑平台(例如,安装的多井托盘)。在某些实施例中,支撑平台包括两个或多个安装容器,比如,6个或更多个、12个或更多个、24个或更多个、48个或更多个、96个或更多个、或者384个或更多个离散安装容器、
支撑平台可以是可移动的。可以连续地移动支撑平台以便调整容器与来自细胞分选器的流动的兴趣被分析细胞流的对准。如本文中所使用的,“连续”移动指在正对细胞进行分选和收集的连续移动期间内支撑平台不静止(即,具有速度0)于特定位置处。支撑平台的连续移动可以是线性的、弯曲的或者成角度的,并且可以涉及一次或多次移动方向变化。在一些实例中,支撑平台以恒定速度连续地移动。在某些情况下,支撑平台以变化的速度连续地移动,其中,在一些实例中,支撑平台的速度不可以下降到低于适当阈值。在这种情况下,支撑平台的速度可以是平均速度。在某些实施例中,支撑平台以0.2井/秒或更多、0.5井/秒或更多、1井/秒或更多,比如,2井/秒或更多、3井/秒或更多、4井/秒或更多、5井/秒或更多、6井/秒或更多、7井/秒或更多、8井/秒或更多、9井/秒或更多、或者甚至10井/秒或更多的速度连续地移动。连续移动速度可以在支撑平台的轨迹期间根据各种因素(比如,多井托盘中的容器的间距和分选液滴频率等)而变化。在某些实例中,支撑平台连续地移动,但具有速度变化(即,移动方向变化)。
如本文中所使用的,术语“对准”指安装在支撑平台上的(多个)容器与流动的被分析细胞流的接收位置的相对位置。当安装在平台上的容器能够从细胞分选器中接收或收集兴趣偏转微滴时,支撑平台被称为与偏转微滴接收位置对准。在一些实例中,支撑平台可在两个维度上连续地移动,比如,在与来自细胞分选器的流动的兴趣细胞流的轴线(例如,z轴)正交的x-y平面中。如此,支撑平台可以被配置成用于在支撑平台连续地移动的同时顺序地将多井托盘的井与偏转微滴接收位置对准。术语“在两个维度上连续地移动”意味着包括在x-y平面中的线性移动,比如,在x维度上的移动(例如,如图3中所描述的,沿着行a、a1至a6)、随后是在y方向上的线性移动(例如,从行a到行b)、随后是在x方向上的线性移动(例如,沿着行b,从b6到b1或者从b1到b6)等。在一些实例中,支撑平台包括两个或更多个容器,并且所述系统被配置成用于在z维度上经由支撑平台在x-y平面中的连续移动来自动且顺序地将所述两个或更多个容器与偏转微滴接收位置对准。
图3展示了轨迹(301),所述轨迹表示偏转微滴接收位置与安装在相对于细胞分选器而连续地移动的支撑平台上的多井托盘的对准。图5展示了随着平台连续地移动,井a4(图3)与偏转微滴接收位置的空间(区域501)对准和时间(区域502)对准。为了简单起见,在所述图中未指示与井a1至a3、a5至a6(图3)与偏转微滴接收位置的空间对准和时间对准相对应的区域。
在其他实例中,支撑结构可以在三个维度上移动。在支撑平台被配置成移动的情况下,支撑平台可以被配置成连续地或者以离散间隔移动。在一些实施例中,在安装的多井托盘从细胞分选器中接收或收集微滴的时间内,支撑平台可以按连续运动而移动。
在某些实例中,支撑平台被配置成在从细胞分选器中收集细胞期间不以离散间隔移动,例如,不按如由图4中的图示所描绘的起停运动而移动。在某些实施例中,支撑平台可以以离散间隔移动,如例如,以0.01微米或更大增量,如0.05微米或更大,如0.1微米或更大,如0.5微米或更大,如1微米或更大,如10微米或更大,如100微米或更大,如500微米或更大,如1mm或更大,如5mm或更大,如10mm或更大并且包括25mm或更大增量。
可以采用任何移位方案来移动支撑结构,比如,使用电动机致动的平移台、导杆平移组件、齿轮传动的平移设备(比如,采用除了其他类型的电动机以外的步进电动机、伺服电动机、无刷电动机、有刷dc电动机、微型步进驱动电动机、高分辨率步进电动机的部件)来移动支撑平台。
在某些实施例中,主题系统被配置成用于直接或间接地评估容器和/或支撑平台与偏转微滴接收位置的对准。可以利用任何合宜的部件和方法来评估对准。在一些实施例中,主题系统包括用于检测指示对准的光信号的一个或多个光电检测器。除了其他光电检测器以外,主题系统中的光电检测器可以是任何合宜的位置感测检测方案,包括但不限于光学传感器或光电检测器,比如,有源像素传感器(aps)、象限光电二极管、图像传感器、电荷耦合设备(ccd)、增强型电荷耦合设备(iccd)、发光二极管、光子计数器、辐射热测量计、热电检测器、光敏电阻、光伏电池、光电二极管、光电倍增管、光电晶体管、量子点光电导体或光电二极管以及其组合。可以通过评估支撑平台的任何一个点的相对对准或定位相对于细胞分选器的自然流动流或流动流接收位置而绘制安装在支撑平台上的所有容器的相对定位。
控制器
主题系统可以包括控制器,所述控制器使支撑平台(并且由此安装的多井托盘)的连续运动与对来自细胞分选器的细胞的递送同步。在一些实施例中,描述了一种包括计算机可用介质的计算机程序产品,所述计算机可用介质具有存储于其中的控制逻辑。所述控制逻辑当由计算机的处理器执行时使所述处理器执行本文中所描述的功能。控制器的逻辑可以标识(多个)时隙,在所述时隙中,被分析细胞可以被引导至特定井并且根据多井托盘移动时的相对定位而被收集。如本文中所使用的,术语“同步”指仅在容器被适当地定位成用于接收所转移的流动流时发生的将兴趣流动流转移到接收位置的过程。从流动流转移到接收位置的液体将被收集到容器口内的任何时间,容器被认为是定位在接收位置处。如本文中所使用的,术语“时隙”指在一个离散安装容器处于用于接收和收集细胞分选器的转移流动流(例如,用于在偏转微滴接收位置处接收偏转微滴)的适当位置中的支撑平台轨迹期间的时间段。在一些情况下,通过标绘偏转微滴接收位置(从正交z轴突出的)与(例如,所提出的)平台在x-y平面中的连续移动的相对定位来确定支撑平台的轨迹。
可以在主题系统中利用任何合宜的控制器。控制器可以可操作地耦合至支撑平台和/或细胞分选器并且可以提供用于执行所述系统(例如,如本文中所描述的系统)的功能的指令。在一些实施例中,所述系统包括可操作地耦合至存储器的处理器,所述存储器包括存储于其上的指令,所述指令用于确定容器与偏转微滴接收位置的时间对准和空间对准。图5展示了随着支撑平台连续移动,井a4(图3)与偏转微滴接收位置的空间(区域501)对准和时间(区域502)对准的确定期间(即,时隙)。为了简单起见,在所述图中未指示与井a1至a3、a5至a6(图3)与偏转微滴接收位置的空间对准和时间对准的期间相对应的区域。如所期望的,随着平台连续地移动,可以在多井托盘的特定位置处收集偏转细胞的空间对准和时间对准期间(即,时隙)可以取决于许多变量。如支撑平台的速度和所提出的轨迹等变量、所使用的特定容器(例如,井、管或小瓶)的口宽度以及细胞分选与细胞收集之间的距离和/或时间延迟可以考虑在内以便确定空间对准和时间对准的区域。
在一些实例中,所述指令包括相对于偏转微滴接收位置而绘制支撑平台的轨迹,以及确定安装在支撑平台上的多个容器将被适当地定位成用于接收偏转细胞的时隙。如此,时隙指容器与偏转微滴接收位置空间对准的时间段。在一些实例中,确定容器的时间对准和空间对准包括用于确定支撑平台相对于偏转微滴接收位置的轨迹的指令以及用于确定每个容器的时间对准和空间对准的区域的指令。在某些实施例中,容器是安装在支撑平台上的多井托盘的一个井。
所述系统可以被配置成用于将对来自细胞分选器的细胞的递送与容器用于接收偏转微滴的适当定位同步。在一些情况下,所述系统被配置成用于只有在容器处于用于接收微滴的适当位置中时偏转兴趣微滴。在一些实施例中,所述系统包括可操作地耦合至存储器的处理器,所述存储器包括存储于其上的指令,所述指令用于在容器与偏转微滴接收位置对准时向细胞分选器发送偏转信号。当容器在空间上和时间上出现在接收位置处从而使得其可以接收被偏转到偏转微滴接收位置的液滴时,容器被看作与偏转微滴接收位置对准。处理器可以被配置成用于根据存储在存储器中的可执行指令来控制细胞分选器的偏转器,所述指令规定要在每个时隙期间偏转的期望微滴数量。偏转信号指任何合宜的直接或间接(多个)指令或(多个)信号,所述指令或信号对细胞分选器进行配置以便在期望时间段(例如,时隙)内将兴趣微滴(如果出现的话)偏转到偏转微滴接收位置。偏转信号可以分成可以进行操作以便发起偏转或者以便阻止进一步偏转的两个或更多个部分或子信号。
在所述系统的一些实施例中,偏转信号包括初始偏转子信号和最终偏转子信号。所述存储器可以包括用于通过在时隙开始时向细胞分选器发送初始偏转子信号来产生偏转信号的指令,所述初始偏转子信号将偏转器配置为在被分析微滴出现时对其进行偏转。用于产生偏转信号的指令进一步包括在时隙结束时向细胞分选器发送最终偏转子信号,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。在所述系统的一些实施例中,用于产生偏转信号的指令进一步包括在时隙期间已经偏转单个被分析微滴之后向细胞分选器发送最终偏转子信号,其中,最终偏转信号将偏转器配置为不对被分析微滴进行偏转。在一些情况下,在系统被配置成用于偏转每容器目标数量的微滴的情况下,在时隙期间发送最终偏转子信号以便阻止进一步偏转微滴被偏转到偏转微滴接收位置。在某些实例中,所述系统被配置成用于偏转每容器5个微滴或更少,比如,每容器5个、4个、3个、2个或1个微滴。
流式细胞仪系统包括细胞分选器,所述细胞分选器提供取决于各种因素(比如,样本中的兴趣细胞的浓度、流动流的速度和体积、检测和/或标识流动流中的细胞的方式以及微滴形成的方式)的偏转微滴频率。包含兴趣细胞的微滴是否可用于在时隙期间进行偏转取决于流动的被分析微滴流中的这种细胞的频率并且取决于容器处于偏转微滴接收位置处的适当位置中的时隙的频率。时隙频率取决于各种因素,比如,支撑平台的速度和所提出的轨迹,所使用的特定容器(例如,井、管或小瓶)的口宽度以及支撑平台上的容器之间的间距。在一些情况下,兴趣多井托盘在井之间具有规则的间距,所述规则的间距在支撑平台的连续移动期间提供一致的时隙频率。在一些实施例中,所述支撑平台包括多个容器,并且所述系统被配置成用于在z维度上经由所述支撑平台在x-y平面中的连续移动来自动且顺序地将所述两个或更多个容器与所述偏转微滴接收位置对准。
所述处理器可以被配置成用于根据存储在存储器中的可执行指令来控制支撑平台的连续移动,所述可执行指令在确定空间对准和时间对准的区域以及对连续移动进行控制的参数时将来自细胞分选器的偏转微滴频率考虑在内。如此,在所述系统的一些实例中,所述存储器包括用于确定来自细胞分选器的偏转微滴频率的算法。所述存储器可以包括用于将(多个)时隙的长度和/或频率与偏转微滴频率匹配的算法,由此确定细胞分选器在时隙期间偏转单个液滴。如本文中所使用的,术语“匹配”指在选择对支撑平台的连续移动进行控制的一个或多个参数(比如,移动速度和在x-y平面中的空间路径)时将来自细胞分选器的偏转微滴的确定频率考虑在内并且由此提供令人期望的时隙长度和/或频率的算法。如此,在一些情况下,用于确定多个容器与偏转微滴接收位置的空间对准和时间对准的区域的指令包括选择(多个)时隙的期望频率。在一些情况下,所提出的支撑平台在x-y平面中相对于偏转微滴接收位置(z轴)的空间路径可以根据多井托盘的构型(例如,图3)而默认选择。在这种情况下,所述指令可以包括用于自动选择期望支撑平台速度以便提供与细胞分选器的微滴偏转的确定频率相匹配的时隙频率的算法。应当进一步理解的是,可以响应于条件变化(比如,来自细胞分选器的偏转细胞的频率的变化或者每容器的期望偏转细胞数量的变化)而调整支撑平台的连续移动。可以响应于条件和/或期望参数的变化而自动调整所述系统的任何合宜参数。在一些实例中,所述存储器包括用于响应于来自细胞分选器的偏转微滴频率的变化而自动调整支撑平台的速度(例如,沿着设置的空间路径)的指令。因此,如果偏转微滴频率减小因数2,则存储器可以包括用于减小支撑平台的速度由此按类似的因数2减小时隙频率的指令。在一些实例中,存储器包括用于自动调整细胞分选器的一个或多个参数以便提供与可以收集微滴的时隙的频率相匹配的偏转微滴频率。可以自动调整兴趣细胞分选器参数,包括但不限于:鞘液压力、微滴充电电压、偏转板电压、电荷校正值、液滴延迟、液滴驱动频率、液滴振幅以及电荷相位。
存储器可以是其中的处理器可以存储和检索数据的任何适当设备,比如,磁性设备、光学设备或固态存储设备(包括磁盘或光盘或磁带或ram,或任何其他适当设备,或者固定式或者便携式)。处理器可以包括从携带必要程序代码的计算机可读介质中适当编程的通用数字微处理器。可以通过通信信道来向处理器远程提供编程,或将编程预先保存到计算机程序产品(比如,存储器或使用与存储器相关的那些设备中的任何设备的其他一些便携式或固定式计算机可读存储介质)中。例如,磁盘或光盘可以携带编程,并且可以通过盘写入器/读取器来读取。主题系统还包括例如以计算机程序产品、计算机可读介质、算法等的形式的用于控制主题系统和实践本文中所描述的方法的编程。
计算机可读介质
还提供了一种包括存储器的计算机可读介质,所述存储器包括存储于其上的指令(例如,如本文中所描述的指令)。本文中所描述的指令和算法可以记录于任何合宜的计算机可读介质(例如,可由计算机直接读取和访问的任何介质)上。这种介质包括但不限于如软盘、硬盘存储介质和磁带等磁存储介质;如cd-rom等光存储介质;如ram和rom等电存储介质;便携式闪存驱动器;如磁存储介质/光存储介质等这些类别的混合。
在一些实施例中,所述指令包括:用于在x-y平面中连续地移动包括容器的支撑平台的指令;用于确定容器与偏转微滴接收位置的时间对准和空间对准的算法;以及用于在容器与偏转微滴接收位置对准时向细胞分选器发送偏转信号的指令,其中,细胞分选器包括偏转器,所述偏转器能够将被分析微滴从被分析微滴流偏转到偏转微滴接收位置。
在某些实施例中,所述存储器包括用于确定容器与偏转微滴接收位置对准的时隙的指令。在一些实例中,所述偏转信号包括初始偏转子信号和最终偏转子信号;并且所述存储器包括用于通过在所述时隙开始时向所述细胞分选器发送初始偏转子信号来产生所述偏转信号的指令,所述初始偏转子信号将偏转器配置为在被分析微滴出现时对其进行偏转。在一些实例中,所述存储器进一步包括用于通过在所述时隙结束时向所述细胞分选器发送最终偏转子信号来产生所述偏转信号的指令,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。在一些情况下,所述存储器进一步包括用于在所述时隙期间已经偏转单个被分析微滴之后向所述细胞分选器发送最终偏转子信号的指令,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。在某些情况下,所述指令可以规定在时隙期间将两个或更多个被分析微滴收集到容器中。
在一些实施例中,所述存储器包括用于在x-y平面中自动且连续地移动支撑平台以便在z维度上顺序地将所述两个或更多个容器与偏转微滴接收位置对准的指令。在某些实施例中,所述存储器包括用于将所述时隙的长度与所述偏转微滴频率匹配的算法,由此确定所述细胞分选器在所述时隙期间偏转单个液滴。
在一些实例中,所述存储器包括用于响应于来自所述细胞分选器的所述偏转微滴频率的变化而调整所述支撑平台的速度的指令。
流式细胞仪
在某些实施例中,所述系统包括流式细胞仪。在这种实施例的一些实例中,主题系统可以被配置成用于例如通过光散射来检测对来自流动流的微滴的偏转和或收集。前向散射光可以从照射的流动流中收集并且可由一个或多个前向散射检测器收集。在某些实施例中,前向散射检测器被定位在流动流与光源的相反侧上并且被定位成用于收集和检测前向散射光。在某些实施例中,主题系统被配置成用于通过检测来自通过全内反射而在上游传播的光的光信号来评估与流动流的对准。
在某些方面,所述系统还可以包括光源,所述光源被配置成用于将光引导至流道的试验区域。所述系统可以包括检测器,所述检测器被配置成用于从流道的试验区域接收信号,其中,所述信号由荧光成分提供。可选地,进一步地,样本分析系统可以包括用于检测一个或多个附加信号的一个或多个附加检测器和/或光源。在某些方面,所述系统可以进一步包括被配置成用于检测荧光信号的存在的基于计算机的系统。主题系统可以包括许多附加部件,比如,数据输出设备(例如,监视器和/或扬声器)、数据输入设备(例如,界面接口、键盘等)、流体处理部件、电源等。
根据本发明的实施例的可以被修改以便包括相对于微滴分选位置的连续移动容器的兴趣流式细胞仪(如以上所描述的)包括但不限于以下文献中所讨论的流式细胞仪:flowcytometry:apracticalapproach(《流式细胞术:实用方法》)(编者:ormerod(奥默罗德),牛津大学出版社(1997));flowcytometryprotocols(《流式细胞术方案》)(编者:雅罗什斯基(jaroszeski)等人,methodsinmolecularbiologyno.91(《分子生物学方法第91期》),胡玛纳出版社(1997));practicalflowcytometry,3rded.(《实用流式细胞术:第三版》)(wiley-liss(1995));annclinbiochem(《临床生化纪事》)(virgo(弗戈)等人(2012),1月,49(第1部分):17-28);seminthromhemost(《血栓与止血研讨》)(linden(林登)等人,2004年10月,30(5):502-11);jpathol(《病理学杂志》)(alison(艾莉森)等人,2010年12月,222(40):335-344);以及critrevtherdrugcarriersyst(《治疗性药物载体系统的关键评论》)(herbig(赫比格)等人(2007),24(3):203-255),所述文献的公开内容通过引用结合在此。在某些实例中,兴趣流式细胞术系统包括bd生物科学facscantotm流式细胞仪、bd生物科学facsvantagetm系统、bd生物科学facsorttm系统、bd生物科学facscounttm系统、bd生物科学facscantm系统、以及bd生物科学facscaliburtm系统、bd生物科学influxtm细胞分选器、bdaccuritmc6、bdfacsversetm、bdlsrfortessatmx-20、bdlsrfortessatm、bd生物科学jazztm细胞分选器以及bd生物科学ariatm细胞分选器等。
在某些实施例中,主题系统是结合了以下美国专利申请号中描述的流式细胞仪的一个或多个部件的流式细胞仪系统:3,960,449;4,347,935;4,667,830;4,704,891;4,770,992;5,030,002;5,040,890;5,047,321;5,245,318;5,317,162;5,464,581;5,483,469;5,602,039;5,620,842;5,627,040;5,643,796;5,700,692;6,372,506;6,809,804;6,813,017;6,821,740;7,129,505;7,201,875;7,544,326;8,140,300;8,233,146;8,753,573;8,975,595;9,092,034;9,095,494和9,097,640,所述专利的公开内容通过引用结合在此。
方法
如以上所概述的,本发明的方面包括用于使用主题系统来将细胞分选到容器中的方法。在一些实施例中,所述方法包括:将包括细胞的样本装载到例如如以上所描述的用于分选细胞的系统中,以及在操作所述系统的同时分选所述细胞,从而使得所述系统进行操作以便在两个维度上连续地移动所述支撑平台并且以便在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送所述偏转信号。
可以利用任何合宜的方案来将样本装载到用于分选细胞的系统(例如,如本文中所描述的系统)中。在一些情况下,所述系统是流式细胞仪,并且装载样本包括将样本引入到流式细胞仪的流动流中。包括(或者疑似包括)兴趣细胞的任何合宜的样本可以被作为使用主题系统来进行分选的目标。可以将兴趣细胞作为根据各种参数(比如,经由将特定荧光标签附接到兴趣细胞上来标识的表型特性)而与细胞分选器的流动流分隔的目标。在一些实施例中,所述系统被配置成用于偏转被确定为包括目标细胞的被分析微滴。各种细胞可以被作为使用主题方法来进行分选的目标。兴趣目标细胞包括但不限于干细胞、t细胞、树突细胞、b细胞、粒细胞、白血病细胞、淋巴瘤细胞、病毒细胞(例如,hiv细胞)、nk细胞、巨噬细胞、单核细胞、纤维母细胞、上皮细胞、内皮细胞和红细细胞。兴趣目标细胞包括具有合宜的细胞表面标记或抗原的细胞,所述标记或抗原可以通过合宜的亲和剂或其偶联物来捕获或标记。例如,目标细胞可以包括细胞表面抗原,比如,cd11b、cd123、cd14、cd15、cd16、cd19、cd193、cd2、cd25、cd27、cd3、cd335、cd36、cd4、cd43、cd45ro、cd56、cd61、cd7、cd8、cd34、cd1c、cd23、cd304、cd235a、t细胞受体阿尔法/贝塔、cd253、cd95、cd20、cd105、cd117、cd120b、notch4、lgr5(n-端)、ssea-3、tra-1-60抗原、双唾液酸神经节苷脂gd2和cd71。在一些实施例中,目标细胞选自包含hiv的细胞、调节性t细胞、抗原特异性t细胞群、来自全血的肿瘤细胞或均从造血前体细胞(cd34+)、骨髓或脐带血。
主题方法包括在操作主题系统(例如,如本文中所描述的系统)的同时分选细胞。所述系统可以部分或完全自动地进行操作。在一些实例中,所述系统进行操作以便在两个维度上连续地移动所述支撑平台并且以便在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送所述偏转信号。“自动”指支撑平台的连续移动,并且对来自细胞分选器的微滴的偏转几乎不需要人类干预或手动输入。在一些实施例中,兴趣系统可以被部分或完全自动化,从而使得支撑平台的连续移动和对来自细胞分选器的微滴的偏转是处理器控制的。在某些实施例中,主题系统被配置成用于在没有任何人类输入的情况下将支撑平台的连续移动与对来自细胞分选器的微滴的偏转同步。在某些实例中,人类输入可以包括选择要安装在支撑平台上的多井托盘以及确定支撑平台的空间轨迹(见例如图3和图2)。
在所述方法的某些实施例中,所述系统进行操作以便确定所述容器与所述偏转微滴接收位置对准的时隙。在所述方法的一些实例中,所述偏转信号包括初始偏转子信号和最终偏转子信号,并且所述系统进行操作以便在所述时隙开始时向所述细胞分选器发送初始偏转子信号来产生所述偏转信号,所述初始偏转子信号将所述偏转器配置为当被分析微滴出现时对其进行偏转。在所述方法的某些情况下,所述系统进行操作以便在所述时隙结束时向所述细胞分选器发送最终偏转子信号,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。在所述方法的一些实施例中,所述系统进行操作以便在所述时隙期间已经偏转单个被分析微滴之后向所述细胞分选器发送最终偏转子信号,其中,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。在所述方法的某些实施例中,所述支撑平台包括两个或更多个容器;并且所述方法包括在x-y平面中自动且连续地移动所述支撑平台以便在z维度上顺序地将所述两个或更多个容器与所述偏转微滴接收位置对准,由此将被分析细胞收集到所述两个或更多个容器中。在所述方法的某些实例中,支撑平台包括12个或更多个容器。
在所述方法的一些实例中,确定分析微滴流包括被分选目标细胞。在所述方法的某些实施例中,所述细胞分选器只有在确定目标细胞出现时才偏转被分析微滴。在某些实例中,所述方法包括将单个微滴偏转到所述两个或更多个容器中的每个容器中。在某些情况下,所述方法包括将单个目标细胞收集到所述12个或更多个容器中的每个容器中。
在所述方法的一些实施例中,所述系统进行操作以便将所述(多个)时隙的长度和/或频率与所述偏转微滴频率匹配,由此确定所述细胞分选器在所述时隙期间偏转单个液滴。在一些情况下,所述方法进一步包括响应于来自所述细胞分选器的偏转微滴频率的变化而调整所述支撑平台的速度。
在一些实例中,将细胞分选到6个或更多个容器(比如,12个或更多个、24个或更多个、48个或更多个、96个或更多个或者384个或更多个离散容器)中的经过时间比包括以相同速度的不连续运动来移动支撑平台(例如,以如图4中所描述的起停运动,其中,当平台移动时,其以与连续移动平台相同的速度移动)的控制方法快至少2倍,比如,比所述控制方法快至少3倍、5倍或甚至10倍。“经过时间”指支撑平台从第一井与接收位置之间的对准位置移动到与多井托盘的最后一个“井”的对准位置所耗费的时间。
在所述方法的某些实施例中,所述方法进一步包括检测和/或分析目标细胞。在一些实例中,所述方法进一步包括以流式细胞术方式分析目标细胞。在流式细胞仪中检测细胞可以包括在流式细胞仪的探询点处使用一个或多个激光器来激发荧光染料,以及随后使用一个或多个光学检测器来检测来自染料的荧光发射。除了检测颗粒以外,可能期望确定所分选或分隔的颗粒(例如,细胞)的数量。因此,在一些实施例中,所述方法进一步包括对标记颗粒(例如,目标细胞)进行计数和/或分选。在对颗粒进行检测、计数和/或分选时,包括颗粒的液体介质首先被引入到流式细胞仪的流动路径中。当处于流动路径中时,颗粒基本上一次一个地穿过一个或多个感测区域(例如,探询点),在所述感测区域处,颗粒中的每个颗粒单独暴露于单波长的光源中,并且对于每个颗粒,单独地记录如所期望的对光散射参数和/或荧光发射的测量结果(例如,两个或更多个光散射参数和对一个或多个荧光发射的测量结果)。如所期望的,实时分析针对每个颗粒而记录的数据,并且将所述数据存储在如计算机等数据存储装置和分析装置中。美国专利号4,284,412描述了配备有单个光源的兴趣流式细胞仪的构型和用途,而美国专利号4,727,020描述了配备有两个光源的流式细胞仪的构型和用途。还可以采用具有多于两个光源的流式细胞仪。
更具体地,在流式细胞仪中,悬浮液中的颗粒基本上一次一个地进入流动路径穿过一个或多个感测区域(或“探询点”),其中,在每个区域中,由能量源照亮每个颗粒。能量源可以包括发射单波长的光的照明器,比如,由激光(例如,he/ne或氩)或具有适当滤光片的水银弧光灯提供的光。例如,在488nm处的光可以用作具有单个感测区域的流式细胞仪中的发射波长。对于发射两个不同的波长的光的流式细胞仪,可以采用附加波长的发射光,其中,特定兴趣波长包括但不限于:535nm、635nm等。
与感测区域串联,检测器(例如如光电倍增管(或“pmt”)等聚光器)用于随着颗粒穿过感测区域并且由能量源照亮而记录穿过每个颗粒的光(在某些情况下被称为前向光散射)、与颗粒流动穿过感测区域的方向正交反射的光(在一些情况下被称为正交或侧向光散射)以及从颗粒发射的荧光(如果其标记有(多个)荧光标记)。前向光散射(或fsc)、正交光散射(ssc)和荧光发射(fl1、fl2等)中的每一者包括针对每个颗粒(即,每个“事件”)的单独参数。因此,可以从标记有两个不同荧光标记的颗粒中收集(并且记录)两个、三个或四个参数。
相应地,如所期望的,在以流式细胞术方式来测定颗粒时,可以通过使颗粒暴露于激发光以及测量在一个或多个检测通道中的每个颗粒的荧光来检测和唯一地标识颗粒。激发光可以来自一个或多个光源并且可以是狭窄的或宽带的。激发光源的示例包括激光器、发光二极管和弧光灯。可以在使用单个光源来进行激发之后测量,或可以在使用不同的光源来进行激发以后单独测量用于标识颗粒和与其相关联的结合复合物的检测通道中发射的荧光。如果分离的激发光源用于激发颗粒标记,则可以选择标记,从而使得所有标记都可由所使用的激发光源中的每个激发光源来激发。
流式细胞仪进一步包括如计算机等数据采集装置、分析装置和记录装置,其中,多个数据通道记录随着颗粒穿过感测区域而来自每个颗粒发射的光散射和荧光的每个检测器的数据。分析系统的目的是对颗粒进行分类和计数,其中,每个颗粒将自己呈现为一组数字化参数值。在本发明的方法中,在以流式细胞术方式测定(例如,检测、计数和/或分选)颗粒时,流式细胞仪可以被设置为根据所选参数而触发,以便将兴趣颗粒与背景和噪声区分。“触发”指用于检测参数的预设阈值并且可以用作用于检测颗粒穿过激光束的方式。检测到超过针对所选参数的阈值的事件触发针对颗粒的光散射和荧光数据的采集。并未针对引起低于阈值的反应的被测定介质中的颗粒或其他组成部分采集数据。触发参数可以是颗粒穿过光束而引起的对前向散射光的检测。然后,流式细胞仪检测并收集针对颗粒的光散射和荧光数据。
然后,基于针对整个群收集的数据,通过“门控”来进一步分析特定兴趣亚群。为了选择适当的门,标绘数据以便获得可能的最佳亚群分隔。通过在二维点图上标绘前向光散射(fsc)对侧向(即,正交)光散射(ssc)来执行此程序。然后,流式细胞仪操作员选择期望颗粒亚群(即,在门内的那些细胞)并且排除不在门内的颗粒。期望的话,操作员可以通过使用计算机屏幕上的光标来围绕期望亚群划线从而选择门。然后,通过标绘那些颗粒的其他参数(比如,荧光)来进一步分析门内仅有的那些颗粒。
如以上所讨论的,对颗粒的流式细胞术分析产生关于颗粒的定性信息和定量信息。期望的话,以上分析产生样本中的兴趣颗粒的计数。如此,以上流式细胞术分析方案提供了关于样本中的一种或多种不同类型的颗粒的数量。
实用性
如本文中所描述的主题系统、方法和计算机可读介质用于期望将颗粒收集自动化的各种不同应用,比如,用于将偏转微滴收集到流式细胞仪中的多井托盘中。本公开还用于期望将从生物样本中制备的细胞可以用于研究、实验室测试或用治疗的应用中。在一些实施例中,主题方法和设备可以促进获得从目标流体样本或组织生物样本中制备的个别细胞。例如,主题方法和系统促进从流体样本或组织样本中获得细胞以用作如癌症等疾病的研究或诊断样本。同样,主题方法和系统促进从流体样本或组织样本中获得细胞以用于治疗。与传统流式细胞术系统相比,本公开的方法和设备以提高的效率和低成本来从生物样本(例如,器官、组织、组织碎片、流体)中分隔和收集细胞。
以下示例是通过说明的方式而不是通过限制的方式来提供的。
实验
示例1:系统设计
设计了一种系统(例如,100,图1),所述系统包括分选器仪器(例如,101,图1);平台(例如,102,图1),所述平台支承容器托盘并且能够相对于分选器而连续地移动;以及控制器(例如,103,图1),所述控制器协调分选器与平台之间的相互作用。图1描绘了系统的框图。当分选器准备好进行分选时,其通知控制器。然后,控制器发起平台的移动。当平台处于将细胞存放在特定井中是可能的且足够可靠的位置中时,控制器通知分选器将液滴转移到井中。
起停轨迹
图2描绘了如从顶部观察的24井托盘(200)的示意图。虚线(201)示出了起停设计中分选器喷嘴相对于托盘的轨迹。所述轨迹开始于井a1的中心202并且结束于d1。
图4展示了平台随着时间沿着起停实施方式中的一条轴线的位移。在时间0处,喷嘴被定位成与第一井a1的中心相对。喷嘴在那里静止约0.75秒,然后在0.25秒内移动到a2的中心,再次静止0.75秒等等。耗费了将近6秒来处理6个井。
连续轨迹
图3描绘了本发明的实施例中的24井托盘(300)的一部分以及喷嘴的轨迹(虚线301)的一部分的示意图。此轨迹部分开始于井a1左方的点302并且延伸经过井a6。阴影区域304标记将液滴存放到井中是可能且可靠的区域。当喷嘴位于这种区域之内时,分选器从使得存放成为可能的控制器处取得命令。
图5展示了平台随着时间沿着一条轴线的连续位移轨迹。喷嘴开始于井a1的左边缘并且以与其在图4中所描绘的起停实施方式中移动的速度相同的速度连续地移动到井a6的右边缘(见图3)。耗费少于四倍的时间(1.5秒)来处理6个井。在两条虚线之间的垂直轴线上的区域501示出了将细胞存放到井a4(y轴)中是可靠的位移范围。在两条虚线之间的水平轴线上的区域502示出了将细胞存放到井a4(y轴)中是可靠的相应时间间隔(大约0.5秒)。
虽然存在所附条款,但是还通过以下条款来限定本文中阐述的公开内容:
1.一种用于分选细胞的系统,所述系统包括:
细胞分选器,所述细胞分选器被配置成用于产生被分析微滴流并且包括偏转器,所述偏转器能够将被分析微滴从所述被分析微滴流偏转到偏转微滴接收位置;
支撑平台,所述支撑平台包括容器并且被配置成在两个维度上连续地移动;以及
处理器,所述处理器可操作地耦合至存储器,所述存储器包括存储于其上的指令,所述指令用于确定所述容器与所述偏转微滴接收位置的对准并且在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送偏转信号。
2.根据条款1所述的系统,其中,所述存储器包括用于确定所述容器与所述偏转微滴接收位置对准的时隙的指令。
3.根据条款1或2所述的系统,其中,所述偏转信号包括初始偏转子信号和最终偏转子信号;并且所述存储器包括用于通过在所述时隙开始时向所述细胞分选器发送初始偏转子信号来产生所述偏转信号的指令,所述初始偏转子信号将所述偏转器配置为在被分析微滴出现时对其进行偏转。
4.根据条款3所述的系统,其中,用于产生所述偏转信号的所述指令进一步包括在所述时隙结束时向所述细胞分选器发送最终偏转子信号,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。
5.根据条款3所述的系统,其中,用于产生所述偏转信号的所述指令进一步包括在所述时隙期间已经偏转单个被分析微滴之后向所述细胞分选器发送最终偏转子信号,其中,所述最终偏转信号将所述偏转器配置为不对被分析微滴进行偏转。
6.根据前述条款中任一项所述的系统,其中,所述存储器包括用于确定来自所述细胞分选器的偏转微滴频率的算法。
7.根据条款6所述的系统,其中,所述存储器包括用于将所述时隙的长度与所述偏转微滴频率匹配的算法,由此确定所述细胞分选器在所述时隙期间偏转单个液滴。
8.根据条款7所述的系统,其中,所述存储器包括用于响应于来自所述细胞分选器的所述偏转微滴频率的变化而自动调整所述支撑平台的速度的指令。
9.根据前述条款中任一项所述的系统,其中,所述支撑平台包括两个或更多个容器,并且所述系统被配置成用于在z维度上经由所述支撑平台在x-y平面中的连续移动来自动且顺序地将所述两个或更多个容器与所述偏转微滴接收位置对准。
10.根据前述条款中任一项所述的系统,其中,所述系统被配置成用于偏转被确定为包括目标细胞的被分析微滴。
11.根据条款1所述的系统,其中,所述系统被配置成用于将单个微滴偏转到所述容器中。
12.根据前述条款中任一项所述的系统,其中,所述平台包括被配置为多井托盘的两个或更多个容器。
13.根据前述条款中任一项所述的系统,其中,所述系统是流式细胞仪系统。
14.一种包括存储器的计算机可读介质,所述存储器包括存储于其上的指令,所述指令包括:
用于在x-y平面中连续地移动包括容器的支撑平台的指令;
用于确定所述容器与所述偏转微滴接收位置的对准的算法;以及
用于在所述容器与偏转微滴接收位置对准时向细胞分选器发送偏转信号的指令,其中,所述细胞分选器包括偏转器,所述偏转器能够将被分析微滴从被分析微滴流偏转到所述偏转微滴接收位置。
15.根据条款14所述的介质,其中,所述存储器包括用于确定所述容器与所述偏转微滴接收位置对准的时隙的指令。
16.根据条款15所述的介质,其中,所述偏转信号包括初始偏转子信号和最终偏转子信号;并且
所述存储器包括用于通过在所述时隙开始时向所述细胞分选器发送初始偏转子信号来产生所述偏转信号的指令,所述初始偏转子信号将偏转器配置为在被分析微滴出现时对其进行偏转。
17.根据条款16所述的介质,其中,所述存储器进一步包括用于通过在所述时隙结束时向所述细胞分选器发送最终偏转子信号来产生所述偏转信号的指令,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。
18.根据条款16所述的介质,其中,所述存储器进一步包括用于在所述时隙期间已经偏转单个被分析微滴之后向所述细胞分选器发送最终偏转子信号的指令,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。
19.根据前述条款中任一项所述的介质,其中,所述支撑平台包括两个或更多个容器。
20.根据条款19所述的介质,其中,所述存储器包括用于在x-y平面中自动且连续地移动所述支撑平台以便在z维度上顺序地将所述两个或更多个容器与所述偏转微滴接收位置对准的指令。
21.根据前述条款中任一项所述的介质,其中,所述存储器包括用于将所述时隙的长度与所述偏转微滴频率匹配的算法,由此确定所述细胞分选器在所述时隙期间偏转单个液滴。
22.根据条款21所述的介质,其中,所述存储器包括用于响应于来自所述细胞分选器的所述偏转微滴频率的变化而调整所述支撑平台的速度的指令。
23.一种用于将细胞分选到容器中的方法,所述方法包括:
(a)将包括细胞的样本装载到用于分选细胞的系统中,所述系统包括:
细胞分选器,所述细胞分选器被配置成用于产生被分析微滴流并且包括偏转器,所述偏转器能够将被分析微滴偏转到偏转微滴接收位置;
支撑平台,所述支撑平台包括容器并且被配置成在两个维度上连续地移动;以及
处理器,所述处理器可操作地耦合至存储器,所述存储器包括存储于其上的指令,所述指令用于确定所述容器与所述偏转微滴接收位置的对准并且在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送偏转信号;以及
(b)在操作所述系统的同时分选所述细胞,从而使得所述系统进行操作以便在两个维度上连续地移动所述支撑平台并且在所述容器与所述偏转微滴接收位置对准时向所述细胞分选器发送所述偏转信号。
24.根据条款23所述的方法,其中,所述系统进行操作以便确定所述容器与所述偏转微滴接收位置对准的时隙。
25.根据条款24所述的方法,其中,所述偏转信号包括初始偏转子信号和最终偏转子信号;并且
所述系统进行操作以便通过在所述时隙开始时向所述细胞分选器发送初始偏转子信号来产生所述偏转信号,所述初始偏转子信号将所述偏转器配置为在被分析微滴出现时对其进行偏转。
26.根据条款25所述的方法,其中,所述系统进行操作以便在所述时隙结束时向所述细胞分选器发送最终偏转子信号,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。
27.根据条款25所述的方法,其中,所述系统进行操作以便在所述时隙期间已经偏转单个被分析微滴之后向所述细胞分选器发送最终偏转子信号,其中,所述最终偏转子信号将所述偏转器配置为不对被分析微滴进行偏转。
28.根据前述条款中任一项所述的方法,其中,所述支撑平台包括两个或更多个容器;并且所述方法包括在x-y平面中自动且连续地移动所述支撑平台以便在z维度上顺序地将所述两个或更多个容器与所述偏转微滴接收位置对准,由此将被分析细胞收集到所述两个或更多个容器中。
29.根据前述条款中任一项所述的方法,其中,所述支撑平台包括12个或更多个容器。
30.根据前述条款中任一项所述的方法,其中,所述分析微滴流包括被分选目标细胞。
31.根据前述条款中任一项所述的方法,其中,所述细胞分选器只有在确定目标细胞出现时才偏转被分析微滴。
32.根据条款28所述的方法,其中,所述方法包括将单个微滴偏转到所述两个或更多个容器中的每个容器中。
33.根据条款29所述的方法,其中,所述方法包括将单个目标细胞收集到所述12个或更多个容器中的每个容器中。
34.根据前述条款中任一项所述的方法,其中,所述系统进行操作以便将所述时隙的长度与所述偏转微滴频率匹配,由此确定所述细胞分选器在所述时隙期间偏转单个液滴。
35.根据条款34所述的方法,进一步包括响应于来自所述细胞分选器的所述偏转微滴频率的变化而自动调整所述支撑平台的速度。
36.根据条款29所述的方法,其中,将细胞分选到所述12个或更多个容器中的经过时间比包括不连续地移动所述支撑平台的控制方法少至少2倍。
尽管已经出于清楚理解的目的通过说明和示例的方式较为详细地描述了前述发明,但是本领域的技术人员根据本发明的教导很容易明白的是,在不偏离所附权利要求书的精神或范围的情况下,可以对其进行某些改变和修改。
因此,前述内容仅说明了本发明的原理。将理解的是,本领域的技术人员将能够设计不同的安排,尽管在本文中没有明确地描述或显示这些不同的安排,但是这些不同的安排将本发明的原理具体化并且包括在其精神和范围之内。另外,本文中所叙述的所有示例和条件性语言主要旨在辅助读者理解本发明的原理和诸位发明人所贡献的概念以便推动本领域发展,并且将被解释为不限于这种特别叙述的示例和条件。并且,本文中引用本发明的原理、方面和实施例的所有陈述及其特定示例旨在涵盖其结构等效物和功能等效物两者。另外,这种等效物旨在包括当前已知的等效物以及将来开发的等效物两者,即,所开发的执行相同功能的任何要素,而不考虑结构。因此,本发明的范围不旨在受限于本文中所示出和描述的示例性实施例。相反,本发明的范围和精神通过以下内容来具体化。
- 还没有人留言评论。精彩留言会获得点赞!