天门冬氨酸氨基转移酶检测试剂盒的制作方法
本发明属于临床体外诊断试剂技术领域,涉及天门冬氨酸氨基转移酶检测试剂盒。
背景技术:
:
天门冬氨酸氨基转移酶(AST)也称为谷草转氨酶,主要存在于心肌细胞中,肝细胞次之。在心肌细胞内含量较多,当心肌梗死时,血清中AST活力增高,在发病后6-12h之内显著增高,在48h达到高峰,约在3-5天恢复正常。血清中AST也可来源于肝细胞,各种肝病可引起血清中AST的升高,中毒性肝炎还可更高。肌炎症、胸膜炎、肾炎等也可引起血清AST的轻度增高,还可能存在心肌细胞、肝细胞及骨骼肌损伤。临床上主要用于病毒性肝炎、阻塞性黄疸、心肌梗死的辅助诊断。
目前体外检测天门冬氨酸氨基转移酶(AST)的方法主要有赖氏法、酶偶联比色法及连续监测法(速率法)。赖氏法的缺点是标本AST活性高时,草酰乙酸对AST显示的反馈抑制,使测定结果偏低;酶偶联比色法所用的氯化硝基四氮唑蓝(NBT)有毒,可能有致癌性,不满足绿色原则;连续监测法的优点是可以确定线性期并计算每分钟吸光度的变化(ΔA/min),根据此值再准确地计算酶活性,可以利用全自动生化分析仪进行检测;酶和底物反应的特异性好,检测结果准确度高。以上三种方法相比较,采用连续监测法较佳。
本发明的试剂盒主要采用连续监测法进行检测,该方法是国际临床化学和实验室医学联盟(IFCC)推荐方法。其检测原理为:AST催化L-天门冬氨酸的氨基转移至α-酮戊二酸,生成草酰乙酸和L-谷氨酸。苹果酸脱氢酶(MDH)催化草酰乙酸还原的同时将还原型辅酶(NADH)氧化成氧化型辅酶(NAD+),由于NADH在340nm处有特征吸收,所以NADH的下降速率和AST的活力成正比。反应式如下:
本发明涉及的天门冬氨酸氨基转移酶检测试剂盒,无需样本前处理,可直接利用全自动生化分析仪进行大批量样本检测,操作简单、准确度高、稳定性好,适合临床应用推广。
技术实现要素:
:
本发明的目的在于提供天门冬氨酸氨基转移酶检测试剂盒供临床应用,主要解决现有AST检测领域存在的准确度低、操作繁琐、污染环境、试剂不稳定等问题。
为了解决本发明内源性α-酮戊二酸对天门冬氨酸(AST)测定的干扰,采用如下技术方案:采用两步法检测,血清与(缺少α-酮戊二酸)的底物溶液混合,37℃保温5min,使样品中所含内源性α-酮戊二酸引起的副反应进行完毕。然后加入α-酮戊二酸启动AST的催化反应,在主波长340nm处连续监测吸光度下降速率,根据线性反应期吸光度下降速率(-ΔA/min),计算出AST活力。
本发明提供的试剂盒由试剂1和试剂2组成,其中试剂1的组成和成份如下:
Tris-HCl缓冲液120mmol/L-180mmol/L,PH=8.2
L-天门冬氨酸400mmol/L-600mmol/L
还原型辅酶(NADH)0.2mmol/L-0.4mmol/L
苹果酸脱氢酶(MDH)800U/L-1200U/L
酶保护剂
稳定剂
防腐剂
试剂2的组成和成份如下:
Tris-HCl缓冲液60mmol/L-100mmol/L,PH=7.4
α-酮戊二酸60mmol/L-80mmol/L
稳定剂
防腐剂
所述酶保护剂选自牛血清白蛋白(BSA)或甘油与糖类中的一种或多种组合物,其用量为BSA0.1%-2%,甘油5%-20%,优选为BSA 0.5%-1.5%,甘油10%-15%。
以上所述糖类可选自葡萄糖、蔗糖、麦芽糖、果糖中的一种或多种,其用量为1g/L-15g/L,优选为5g/L-10g/L。
所述试剂1和试剂2的稳定剂均选自KCl及表面活性剂组合物,其用量为KCl 1g/L-15g/L,优选为5g/L-10g/L。
以上所述表面活性剂可选自吐温-20(Tween-20)、吐温-80(Tween-80)、曲拉通X-100(Triton X-100)、聚乙二醇6000(PEG 6000)及聚乙二醇8000(PEG 8000)中的一种或多种,其用量为0.1%-2%,优选为0.5%-1.5%。
所述试剂1和试剂2的防腐剂均可选自NaN3或Proclin-300,其用量为NaN30.1g/L-2g/L,Proclin-300 0.1%-2%,优选为NaN30.6g/L-1g/L,Proclin-300 0.5%-1%。
本发明天门冬氨酸氨基转移酶(AST)检测试剂盒适用于各类全自动生化分析仪,现于全自动生化分析仪BS-420上的应用,其具体使用方法如下:
表1样本检测操作程序
计算方法:样品中的AST含量(U/L)=ΔAT/min×F
ΔAT/min:测定管平均每分钟相对空白管吸光度变化
注:TV:试剂样品总体积,SV为样品体积; 6.22:NADH在340nm处的毫摩尔分子吸光系数;
1.0:比色皿光径(cm);1000:U/mL到U/L的转换系数。
本发明所使用的质控品为罗氏高、低值质控品;所测样品为不溶血血清。
有益效果:本发明天门冬氨酸氨基转移酶检测试剂盒为液体双试剂,采用两步法,有效消除内源性α-酮戊二酸干扰,提高了AST测定的准确度;本发明试剂盒中加入酶保护剂和稳定剂,提高了AST试剂盒的稳定性,于37℃水浴可稳定至少一周,说明2-8℃保存可以至少稳定一年。
以下结合具体实施例进一步说明本发明,应理解,具体实施方式仅用于说明本发明,而非限制本发明。
附图说明:
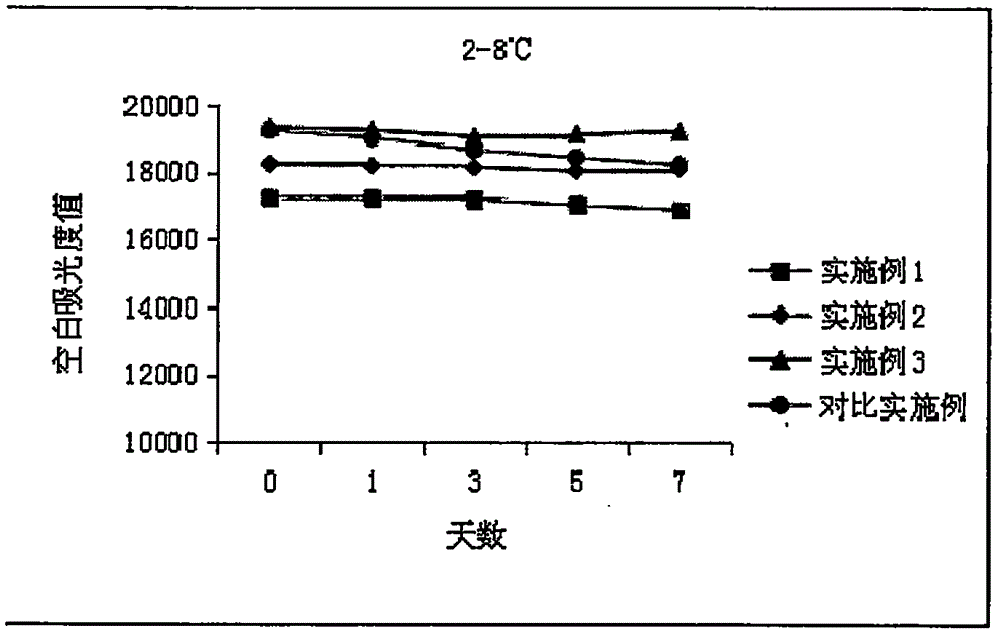
图1是本发明实施例1-3及对比实施例2-8℃保存一周的空白吸光度变化对比试验结果图;
图2是本发明实施例1-3及对比实施例37℃水浴一周的空白吸光度变化对比试验结果图。
具体实施方式
实施例1
天门冬氨酸氨基转移酶检测试剂盒,由试剂1和试剂2组成,具体成分及含量如下:
试剂1的组成:
Tris-HCl缓冲液120mmol/L,PH=8.2
L-天门冬氨酸400mmol/L
NADH 0.2mmol/L
苹果酸脱氢酶800U/L
KCl 5g/L
吐温-20 0.5%
BSA 1%
蔗糖5g/L
Proclin-300 0.5%
试剂2的组成:
Tris-HCl缓冲液100mmol/L,PH=7.4
α-酮戊二酸60mmol/L
KCl 6g/L
PEG 6000 0.5%
Proclin-300 0.5%
实施例2
天门冬氨酸氨基转移酶检测试剂盒,由试剂1和试剂2组成,具体成分及含量如下:
试剂1的组成:
Tris-HCl缓冲液150mmol/L,PH=8.2
L-天门冬氨酸500mmol/L
NADH 0.3mmol/L
苹果酸脱氢酶1000U/L
KCl 8g/L
曲拉通X-100 1%
甘油10%
麦芽糖6g/L
Proclin-300 1%
试剂2的组成:
Tris-HCl缓冲液80mmol/L,PH=7.4
α-酮戊二酸70mmol/L
KCl 8g/L
PEG 8000 1%
Proclin-300 1%
实施例3
天门冬氨酸氨基转移酶检测试剂盒,由试剂1和试剂2组成,具体成分及含量如下:
试剂1的组成:
Tris-HCl缓冲液180mmol/L,PH=8.2
L-天门冬氨酸600mmol/L
NADH 0.4mmol/L
苹果酸脱氢酶1200U/L
KCl 10g/L
曲拉通X-100 1.5%
PEG 8000 1.5%
甘油15%
果糖6g/L
葡糖糖6g/L
NaN3 1g/L
试剂2的组成:
Tris-HCl缓冲液60mmol/L,PH=7.4
α-酮戊二酸80mmol/L
KCl 10g/L
吐温-80 1%
PEG 6000 1%
NaN3 0.6g/L
对比实施例
不加稳定剂和酶保护剂的天门冬氨酸氨基转移酶检测试剂盒,由试剂1和试剂2组成,具体成分及含量如下:
试剂1的组成:
Tris-HCl缓冲液180mmol/L,PH=8.2
L-天门冬氨酸600mmol/L
NADH 0.4mmol/L
苹果酸脱氢酶1200U/L
NaN3 1g/L
试剂2的组成:
Tris-HCl缓冲液60mmol/L,PH=7.4
α-酮戊二酸80mmol/L
NaN3 0.6g/L
将本发明实施例1-3及对比实施例进行准确度验证试验。质控品选用罗氏高值质控(AST靶值:102U/L,靶值范围(±10%):91.8U/L-112.2U/L);罗氏低值质控(AST靶值:38U/L,靶值范围(±10%):34.2U/L-41.8U/L)。采用BS-420全自动生化分析仪进行检测,具体操作方法如表一所述,采用单点定标法定标后,AST测定值及空白吸光度值可从仪器上直接读取,为了减少偶然误差,重复测定三次取均值。
实施例1-3及对比实施例准确度结果如下:
表2实施例1-3及对比实施例准确度比较
将本发明实施例1-3及对比实施例进行稳定性验证试验。将以上四种试剂盒每种平均分成两份,一份至于2-8℃保存,另一份至于37℃水浴中保存,每隔一天测定一次,连续监测一周,观察空白吸光度变化及血清测定值(血清定值52.3U/L,允许误差范围(±10%):47.07U/L-57.53U/L),通过空白吸光度的变化和准确度的测定比较试剂稳定性。
表3实施例1试剂盒稳定性数据
表4实施例2试剂盒稳定性数据
表5实施例3试剂盒稳定性数据
表6对比实施例试剂盒稳定性数据
由表2可知实施例1-3制得的试剂盒准确度均在允许的误差范围(±10%)内,而对比实施例制得的试剂盒准确度超出了误差允许范围;由图1和图2可以看出,实施例1-3制得的试剂盒的稳定性明显强于对比实施例制得的试剂盒。实施例1-3制得的试剂盒虽然试剂空白有一定程度的下降,但是下降的幅度不大,在允许范围内,说明加入合适的稳定剂和酶保护剂可以减缓NADH的衰减、保护酶的活性,进而提高试剂盒的稳定性,延长试剂盒的保存期。
- 还没有人留言评论。精彩留言会获得点赞!