一种富含谷胱甘肽酵母抽提物中氧化型谷胱甘肽杂质的检测方法与流程
本发明涉及一种富含谷胱甘肽酵母抽提物中氧化型谷胱甘肽杂质的检测方法,具体涉及一种富含谷胱甘肽酵母发酵产品中氧化型谷胱甘肽杂质的测定方法。
背景技术:
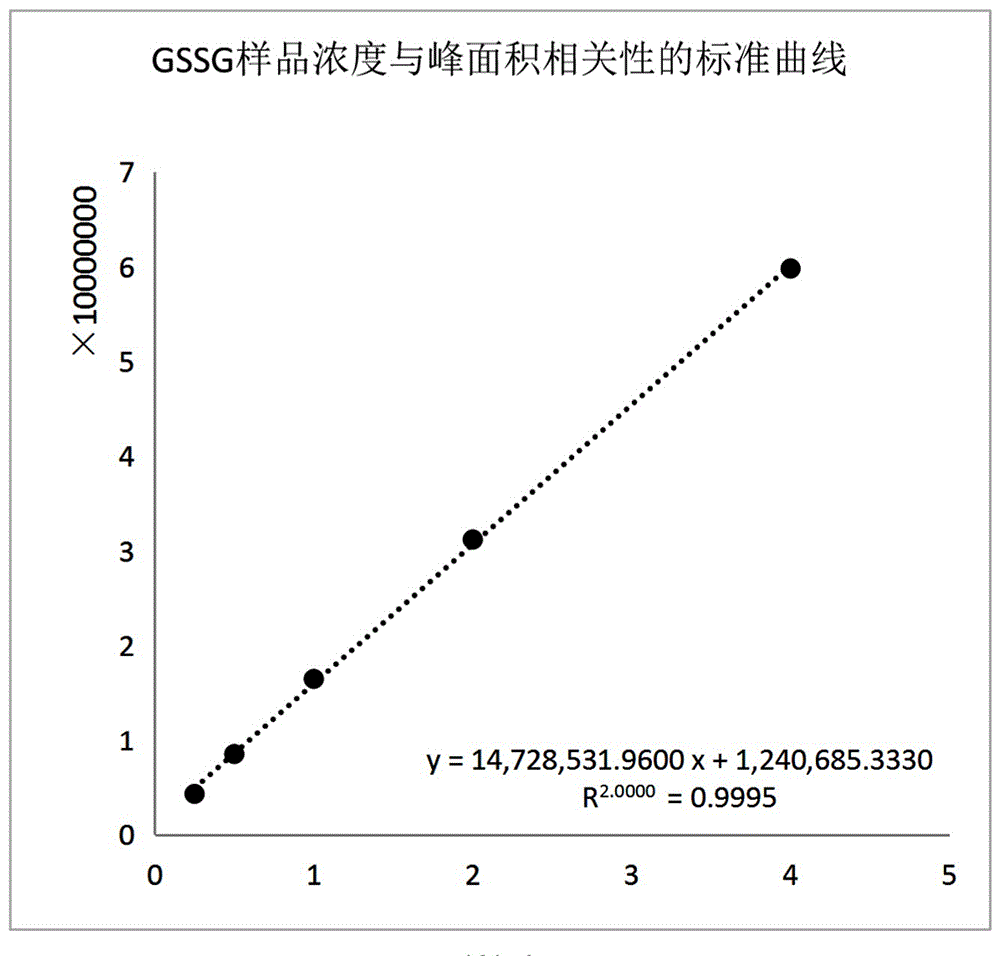
:还原型谷胱甘肽(Glutathione,GSH)作为一种重要的药物试剂,在临床上用途极广,同时还原型谷胱甘肽的抗氧化性能又使得它在食品和化妆品加工业中作为添加剂而受到青睐。但是,还原型谷胱甘肽及其水溶液极不稳定,容易发生质变,生成氧化型谷胱甘肽(GSSG),半胱氨酰甘氨酸(Cys-Gly),胱氨酸(Cy2)和甘氨酸(Gly),其中氧化型谷胱甘肽是主要质变成分。如何快速、简单、高效检测富含谷胱甘肽酵母抽提物产品中氧化型谷胱甘肽杂质的含量,不但对酵母发酵生产GSH工艺质量控制至关重要,而且对GSH在食药领域相关产品的质量标准控制与提高也显得尤为关键。目前文献已有报道采用HPLC方法检测氧化型谷胱甘肽含量,但氧化型谷胱甘肽在色谱柱中保留时间过短,容易与酵母细胞中其他化学成分叠加无法可控的与其他杂质区别。技术实现要素:本发明的目的在于,提供一种富含谷胱甘肽酵母抽提物中氧化型谷胱甘肽杂质的检测方法,该方法能够有效地检测谷胱甘肽产品中杂质氧化型谷胱甘肽的含量,从为富含还原型谷胱甘肽酵母抽提物的生产工艺质量控制提供有效保障。本发明的目的是这样实现的:一种富含谷胱甘肽酵母抽提物中氧化型谷胱甘肽杂质的检测方法,其特征在于包括以下步骤:(1)选择对照物质:选择氧化型谷胱甘肽作为对照物质,纯度>99.9%;(2)制备标准品溶液:取氧化型谷胱甘肽标准品80mg,加入去离子水溶解,定容至10mL,摇匀,得到氧化型谷胱甘肽标准储备液(8mg/mL);依次配制成4mg/mL、2mg/mL、1mg/mL、0.5mg/mL和0.25mg/mL的储备液;(3)制备供试品溶液:取安琪酵母股份有限公司生产的酵母粉1g,加入10mL去离子水,80℃下提取15分钟,迅速置于冰水中冷却至室温,4000rpm/min下离心10分钟,取上清液,得到供试品溶液;(4)液相色谱测定:分别取氧化型谷胱甘肽标准品溶液注入高效液相色谱仪,记录峰面积,以氧化型谷胱甘肽浓度为横坐标,相应的峰面积为纵坐标进行线性回归分析,制得线性方程。取稀释n倍的供试品溶液(所述的稀释的供试品溶液为稀释后氧化型GSH浓度介于1.0至3.0mg/mL之间的供试品溶液,进一步优选为稀释后氧化型GSH浓度为2.0mg/mL的供试品溶液)注入高效液相色谱仪,供试品色谱图中出峰时间及峰形与对照品溶液色谱图中氧化型谷胱甘肽的出峰时间及峰形进行比对,判定供试品溶液含有氧化型谷胱甘肽物质。将供试品色谱图中氧化型谷胱甘肽峰面积数值(介于氧化型谷胱甘肽标准品最小与最大浓度对应的峰面积之间)代入线性方程,即可计算出供试品中氧化型谷胱甘肽的含量。所用的高效液相色谱仪中色谱柱为:VenusilXBPC18柱(5μm×10×250mm);流动相为甲醇-水二元流动相,其中水相包括1L去离子水,2.2g/L庚烷磺酸钠,6.8g/L磷酸二氢钾,pH调节范围为2.0-3.0,优选为2.5。甲醇:水相的混合体积比范围为20:80-2:98,优选为16:84。流动相使用前经0.45μm滤膜抽滤并脱气;流速:1mL/min;进样体积:10μm;柱温:25℃;检测波长:203nm。所用的甲醇-水二元流动相中,水相pH调节范围为2.0-3.0。在此范围内,固定甲醇:水相的混合体积比,pH越小,氧化型谷胱甘肽的保留时间越长。固定水相pH,甲醇:水相的混合体积比范围为20:80-8:92混合体积比越小,氧化型谷胱甘肽的保留时间越长。固定甲醇:水相的混合体积比为16:84,通过调节水相pH值,氧化型谷胱甘肽的保留时间可控制在6.0-30.0分钟内。通过步骤(4)中供试品溶液所得色谱图中氧化型谷胱甘肽的峰面积,按下述计算公式可得到供试品中氧化型谷胱甘肽的含量。计算公式如下:其中x-供试品峰面积,n-供试品稀释倍数,y-供试品中氧化型谷胱甘肽的含量,单位为mg/mL。根据权利要求2所述的酵母抽提物中氧化型谷胱甘肽的检测方法,其特征在于:所用的甲醇-水二元流动相中,优化合适条件为pH值2.5,甲醇:水相的混合体积比为16:84。通过步骤(4)制得的线性方程相关系数平方R2为0.9995,该方法的检测浓度范围为0.25-4.00mg/mL之间呈现良好的线性关系;按信噪比S/N为3计,氧化型谷胱甘肽最小检测浓度为7μg/mL。本发明提供的富含谷胱甘肽酵母抽提物中氧化型谷胱甘肽杂质的检测方法,该方法操作简单、高效,可定性或定量检测谷胱甘肽产品中氧化型谷胱甘肽的含量,为控制富含还原型谷胱甘肽的酵母产品提供了良好的生产质量保障。附图说明图1是标准品溶液在高甲醇浓度二元流动相下的高效液相色谱图。图2是氧化型谷胱甘肽标准曲线图。图3是第1批次的酵母抽提物样品供试品溶液高效液相色谱图。具体实施方式实施例1高效液相色谱仪分析条件优化二元流动相为甲醇-水相(水相中,1L去离子水,含有2.2g/L庚烷磺酸钠,6.8g/L磷酸二氢钾,pH值为4.5),甲醇:水相的混合体积比8:92,在色谱柱VenusilXBPC18柱(5μm×10×250mm)上进行标准品分析实验。结果氧化型谷胱甘肽在色谱柱上出峰时间为3min保留时间过短。用磷酸分别调节二元流动相中水相的pH为4.5,4.0,3.5,3.0,2.5,甲醇:水相的混合体积比8:92,在色谱柱VenusilXBPC18柱(5μm×10×250mm)上进行标准品分析实验。结果表明:二元流动相中水相pH值对氧化型谷胱甘肽在色谱柱上的保留时间有重要影响。pH值越小,保留时间越长;当pH值低于3.0时,氧化型谷胱甘肽将难以洗脱下来。当二元流动相为甲醇-水相(水相中,1L去离子水,含有2.2g/L庚烷磺酸钠,6.8g/L磷酸二氢钾,水相的pH值为2.5),调节甲醇:水相的混合体积比,在色谱柱VenusilXBPC18柱(5μm×10×250mm)上进行标准品分析实验。结果表明:甲醇:水相的混合体积比越小,氧化型谷胱甘肽的保留时间越长超过8:92难以洗脱。用磷酸分别调节二元流动相中水相的pH为2.3,2.4,2.5,2.6,2.7,2.8,2.9,甲醇:水相的混合体积比16:84,在色谱柱VenusilXBPC18柱(5μm×10×250mm)上进行标准品分析实验。结果表明:当水相pH为2.5时,洗脱出来的氧化型谷胱甘肽保留时间为20min,且与还原型谷胱甘肽同方法保留时间相差较大分离较高。图1是标准品溶液在高甲醇浓度二元流动相下的高效液相色谱图。色谱柱为:VenusilXBPC18柱(5μm×10×250mm);流动相为甲醇-水二元流动相,其中水相包括1L去离子水,2.2g/L庚烷磺酸钠,6.8g/L磷酸二氢钾,pH值为2.5。甲醇:水相的混合体积比为16:84。流动相使用前经0.45μm滤膜抽滤并脱气;流速:1mL/min;进样体积:10μm;柱温:25℃;检测波长:203nm。实施例2氧化型谷胱甘肽标准曲线与回归方程制作取氧化型谷胱甘肽标准品80mg,加入去离子水溶解,定容至10mL,摇匀,得到氧化型谷胱甘肽标准储备液(8mg/mL);依次配制成4mg/mL、2mg/mL、1mg/mL、0.5mg/mL和0.25mg/mL的储备液;进行HPLC测定,记录峰面积,以氧化型谷胱甘肽浓度为横坐标,相应的峰面积为纵坐标进行线性回归,得线性为:y=14728532x+1240685,R2=0.9995(其中x为氧化型GSH浓度,y为相应的峰面积);结果表明氧化型谷胱甘肽质量浓度在0.25-4mg/mL之间呈现良好的线性关系;按信噪比S/N为3计,氧化型谷胱甘肽最小检测浓度为7μg/mL。实施例3氧化型谷胱甘肽样品精密度与准确度测定分别配置高中低三种不同浓度的氧化型谷胱甘肽样品,按实施例2“氧化型谷胱甘肽标准曲线与回归方程制作”项下操作,日内测定5次,日间测定3天,记录峰面积带入氧化型谷胱甘肽标准曲线,计算回收率和日内、日间相对标准差。结果见表1。表1精密度和准确度测定结果加样浓度mg/mL测得浓度mg/mL日内RSD%回收率%0.280.2750.0061.3598.331.000.9670.0110.5496.703.203.1180.0851.7197.43加样浓度mg/mL测得浓度mg/mL日间RSD%回收率%0.340.3350.9698.631.201.1810.8898.393.523.5820.62101.77实施例4供试品中氧化型谷胱甘肽含量检测取安琪酵母股份有限公司生产的不同批次酵母粉各1g,加入10mL去离子水,80℃下提取15分钟,迅速置于冰水中冷却至室温,4000rpm/min下离心10分钟,取上清液,稀释5倍得到供试品溶液,进行氧化型谷胱甘肽含量(mg/mL)检测。依据公式,转化成酵母粉中氧化型谷胱甘肽含量(mg/g)。结果见表2。表2不同批次酵母抽提物中氧化型谷胱甘肽含量测定结果不同生产批次酵母抽提物第1批次第2批次第3批次供试品溶液浓度(mg/mL)0.5010.5090.560还原型GSH含量(mg/g)25.0525.4528.00当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1