一种大麻品种间差异性比较的形态学观察方法与流程
本发明属于植物形态学技术领域,涉及一种大麻品种间形态学差异性的评价方法。
背景技术:
大麻(Cannabis sativa L.),又称线麻、火麻等,是大麻科(Cannabinaceae),大麻属,一年生直立草本。原产锡金、不丹等国,现各国均有野生或栽培,我国各地也有栽培。根据植株中四氢大麻酚含量和用途划分,可将大麻划分为纤维用、籽用(THC<0.3%)和药用(THC>0.3%)3类。大麻纤维是人类历史上应用最早的纤维,其韧度高、可自然分解,是优秀的纺织原料。用大麻纤维编织的衣物具有抑菌防臭、吸湿排汗、耐晒防腐、防紫外线效果好等优良品质。大麻籽油可通过压榨或浸取等方法获得,其在工业上可作为肥皂和油漆等产品的原料,经精炼后亦可食用。除此之外,大麻还是板材等建筑材料的优质原料。大麻全草均可入药,其主要活性成分包括:大麻酚(CDB)、大麻二酚(CBN)、大麻环萜酚(CBC)和四氢大麻酚(THC)等。在古代,草药医师就已经开始用大麻止痛,治疗慢性风湿性关节炎、惊厥等各种疾病。现代研究还表明大麻的部分成分对治疗青光眼、多发性硬化症、中风后遗症、癌症化疗引起的恶心与呕吐等有特效。
目前,大麻植物育种主要采用系统育种法和杂交育种法。种植资源主要来源于各科研机构间的相互交换或由乌克兰、俄罗斯和波兰等国引进。新品种通常也是利用这些种质资源进行杂交选育和筛选后所得。但种质资源引入时常无法得到引入品种亲本信息,导致通过不同途径所引入的大麻品种的外形和工艺性状可能极为相似,甚至是同一品种的近缘种情况,给新品种选育工作带来极大不便,而与之相对应也增加了科研资源的消耗。因此,为提高科研资源利用率、筛选合适亲本、提高新品种选育效率,利用简单、快速、低成本的评价方法对大麻品种间差异性进行初步评价的工作十分必要,但目前大麻品种间形态学差异性的评价方法尚未见报导。
技术实现要素:
本发明的目的是提供一种简单、快速、低成本的大麻品种间差异性比较的形态学观察方法。
本发明的目的是通过以下技术方案实现的:
一种大麻品种差异性比较形态学观察方法,包括如下步骤:
一、获取观察植株
选取相同栽培条件下种植的处于同一幼苗期、现蕾期、盛花期或工艺成熟期的大麻品种植株作为待比较植株;
二、收集植株形态学数据
(1)将取材部位分为如下4个区:
A区:大麻茎下1/3处;B区:大麻茎1/2处;C区:大麻茎上1/3处;D区:大麻茎顶端。
(2)外形数据观测:
(a)幼苗期观测指标:
株高、B区直径、第一真叶叶长、叶片长、叶片宽、叶柄长。
(b)现蕾期、盛花期、工艺成熟期观测指标:
株高、A区直径、B区直径、B区节长、C区直径、叶长、中裂片长、中裂片宽、叶柄长。
(3)显微结构数据观测
(a)取材:
分别截取茎A、B、C区0.5~3cm长茎杆,D区截取从植株顶端至其下0.5~3cm处茎杆。
幼苗期取第一真叶,现蕾期、盛花期、工艺成熟期切取距离C区最近叶片中裂片中央区域2~4cm2叶片。
将上述材料置于FAA固定液或70~100%乙醇中固定24h以上。
(b)茎结构观测:
取固定好的茎材料,用双面刀片制作茎横切面徒手切片将切片置于载玻片上,滴加蒸馏水或50%甘油,盖上盖玻片,显微镜下观察并测量。
(c)叶片毛状体数量观测:
将叶片腹面朝上置于载玻片上,滴加蒸馏水或50%甘油,盖上盖玻片,显微镜下观察并计数。
(d)幼苗期观测指标:
B区髓直径、B区髓腔直径、叶片毛状体数、乳汁管数量。
(e)现蕾期观测指标:
A区髓直径、A区初生纤维层厚度、B区髓直径、B区初生纤维层厚度、B区初生纤维层面积、C区髓直径、C区初生纤维层厚度、叶片毛状体数、乳汁管数量。
(f)盛花期、工艺成熟期观测指标:
A区髓直径、A区初生纤维层厚度、A区次生纤维层厚度、B区髓直径、B区初生纤维层厚度、B区初生纤维层面积、C区髓直径、C区初生纤维层厚度、叶片毛状体数、乳汁管数量。
三、数据变型
对上述获得的大麻形态指标转化为表1所示代码作为参比特征,其中:
幼苗期参比特征:A、B、C、E、F、G、M、N;
现蕾期参比特征:A、B、C、D、E、F、G、H、J、K、L、M、O、P;
盛花期及工艺成熟期参比特征:A、B、C、D、E、F、G、H、I、J、K、L、M、O、P。
四、大麻品种差异性比较
(1)差异显著性分析
对处于同一发育时期的待比较品种,利用统计软件对参比特征进行单因素方差分析。
(2)形态指标差异性评分
经单因素方差分析后,差异不显著计“0”分,差异显著计“1”分,差异极显著计“2”分;待完成所有形态指标的差异性评分后,计算总得分,分值越高则表示待比较植株在此发育时期的形态学差异性就越大,反之则小。
本发明具有如下优点:
1、该方法适用于品种间差异性的快速比较。
2、实验效率高、操作方法简便,可操作性强。
3、实验成本低,仪器方面仅需1套具有测量功能的显微成像系统,实验涉及工具及试剂仅有双面刀片、乙醇、甲醛、冰醋酸、甘油和蒸馏水。
4、若用乙醇作为固定液,则整个实验过程均未使用有毒药品,安全性高。
附图说明
图1为材料取材区域划分示意图;
图2为B区初生纤维层面积测量部位示意图;
图3为D区乳汁管数量统计位置示意图。
具体实施方式
下面结合附图对本发明的技术方案作进一步的说明,但并不局限于此,凡是对本发明技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,均应涵盖在本发明的保护范围中。
具体实施方式一:本实施方式提供了一种大麻品种差异性比较形态学观察方法,具体实施步骤如下:
1、获取观察植株
选取相同栽培条件下种植的处于同一发育时期待比较大麻品种植株(如外形和工艺性状极为相似或需判断是否是近缘种的大麻品种)各5株作为材料。发育时期可选择,幼苗期(4~6叶期)、现蕾期、盛花期及工艺成熟期。
2、收集形态学数据
为便于描述,将取材部位分为4个区。A区:大麻茎下1/3处;B区:大麻茎1/2处;C区:大麻茎上1/3处;D区:大麻茎顶端。幼苗叶特征为第一真叶特征。现蕾期、盛花期及工业成熟期叶特征为C区叶特征或距离C区最近叶特征。具体区域划分如图1所示。
(1)外形数据观测方法及部位
(a)外形数据观测方法:
外形数据用卷尺及游标卡尺测量。
(b)幼苗期观测指标:
株高、B区直径、第一真叶叶长、叶片长、叶片宽、叶柄长。
(c)现蕾期观测指标:
株高、A区直径、B区直径、B区节长、C区直径、叶长、中裂片长、中裂片宽、叶柄长。
(d)盛花期观测指标:
同现蕾期。
(e)工艺成熟期观测指标:
同现蕾期。
(2)显微结构数据观测方法及部位
(a)取材:
分别截取茎A、B、C区0.5~3cm长茎杆,D区截取从植株顶端至其下0.5~3cm处茎杆。切取距离C区最近叶片中裂片(幼苗期取第一真叶)中央区域2~4cm2叶片。将上述材料置于FAA固定液(甲醛、冰醋酸、70%乙醇,按照1:1:18体积比混合而成)或70~100%乙醇(85%以上乙醇固定的叶片,在观察前需用蒸馏水浸泡5min)中固定24h以上。
(b)茎结构观测方法:
取固定好的茎材料,用双面刀片制作茎横切面徒手切片,切片厚度10~500μm均可。将切片置于载玻片上,滴加蒸馏水或50%甘油,盖上盖玻片,显微镜下观察并测量。
(c)叶片毛状体数量观测方法:
将叶片腹面朝上置于载玻片上,滴加蒸馏水或50%甘油,盖上盖玻片,显微镜下观察并计数。
(d)幼苗期观测指标:
B区髓直径;B区髓腔直径;叶片毛状体数;乳汁管数量。
(e)现蕾期观测指标:
A区髓直径;A区初生纤维层厚度;B区髓直径;B区初生纤维层厚度;B区初生纤维层面积;C区髓直径;C区初生纤维层厚度;叶片毛状体数;乳汁管数量。
(f)盛花期观测指标:
A区髓直径;A区初生纤维层厚度;A区次生纤维层厚度;B区髓直径;B区初生纤维层厚度;B区初生纤维层面积;C区髓直径;C区初生纤维层厚度;叶片毛状体数;乳汁管数量。
(e)工艺成熟期观测指标:
同盛花期。
(f)观测指标补充说明:
①所有观测数值均为所观测部位各指标最大值(例如,大麻茎横切面外围轮廓似椭圆形时,该部位直径为椭圆形的长轴长度)。
②初生纤维层厚度:茎横切面随机测得5个初生纤维层厚度的平均值。
③次生纤维层厚度:茎横切面随机测量5个次生纤维层厚度的平均值。
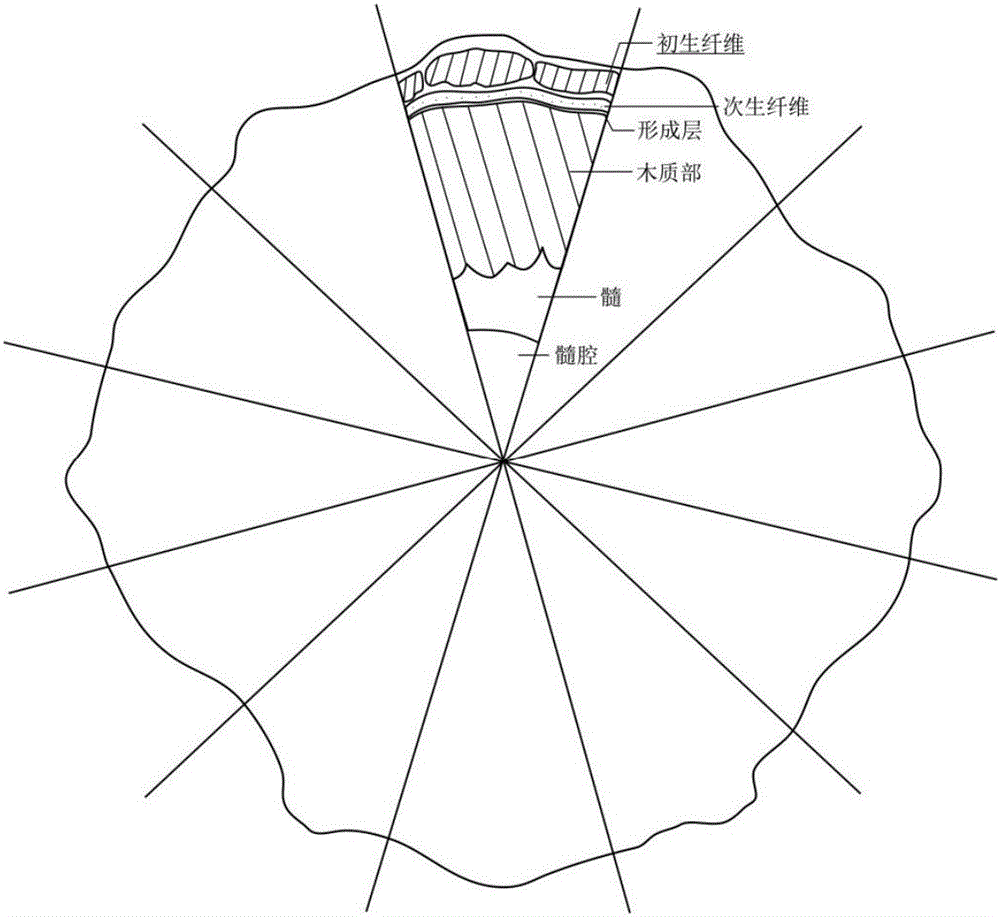
④初生纤维层面积:以B区茎横切面中心为原点,将茎按照辐射状均等分割为12份,若茎横切面近圆形,则随机选取其中一份,用显微成像系统直接测量初生纤维层横切面面积。若茎横切面近椭圆形,则测量椭圆形最短轴附近初生纤维层面积,具体取样位置如图2所示。
⑤乳汁管数量:以D区茎横切面近椭圆形,中心为原点,将茎按照辐射状均等分割为12份,测量椭圆形最短轴附近1份区域中乳汁管数量,具体取样位置如图3所示。
⑥叶片毛状体数:叶片腹面中随机选取3个视野(避开叶脉),利用显微成像系统对每个视野中1mm2面积中的毛状体数量进行统计,取平均值。
3、数据变型
除株高、叶长及乳汁管数量3个指标直接使用外,其余测量数据需进行变型处理,并用字母A、B、C……作为直接使用指标及变型后新形成指标的代码,具体内容见表1。
表1大麻形态指标汇总表
4、大麻品种差异性比较
(1)差异显著性分析
对处于同一发育时期的待比较品种,利用SPSS、DPS或EXCEL等统计软件对表1中的指标进行单因素方差分析(不同发育时期参比特征不尽相同,具体内容如下,幼苗期参比特征:A、B、C、E、F、G、M、N;现蕾期参比特征:A、B、C、D、E、F、G、H、J、K、L、M、O、P;盛花期及工艺成熟期参比特征:A、B、C、D、E、F、G、H、I、J、K、L、M、O、P)。
(2)形态指标差异性评分
处于相同发育时期不同品种的同一指标,经单因素方差分析后,差异不显著计“0”分,差异显著计“1”分,差异极显著计“2”分。
待完成所有形态指标的差异性评分后,计算总得分。此得分既为此2个品种的形态学差异性得分。分值越高则表示此不同植株在此发育时期的形态学差异性就越大,反之则小。在杂交育种选择亲本时建议先选择工艺性状好,且形态学差异性大的品种作为杂交育种的父母本。
具体实施方式二:本实施方式提供了一种大麻品种差异性比较形态学观察方法,具体实施步骤如下:
1、获取观察植株
采集相同栽培条件下种植的大麻品种“火麻1号”及“Silesia”盛花期植株各5株。
2、收集形态学数据
(1)外形数据观测方法及指标
(a)外形数据观测方法:
外形数据用卷尺及游标卡尺测量。
(b)观测指标:
株高、A区直径、B区直径、B区节长、C区直径、叶长、中裂片长、中裂片宽、叶柄长。
(2)显微结构数据观测方法及指标
(a)取材:
分别截取茎A、B、C区3cm长茎杆,D区截取从植株顶端至其下3cm处茎杆。
切取距离C区最近叶片中裂片中央区域4cm2叶片。
将上述材料置于FAA固定液(甲醛、冰醋酸、70%乙醇,按照1:1:18体积比混合而成)中固定24h以上。
(b)茎结构观测方法:
取固定好的茎材料,用双面刀片制作茎横切面徒手切片。将切片置于载玻片上,滴加蒸馏水,盖上盖玻片,显微镜下观察并测量。
(c)叶片毛状体数量观测方法:
将叶片腹面朝上置于载玻片上,滴加蒸馏水上盖玻片,显微镜下观察并计数。
(d)观测指标:
A区髓直径;A区初生纤维层厚度;A区次生纤维层厚度;B区髓直径;B区初生纤维层厚度;B区初生纤维层面积;C区髓直径;C区初生纤维层厚度;叶片毛状体数;乳汁管数量。
3、数据变型
依据表1内容,对观测数据进行变型处理,保留A、B、C、D、E、F、G、H、I、J、K、L、M、O、P代码指标。
4、大麻品种差异性比较
(1)差异显著性分析
利用SPSS、DPS或EXCEL等统计软件对处于盛花期的大麻品种“火麻1号”及“Silesia”的A、B、C、D、E、F、G、H、I、J、K、L、M、O、P指标分别进行单因素方差分析。
(2)形态指标差异性评分
处于盛花期的大麻品种“火麻1号”及“Silesia”的A、B、C、D、E、F、G、H、I、J、K、L、M、O、P指标,经单因素方差分析后,差异不显著计“0”分,差异显著计“1”分,差异极显著计“2”分。
待完成所有形态指标的差异性评分后,计算总得分。此得分既为“火麻1号”及“Silesia”盛花期形态学差异性得分,结果如表2所示,“火麻1号”与“Silesia”在盛花期的差异性得分为“22”分。
表2差异性评价得分表
具体实施方式三:本实施方式提供了一种大麻品种差异性比较形态学观察方法,具体实施步骤如下:
1、获取观察植株
采集相同栽培条件下种植的大麻品种“Silesia”及“格里昂”现蕾期植株各5株。
2、收集形态学数据
(1)外形数据观测方法及指标
(a)外形数据观测方法:
外形数据用卷尺及游标卡尺测量。
(b)观测指标:
株高、A区直径、B区直径、B区节长、C区直径、叶长、中裂片长、中裂片宽、叶柄长。
(2)显微结构数据观测方法及指标
(a)取材:
分别截取茎A、B、C区3cm长茎杆,D区截取从植株顶端至其下2cm处茎杆。
切取距离C区最近叶片中裂片中央区域3cm2叶片。
将上述材料置于70%乙醇中固定24h以上。
(b)茎结构观测方法:
取固定好的茎材料,用双面刀片制作茎横切面徒手切片。将切片置于载玻片上,滴加50%甘油,盖上盖玻片,显微镜下观察并测量。
(c)叶片毛状体数量观测方法:
将叶片腹面朝上置于载玻片上,滴加50%甘油,盖上盖玻片,显微镜下观察并计数。
(d)观测指标:
A区髓直径、A区初生纤维层厚度、B区髓直径、B区初生纤维层厚度、B区初生纤维层面积、C区髓直径、C区初生纤维层厚度、叶片毛状体数、乳汁管数量。
3、数据变型
依据表1内容,对观测数据进行变型处理,保留A、B、C、D、E、F、G、H、J、K、L、M、O、P代码指标。
4、大麻品种差异性比较
(1)差异显著性分析
利用SPSS、DPS或EXCEL等统计软件对处于盛花期的大麻品种“Silesia”及“格里昂”的A、B、C、D、E、F、G、H、J、K、L、M、O、P指标分别进行单因素方差分析。
(2)形态指标差异性评分
处于盛花期的大麻品种“Silesia”及“格里昂”的A、B、C、D、E、F、G、H、J、K、L、M、O、P指标,经单因素方差分析后,差异不显著计“0”分,差异显著计“1”分,差异极显著计“2”分。
待完成所有形态指标的差异性评分后,计算总得分。此得分既为“Silesia”及“格里昂”现蕾期形态学差异性得分,结果如表3所示,“Silesia”及“格里昂”在现蕾期的差异性得分为“11”分。
表3差异性评价得分表
- 还没有人留言评论。精彩留言会获得点赞!