三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡及检测方法与流程
本发明涉及食品药品安全检测领域,尤其涉及一种将免疫化学检测技术应用于保健品、中成药违法添加化学药品的检测,尤其是三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡及检测方法。
背景技术:
在上世纪90年代初期,辉瑞公司的一种用于治疗冠心病的pde-5抑制剂药物,在临床试验中发现能够有效治疗阳痿,这就是枸橼酸西地那非,之后,另两种pde-5抑制剂药物拜尔公司的伐地那非和礼莱公司的他达拉非相继在市场上产生了巨大的商业利益。
受巨大的市场利益驱动,不法分子合成在天然壮阳产品中违法添加各种pde-5抑制剂,增加壮阳效果以促进销售,谋取非法利益的行为。这种行为对公众健康的危害,已经成为令人担忧的全球性的问题。
违法添加pde-5抑制剂药物的危害性体现在:首先,pde-5抑制剂药物会引起一系列副作用,如头痛、面部潮红、消化不良、视力模糊和肌肉酸痛。美国fda官方网页发布的药物不良反应信息显示,服用viagra可能导致失明,服用viagra、levitra和cialis会导致听力突然下降甚至失聪。因此,世界各国对pde-5抑制剂药物都严格按照处方药管理,在没有医生指导下服用违法添加的该类药品是危险的。其次,pde-5抑制剂药物与硝酸酯药物的相互作用会导致严重的低血压。硝酸酯药物广泛应用于糖尿病、高血压,高血脂和冠心病的治疗,患有这些疾病而又伴随阳痿症状的病人,往往求助于天然壮阳药品。如果这些病人服用了硝酸酯药物的同时,在不知情的情况下,有服用了含违法的pde-5抑制剂药物的中成药(保健品),将会导致可怕的后果。
他达拉非(tadalafil)出现较晚,其起效剂量更低,药效持续时间更长。不法分子还对他达拉非的结构进行修饰改造,合成了一系列的他达拉非衍生物进行非法添加。由于在保健品中添加成本更低、效果更明显,拉非类药品在中成药(保健品)中违法添加的情况,大有超过另两种pde-5药物的趋势。
相比于另两种pde-5药物,拉非类药品的强力高效是危险性增加,违法添加剂量更小导致筛查检测难度更大,必须加大相应检测技术的研发力度。而近年来,世界各国的检测部门和科研机构为开发违法pde-5药物筛查方法做了大量的工作,主要有以下几种技术:1、薄层层析(tlc)技术。tlc技术简单易行,检测成本低廉,适用大规模初步鉴定。t.s.reddy等使用碘化铋钾显色,建立了高效薄层层析(hptlc)技术,在标准品的参照下,筛查天然药品中违法添加的pde-5药物取得了良好的效果。2、高效液相色谱(hplc)和液质联用(lc-ms)技术。高效液相色谱(hplc)技术被广泛应用于pde-5药物的筛查,其最大的优势是可以实现定量检测,液质联用(lc-ms)能够结合检品的质谱信息对违法添加的pde-5药物进行确证检验。3、hplc和lc-ms只能检测已知的pde-5药物,对于分子结构被蓄意修饰的新出现的pde-5的类似物,由于色谱行为和质谱行为与已知药物存在差异,只有液相/串联离子阱质谱(lc/esi-ms/ms)技术能够检测。该技术把lc分离得到的检品用电喷雾电离(esi)转换为准分子离子,经碰撞室(cid)进行解离产生的特征离子碎片在二级质谱(ms2)进行检测,综合分析检品液相分离结果以及串联质谱得到的化合物结构信息,可以在同一过程中检测出已知的和未知的pde-5药物。4、除了昂贵的lc/esi-ms/ms,只有通过水解产物分析,推测新出现的pde-5的类似物的分子结构。通过对检品进行酸解,用lc-ms对水解产物进行分析,掌握该检品的各水解产物的柱保留时间和m/z值,与已知的pde-5药物标准品的水解产物的lc-ms检测结果进行比较,可以推测目标检品的精确结构。
以上的仪器检测方法虽然灵敏、准确、可靠,但是设备昂贵复杂、运行条件苛刻、对人员素质要求高、不能进行现场检测,其打假检测工作效果存在局限性。必须有快速、灵敏、可靠、价廉的现场检测方法加以补充。
现有的拉非类药品快速检测方法主要是化学检测方法和薄层色谱检测方法,检测的灵敏度和抗干扰能力有提高的需要。免疫学检测方法灵敏、特异、快速和价廉,在环境监测和食品安全领域已广泛应用,在食品药品安全快速检测中也越来越被给予厚望。目前报道的检测小分子化合物的免疫学方法,都是基于检测抗原和检测抗体的“二元体系免疫竞争法”,其将信号物质标记于检测抗体上,与层析膜上固定的检测抗原形成免疫复合物,产生检测信号。“二元体系免疫竞争法”存在以下缺点:1、需对每种检测抗体分别标记信号物质,导致信号物质无法统一制备;2、检测抗体在液相,稳定性不足;3、检测信号强度和灵敏度较低。
本发明的前期工作中,以突出拉非类药品共同基团的人工抗原免疫动物,诱导产生能够识别拉非类药品及其类似物共同基团的特异性抗体,为开发检测违法添加拉非类药品的荧光量子点免疫层析方法打下了基础。
技术实现要素:
基于此,本发明的目的在于,提供一种三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡及检测方法,具有增加检测信号强度和稳定性、提高检测灵敏度的优点。
本发明的目的是通过以下技术方案实现的:
三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡,包括衬板、以及依次粘附于衬板上且相邻之间部分叠置的检测抗原释放垫、量子点探针释放垫、层析膜和吸水垫;所述检测抗原释放垫包含由卵清白蛋白和拉非类药品偶联而成的检测抗原;所述量子点探针释放垫包含标记有抗卵清白蛋白抗体的量子点探针;所述层析膜设有检测线和质控线,所述检测线固定抗拉非类药品抗体,所述质控线固定卵清白蛋白抗原。
相比于传统的“二元体系免疫竞争法”,本发明的检测卡利用了“三元体系免疫竞争法”原理,在“检测抗原”和“检测抗体”这两个免疫检测要素之外,增加了针对检测抗原载体蛋白的“标记抗体”。本发明在载体蛋白(卵清白蛋白)上共价连接检测物质(拉非类药品)合成检测抗原,将标记抗体(抗卵清白蛋白抗体)标记于量子点上,将检测抗体(抗拉非类药品抗体)固定于层析膜上,从而检测抗体捕获检测抗原上偶联的检测物质,标记抗体结合检测抗原上偶联的载体蛋白,形成双抗体夹心免疫复合物,产生荧光检测信号。当检测抗体被游离的检测物质结合,荧光强度将被抑制,从而产生抑制检测信号。
具体的,检测时将样品溶液滴到检测抗原释放垫上,样品溶液运动的过程中将检测抗原和量子点探针溶解,并携带到检测线和质控线,被携带的量子点探针标记的抗卵清白蛋白(ova)抗体、检测抗原与检测线上的抗拉非类药品抗体形成双抗体夹心免疫结合物,使检测线产生荧光信号;被携带的量子点探针标记的抗ova抗体与质控线上固定的ova抗原结合,在质控线上堆积形成荧光信号。当样品中存在游离的拉非类药品达到一定浓度,检测线上免疫反应就会被竞争阻断,荧光信号被抑制;而质控线上的荧光信号,不受拉非类药品浓度的影响。
目前利用荧光量子点免疫层析方法检测拉非类药品的相关报道较少,本发明为食品药品安全检测工作提供新的工具。量子点是由200-10000原子集聚在三个球形空间的纳米半导体晶体,球形晶核直径2-8nm,为了增加量子点的水溶性和生物相容性,球形晶核外层通常会被有机分子包覆引入功能基团,直径会提高到15-30nm,具有很好的胶体性能和动力学特性,适合作为生物学检测的纳米标记材料。与传统有机荧光染料填充的纳米微球相比,量子点具有宽且呈连续分布的激发谱、窄而对称的发射峰;稳定性强、抗光漂白性强;光能力转化效率高、亮度是有机染料的数十倍甚至更多。
相对于现有技术,本发明的检测卡具有以下优点:1、统一用抗载体蛋白抗体标记的量子点产生检测信号,只需集中制备一种作为荧光探针,有利于检测工作的规模化和标准化;2、检测抗体固定在层析膜上,通过对膜的封闭和干燥,对抗体的活性保护作用更为有利,增加抗体稳定性;3、免疫结合时空间位阻更小,提高检测信号强度和灵敏度;4、特异性强,检测时间短(5-10分钟),可现场操作,且借助便携360nm光源即可激发荧光信号,肉眼判读结果,检测成本低,操作简便,适合基层检测人员操作。
进一步地,所述检测抗原释放垫采用玻璃纤维素膜吸收含有检测抗原、表面活性剂、甘露醇、蔗糖的pbs溶液制得。优选的,采用厚度为0.85mm的玻璃纤维素膜充分吸收含有10μg/ml检测抗原、50μg/ml表面活性剂、30mg/ml甘露醇、50mg/ml蔗糖的pbs溶液。其中,甘露醇作为冻干支架用于确保检测过程中检测抗原迅速溶解;蔗糖用于调节检测溶液黏度控制层析展开速度;表面活性剂用于消除检测过程的非特异性吸附,优选聚乙二醇辛基苯基醚(tritonx-100);检测抗原由ova和拉非类药品共价偶联合成,既能被膜上检测抗体结合,又能被量子点上的标记抗体结合。
进一步地,所述量子点探针释放垫采用人造纤维素膜吸收含有量子点荧光探针、聚乙二醇、甘露醇、蔗糖、甘氨酸的pbs溶液制得。优选的,采用厚度为0.34mm的人造纤维素膜吸收含有20μg/ml量子点荧光探针、60μg/ml聚乙二醇(peg-500)、10mg/ml甘露醇、60mg/ml蔗糖、10mg/ml甘氨酸的pbs溶液。其中,甘露醇作为冻干支架用于确保检测过程中量子点探针迅速溶解;聚乙二醇、蔗糖用于调节检测溶液黏度控制层析展开速度;甘氨酸用于消除检测过程的非特异性吸附;量子点荧光探针由量子点表面标记抗ova抗体构成,能够结合被捕获在检测线上的检测抗原和固定在质控线上的ova抗原,分别产生荧光检测信号。
进一步地,所述层析膜采用硝酸纤维素膜,所述检测线由含有抗拉非类药品抗体和蔗糖的pbs溶液喷涂在硝酸纤维素膜上制得。优选的,将含有0.3mg/ml抗拉非类药品抗体和10mg/ml蔗糖的0.05mpbs溶液(ph7.4),以1.0~4.0μg/cm的量喷涂在硝酸纤维素膜上。检测线荧光信号形成的基础是抗体与检测抗原所偶联拉非类药品的免疫反应,会被检品中游离的拉非类药品竞争抑制。
进一步地,所述质控线由含有卵清白蛋白和蔗糖的pbs溶液喷涂在硝酸纤维素膜上制得。优选的,将含有0.2mg/mlova和10mg/ml蔗糖的0.05mpbs溶液(ph7.4),以1.0~3.0μg/cm的量喷涂在硝酸纤维素膜上。质控线荧光信号形成的基础是量子点的抗ova抗体与质控ova抗原的免疫反应,与拉非类药品检品无关,不会被检品中游离的拉非类药品竞争抑制。
三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测方法,包括以下步骤:
s1:制备检测抗原、量子点探针、检测线和质控线;所述检测抗原由卵清白蛋白和拉非类药品偶联而成,所述量子点探针标记有抗卵清白蛋白抗体,所述检测线固定抗拉非类药品抗体,所述质控线固定卵清白蛋白抗原;
s2:将样品溶液、检测抗原和量子点探针混合,一起输送至检测线和质控线,根据检测线和质控线上的荧光信号来判断样品中是否含有拉非类药品。
拉非类药品是小分子化合物,常规检测小分子化合物的免疫检测原理是“检测抗原”与“检测抗体”形成的“二元体系免疫竞争法”,针对该方法在量子点侧向免疫层析中的不足,本发明在“检测抗原”与“检测抗体”的基础上,加入“标记抗体”形成“三元体系免疫竞争法”,并对各免疫反应要素在层析系统中的组合也进行了调整,将检测抗体固定在检测线,在量子点上标记抗ova抗体构成荧光探针,与检测抗原(ova-拉非类药品)“桥连”形成“双抗体夹心”免疫复合物,荧光探针积累形成检测信号,增加了检测的信号强度和稳定性,提高了检测灵敏度,当检测抗体被游离的检测物质结合,荧光强度将被抑制,从而产生抑制检测信号。利用本发明的检测方法对样品溶液中拉非类药品的最低检出限度为2.0ng/ml,对保健品、中成药中违法添加拉非类药品及其类似物的最低检出限度为2.0μg/kg,且可在5分钟内完成快速检测。
进一步地,步骤s2中,通过以下方法进行判断:检测线和质控线都显示荧光信号,断定结果为阴性,样品中不含拉非类药品;检测线不显示荧光信号,质控线显示荧光信号,断定结果为阳性,样品中含有拉非类药品。其中,质控线是为了检验方法有效与否而设定,质控线显示荧光信号表明方法有效,质控线不显示荧光信号表明方法本身无效;而检测线形成双抗体夹心免疫复合物时产生荧光信号,当样品中存在游离的拉非类药品时,检测线上的免疫反应就会被竞争阻断,从而荧光信号消失。
进一步地,所述量子点探针在365nm光源激发下,产生630nm的发射光。
为了更好地理解和实施,下面结合附图详细说明本发明。
附图说明
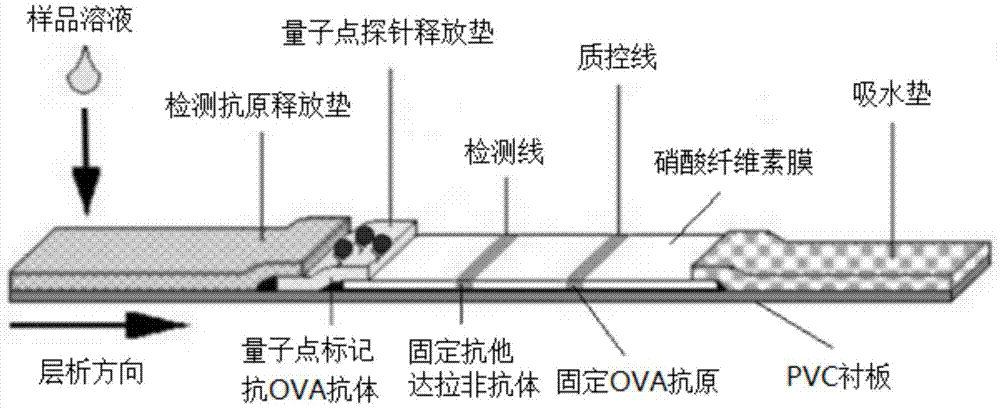
图1为实施例的三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡的结构示意图。
图2a为检测线上发生免疫反应、产生荧光信号的示意图。
图2b为检测线上免疫反应被竞争阻断、荧光信号消失的示意图。
图3为质控线上发生免疫反应、产生荧光信号的示意图。
图4为荧光免疫检测结果产生的原理及检测结果的判断原则。
具体实施方式
请参阅图1,其为本实施例的三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测卡,包括pvc衬板、以及依次粘附于pvc衬板上且相邻之间部分叠置的检测抗原释放垫、量子点探针释放垫、硝酸纤维素膜(nc膜)和吸水垫;所述检测抗原释放垫包含由ova和拉非类药品(他达拉非)偶联而成的检测抗原;所述量子点探针释放垫包含标记有抗ova抗体的量子点探针;所述硝酸纤维素膜设有检测线和质控线,所述检测线固定抗拉非类药品抗体,所述质控线固定ova抗原。
具体的,检测抗原释放垫的制备方法如下:采用厚度为0.85mm的玻璃纤维素膜充分吸收含有10μg/ml检测抗原、50μg/mltritonx-100、30mg/ml甘露醇、50mg/ml蔗糖的pbs溶液,冷冻干燥后备用。
具体的,量子点探针释放垫的制备方法如下:采用厚度为0.34mm的whatman85人造纤维素膜吸收含有20μg/ml量子点荧光探针、60μg/mlpeg-500、10mg/ml甘露醇、60mg/ml蔗糖、10mg/ml甘氨酸的pbs溶液,冷冻干燥后备用。
具体的,检测线的制备方法如下:将含有0.3mg/ml抗拉非类药品特异性抗体和10mg/ml蔗糖的0.05mpbs溶液(ph7.4),以1.00μg/cm的量喷涂在硝酸纤维素膜上,形成检测线。
具体的,质控线的制备方法如下:将含有0.2mg/mlova和10mg/ml蔗糖的0.05mpbs溶液(ph7.4),以1.00μg/cm的量喷涂在硝酸纤维素膜上,形成质控线。
拉非类药品及其类似物的特异性抗体诱导产生方法、抗ova抗体诱导产生方法、以及在量子点上标记抗ova抗体、制备量子点荧光探针的方法均采用现有技术。
本实施例的三元体系免疫竞争法检测拉非类药品的量子点免疫层析检测方法如下:
取0.2g(或0.2ml)样品,溶解在2.0ml无水乙醇中充分抽提目标检品,抽提液静止10分钟使杂质充分沉淀,取0.2ml上清液加入到20ml样品缓冲液,充分摇匀成为样品溶液;用滴管在检测抗原释放垫上滴加3-4滴样品溶液,样品溶液向硝酸纤维素膜运动的过程中使检测抗原和量子点探针释放,并先后越过检测线和质控线,根据检测线和质控线上的荧光信号来判断样品中是否含有拉非类药品。
在硝酸纤维素膜检测线上的抗拉非类药品抗体、量子点探针上标记的抗ova抗体,分别与检测抗原结合,形成双抗体夹心免疫结合物,使检测线产生荧光检测信号,如图2a所示。当样品中存在游离的拉非类药品达到一定浓度,检测线上免疫反应就会被竞争阻断,荧光信号会消失,如图2b所示。量子点探针通过标记的抗ova抗体与硝酸纤维素膜质控线上固定的ova抗原结合,在质控线上堆积形成荧光信号,如图3所示。质控线是检验方法本身有效与否而设定,显色有效,不显色表明方法本身无效。
如图4所示,量子点探针在365nm光源激发下,产生630nm的发射光,检测结果的判断原则为:检测线和质控线都显示荧光信号,断定结果为阴性(a),样品中不含拉非类药品;检测线不显示荧光信号,质控线显示荧光信号,断定结果为阳性(b和c),样品中含有拉非类药品,其中,阳性结果b中拉非类药品浓度为1.0ng/ml,阳性结果c中拉非类药品浓度高于2.0ng/ml。
相对于现有技术,本发明采用的“三元体系免疫竞争法”具有以下优点:1、统一用抗载体蛋白抗体标记的量子点产生检测信号,只需集中制备一种作为荧光探针,有利于检测工作的规模化和标准化;2、检测抗体固定在层析膜上,通过对膜的封闭和干燥,对抗体的活性保护作用更为有利,增加抗体稳定性;3、免疫结合时空间位阻更小,提高检测信号强度和灵敏度。利用本发明的检测方法对样品溶液中对拉非类药品的最低检出限度为2.0ng/ml,对保健品、中成药中违法添加拉非类药品及其类似物的最低检出限度为2.0μg/kg,且可在5分钟内完成快速检测。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!