一种猪圆环病毒2型病毒样颗粒的定量检测方法与流程
本发明属于生物技术领域,涉及病毒样颗粒的定量检测方法,具体涉及一种猪圆环病毒2型病毒样颗粒的定量检测方法。
背景技术:
猪圆环病毒(porcinecircovirus,pcv)属于圆环病毒科(circoviridae)圆环病毒属(circovirus),是迄今为止发现的最小的病毒,其粒子直径最小仅17nm,dna基因组长1.7kb,病毒粒子为二十面体对称、无囊膜、单股环状dna病毒。已知pcv有两个血清型,非致病性的pcv1和致病性pcv2。pcv2是引起断奶仔猪多系统衰竭综合征(postweaningmultisystemicwastingsyndrome,pmws)的主要病原,与猪瘟病毒(csfv)或猪繁殖与呼吸综合征病毒(prrsv)等混合感染可增强该疾病的严重程度,可造成10%~30%不等的死亡率,较严重的猪场在爆发本病时死淘率高达40%,给养猪业造成严重威胁。目前,pcv2疫苗免疫接种是防控pcv2的主要手段,其抗原含量是影响疫苗免疫效果的最主要的因素。在田间使用时,如无足够与生产实际要求的免疫抗原量,虽然可控制临床发病,但往往因免疫力不足造成猪只感染,表现为长期带毒和亚临床感染,严重影响猪只生长性能,造成较大经济损失。
pcv2病毒样颗粒(virus-likeparticles,vlps)是重组表达的pcv2cap蛋白经自组装形成的60聚体,分子量约为1800kda,与天然病毒粒子结构相近,所以免疫原性优于cap蛋白。vlps的形态结构与天然病毒高度相似,免疫原性良好,且不含有病毒基因,因此是一种理想的疫苗形式。
病毒样颗粒疫苗的vlps结构评价和抗原定量检测是病毒样颗粒疫苗质量控制的重要组成部分,但由于病毒样颗粒是多蛋白组装的大分子物质,一般的生物学定量检测方法难以在定量的同时区分vlps与蛋白单体,也无法鉴定溶液中病毒样颗粒的稳定状态。目前pcv2抗原定量检测方法主要是酶联免疫吸附测定enzymelinkedimmunosorbentassay(elisa)方法和sds-page法,而这两种方法均不适用于pcv2vlps的定量检测:elisa定量方法是将已知的抗原或抗体吸附在固相载体(聚苯乙烯微量反应板)表面,使酶标记的抗原-抗体反应在固相表面进行,然后进行抗原或抗体的定量,该方法无法区分pcv2vlps和cap蛋白单体,同时其捕获抗体对不同基因型的抗原亲和力的差异也限制了该方法的应用;sds-page法是一种半定量方法,无法准确定量样品中抗原浓度,并且同样也不能区分pcv2vlps和cap蛋白单体。
高效液相色谱法(hplc)是一种操作简单、高效和灵敏度高分析方法,检测灵敏度可达ng级,分析速度快,同一样品重复上样后检测结果的相对平均偏差一般不超过2%,目前,hplc广泛应用到生物化学、食品分析、医药研究、环境分析、无机分析等各种领域。因此,利用hplc检测技术进行pcv2vlps的定量分析,不仅能缩短传统的elisa方法和sds-page法的检测时间,还能提高检测灵敏度与稳定性,有利于完善pcv2vlps疫苗生产的质量控制,提高疫苗产品质量。
然而,现有hplc检测方法应用于pcv2vlps难以适用于pcv2vlps的定量检测,国内外文献和专利检索也未检索到相关报道,其原因包括:1、pcv2vlps是由60聚体cap蛋白组装成的高分子复合物,常规的反相hplc和正相hplc在检测时不能保持vlps的构象;2、酵母细胞破碎后释放出大量的蛋白、核酸和多糖等内溶物,其中一些物质会干扰pcv2vlps检测信号,甚至可能与pcv2vlps相互作用,影响检测效果;3、由于pcv2vlps纯化及定量困难,目前用制作标准曲线的无商品化的标准品。
技术实现要素:
为解决上述问题,提供了一种操作简单、灵敏度高、重复性和适用性高的pcv2病毒样颗粒检测方法,本发明根据pcv2vlps的结构特征,设计采用分子排阻层析的色谱检测方法,结合样品处理、标准品的制备以及检测条件优化,建立了高效的hplc检测pcv2vlps的纯度及定量方法,解决了生产实际中病毒样颗粒的难以快速定量的关键技术问题。本发明具体采用了如下技术方案:
本发明提供了一种猪圆环病毒2型病毒样颗粒的定量检测方法,用于对待测样品中的猪圆环病毒2型病毒样颗粒进行定量检测,其特征在于,包括如下步骤:步骤s1,稀释待测样品并进行过滤澄清或离心澄清;步骤s2,取蛋白含量已被确定的猪圆环病毒2型病毒样颗粒标准品进行系列稀释,并对稀释后的系列标准品进行hplc检测,建立以浓度为横坐标、峰高为纵坐标的回归方程;步骤s3,对稀释后的待测样品进行hplc检测得到对应的样品峰高;步骤s4,根据回归方程及样品峰高计算得到待测样品中的猪圆环病毒2型病毒样颗粒浓度,其中,步骤s2及步骤s3中的hplc所采用的色谱柱为凝胶色谱柱,采用的检测器为紫外检测器,其检测波长为280nm。
本发明提供的上述猪圆环病毒2型病毒样颗粒的定量检测方法,还可以具有这样的技术特征,其中,凝胶色谱柱为agilentbiosec-5或tskgelg4000swxl。
本发明提供的上述猪圆环病毒2型病毒样颗粒的定量检测方法,还可以具有这样的技术特征,其中,步骤s1中,待测样品的稀释采用磷酸缓冲液进行,该磷酸缓冲液中含有150mmnacl、2.7mmkcl、1.5mmkh2po4以及8mmk2hpo4。
本发明提供的上述猪圆环病毒2型病毒样颗粒的定量检测方法,还可以具有这样的技术特征,其中,待测样品选自重组工程菌的发酵液、细胞培养液、分离纯化液或抗原成品中的任意一种。
本发明提供的上述猪圆环病毒2型病毒样颗粒的定量检测方法,还可以具有这样的技术特征,其中,待测样品采用含1%tritonx-100的磷酸盐缓冲液进行20倍稀释。
本发明提供的上述猪圆环病毒2型病毒样颗粒的定量检测方法,还可以具有这样的技术特征,其中,病毒样颗粒在hplc的保留时间为15.5min。
本发明还提供了另一种猪圆环病毒2型病毒样颗粒的定量检测方法,其特征在于,包括如下步骤:步骤s1,稀释待测样品并进行过滤澄清或离心澄清;步骤s2,取蛋白含量已被确定的猪圆环病毒2型病毒样颗粒标准品进行系列稀释,并对稀释后的系列标准品进行hplc检测,建立以浓度为横坐标、峰面积为纵坐标的回归方程;步骤s3,对稀释后的待测样品进行hplc检测得到对应的样品峰面积;步骤s4,根据回归方程及样品峰面积计算得到待测样品中的猪圆环病毒2型病毒样颗粒浓度,其中,步骤s2及步骤s3中的hplc所采用的色谱柱为凝胶色谱柱,采用的检测器为紫外检测器,其检测波长为280nm。
发明作用与效果
根据本发明提供的猪圆环病毒2型病毒样颗粒的定量检测方法,由于采用了基于凝胶色谱柱的hplc中来对病毒样颗粒进行检测,因此能够有效地分离病毒样颗粒和杂质,达到检测病毒样颗粒的目的。进一步,采用本发明的凝胶色谱柱以及hplc条件还能够使非多聚化形式的病毒样颗粒和多聚化形式的病毒样颗粒得到分离,从而能够区分病毒样颗粒的不同聚合形式,更适用于实际生产过程的产品检测和质量控制。
附图说明
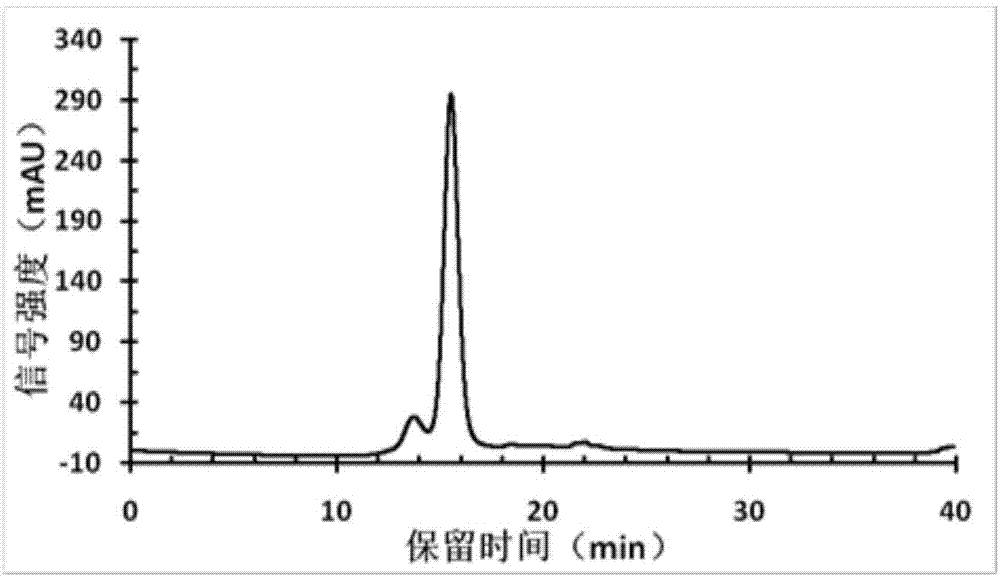
图1为本发明实施例的pcv2病毒样颗粒标准品的hplc检测结果;
图2为本发明实施例中pcv2病毒样颗粒标准品hplc特征峰的sds-page电泳(a)和免疫印迹westernblot(b)检测结果;
图3是本发明实施例中pcv2病毒样颗粒标准品hplc保留时间13.7min和15.5min特征峰的电子显微镜观察结果;
图4是本发明实施例的hplc方法定量pcv2病毒样颗粒的标准曲线;
图5为本发明实施例的酵母破菌液样品中掺入pcv2-vlps标准品后的hplc检测结果。
具体实施方式
本发明所采用的猪圆环病毒2型病毒样颗粒(以下称病毒样颗粒)的定量检测方法主要包括以下步骤:
步骤s1,稀释待测样品并进行过滤澄清或离心澄清;
步骤s2,取蛋白含量已被确定的猪圆环病毒2型病毒样颗粒标准品进行系列稀释,并对稀释后的系列标准品进行hplc检测,建立以浓度为横坐标、峰高为纵坐标的回归方程;
步骤s3,对稀释后的待测样品进行hplc检测得到对应的样品峰高;
步骤s4,根据回归方程及样品峰高计算得到待测样品中的猪圆环病毒2型病毒样颗粒浓度。
以下结合附图以及实施例来说明本发明的具体实施方式。下述各实施例中,样品或标准品稀释所采用的磷酸缓冲液中含有150mmnacl、2.7mmkcl、1.5mmkh2po4以及8mmk2hpo4,其他试剂如无特殊说明均从一般商业途径获得,未注明的实验条件均参照常规实验条件或遵照供应商建议的条件。
<实施例>
1、仪器与试剂
angilent高效相色谱仪infinity1260,配备紫外检测器。
hplc检测流动相的配制:取13.4g磷酸氢二钠七水合物、6.9g磷酸二氢钠一水合物和14.2g无水硫酸钠,用800mlmilli-q水溶解,定容至1000ml,0.22μm滤膜过滤。
2、pcv2病毒样颗粒标准品制备
目前,国内外尚不存在商业化的pcv2病毒样颗粒标准品。因此,本发明以含pcv2病毒样颗粒的vlps样品,用离子交换层析和sephacryls-500hr分子筛凝胶层析进行了纯化,将得到的高纯度病毒样颗粒作为标准品。
图1为本发明实施例的pcv2病毒样颗粒标准品的hplc检测结果。
如图1所示,经过hplc检测,标准品中的病毒样颗粒纯度>98%。此外,hplc检测呈现两个特征峰,其中保留时间15.5min的峰前有一肩峰,其保留时间为13.7min。
图2为本发明实施例中pcv2病毒样颗粒标准品hplc特征峰的sds-page电泳(a)和免疫印迹westernblot(b)检测结果,其中:泳道1为收集的保留时间13.7min特征峰;泳道2为收集的保留时间15.5min特征峰。
图3是本发明实施例中pcv2病毒样颗粒标准品hplc保留时间13.7min和15.5min特征峰的电子显微镜观察结果。
分别收集hplc检测中呈现的两个特征峰,用sds-page电泳和免疫印迹westernblot(b)进行检测,结果如图2所示,说明两个特征峰的组分都是cap蛋白。
进一步用电子显微镜进行了观察,结果如图3所示,说明这两个特征峰都是cap蛋白组装形成的病毒样颗粒,其中13.7min特征峰是病毒样颗粒多聚化形式。
3、色谱柱的柱效检测
进行hplc检测前需先进行色谱柱的柱效检测,其具体过程如下:
打开相色谱仪infinity1260,用0.5ml/minmilli-q水冲洗20min之后换上色谱柱流动相水冲洗20min;然后安装保护柱及凝胶色谱柱,柱温24℃,打开紫外检测器,待基线平稳后进行归零校正。用0.01g/l对氨基苯甲酸为标准品进行了柱效检测,检测结果如下:
保留时间为27.946min,峰高41.3mau,半峰宽为0.425min。理论塔板数的计算公式为:n=5.54*(ve/w1/2)2,n为理论塔板数,ve为保留时间,w1/2为半峰宽,因此色谱柱tskgelg4000swxl的理论塔板数为23953,达到出厂标准要求≥16000,可应用于后续的病毒样颗粒hplc检测。
4、pcv2病毒样颗粒标准品检测及标准曲线绘制
将制备得到的pcv2病毒样颗粒标准品用bca方法进行蛋白定量,然后用磷酸缓冲液稀释成浓度为4.1μg/ml、8.2μg/ml、16.3μg/ml、32.6μg/ml、43.5μg/ml、65.2μg/ml、104.4μg/ml和130.5μg/ml等的标准品溶液。取100μl进行检测,流动相含50mmnah2po4、50mmna2hpo4、100mmna2so4,ph为6.75,流速0.6ml/min,检测波长280nm。记录保留时间为15.5min特征峰高,每组重复3次,结果如表1所示。
表1:不同浓度pcv2病毒样颗粒标准品检测结果
由于4.1μg/ml这个点的峰高值过低,与其它检测点线性关系较差,因此在绘制标准曲线时予以去除。
图4是本发明实施例的hplc方法定量pcv2病毒样颗粒的标准曲线。
以pcv2vlps的浓度与保留时间15.5min特征峰高作线性回归,结果如图4所示,表明在hplc检测pcv2vlps时,其浓度与特征峰高的线性关系是y=2.7841x+2.9523(y是pcv2vlps质量浓度,单位μg/ml;x是保留时间15.5min峰高值,单位mau);r2值为0.9988,说明pcv2vlps的特征峰峰高与浓度的线性关系较高,证明该本发明的检测方法可用于pcv2vlps的定量检测。
5、样品检测精密度与回收率
将pcv2病毒样颗粒标准品添加到酵母细胞液中,添加后浓度为65.2μg/ml,取100μl用hplc平行检测6次,记录每次检测保留时间15.5min的峰高值,计算回收率和精度,结果如下表2所示。
表2:检测的精密度与回收率
6、试样测定
以对酵母重组表达的菌株发酵表达的pcv2病毒样颗粒抗原量进行定量,样品用含1%tritonx-100的磷酸盐缓冲液稀释20倍后取100μl检测。
图5为本发明实施例的酵母破菌液样品中掺入pcv2-vlps标准品后的hplc检测结果。
如图5所示,上述样品的检测结果图谱中,保留时间15.5min处有pcv2病毒样颗粒的特征峰。重复检测3次,峰高值依次为26.7mau、27.1mau、26.7mau,通过标准曲线可以计算出检测的样品的浓度为77.66μg/ml,从而得出发酵液上清中的pcv2病毒样颗粒抗原浓度为1553μg/ml。
实施例作用与效果
根据本实施例提供的猪圆环病毒2型病毒样颗粒的定量检测方法,由于采用了基于凝胶色谱柱的hplc中来对病毒样颗粒进行检测,因此能够有效地分离病毒样颗粒和杂质,达到检测病毒样颗粒的目的。本实施例的检测方法的回收率为104%,相对标准偏差为1.48%,因此能够达到检测方法的定量要求,可以作为猪圆环病毒2型病毒样颗粒的定量检测方法应用。
进一步,采用本实施例的凝胶色谱柱以及hplc条件还能够使非多聚化形式的病毒样颗粒和多聚化形式的病毒样颗粒得到分离,从而能够区分病毒样颗粒的不同聚合形式,更适用于实际生产过程的产品检测和质量控制。另外,hplc具有容易流程化、操作简便等优点,也使得本实施例的定量检测方法十分适用于工业化生产过程中的中间品或产品检测(例如重组工程菌的发酵液、细胞培养液、分离纯化液或抗原成品等)。
以上详细描述了本发明的较佳具体实施例。应当理解,本领域的普通技术无需创造性劳动就可以根据本发明的构思做出诸多修改和变化。因此,凡本技术领域中技术人员依本发明的构思在现有技术的基础上通过逻辑分析、推理或者有限的实验可以得到的技术方案,皆应在由权利要求书所确定的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!