一种楸树叶片丙二醛含量的测定方法与流程
本发明涉及一种植物组织中次生代谢产物的检测方法,具体地,涉及一种楸树叶片丙二醛含量的测定方法。
背景技术:
丙二醛(mda)是植物受到逆境胁迫或衰老过程中发生膜脂过氧化而产生的最终分解产物,mda从膜上产生的位置释放出来后,可与蛋白质,核酸反应,改变这些大分子的构型,或使之产生交联反应,从而丧失功能,还可使纤维素分子间桥键松弛,或抑制蛋白质的合成,因此,mda的积累会对膜和细胞造成一定的伤害,其含量可反映植物遭受逆境伤害的程度。
mda在酸性和高温条件下,可与硫代巴比妥酸(tba)反应生成红棕色三甲基复合物,其最大吸收波长为532nm,在600nm处有最小吸收峰。目前,运用分光光度法检测植物中mda的含量,其核心技术在于运用5%~10%的三氯乙酸(tca)提取植物样品中的丙二醛,并在高温下使其与tba反应,最终使用分光光度计检测吸光值计算出mda的含量。这一技术已普遍应用于植物材料中mda含量的检测。
楸树为紫葳科梓树属。良种选育是楸树遗传改良的主要目标,品种的抗逆性评价是品种选择的重要方面。逆境胁迫下mda含量变化是衡量品种抗逆性的间接指标之一,具有检测方法简便、速度快、成本低、准确性高等特点,但是,在实际检测过程中发现,现有的mda检测方法(标准曲线法和分光光度法)却不适用于楸树叶片中的mda含量检测,无法测定楸树叶片中mda的含量,分析可能是由于叶片中其他物质干扰所致。
因此,若能开发出一种楸树叶片mda含量检测方法,势必会简化楸树品种的抗逆性评价方法,加速楸树良种的选育进程。
技术实现要素:
为了解决楸树叶片中丙二醛(mda)含量无法检测的问题,本发明目的是提供一种准确检测楸树叶片中丙二醛(mda)含量的方法。
为了实现本发明目的,本发明的一种楸树叶片丙二醛含量的测定方法,先对新鲜采集的楸树叶片进行冰浴研磨,然后在恒温酸性条件下提取mda,再在高温下与硫代巴比妥酸(tba)进行显色反应,并排除糖类物质干扰,最终使用分光光度计检测吸光值计算出mda的含量。
前述方法中,准确称取新鲜叶片4.5g,冰浴,研磨至匀浆。
前述方法中,酸性条件为加入浓度为0.5%~1.0%三氯乙酸(tca)溶液45ml;温度为40℃~70℃;提取时间为30min~40min。
前述方法中,提取液的获取通过定量滤纸过滤,滤去残渣即可。
前述方法中,取滤液1.5ml,加入浓度为0.0002g/l的硫酸铁(fe2(so4)3)溶液150~450μl。
前述方法中,显色反应在沸水浴中反应的时间为25min~35min。
具体地,前述方法包括以下步骤:
(1)准确称取新鲜叶片4.5g,冰浴,研磨至匀浆。
(2)将匀浆转入具塞锥形瓶,用浓度为0.5%~1.0%三氯乙酸(tca)溶液冲洗研钵3次,并全部转入具塞锥形瓶,tca溶液的总量为45ml。
(3)将具塞锥形瓶置于温度为50℃~70℃恒温摇床中振荡25min~40min。
(4)将具塞锥形瓶取出,用定量滤纸过滤溶液,获得丙二醛提取液。
(5)取滤液1.5ml转入5ml离心管,加入浓度为0.02mol/l的tba溶液1.5ml,同时加入浓度为0.0002g/l的fe2(so4)3溶液150~450μl。
(6)将离心管转入沸水浴中25min~35min,完成显色反应。
(7)用双通道分光光度计或酶标仪测定反应液在450nm,532nm,600nm波长下的吸光值。
(8)按式a计算mda的浓度,按式b计算叶片样品中的mda含量。
c=6.45×(a532-a600)-0.56×a450式a
y=cv/w式b
上式中,c—mda浓度(μmol/l)
v—提取液体积(ml)
w—植物组织鲜重(g)
y—mda含量(μmol/g)。
附图说明
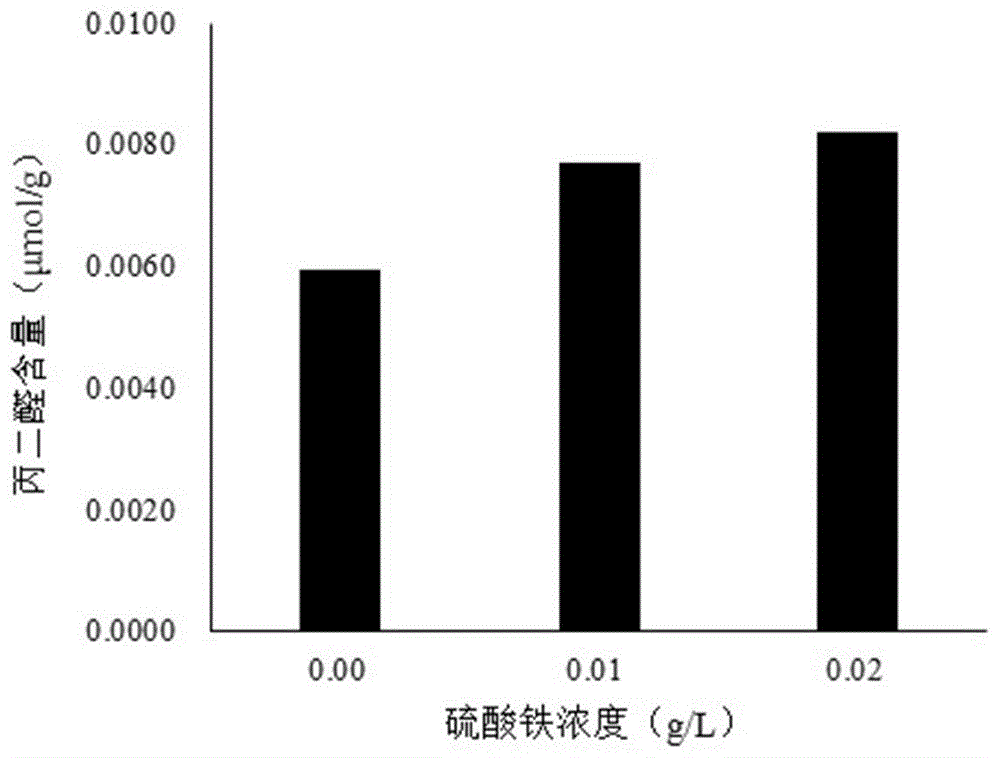
图1为加入不同浓度硫酸铁下楸树叶片丙二醛含量的差异。
图2为加入硫酸铁浓度为0.01g/l时对检测效果的影响。
图3为不同三氯乙酸浓度下楸树叶片提取液中丙二醛浓度的差异。
图4为不同提取温度下楸树叶片提取液中丙二醛浓度的差异。
图5为不同反应时间下楸树叶片提取液中丙二醛浓度的差异。
具体实施方式
为了使本领域的技术人员可以更好地理解本发明,下面结合附图和实施例对本发明技术方案进一步说明。
本发明中涉及到的百分号“%”,若未特别说明,是指质量百分比;但溶液的百分比,除另有规定外,是指100ml溶液中含有溶质的克数。
实施例1硫酸铁不同浓度下楸树叶片丙二醛含量的检测效果
(1)材料
以1年生楸树组培苗幼嫩叶片为材料。
(2)试剂配制
三氯乙酸(tca)溶液:配置三氯乙酸溶液浓度为0.75%。
硫代巴比妥酸(tba)溶液:0.02mol/l。
硫酸铁(fe2(so4)3)溶液:0.01g/l和0.02g/l。
(3)测定过程
将叶片样品加液氮研磨成粉,称取样品粉末4.50g(精确至0.01g),置于具塞锥形瓶中,准确加入45mltca溶液摇匀加塞,置于恒温震荡器上50℃摇30min,旋转频率为110rpm,取出,用滤纸过滤,取滤液备用。
分别取9份提取液至于25ml具塞刻度试管中,每份1.5ml,编号为1-1、1-2、1-3、2-1、2-2、2-3、3-1、3-2、3-3,不加提取液的对照3份,编号分别为0-1、0-2、0-3。首先,在每份提取液中加入1.5mltba溶液;然后,1-1、1-2、1-3中不加fe2(so4)3溶液,2-1、2-2、2-3中加入150μl浓度为0.01g/l的fe2(so4)3溶液,3-1、3-2、3-3中加入150μl浓度为0.02g/l的fe2(so4)3溶液;最终,将试管放入沸水浴中加热30min,取出室温冷却后用分光光度计测定450nm、532nm和600nm的吸光值。
(4)测定结果
按照式a和b计算叶片中的mda浓度和含量,并取同一处理下3次重复的平均值,结果如图1和图2所示。不加fe2(so4)3溶液的反应液所测的mda含量最低,加入fe2(so4)3浓度分别为0.01g/l和0.02g/l时测得的mda含量分别为0.0077μmol/g和0.0082μmol/g。同时,当加入fe2(so4)3浓度为0.01g/l时,对照(空白)中测定的mda含量为0,而加入提取液(叶片)的mda含量为0.0077μmol/g。由此说明,加入fe2(so4)3能够有效提升楸树叶片丙二醛含量的测定结果,而且这一测定方法是可行的。
实施例2三氯乙酸不同浓度下楸树叶片丙二醛含量的检测效果
(1)材料
以3株1年生楸树嫁接苗幼嫩叶片为材料,分别编号为样品1、样品2和样品3。
(2)试剂配制
三氯乙酸(tca)溶液:配置三氯乙酸溶液浓度为0.5%和1.0%。
硫代巴比妥酸(tba)溶液:0.02mol/l。
硫酸铁(fe2(so4)3)溶液:0.02g/l。
(3)测定过程
首先,按照2种浓度tca溶液3次重复的设计,分别准确称取样品1、样品2和样品3各6份,每份1.00g,放入研钵中,分别加入2ml浓度为0.5%和1.0%的tca,研磨至匀浆,将匀浆转移至25ml离心管中,并用8ml浓度为0.5%和1.0%的tca冲洗干净;然后,将离心管至于50℃恒温震荡器中振荡30min,旋转频率为110rpm;最终,取出震荡后的离心管,用定性滤纸过滤,滤液备用。
在18份提取液中各取1.5ml分别至于25ml具塞刻度试管中,分别加入1.5mltba溶液和150μlfe2(so4)3溶液,将试管放入沸水浴中加热30min,取出室温冷却后用酶标仪测定450nm、532nm和600nm的吸光值。
(4)测定结果
按照式a计算叶片中的mda浓度,并取同一处理下3次重复的平均值,结果如图3所示。
用浓度为0.5%和1.0%的tca溶液进行楸树嫁接苗幼嫩叶片中mda的提取,经tba显色反应后,均能测得mda的浓度,但使用浓度为1.0%的tca溶液提取所测得的浓度更高,因此,更适用于楸树叶片mda的测定。
实施例3不同温度对丙二醛提取效果的影响
(1)材料
以楸树1年生种子苗叶片为材料。
(2)试剂配制
三氯乙酸(tca)溶液:浓度为0.75%。
硫代巴比妥酸(tba)溶液:浓度为0.02mol/l。
硫酸铁(fe2(so4)3)溶液:浓度为0.02g/l。
(3)测定过程
首先,按照3种温度3次重复的设计,分别准确称取样品9份,每份1.00g,放入研钵中,分别加入2ml浓度为0.75%tca,研磨至匀浆,将匀浆转移至25ml离心管中,并用8ml浓度为0.75%的tca冲洗干净;然后,分别将离心管至于50℃、60℃、70℃恒温震荡器中振荡30min,旋转频率为110rpm;最终,取出震荡后的离心管,用定性滤纸过滤,滤液备用。
在9份提取液中各取1.5ml分别至于25ml具塞刻度试管中,分别加入1.5mltba溶液和150μlfe2(so4)3溶液,将试管放入沸水浴中加热30min,取出室温冷却后用分光光度计测定450nm、532nm和600nm的吸光值。
(4)测定结果
按照式a计算叶片中的mda浓度,并取同一处理下3次重复的平均值,结果如图4所示。50℃、60℃、70℃恒温震荡提取所获得的提取液,经tba显色反应后,测得的mda浓度无明显差异,其中以50℃较好。
实施例4不同反应时间对丙二醛与硫代巴比妥酸反应的影响
(1)材料
以楸树1年生种子苗经低温(-4℃)处理后的叶片为材料。
(2)试剂配制
三氯乙酸(tca)溶液:浓度为0.75%。
硫代巴比妥酸(tba)溶液:浓度为0.02mol/l。
硫酸铁(fe2(so4)3)溶液:浓度为0.02g/l。
(3)测定过程
首先,按照6种反应时间3次重复的设计,分别准确称取样品18份,每份1.00g,放入研钵中,分别加入2ml浓度为0.75%tca,研磨至匀浆,将匀浆转移至25ml离心管中,并用8ml浓度为0.75%的tca冲洗干净;然后,分别将离心管至于50℃恒温震荡器中振荡30min,旋转频率为110rpm;最终,取出震荡后的离心管,用定性滤纸过滤,滤液备用。
在18份提取液中各取1.5ml分别至于25ml具塞刻度试管中,分别加入1.5mltba溶液和150μlfe2(so4)3溶液,将试管放入沸水浴中加热15min、20min、25min、30min、35min、40min(每种时间下3份样品),取出室温冷却后用分光光度计测定450nm、532nm和600nm的吸光值。
(4)测定结果
按照式a计算叶片中的mda浓度,并取同一处理下3次重复的平均值,结果如图5所示。随反应时间的延长,测得的mda浓度成先升高后稳定的趋势,说明反应时间对mda与tba的显色反应有明显的影响。反应30min和35min时,反应效果最好,检测结果最高。因此,选择30min-35min为适宜的反应时间。
以上所述实施例仅表达了本发明的优选实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形、改进及替代,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!