一种铬酵母中六价铬的测定方法与流程
本发明涉及酵母元素的测定领域,具体涉及铬酵母元素中六价铬元素含量测定方法。
背景技术:
铬(cr)是人体的必需微量元素,参与糖代谢调节、促进蛋白质合成和生长发育等。铬缺乏可导致葡萄糖和脂类代谢的改变,并与糖尿病、心血管疾病和神经系统疾病有关。目前,铬营养素补充剂有无机铬(如三氯化铬、硝酸铬)及有机铬(如烟酸铬、吡啶甲酸铬、铬酵母)。无机铬生物活性及吸收率很低、效果差;烟酸铬和甲基吡啶铬虽是有机铬,但作为铬的合成品,其生物亲合力低。因此,目前最有效的补铬剂是铬酵母,铬酵母是以酵母为载体,使无机铬转化为有机铬的发酵产品。其中铬以有机大分子形式存在,无毒无副作用,生物利用度高,吸收效果好,提高胰岛素生物效应。在国内,2005年发布的《营养素补充剂申报与审评规定》(试行)将铬酵母作为铬营养素补充剂的化合物来源,每日摄入量为15-150微克/天(以铬计);作为功能性原料,每日摄入量不得超过250微克/天,在保健食品领域已有多年的安全使用历史。在国外,2012年11月欧洲食品安全局(efsa)认为,在总铬每日摄入量不超过who制定的250微克/天的条件下,铬酵母作为食物原料是安全的。铬酵母还可有效遏制糖尿病的扩大化及年轻化倾向,是目前世界上正在研究的一种理想的铬源。另外,铬酵母本身富含蛋白质、糖类和b族维生素等营养物质,除可作为铬源使用外,还同时提供其他有益营养素。
不同形态的cr在生物体内会产生完全不同的作用,铬的毒性与其价态密切相关,铬从-2到+6价态都有,三价铬cr(iii)和六价铬cr(vi)是自然界中最常见的稳定价态,cr(vi)毒性最大,其致畸、致癌和致突变毒性比cr(iii)高10~100倍。国际癌症研究机构把cr(vi)归为1类“对人致癌”物的范围。cr(vi)比cr(iii)易吸收,有机铬比无机铬易吸收。因此,cr(iii)才是真正意义上人和动物机体必需的微量元素,而cr(vi)则是严格管控的元素。因此建立铬酵母中铬形态分析方法,准确检测六价铬的含量,对于正确评价铬酵母的毒性有着重要的意义。
铬形态的分析方法主要有分光光度法、原子吸收光谱法、离子光谱法、离子色谱与电感耦合等离子体质谱联用法、高效液相色谱与电感耦合等离子体联用法等。分光光度法操作复杂,试剂稳定性差,易受其他金属离子的的干扰,灵敏度差;原子吸收光谱法无法直接区分cr(ⅲ)和cr(ⅵ),只能通过差减法或者其他前处理技术来完成cr(vi)的检测;离子色谱定性能力较差。电感耦合等离子体质谱联用法以独特的接口技术将电感耦合等离子体的高温电离特性与质谱的灵敏快速扫描相结合而形成的一种高灵敏的分析方法,离子色谱或高效液相色谱与电感耦合等离子体质谱联用是目前分析铬形态重要的方法。此外,铬的2种价态在检测过程的转化是存在的,在碱性条件下,cr(iii)容易被氧化成cr(vi),一般用较弱的氧化剂如过氧化氢即可被氧化;在酸性条件下,cr(iii)不容易被氧化成cr(vi),但在有较强的氧化剂如高锰酸钾存在、温度高于30℃下,cr(iii)离子可能被氧化成cr(vi)。因此铬价态分析的检测技术仍将是今后分析领域的研究重点之一。由于铬酵母基质复杂,不同的提取方式和检测条件对测定结果有很大的影响,因此需要寻找合适的样品预处理方法,避免分析过程中不同形态铬之间的转化,同时需要寻找更加合理、简单而有效的不同铬价态的分离技术,从而进一步提高检测方法的灵敏度和选择性。目前关于铬酵母中cr(vi)的hplc-icp-ms检测方法的报道仅有2篇,均采用强碱性溶液提取铬酵母中cr(vi),导致铬酵母中大量cr(iii)转化为cr(vi),因此现有方法无法准确测定铬酵母中cr(vi)的含量。
2006年,yang等使用同位素稀释法,用naoh-na2co3碱性提取液提取酵母中的六价铬,阴离子交换液相色谱(lc)分离和扇形场电感耦合等离子体质谱(sf-icp-ms)检测同时测定酵母中cr(iii)和cr(vi)。2014年,guo等同样使用naoh-na2co3碱性提取液在90-95℃水浴1h提取铬酵母中的cr(vi),使用阴离子交换色谱柱分离,电感耦合等离子体质谱法(icp-ms)测定cr(vi)的含量。
化妆品中cr(vi)用氢氧化钠溶液提取,液相色谱-电感耦合等离子体质谱测定[8]。保健品中cr(vi)用氢氧化钠和碳酸钠碱性溶液提取,离子色谱-电感耦合等离子体质谱法测定。化妆品和保健品中cr(vi)提取溶液的ph值与铬价态密切相关,铬酵母是经酵母生化转化而来,铬所处微环境复杂,碱性条件下提取很容易使酵母铬的cr(iii)氧化成cr(vi),所以上述两种方法不适用于铬酵母中cr(vi)检测。
[1]yangl,cicerie,mesterz,sturgeonre.applicationofdouble-spikeisotopedilutionfortheaccuratedeterminationofcr(iii),cr(vi)andtotalcrinyeast.analbioanalchem.2006,386:1673-1680.
[2]guox,liuw,baix,hex,zhangb.speciationofchromiuminchromiumyeast.worldjmicrobiolbiotechnol.2014;30:3245-3250.
[3]sn/t3821-2014出口化妆品中六价铬的测定液相色谱-电感耦合等离子体质谱法.
[4]sn/t2210-2008保健食品中六价铬的测定离子色谱-电感耦合等离子体质谱法.
元素形态分析最重要的是元素形态的“原位”分析,保持元素原始形态不变的样品前处理方法的开发是元素形态分析的关键。已有研究表明,在碱性条件下,cr(iii)容易被氧化成cr(vi),而现有技术中均用naoh-na2co3碱性提取液,ph约为12,在此条件下,铬酵母中元素原始形态发生改变,cr(iii)会转换成cr(vi),导致结果不准确。
技术实现要素:
本发明所要解决的技术问题是现有技术食品铬元素的测量特别是六价铬元素不能准确测量,为此,本发明提供一种测定铬酵母中cr(vi)简单方便的测定方法ic-icp-ms方法及样品制备方法,包括:(1)维持铬酵母中元素原始形态不变的样品处理方法;(2)ic-icp-ms分析方法。
具体来说,本发明提供了如下测量方法。
一种铬酵母中六价铬的测定方法,其包括如下步骤:
1)混合标准样品的配制:分别称取cr(iii)和cr(vi)与edta溶液超声混合,在沸水浴加热,得到0.1-50ng/ml混合标准样品溶液;
2)质控样品的处理:称取不含铬的酵母样品,加入cr(iii)和cr(vi)的混合标准样品溶液,加入edta溶液,超声混合,沸水浴加热,上清液过滤后得到质控样品溶液;
3)样品处理:称取铬酵母样品,加入edta溶液溶解,超声混合、沸水浴加热,上清液过滤分离后得到样品溶液;
4)采用离子色谱仪和电感耦合等离子体质谱仪将含铬酵母中的cr(vi)与cr(iii)及杂质有效分离并测定。
优选地,对于本发明所述的测定方法,其中离子色谱仪的色谱柱为:dionexionpacag7;流动相:(0.4-0.8)mmol/ledta-(0.06-0.090)mol/lnh4no3,流动相ph为6.5-7.6。
优选地,对于本发明所述的测定方法,其中,所述电感耦合等离子体质谱仪的质谱条件为:雾化气流量1.0l/min,等离子体气(氩气)流量14.0l/min。
优选地,对于本发明所述的测定方法,其中,所述质谱条件还包括:辅助气氩气流量为0.8l/min,优选采样深度为5mm,或优选质谱冷却水流速为0.91l/min。
优选地,对于本发明所述的测定方法,其中,该方法的cr(iii)检出限为0.5ng/ml,定量限为1ng/ml;cr(vi)的检出限为0.04ng/ml,定量限为0.1ng/ml。
优选地,对于本发明所述的测定方法,其中,该方法的三价铬标准曲线为y=58119x+10216,相关系数为0.9991,线性范围为2-50ng/ml;该方法的六价铬标准曲线为y=57473x+271.1,相关系数为0.9991,线性范围为0.5-50ng/ml。
优选地,对于本发明所述的测定方法,其中,所述步骤2)中的所述cr(iii)和cr(vi)的混合标准样品溶液浓度为,0.1-50ng/ml,其中所述cr(iii)和cr(iv)的质量比例为1:1。
优选地,对于本发明所述的测定方法,其中,步骤1)、步骤2)或步骤3)中的edta溶液浓度均为2-100mmol/l。
优选地,对于本发明所述的测定方法,其中,步骤1)、步骤2)或步骤3)中,所述沸水浴加热进行3-10min。
优选地,对于本发明所述的测定方法,其中,步骤2)中得到质控样品溶液浓度分别为1、20和40ng/ml。
优选地,对于本发明所述的测定方法,其中,步骤1)、步骤2)或步骤3)中,所述超声混合进行10-20min。
优选地,对于本发明所述的测定方法,其中,步骤1)、步骤2)或步骤3)中,所述edta溶液的ph值为6.5-7.6。
本发明针对铬酵母采用本发明特定的样品处理方法,能维持铬酵母中元素原始形态不变,有效提取铬酵母中的cr(vi),并能阻止cr(iii)转换为cr(vi),样品前处理提取过程操作简便,易于重复。
相较于现有方法,本发明的上述方法能够维持铬酵母中元素原始形态不变,防止分析过程中cr(vi)与cr(iii)的互相转换,能有效提取铬酵母中的cr(vi),通过离子色谱将cr(vi)与cr(iii)及其他杂质有效分离并测定,方法灵敏度高,特异性好、分析速度快和准确可靠。
附图说明
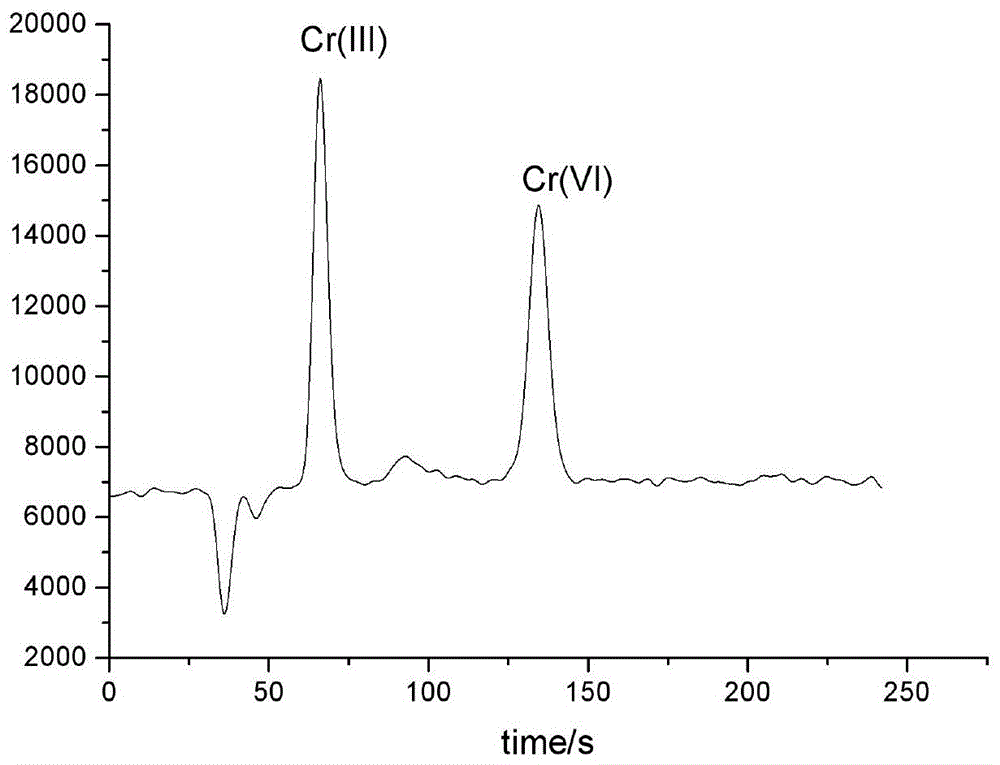
图1是本发明配制的cr(iii)、cr(vi)标准溶液色谱-质谱图;
图2是本发明实施例1的铬酵母样品色谱质谱图。
具体实施方式
本发明旨在对铬酵母中的三价铬和六价铬进行准确测定。博士论文“碰撞反应池-电感耦合等离子体质谱在食品分析中的应用”(作者聂西度,导师梁逸曾教授,中南大学,2013年)也公开了采用icp-ms方法测定土豆和坚果中的铬元素,然而该方法中仅仅探讨研究了测定总铬含量,并没有分开测定三价铬和六价铬元素。另外,专利公开号为“cn10685546a”也公开了一种采用ic-icp-ms测定茶叶中的三价铬和六价铬的方法,然而,由于铬酵母中铬含量高达1000-2000μg/g,是茶叶、坚果、土豆中铬含量的几千至数万倍,且cr(iii)含量也远高于cr(vi)。cr含量较高,则必须保证提取完全,同时保证cr(iii)和cr(vi)之间不发生价态转换。另一方面铬酵母是以食品加工用酵母、含三价铬的培养基经种子培养、发酵罐发酵、离心、过筛、分装制得,因此铬酵母本身富含蛋白质、糖类和b族维生素等营养物质,成分复杂多样,对cr(vi)的测定会产生较多干扰。因此从样品本身特性来说,铬酵母中cr(vi)的测定难度就高于其他样品。
本发明为了准确测定铬酵母中六价铬,保持测定中cr(iii)和cr(vi)之间不发生价态转换,在测定中,利用超声加速样品溶解,在沸水浴(100℃)中加速edta与cr(iii)的络合,防止cr(iii)转换成cr(vi)。
具体来说,为了准确测定铬酵母中的三价铬和六价铬元素含量,在本发明的一种优选实施方式中,本发明的测定铬酵母中cr(vi)的ic-icp-ms方法完整技术方案如下:
1)检测的前期准备:
(1)设备:电感耦合等离子体质谱仪:thermoicaprqicp-ms(美国赛默飞);离子色谱仪:thermodionexics-5000+(as-dv全自动进样器、sp高压毛细管泵)(美国赛默飞);超声仪:天津恒奥超声波清洗器hu10260,功率260w(0-100%),频率40khz。离心机:z326高速冷冻离心机(德国hermle)。
(2)试剂:氨水、硝酸铵、二水合乙二胺四乙酸(edta),国产分析纯。六价铬标准物质(1000μg/ml,中国计量科学研究院gbw(e)080257);三价铬标准物质(1000μg/ml,中国计量科学研究院gbw0861414022)。
2)建立ic-icp-ms分析方法
(1)ic色谱条件:色谱柱:dionexionpacag7(4×50mm);流动相:(0.4-0.8)mmol/ledta-(0.06-0.090)mol/lnh4no3(氨水调ph6.5-7.6);流速:1ml/min,进样量25μl;洗脱:等度洗脱。
(2)质谱条件:质谱条件:雾化气流量1.0l/min,等离子体气(氩气)流量14.0l/min,功率:1550w,辅助气流量:0.8l/min,采样深度5mm,质谱冷却水流速0.91l/min;质量测定数52、53,采用ked模式。
3)标准样品配制
1000μg/mlcr(iii)与1000μg/mlcr(vi)分别取1ml加到100ml量瓶中,2-100mmedta(氨水调节ph6.5-7.6)定容,得到10μg/ml混合溶液。2.5ml10μg/ml混合溶液加到100ml量瓶中,edta定容,得到250ng/ml混合溶液,沸水浴3-10min,冷却,稀释至0.1-50ng/ml。
4)质控样品处理
准确称取不含铬的酵母样品约0.2g,于25ml容量瓶中,加入适量cr(iii)和cr(vi)混合标准样品溶液,加入2-100mmedta,超声10-20min,定容,沸水浴3-10min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得1,20and40ng/ml质控样品溶液。
5)样品处理
准确称取铬酵母样品约0.2g,于25ml容量瓶中,加入2-100mmedta溶解,超声10-20min,定容,沸水浴3-10min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得样品溶液。
6)结果计算
采用外标标准曲线法计算六价铬含量。
以下实施例用于说明本发明,但不能用来限制本发明的范围。实施例中采用的实施条件可以根据具体条件作进一步调整,未说明的实施条件通常为常规实验中的条件。
实施例1:铬酵母中六价铬的测定
1.检测的前期准备:
(1)设备:电感耦合等离子体质谱仪:thermoicaprqicp-ms(美国赛默飞);离子色谱仪:thermodionexics-5000+(as-dv全自动进样器、sp高压毛细管泵)(美国赛默飞);超声仪:天津恒奥超声波清洗器hu10260,功率260w(100%),频率40khz。离心机:z326高速冷冻离心机(德国hermle)。
(2)试剂:氨水、硝酸铵、二水合乙二胺四乙酸(edta),国产分析纯。六价铬标准物质(1000μg/l,中国计量科学研究院gbw(e)080257);三价铬标准物质(1000μg/l,中国计量科学研究院gbw0861414022)。
2.建立icp-ms分析方法
(1)色谱条件:色谱柱:dionexionpacag7(4×50mm);流动相:0.6mmol/ledta-0.076mol/lnh4no3(氨水调ph6.5-7.6);流速:1ml/min。
(2)质谱条件:质谱条件:雾化气流量1.0l/min,等离子体气(氩气)流量14.0l/min,功率:1550w,辅助气流量:0.8l/min,采样深度5mm,质谱冷却水流速0.91l/min;质量测定数52、53,采用ked模式。
3.标准样品配制
1000μg/mlcr(iii)与1000μg/mlcr(vi)分别取1ml加到100ml量瓶中,10mmedta(氨水调节ph7.0)定容,得到10μg/ml混合溶液。2.5ml10μg/ml混合溶液加到100ml容量瓶中,10mmedta定容,得到250ng/ml混合溶液,沸水浴5min,冷却,稀释至0.1-50ng/ml。
4.质控样品处理
准确称取不含铬的酵母样品约0.2g,于25ml容量瓶中,加入适量cr(iii)和cr(vi)混合标准样品溶液,加入10mmedta,超声(天津恒奥超声波清洗器hu10260,功率260w(100%),频率40khz)10min,定容,沸水浴5min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得1,20和40ng/ml质控样品溶液。
5.样品处理
准确称取铬酵母样品约0.2g,于25ml容量瓶中,加入10mmedta溶解,超声10min(超声条件与步骤4相同,以下同),定容,沸水浴5min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得样品溶液。
6.结果分析
(1)三价铬和六价铬标准溶液色谱-质谱图见图1,铬酵母中三价铬和六价铬的色谱-质谱图见图2。
(2)方法学验证
三价铬的检出限为0.5ng/ml,定量限为1ng/ml,标准曲线为y=58119x+10216,相关系数为0.9991,线性范围为2-50ng/ml;六价铬的检出限为0.04ng/ml,定量限为0.1ng/ml,标准曲线为y=57473x+271.1,相关系数为0.9991,线性范围为0.5-50ng/ml。具体测定结果如下面的表1和表2所示。
表1:三价铬分析方法学的准确度、精密度
表2:六价铬分析方法学的准确度、精密度
实施例2:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件相同,区别仅在于:流动相浓度不同为:0.4mmol/ledta-0.090mol/lnh4no3。
3.标准样品配制
1000μg/mlcr(iii)与1000μg/mlcr(vi)分别取1ml加到100ml量瓶中,100mmedta(氨水调节ph6.5)定容,得到10μg/ml混合溶液。2.5ml10μg/ml混合溶液加到100ml容量瓶中,100mmedta定容,得到250ng/ml混合溶液,沸水浴5min,冷却,稀释至0.1-50ng/ml。
4.质控样品处理
准确称取不含铬的酵母样品约0.2g,于25ml容量瓶中,加入适量cr(iii)和cr(vi)混合标准样品溶液,加入100mmedta(氨水调节ph6.5),超声10min,定容,沸水浴5min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得1,20和40ng/ml质控样品溶液。
5.样品处理
准确称取铬酵母样品约0.2g,于25ml容量瓶中,加入100mmedta(氨水调节ph6.5)溶解,超声10min,定容,沸水浴5min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得样品溶液。
6.结果分析
三价铬的检出限为0.5ng/ml,定量限为1ng/ml,标准曲线为y=62368x+9262,相关系数为0.9993,线性范围为2-50ng/ml;六价铬的检出限为0.04ng/ml,定量限为0.1ng/ml,标准曲线为y=60432x+7.177,相关系数为0.9992,线性范围为0.5-50ng/ml。
具体测定结果如下面的表3和表4所示。
表3:三价铬分析方法学的准确度、精密度
表4:六价铬分析方法学的准确度、精密度
实施例3:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件相同,区别仅在于:流动相浓度不同为:0.4mmol/ledta-0.090mol/lnh4no3。
3.标准样品配制
1000μg/mlcr(iii)与1000μg/mlcr(vi)分别取1ml加到100ml量瓶中,2mmedta(氨水调节ph7.6)定容,得到10μg/ml混合溶液。2.5ml10μg/ml混合溶液加到100ml容量瓶中,2mmedta定容,得到250ng/ml混合溶液,沸水浴10min,冷却,稀释至0.1-50ng/ml。
4.质控样品处理
准确称取不含铬的酵母样品约0.2g,于25ml容量瓶中,加入适量cr(iii)和cr(vi)混合标准样品溶液,加入2mmedta(氨水调节ph7.6),超声20min,定容,沸水浴10min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得1,20和40ng/ml质控样品溶液。
5.样品处理
准确称取铬酵母样品约0.2g,于25ml容量瓶中,加入2mmedta(氨水调节ph7.6)溶解,超声20min,定容,沸水浴10min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得样品溶液。
6.结果分析
三价铬的检出限为0.5ng/ml,定量限为1ng/ml,标准曲线为y=66793x+13088,相关系数为0.9993,线性范围为2-50ng/ml;六价铬的检出限为0.04ng/ml,定量限为0.1ng/ml,标准曲线为y=65653x-4788,相关系数为0.9994,线性范围为0.5-50ng/ml。
具体测定结果如下面的表5和表6所示。
表5:三价铬分析方法学的准确度、精密度
表6:六价铬分析方法学的准确度、精密度
实施例4:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件相同,区别仅在于:流动相浓度不同为:0.8mmol/ledta-0.06mol/lnh4no3。
3.标准样品配制
与实施例1相同。
4.质控样品处理
准确称取不含铬的酵母样品约0.2g,于25ml容量瓶中,加入适量cr(iii)和cr(vi)混合标准样品溶液,加入10mmedta(氨水调节ph7.0),超声15min,定容,沸水浴3min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得1,20和40ng/ml质控样品溶液。
5.样品处理
准确称取铬酵母样品约0.2g,于25ml容量瓶中,加入10mmedta(氨水调节ph7.0)溶解,超声15min,定容,沸水浴3min,冷却,定容至刻度线,4000r/min离心10min,上清液过0.45μm滤膜,即得样品溶液。
6.结果分析
三价铬的检出限为0.5ng/ml,定量限为1ng/ml,标准曲线为y=58123x+10065,相关系数为0.9996,线性范围为2-50ng/ml;六价铬的检出限为0.04ng/ml,定量限为0.1ng/ml,标准曲线为y=57450x+1603,相关系数为0.9999,线性范围为0.5-50ng/ml。
具体测定结果如下面的表7和表8所示。
表7:三价铬分析方法学的准确度、精密度
表8:六价铬分析方法学的准确度、精密度
对比例1:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件相同。
3.标准样品配制
对于得到的混合溶液进行80℃的加热10min,除此之外其他与实施例1基本相同。
4.质控样品处理
对于得到的混合溶液进行80℃的加热10min,其他与实施例1相同。
5.样品处理
对于得到的混合溶液进行80℃的加热10min,其他与实施例1基本相同。
6.结果分析
结果发现,在此条件下测定富铬酵母时,由于富铬酵母中三价铬含量过高,三价铬不能与edta不能充分结合,致使样品溶液图谱中三价铬的色谱峰有拖尾不能与六价铬的色谱峰分离,不能准确检测。经分析是由于:仅在80℃水浴时加热10min,富铬酵母中过量的三价铬难以与edta结合完全,会导致部分三价铬出峰干扰六价铬测定。
对比例2:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件相同。
3.标准样品配制
与实施例1基本相同。
4.质控样品处理
不进行超声处理,其他与实施例1相同。
5.样品处理
不进行超声处理,其他与实施例1基本相同。
6.结果分析
结果发现,富铬酵母样品不进行超声,样品中的铬无法全部进入提取溶液中,无法进行准确检测。
对比例3:铬酵母中六价铬的测定
1.检测的前期准备:其准备过程和条件以及所使用仪器与实施例1相同。
2.建立icp-ms分析方法
与实施例1方法和条件基本相同。
3.标准样品配制
与实施例1基本相同。
4.质控样品处理
除了edta的ph值为8之外,与实施例1基本相同。
5.样品处理
除了edta的ph值为8之外,其他与实施例1基本相同。
6.结果分析
结果发现质控样品中三价铬的回收率低于50%,而六价铬的回收率超高了150%,由此可见,当edta提取液ph值为8时部分三价铬转换成了六价铬,发生了价态转换,无法准确检测。
上面的实施例表明,采用本发明的特定的方法和条件表明测定铬酵母中的六价铬速度快、专属性好、准确度高,防止了分析过程中cr(vi)与cr(iii)的互相转换,能有效提取铬酵母中的cr(vi)。
- 还没有人留言评论。精彩留言会获得点赞!