质谱分析用试剂盒、微生物识别用试剂盒、试样的制备方法、分析方法和微生物的识别方法与流程
本发明涉及质谱分析用试剂盒、微生物识别用试剂盒、试样的制备方法、分析方法和微生物的识别方法。
背景技术:
利用基质辅助激光解吸电离(以下称为maldi,matrixassistedlaserdesorption/ionization)法对试样进行电离的质谱分析是可适宜地用于微生物的识别等各种用途的分析方法。利用了maldi法的质谱分析中,在样品板的多个试样配置部位配置分别制得的多个试样(以下称为质谱分析用试样),通过对各试样配置部位照射激光而使质谱分析用试样电离。
还有时在1个样品板上配置例如数十个以上的质谱分析用试样后,将该样品板配置于质谱仪上进行质谱分析,这些质谱分析用试样的制备需要繁杂的操作。
在制备质谱分析用试样时,通过除了基质之外使用适合的基质的添加剂,从而有时可以得到更精密的测定数据(参照专利文献1),但进行在各试样中加入基质的添加剂的操作时,质谱分析用试样的制备成为更繁杂的操作。
现有技术文献
专利文献
专利文献1:日本特开2009-121857号公报
技术实现要素:
发明要解决的问题
期望的是减轻通过基质辅助激光解吸电离法进行质谱分析用试样的制备时操作的繁杂程度。
用于解决问题的方案
根据本发明的第1方式,质谱分析用试剂盒用于通过基质辅助激光解吸电离而使试样电离的质谱分析,所述质谱分析用试剂盒具备:固体状态的、基质试剂和/或基质的添加剂;以及分别配置有前述基质试剂和/或前述添加剂的多个容器。
根据本发明的第2方式,在第1方式的质谱分析用试剂盒中,前述多个容器各自的容量优选为100μl以上且5ml以下。
根据本发明的第3方式,在第2方式的质谱分析用试剂盒中,前述多个容器各自的容量优选为200μl以上且3ml以下。
根据本发明的第4方式,在第1~第3中的任一方式的质谱分析用试剂盒中,前述多个容器的个数优选为5以上。
根据本发明的第5方式,在第1~第4中的任一方式的质谱分析用试剂盒中,优选在前述多个容器中的每一个容器中,混合并配置有前述基质试剂和前述添加剂。
根据本发明的第6方式,在第1~第5中的任一方式的质谱分析用试剂盒中,前述基质试剂优选包含构成固体基质或液体基质的物质。
根据本发明的第7方式,在第1~第6中的任一方式的质谱分析用试剂盒中,优选进一步具备溶剂,所述溶剂配置于与配置有前述基质试剂和/或前述添加剂的前述多个容器不同的溶剂用容器中。
根据本发明的第8方式,在第1~第7中的任一方式的质谱分析用试剂盒中,前述添加剂优选包含具有膦酸基的化合物。
根据本发明的第9方式,微生物识别用试剂盒具备第1~第8中的任一方式的质谱分析用试剂盒。
根据本发明的第10方式,试样的制备方法为用于进行基质辅助激光解吸电离的质谱分析的多个试样的制备方法,其具备如下操作:准备分别配置有固体状态的、基质试剂和/或基质的添加剂的多个容器;以及使用前述基质试剂和/或前述添加剂,制备包含分别对应于前述多个容器的多个试样的质谱分析用试样。
根据本发明的第11方式,在第10的方式的试样的制备方法中,优选在配置有前述添加剂的前述多个容器中的每一个容器中,加入前述试样、基质试剂和溶剂来制备前述质谱分析用试样。
根据本发明的第12方式,在第10的方式的试样的制备方法中,优选在前述多个容器中的每一个容器中,混合并配置有前述基质试剂和前述添加剂,在配置有前述基质试剂和前述添加剂的前述多个容器中的每一个容器中,加入前述试样和溶剂来制备前述质谱分析用试样。
根据本发明的第13方式,分析方法具备如下操作:利用第10~第12中的任一方式的试样的制备方法来制备质谱分析用试样;对前述质谱分析用试样照射激光进行电离;以及对经电离的前述质谱分析用试样进行质谱分析。
根据本发明的第14方式,微生物的识别方法具备如下操作:利用第10~第12中的任一方式的试样的制备方法来制备质谱分析用试样,所述质谱分析用试样含有微生物所包含的多种蛋白质;对前述质谱分析用试样照射激光进行电离;对经电离的前述质谱分析用试样进行质谱分析来制作质谱;以及进行前述质谱中的峰与存储于数据库中的多种微生物所包含的蛋白质的质谱峰的比较;以及基于前述比较来识别前述微生物为何种微生物。
发明的效果
根据本发明,能够减轻利用基质、基质的添加剂进行质谱分析用试样的制备时的、操作的繁杂程度,因此能够有效地进行质谱分析。
附图说明
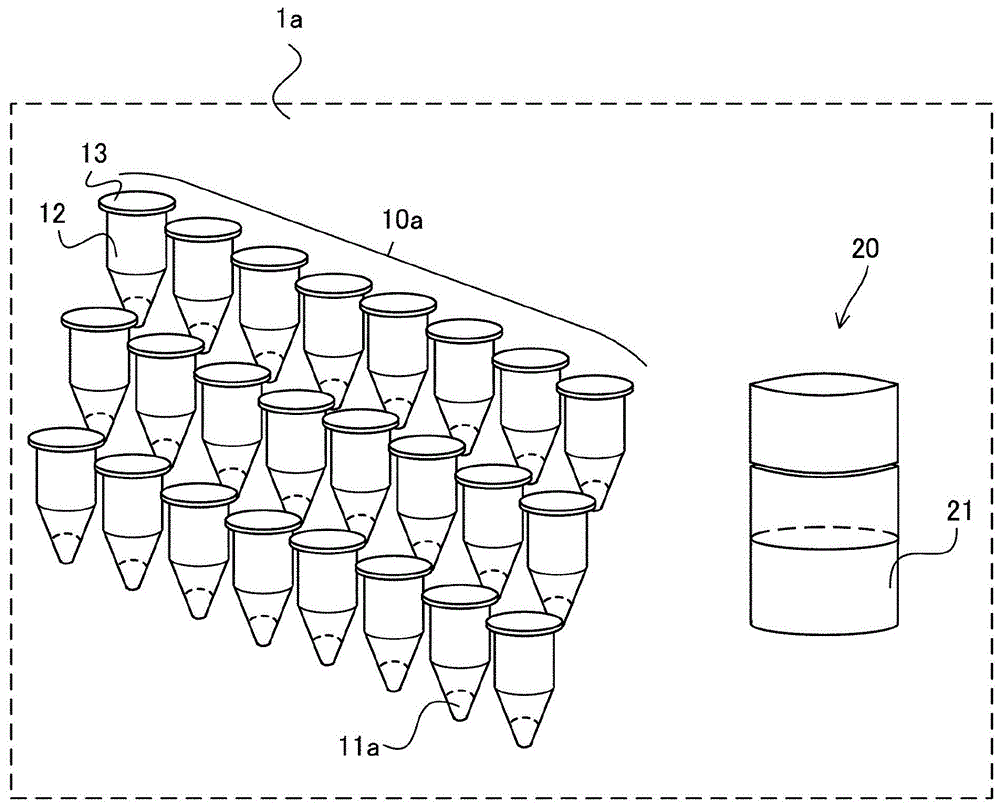
图1是示出一个实施方式的质谱分析用试剂盒的示意图。
图2是示出一个实施方式的试样的制备方法的示意图。
图3是示出一个实施方式的微生物的识别方法的流程的流程图。
图4是示出变形例的质谱分析用试剂盒的示意图。
图5是示出变形例的试样的制备方法的示意图。
图6是示出变形例的微生物的识别方法的流程的流程图。
图7是示出变形例的质谱分析用试剂盒的示意图。
图8是示出变形例的质谱分析用试剂盒的示意图。
图9是示出实施例1中在未使用基质的添加剂的情况下由皮肤常驻菌制得的质谱分析用试样的质谱。
图10是实施例1中使用包含mdpna作为基质的添加剂的质谱分析用试剂盒由皮肤常驻菌制得的质谱分析用试样的质谱。
图11是实施例2中使用包含mdpna作为基质的添加剂的质谱分析用试剂盒由乳酸菌制得的质谱分析用试样的质谱(上半部分)及在未使用基质的添加剂的情况下由乳酸菌制得的质谱分析用试样的质谱(下半部分)。
具体实施方式
以下参照图对用于实施本发明的方式进行说明。
图1是本实施方式的质谱分析用试剂盒的示意图。质谱分析用试剂盒1a具备:固体状态的、基质的添加剂(以下适宜地简称为添加剂)11a、存储有添加剂11a的多个容器(以下称为添加剂用容器)10a、及存储有溶剂21的容器(以下称为溶剂用容器)20。添加剂用容器10a具备添加剂用容器主体12和添加剂用容器盖部13。
需要说明的是,质谱分析用试剂盒1a还可以包含质谱分析中使用的其它物品。另外,质谱分析用试剂盒1a具备包含添加剂11a的添加剂用容器10a即可,也可以不包含溶剂21。
添加剂用容器10a的容量优选基于如下量:在通过maldi法进行电离的质谱分析时,滴加至样品板上的配置试样的部位(以下称为试样配置部位)的质谱分析用试样的量。由此,在添加剂用容器10a中加入试样和基质试剂而可以适宜地制备质谱分析用试样。
需要说明的是,还可以在添加剂用容器10a中制备包含添加剂11a的溶液(以下称为添加剂溶液)后分注于其它容器中,在该其它容器中制备质谱分析用试样。
maldi中,在1个添加剂用容器10a内制备1种质谱分析用试样并配置于多个试样配置部位的情况,若在每个位置滴加1μl的质谱分析用试样,则需要数μl的质谱分析用试样。即使考虑到配置于试样配置部位的质谱分析用试样的量可以设定为0.2μl、1.5μl等不同于1μl的值,添加剂用容器10a的容量也无需那么大。因此,从节约保管时所占的空间的观点出发,添加剂用容器10a的容量优选5ml以下,更优选2ml以下,更进一步优选1.5ml以下,进一步优选1.0ml以下,更进一步优选0.5ml以下。
添加剂用容器10a的容量过小时,变得难以操作,因此添加剂用容器10a的容量优选100μl以上,更优选200μl以上。
图1中示出了24个添加剂用容器10a,但质谱分析用试剂盒1a中包含的存储有添加剂11a的添加剂用容器10a的个数没有特别限定。
maldi用的样品板中,有售设置有例如96个位置、384个位置等试样配置部位的样品板,若一旦将样品板配置于质谱仪上,则还有时在该状态下进行校正等后进行配置于几个位置~数百个位置的试样配置部位的试样的分析。因此,质谱分析用试剂盒1a中包含的添加剂用容器10a的个数优选2以上,更优选5以上,更进一步优选10以上,进一步优选20以上。质谱分析用试剂盒10a中包含的添加剂用容器10a的个数越多,越能够减少用于购入等存储有添加剂11a的添加剂用容器10a来进行补充的操作。
质谱分析用试剂盒1a中包含的添加剂用容器10a的个数过多时,会发生保管期间变长而添加剂11a失去活性、或由于需要增大保管的空间而使收纳其它物品的空间变得狭窄等问题,因此其个数可以适宜地设为1000以下或500以下等。
添加剂用容器10a的形状等没有特别限定,添加剂用容器盖部13可以与添加剂用容器主体12形成为一个整体,还可以分别形成为使添加剂用容器盖部13与添加剂用容器主体12分离的多个部件。另外,添加剂用容器10a可以与其它添加剂用容器10a形成为一个整体,还可以例如8连管那样在规定个数的添加剂用容器10a中的每一个容器中,使添加剂用容器主体12和/或添加剂用容器盖部13形成为一个整体。
配置于各添加剂用容器10a中的添加剂11a用于制备包含基质的质谱分析用试样,在质谱分析中,只要可期待降低噪音或提高分析对象的离子的检测灵敏度等任意的效果就没有特别限定。
添加剂11a优选包含具有膦酸基的化合物。作为具有1个膦酸基的化合物,优选膦酸(phosphonicacid)、甲基膦酸(methylphosphonicacid)、苯基膦酸(phenylphosphonicacid)、1-萘基甲基膦酸(1-naphthylmethylphosphonicacid)等。
作为具有2个以上膦酸基的化合物,优选亚甲基二膦酸(methylenediphosphonicacid;以下称为mdpna)、亚乙基二膦酸(ethylenediphosphonicacid)、乙烷-1-羟基-1,1-二膦酸(ethane-1-hydroxy-1,1-diphosphonicacid)、次氮基三膦酸(nitrilotriphosphonicacid)、亚乙基二氨基四膦酸(ethylenediaminetetraphosphonicacid)等,更优选亚甲基二膦酸(mdpna)。
通过对使用包含具有膦酸基的化合物的添加剂11a而制得的质谱分析用试样进行质谱分析,从而能够降低噪音、或提高微生物的、特别是细胞质成分等所包含的蛋白质等的检测灵敏度、或提高磷酸化肽等肽的检测灵敏度。在质谱分析中检测出正离子的情况下及检测出负离子的情况下也可发挥这样的效果。
添加剂11a以固体状态存储于各自的添加剂用容器10a中。由此,与溶解于溶剂中而以溶质的形式保存的情况相比,能够更长期地维持活性。
包含添加剂11a的添加剂用容器10a的制造方法如下所述。使用适合的溶剂制备以规定的浓度包含添加剂11a的溶液后,使用吸液管、分注装置等将规定量的该溶液分注于各自的添加剂用容器10a中。若将分注有包含添加剂11a的溶液的添加剂用容器10a干燥,则可以得到固体状态的包含添加剂11a的添加剂用容器10a。包含添加剂11a的溶液的干燥方法没有特别限定,可以在将添加剂用容器10a的添加剂用容器盖部13打开的状态下放置,进而还可以进行通过真空干燥器等的减压。
质谱分析用试剂盒1a中,对于存储于与添加剂用容器10a不同的溶剂用容器20中的溶剂21,在制备质谱分析用试样时,可适宜地用于制备包含基质试剂的溶液(以下称为基质溶液)、添加剂溶液等。
溶剂21优选有机溶剂或者将有机溶剂和水系溶剂混合而得到的溶剂,有机溶剂、水系溶剂的种类没有特别限定。若列举一个例子,则溶剂21由如下水溶液构成,所述水溶液包含0%以上且1%以下等的以规定的体积百分比浓度制得的三氟乙酸(tfa)和任意浓度的乙腈(acn)。乙腈的体积百分比浓度可以适宜设定为数十%、特别是50%等。通过使用如此包含有机溶剂而制得的溶剂21来制备包含试样、基质试剂等的溶液,从而能够容易地溶解基质试剂,另外,试样为革兰氏阴性菌等时,能将细胞壁破碎并更容易使所得的质谱分析用试样电离。
存储溶剂21的溶剂用容器20的形状、容量等没有特别限定,可以使用任意大小的小瓶等容器作为溶剂用容器20。
图2是示出使用了质谱分析用试剂盒1a的试样的制备方法的示意图。对于添加剂用容器10a中包含基质试剂的情况,在变形例中进行后述,因此,此处在添加剂用容器10a中不包含基质试剂。
图2的方法中,在除添加剂用容器10a以外的未图示的容器中制备包含试样和基质试剂的溶液(以下称为含有基质的试样溶液)sm后,加入至添加剂用容器10a(箭头a11)中。基质试剂的种类可适宜地进行电离即可,没有特别限定,可以适宜使用以下的变形例中所列举的基质试剂等。进行分析的质谱分析用试剂盒1a的用户(以下简称为用户)使用吸液管p1、未图示的分注装置等将含有基质的试样溶液sm加入至添加剂用容器10a所包含的添加剂11a中。
然后,适宜地使用混合器等将添加剂11a和含有基质的试样溶液充分混合,制备质谱分析用试样sma(箭头a12)。使用吸液管p2、未图示的分注装置等将所制得的质谱分析用试样sma配置于样品板40的各试样配置部位41(箭头a13)中。由此,使用质谱分析用试剂盒1a时,在分成小份的添加剂11a中加入溶液而能够直接制备质谱分析用试样sma,因此能够减轻该制备时操作的繁杂程度。
需要说明的是,还可以在基质试剂中加入溶剂21等溶剂制备基质溶液后,进行将基质溶液加入至添加剂用容器10a中等操作来制备含有添加剂的基质溶液,在制得的含有添加剂的基质溶液中加入试样来制备质谱分析用试样sma。
以下,作为适宜地使用了本实施方式的质谱分析用试剂盒的分析的一个例子,对通过质谱分析进行的微生物的识别方法进行说明。将质谱分析用试剂盒1a用作微生物识别用试剂盒。
需要说明的是,只要是使用添加剂来制作质谱分析用试样的情况,本实施方式的质谱分析用试剂盒就还可以用于除微生物的识别之外的目的。
图3是示出包含本实施方式的质谱分析用试剂盒的试样的制备方法、分析方法和微生物的识别方法的流程的流程图。
在步骤s1001中,准备:包含基质试剂的容器、分别配置有固体状态的添加剂11a的多个容器(添加剂用容器10a)、用于溶解基质试剂和添加剂11a的溶剂;以及含有微生物所包含的蛋白质的试样。该试样优选为由培养微生物得到的单个菌落采集的微生物、使用甲酸等从微生物中提取的提取液。例如,在识别食品等中包含的微生物的情况下,可以如下方式进行:将从食品中提取的含有微生物的液体涂布于培养基等上后,进行培养,从得到的菌落中提取含有微生物的菌体提取物。步骤s1001结束后,开始进行步骤s1003。
在步骤s1003中,在包含基质试剂的容器中加入溶剂来制备基质溶液。对于基质溶液,从有效地利用质谱分析用试剂盒1a的方面考虑,优选使用溶剂21进行制备,但只要可适宜地进行电离,则溶解基质试剂的溶剂就没有特别限定。步骤s1003结束后,开始进行步骤s1005。在步骤s1005中,在基质溶液中加入试样。步骤s1005结束后,开始进行步骤s1007。
在步骤s1007中,将包含试样的基质溶液加入至配置有添加剂11a的多个容器(添加剂用容器10a)中,将试样、基质试剂和添加剂11a混合,从而制备质谱分析用试样sma。步骤s1007结束后,开始进行步骤s1009。在步骤s1009中,将制得的质谱分析用试样sma滴加在样品板40上,进行干燥。步骤s1009结束后,开始进行步骤s1011。
在步骤s1011中,对干燥的质谱分析用试样sma照射激光,进行电离。将样品板40配置于质谱仪上,由该质谱仪的激光装置对质谱分析用试样sma照射激光而进行电离。只要可适宜地进行电离,则对激光的波长等没有特别限定,可以适宜使用n2激光(波长337nm)等。步骤s1011结束后,开始进行步骤s1013。
在步骤s1013中,对经电离的质谱分析用试样sma进行质谱分析而制作质谱。质谱分析的方法只要可以得到能以期望的精度进行微生物的识别的质谱就没有特别限定,从精度良好地检测分子量为数千~20000等的蛋白质的观点出发,优选飞行时间型的质谱分析。因此,进行该质谱分析的质谱仪优选具备飞行管等飞行时间型的质量分离部的质谱仪。
对上述质谱分析中离子进行检测而得到的检测信号通过a/d转换器而进行a/d转换并被输入具备cpu等的处理装置中。处理装置基于经a/d转换的检测信号来制作质谱。飞行时间型质谱分析的情况,处理装置使用预先得到的校正数据基于飞行时间计算出m/z,与各m/z对应地计算出检测出的强度而制作质谱。步骤s1013结束后,开始进行步骤s1015。
在步骤s1015中,进行质谱中的峰与存储于数据库中的多种微生物所包含的蛋白质的质谱峰的比较。该数据库中存储了微生物的菌种(属名和种形容語等)与质谱中观察到的峰的m/z相关联的数据。上述的处理装置基于根据质谱分析的精度而确定的误差范围,判断对应于数据库中所示的m/z的峰是否存在于通过对质谱分析用试样sma进行质谱分析而得到的质谱中,基于该判定计算出相似度。相似度是表示数据库上的微生物与对应于质谱分析用试样sma的微生物的质谱之间的相似程度的参数,相似度越高定义为质谱彼此越相似。步骤s1015结束后,开始进行步骤s1017。
需要说明的是,数据库中可以包括基于在各微生物的菌种的质谱中观察到对应于各m/z的峰的比例、概率等的加权信息,还可以基于该加权信息计算出相似度。
在步骤s1017中,基于在步骤s1015中的比较来识别试样中使用的微生物为何种微生物。上述的处理装置将计算出的相似度在一定水平以上且最高的、数据库上的微生物的菌种识别为试样中包含的微生物的菌种。识别出的菌种适宜地通过液晶监视器等显示装置而显示。步骤s1017结束后,结束处理。
需要说明的是,待识别的微生物的分类优选属、种,但只要基于质谱的差异能进行识别就没有特别限定。微生物的识别的方法只要基于对质谱分析试剂盒1a进行质谱分析而得到的结果进行,则没有特别限定。
上述的实施方式,可以得到以下的作用效果。
(1)本实施方式的质谱分析用试剂盒是通过maldi将试样电离的质谱分析中使用的质谱分析用试剂盒1a,其具备:固体状态的、基质的添加剂11a;以及分别配置有添加剂11a的多个添加剂用容器10a。由此,能够减轻利用添加剂11a进行质谱分析用试样sma的制备时的、操作的繁杂程度,因此能够有效地进行质谱分析。
(2)本实施方式的质谱分析用试剂盒中,还具备配置于与配置有添加剂11a的添加剂用容器10a不同的溶剂用容器20中的溶剂21。由此,一并提供能在制备添加剂溶液、基质溶液等时使用的溶剂21,因此能够减少购入等引起的补充的工时。
(3)本实施方式的试样的制备方法是进行maldi的质谱分析中使用的多个试样的制备方法,其具备如下操作:准备分别配置有固体状态的添加剂11a的多个添加剂用容器10a;使用添加剂11a和基质试剂,制备包含分别对应于多个添加剂用容器10a的多个试样的质谱分析用试样。由此,能够减轻操作的繁杂程度,因此能够有效地进行质谱分析。
(4)本实施方式的试样的制备方法中,在配置有添加剂11a的多个添加剂用容器10a中的每一个容器中加入试样、基质试剂和溶剂来制备质谱分析用试样sma。由此,无需进行包含添加剂11a的添加剂溶液的分注就能够制备质谱分析用试样sma。
(5)本实施方式的分析方法具备如下操作:利用上述的试样的制备方法来制备质谱分析用试样sma;以及对质谱分析用试样sma照射激光来进行电离;对经电离的质谱分析用试样sma进行质谱分析。由此,能够减轻利用添加剂11a进行质谱分析用试样sma的制备时的、操作的繁杂程度,因此能够有效地进行质谱分析。
(6)本实施方式的微生物的识别方法具备如下操作:利用上述的试样的制备方法来制备含有微生物所包含的多种蛋白质的质谱分析用试样sma;对质谱分析用试样sma照射激光来进行电离;对经电离的质谱分析用试样sma进行质谱分析来制作质谱;进行质谱中的峰与存储于数据库中的多种微生物所包含的蛋白质的质谱峰的比较;以及基于该比较来识别上述微生物为何种微生物。由此,能够减轻利用减小质谱分析中噪音或提高检测灵敏度的添加剂11a来进行质谱分析用试样sma的制备时的、操作的繁杂程度,因此能够有效地进行微生物的识别。
如下那样的变形也在本发明的范围内,可以与上述的实施方式进行组合。在以下的变形例中,关于与上述的实施方式同样的结构、显示出功能的部位等,通过相同的符号进行参照,适宜地省略说明。
(变形例1)
作为上述的实施方式中的适合的一个例子,添加剂用容器除了添加剂11a之外还可以包含基质试剂。
图4是表示本变形例的质谱分析用试剂盒的示意图。质谱分析用试剂盒1b具备添加剂用容器10b,添加剂用容器10b具备固体状态的基质试剂与固体状态的添加剂11a的混合物11b,在这点上与上述的实施方式的质谱分析用试剂盒1a不同。
对于混合物11b中的基质试剂的种类,只要适宜地进行电离就没有特别限定。基质试剂是指:在质谱分析用试样sma中,构成固体基质或液体基质的化合物。液体基质是指:在室温下以液体的状态存在、其实际的状态为盐的物质。基质试剂构成固体基质时,基质试剂优选9-氨基吖啶、4-氨基喹哪啶、9-蒽甲酸、氨茴酸酰胺、咖啡酸、姜黄素、4-氯-α-氰基肉桂酸、α-氰基-4-羟基肉桂酸、芥子酸、1,5-二氨基萘、2,5-二羟基苯甲酸、3-羟基焦磷酸或反式-2-[3-(4-叔丁基苯基)-2-甲基-2-亚丙基]丙二腈。
基质试剂构成液体基质时,优选:基质试剂包含胺和有机物质,胺作为质子的受体发挥作用,有机物质成为质子的供体。在此情况下,基质试剂优选在将构成液体基质的胺和有机物质混合并干固的状态下配置于添加剂用容器10a中。
需要说明的是,还可以在添加剂用容器10a中的每一个容器中,配置该胺或有机物质中的任意者。在此情况下,在质谱分析用试样sma的调整中,在添加剂用容器10a中配置有胺时,可以另行制备包含有机物质的溶液并加入至添加剂容器10a中,在添加剂用容器10a中配置有有机物质时,可以另行制备包含胺的溶液并加入至添加剂容器10a中。
构成液体基质的胺是伯胺的情况下,优选包含氮原子可以被oh基取代的、与甲基、乙基、正丙基、异丙基、正丁基、异丁基、正戊基、异戊基、正己基、异己基、正庚基、异庚基、正辛基、异辛基、正壬基、异壬基、正癸基、异癸基、正十一烷基或异十一烷基的残基、或苯基残基键合的伯胺。
构成液体基质的胺是仲胺或叔胺的情况下,优选包含氮原子可以被oh基取代的、与选自由甲基、乙基、正丙基、异丙基、正丁基、异丁基、正戊基、异戊基、正己基、异己基、正庚基、异庚基、正辛基和异辛基的残基、以及苯基残基组成的组中的同源或异源的2个或3个残基键合的仲胺或叔胺。
对于构成液体基质的胺,还优选包含3-氨基喹啉、吡啶、咪唑或c-或n-烷基化咪唑衍生物。
构成液体基质的有机物质优选包含:对香豆酸离子、2,5-二羟基苯甲酸或其异构体(特别是2,6-二羟基苯甲酸)、2-羟基-5-甲氧基苯甲酸或其异构体、焦磷酸、3-羟基焦磷酸、烟酸、5-氯-2-巯基苯并噻唑、6-氮杂-2-硫代胸苷、三氟甲磺酸酯、2’,4’,6’-三羟基苯乙酮一水合物、2’,6’-二羟基苯乙酮、9h-吡哆[3,4-b]吲哚、蒽三酚、反式-3-吲哚丙烯酸、脎类、阿魏酸、2,5-二羟基苯乙酮、1-硝基咔唑、7-氨基-4-甲基香豆素、2-(对羟基苯基偶氮)-苯甲酸、8-氨基吡-2,3,4-三磺酸、2[2e-3-(4-叔丁基-苯基)-2-甲基丙烷-2-烯亚基]丙二腈(dctb)、4-甲氧基-3-羟基肉桂酸或3,4-二羟基肉桂酸。
需要说明的是,还可以将多种液体基质混合来使用。
如以下的实施例所示,在使用作为基质试剂的芥子酸等、作为其添加剂的mdpna等、包含具有膦酸基的化合物的添加剂11a而制备质谱分析用试样sma时,尤其能够提高质谱分析中的s/n比,更精密地进行试样的分析。
包含混合物11b的添加剂用容器10b的制造方法如下所述。使用能用于制备溶剂21等基质溶液的溶剂,制备以规定的浓度包含添加剂11a的添加剂溶液后,在该添加剂溶液中加入基质试剂而制备含有添加剂的基质溶液。然后,使用吸液管、分注装置等将含有规定量的添加剂的基质溶液分注在各添加剂用容器10b中。若将分注有含有添加剂的基质溶液的添加剂用容器10b干燥,则可以得到包含固体状态的混合物11b的添加剂用容器10b。含有添加剂的基质溶液的干燥方法没有特别限定,可以在将添加剂用容器10b的添加剂用容器盖部13打开的状态下放置,进而还可以进行通过真空干燥器等的减压。
图5是示出使用了质谱分析用试剂盒1b的试样的制备方法的示意图。图5的方法中,在除添加剂用容器10b以外的未图示的容器中制备包含试样的溶液s后,加入至添加剂用容器10b中(箭头a21)。用户使用吸液管p3、未图示的分注装置等将包含试样的溶液s加入添加剂用容器10b中包含的混合物11b中。
然后,适宜使用混合器等将试样、添加剂11a和基质试剂充分混合,制备质谱分析用试样sma(箭头a22)。使用吸液管p4、未图示的分注装置等将制得的质谱分析用试样sma配置于样品板40各试样配置部位41(箭头a23)。由此,若使用质谱分析用试剂盒1b,则在分成小份的基质试剂和添加剂11a中加入溶液而能够直接制备质谱分析用试样sma,因此能够减轻该制备时的操作的繁杂程度。
以下,作为适宜地使用本变形例的质谱分析用试剂盒的分析的一个例子,对通过质谱分析的微生物的识别方法进行说明。质谱分析用试剂盒1b用作微生物识别用试剂盒。需要说明的是,只要是使用添加剂来制作质谱分析用试样的情况,本变形例的质谱分析用试剂盒就还可以用于除微生物的识别之外的目的。
图6是包含本变形例的质谱分析用试剂盒的试样的制备方法、分析方法和微生物的识别方法的流程的流程图。
在步骤s2001中,准备:同时配置有固体状态的添加剂11a和固体状态的基质试剂的多个容器(添加剂用容器10b)、及含有微生物所包含的蛋白质的试样。步骤s2001结束后,开始进行步骤s2003。在步骤s2003中,在试样中加入溶剂来制备包含试样的溶液s。对于包含试样的溶液s,从使用溶剂21制备时有效地利用质谱分析用试剂盒1b的方面考虑而优选,但只要可适宜地进行电离,加入试样中的溶剂没有特别限定。步骤s2003结束后,开始进行步骤s2005。
在步骤s2005中,在同时配置有添加剂11a和基质试剂的多个容器10b中加入包含试样的溶液s,进行混合而制备质谱分析用试样sma。步骤s2005结束后,开始进行步骤s2007。从步骤s2007至步骤s2015为止,与从上述的实施方式中的流程图(图3)的步骤s1009至步骤s1017为止是同样的,因此省略说明。步骤s2015结束后,结束处理。
本变形例的质谱分析用试剂盒中,在多个添加剂用容器10b中的每一个容器中,还具备与添加剂11a混合而成的基质试剂。由此,能够进一步减轻利用添加剂11a进行质谱分析用试样sma的制备时的、操作的繁杂程度,因此能够有效地进行质谱分析。
本变形例的试样的制备方法中,多个添加剂用容器10b除了添加剂11a之外进一步包含固体状态的基质试剂,在配置有基质试剂和添加剂11a的多个添加剂用容器10b的的每一个容器中,中加入试样和溶剂来制备质谱分析用试样sma。由此,无需进行包含基质试剂的溶液的分注就能够制备质谱分析用试样sma。
(变形例2)
上述的实施方式中,质谱分析用试剂盒还可以具备:与配置有添加剂11a的多个添加剂用容器10a不同的基质用小瓶、及配置于该基质用小瓶的固体状态的基质试剂。基质试剂的种类没有特别限定,可以制成上述的变形例中所示的构成固体基质或液体基质的物质。
图7是示出本变形例的质谱分析用试剂盒的示意图。质谱分析用试剂盒1c不具备溶剂21,但具备基质用小瓶25a,基质用小瓶25a具备固体状态的基质试剂26,在这点上与上述的实施方式的质谱分析用试剂盒1a不同。由此,由于可在添加剂11a的基础上同时提供基质试剂26,因此能够减少购入等引起的进行补充的工时,另外能够灵活地调整质谱分析用试样sma中的基质的量。基质用小瓶25a的形状、容量等没有特别限定。还可以将基质试剂26与添加剂11a同样地分成小份地配置于多个基质用容器中。
需要说明的是,质谱分析用试剂盒1c还可以适宜具备溶剂21、其它消耗品。另外,基质用小瓶25a不限定于小瓶,可以使用任意的容器。
(变形例3)
上述的实施方式中,质谱分析用试剂盒不包含添加剂11a,还可以具备配置于基质用容器中的基质试剂,所述基质用容器具备与添加剂用容器10a同样的形状。基质试剂的种类没有特别限定,可以设为上述的变形例所示的构成固体基质或液体基质的物质。
图8是表示本变形例的质谱分析用试剂盒的示意图。质谱分析用试剂盒1d不具备溶剂21,但可以具备多个具有与上述的实施方式中的添加剂用容器10a同样的形状的基质用容器25b,该基质用容器25b分别具备固体状态的基质试剂26,在这点上与上述的实施方式的质谱分析用试剂盒1a不同。由此,能够节省分注等工时而迅速地制备质谱分析用试样。
需要说明的是,质谱分析用试剂盒1d还可以适宜具备将添加剂11a分成小份或未分成小份进行配置的容器、溶剂21等其它消耗品。另外,可以在基质用容器25b中的每一个容器中,配置构成液体基质的胺或有机物质中的任意者。在此情况下,通过分别制备包含胺的溶液和包含有机物质的溶液并进行混合而可以得到基质溶液。
从节约保管时所占的空间的观点出发,基质用容器25b的容量优选5ml以下,更优选2ml以下,更进一步优选1.5ml以下,进一步优选1.0ml以下,更进一步优选0.5ml以下。
基质用容器25b的容量过小时,变得难以操作,因此基质用容器25b的容量优选100μl以上,更优选200μl以上。
图8示出24个基质用容器25b,但存储有质谱分析用试剂盒1d中包含的基质试剂26的基质用容器25b的个数没有特别限定。
质谱分析用试剂盒1d中包含的基质用容器25b的个数优选2以上,更优选5以上,更进一步优选10以上,进一步优选20以上。质谱分析用试剂盒1d中包含的基质用容器25b的个数越多,越能够减少用于购入基质试剂26所存储的基质用容器25b等来进行补充的操作。
质谱分析用试剂盒1d中包含的基质用容器25b的个数过多时,会发生如下问题:保管期间变长而基质试剂26失去活性,或需要增大保管的空间而使收纳其它物品的空间变得狭窄等,因此该个数可以适宜设为1000以下或500以下等。
(变形例4)
上述的实施方式和变形例中,将质谱分析用试剂盒1a、1b、1c、1d用于预混料法,所述预混料法在制备包含试样、基质试剂及添加剂11a的质谱分析用试样后滴加至样品板上。然而,还可以将质谱分析用试剂盒1a、1b、1c、1d用于在样品板上形成试样/基质混晶后加入添加剂溶液的离子镀法。质谱分析用试剂盒1a、1b、1c中,由于将添加剂11a或基质试剂26分成了小份,因此在例如需要对添加剂11a或基质试剂26进行冷冻保存时等,无需重复多次冷冻融解,且能够更长期地维持添加剂11a或基质试剂26的活性。
实施例
以下示出实施例,但本发明不限定于下述的实施例。
(实施例1:皮肤常驻菌中包含的蛋白质的质谱分析)
<1-1.包含试样的溶液的制备>
将擦拭皮肤而获得的、含有微生物的试样涂布于gam培养基上,在37℃下进行厌氧培养。将在琼指平板上形成的单个菌落分散于20μl的包含1%三氟乙酸(tfa)的50%乙腈(acn)溶液中,得到菌体提取物。
<1-2.质谱分析用试剂盒的制作>
在芥子酸(以下称为sa)中加入含有1%tfa的50%acn水溶液,制备了20mg/ml的sa溶液。在mdpna中加入含有1%tfa的50%acn水溶液,制备了2mg/100mlmdpna溶液。
(1)sa试剂盒(比较例):将上述20mg/ml的sa溶液各5μl地加入pcr管中,将溶剂干燥。因此,加入10μl的溶液时制成10mg/mlsa溶液。
(2)含有mdpna的sa试剂盒(实施例):将上述20mg/ml的sa溶液和2mg/100ml的mdpna等量地进行混合,各10μl地加入pcr管中并将溶剂干燥。因此,加入10μl的溶液时制成含有mdpna的10mg/mlsa。
<1-3.maldi所致的质谱分析>
(1)将菌体提取物10μl加入至上述sa试剂盒中并进行充分混合,各1μl地滴加至maldi样品板上,进行干燥而得到试样/基质混晶。
(2)将菌体提取物10μl加入至含有上述mdpna的sa试剂盒中并进行充分混合,各1μl地滴加至maldi样品板上,进行干燥而得到试样/基质混晶。
对于(1)(2)各自的试样/基质混晶,通过线性模式进行飞行时间型质谱分析,测定了m/z3000-15000的范围。
图9是示出使用sa试剂盒而制得的试样的maldi质谱的图。试样1至5中均只检测出噪音,清晰的峰1根也没检测出。
图10是示出使用含有mdpna的sa试剂盒而制得到试样的maldi质谱的图。在使用含有mdpna的sa试剂盒而制得的试样的质谱中,能检测到清晰的峰。
(实施例2:乳酸菌中包含的蛋白质的质谱分析)
<2-1.包含试样的溶液的制备>
培养乳酸菌发酵乳杆菌(lactobacillusfermentum),用氧化锆珠进行破碎处理,以15000rpm进行10分钟离心分离并去除碎片。将得到的上清液溶解于含有1%tfa的50%acn水溶液中,得到菌体破碎液。
<2-2.maldi所致的质谱分析>
(1)以1:10的比混合菌体破碎液和基质溶液(sa10mg/ml)而制备混合液,滴加至maldi样品板上各1μl并进行干燥,得到试样/基质混晶(比较例)。
(2)加入10μl的溶剂时,在制成1%mdpna(1mg/100ml)的mdpna试剂盒中加入上述混合液10μl并进行混合,滴加至maldi样品板上各1μl并进行干燥,得到含有mdpna的试样/基质混晶(实施例)。
对于(1)(2)各试样/基质混晶,通过线性模式进行飞行时间型质谱分析,测定m/z4000-20000的范围。
图11是示出将使用mdpna试剂盒而制得的发酵乳杆菌(l.fermentum)的maldi质谱与未使用mdpna试剂盒而制得的发酵乳杆菌(l.fermentum)的质谱进行比较的图。上半部分的使用含有mdpna的试剂盒而制得的试样与下半部分的使用了sa试剂盒的对照区相比,可知显著地观测到s/n良好的峰。
本发明不限定于上述实施方式的内容。在本发明的技术思想的范围内考虑出的其它方式也包括在本发明的范围内。
以下的优先权基础申请的公开内容作为引用文引入其中。
日本专利申请2018年第078584号(2018年4月16日申请)
附图标记说明
1a、1b、1c、1d…质谱分析用试剂盒、10a,10b…添加剂用容器、11a…添加剂、11b…混合物、20…溶剂用容器、21…溶剂、25a…基质用小瓶、25b…基质用容器、26…基质试剂、40…样品板、41…试样配置部位、s…试样、sm…含有基质的试样溶液、sma…质谱分析用试样。
- 还没有人留言评论。精彩留言会获得点赞!