一种定性检测HLA-B27的试剂盒及其检测方法与流程
本发明属于免疫学检测技术领域,特别是涉及一种定性检测hla-b27的试剂盒及其检测方法。
背景技术:
强直性脊柱炎是一种发病率较高的脊柱关节炎,它是以骶髂关节以及脊柱附属关节等组织炎症性病变的自身免疫性疾病。由于强直性脊柱炎发病时间较长、病程进展缓慢、早期无明显的组织性病变,致使其早期诊断往往比较困难,一旦通过影像学观察到相关组织病变并确诊为强直性脊柱炎,往往是在病程的中后期,会造成患者中轴脊柱的不可逆损伤。强直性脊柱炎主要发病群体是青壮年,且男性多于女性,发病早期的身体不适也容易被忽视,这也致使强直性脊柱炎成为了一种致残率较高的疾病,因此强直性脊柱炎的早期诊断尤为重要。研究发现,人类白细胞抗原b27(humanleucocyteantigen-b27)在强直性脊柱炎的早期诊断中也发挥着重要的作用,90%以上的强直性脊柱炎患者表现为hla-b27阳性,而正常人群的hla-b27阳性仅为5%左右。在临床诊断中,hla-b27阳性是强直性脊柱炎患者最终确诊的一个重要指标。
目前监测hla-b27的方法有为了细胞毒法、酶联免疫吸附测定、流式细胞术、序列特异引物引导的pcr反应等,前两种方法敏感性、特异性较差,已逐渐被流式细胞仪替代。而现有的采用流式细胞仪法的hla-b27的检测方法多为使用美国bd公司开发的试剂盒,该方法操作步骤较复杂,需要裂解洗涤步骤,同时该试剂盒属于封闭系统,仅能在bd的部分流式细胞仪上使用特定的软件检测,由于市面上国产化流式细胞仪增加,机型种类丰富加上bd公司的试剂成本较高,对于目前的情况难以满足强制性脊柱炎的普筛推广。
技术实现要素:
本发明的目的是弥补现有技术的不足,提供一种定性检测hla-b27的试剂盒及其检测方法,利用本发明的试剂盒对hla-b27进行的定性检测能够降低假阳性的比率,特异性较高,并且操作简单,无需对红细胞裂解液进行清洗,减少了生物危害性,同时,本发明的试剂盒适用范围广,进一步降低了检测成本。
为了达到上述的目的,本发明采取以下技术方案:
一种定性检测hla-b27的试剂盒,所述试剂盒包括单克隆抗体混合物hla-b27fitc、hla-b7和cd3percp,红细胞裂解液,以及标准荧光微球。
本发明中的单克隆抗体为国产化单克隆抗体,同时hla-b27和cd3使用的是fitc和percp荧光素,两则之间荧光通道间干扰极小,基本不存在荧光补偿。
进一步地,本发明的试剂盒中各单克隆抗体的质量比为:hla-b27fitc:purifiedhla-b7:cd3percp=0.01~1.00:0.1~10.0:0.0125~0.125。
进一步地,本发明的试剂盒中红细胞裂解液包括甲醛、二乙二醇、柠檬酸钠、肝素钠和纯化水,其中,甲醛、二乙二醇、柠檬酸钠和肝素钠在细胞裂解液中的质量浓度分别为2.5%~25%、10%~35%、2%~5%和5ku~20ku。
本发明的红细胞裂解液裂解人外周血样本,使样本仅保留白细胞,并维持至少24小时样本稳定性;常规同类方法检测使用的裂解液需要离心弃去裂解液,富集白细胞才能检测,而本发明的红细胞裂解液不需要离心清洗,减少hla-b27检测的操作步骤,增加了检测效率,并减少出错率及生物危害性。
进一步地,本发明的试剂盒中的标准荧光微球为fitc8000~12000mesf,浓度为20000个/ml,来源于bangslaboratories,inc。
本发明采用标准荧光微球能够对不同厂家及配置的流式细胞仪做标准设置的配置,使本发明的试剂盒适用范围更广。
进一步地,本发明的试剂盒中含有单克隆抗体20μl,红细胞裂解液450μl,标准荧光微球1ml。
本发明还提供一种定性检测hla-b27的检测方法,该检测方法利用上述的定性检测hla-b27的试剂盒,包括如下步骤:
(1)取试剂盒中的单克隆抗体混合物和50μl的外周血室温避光孵育15分钟,加入稀释1倍后的试剂盒中的红细胞裂解液室温避光孵育15分钟,得到检测样本;
(2)使用标准荧光微球对不同厂家及配置的流式细胞仪做标准设置的配置;
(3)将检测样本上流式细胞仪检测,测定cd3+hla-b27+群的中位值荧光强度;
(5)根据确定的hla-b27定性阈值,判断人外周血样本hla-b27阴阳性结果。
进一步地,所述步骤(5)采用临床确定的hla-b27阴性和阳性样本使用roc曲线确定hla-b27的定性阈值。
进一步地,不同仪器的定性阈值范围如下:
aceanovocyte,阳性阈值9000,阴性阈值10000;
bdfacscalibri,阳性阈值800,阴性阈值900;
bcdxflex,阳性阈值1500,阴性阈值1600;
ubdiagcyto,阳性阈值2000,阴性阈值2100。
进一步地,所述步骤(2)使标准荧光微球的信号值为104±5%。
本发明具有以下技术特点:
1)本发明使用国产化的单克隆抗体,同时hla-b27和cd3使用的是fitc和percp荧光素,两则之间荧光通道间干扰极小,基本不存在荧光补偿,能够有效提高本发明的检测特异性。
2)本发明的红细胞裂解液不仅能够保证红细胞的有效破碎,同时降低细胞的自发荧光,而且检测样本制备过程无需离心,过程更加简单,提高了样本制备效率,缩短了整个检测时间。
3)本发明使用标准荧光微球对不同的流式细胞仪(至少含488nm激光)进行仪器标准设置的配置,使得该方法(或试剂盒)能在不同配置的流式细胞仪上使用。
4)本发明制定外周血样本hla-b27定性阈值,采用临床确定的500多例hla-b27阴性和阳性样本使用roc曲线确定hla-b27的定性阈值,对人外周血检测的cd3+hla-b27+值判断其hla-b27阴性和阳性结果。
附图说明
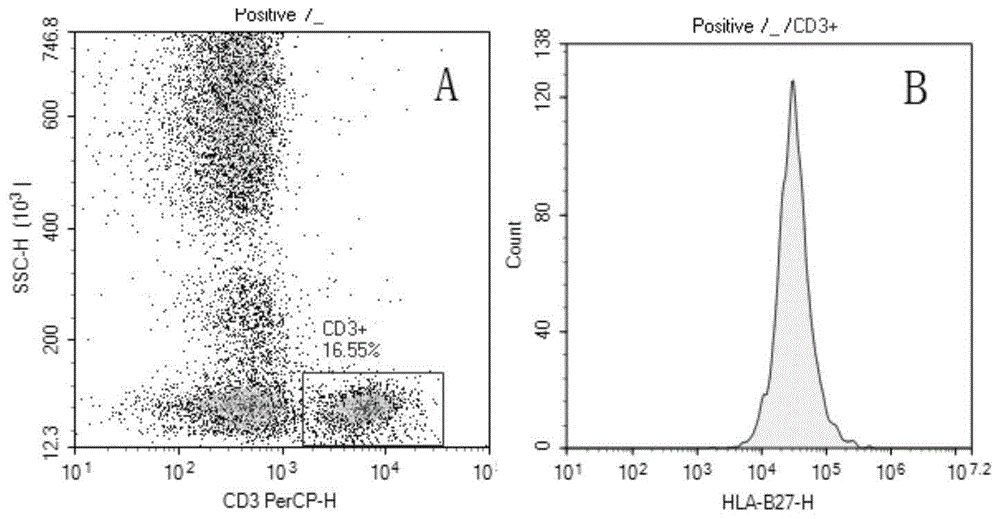
图1hla-b27阳性样本,检测机型aceanovocyte(a为cd3vsssc图,用于圈出t淋巴细胞,b为hla-b27vscount图,读取cd3+群,显示为cd3+hla-b27+荧光强度峰。
图2hla-b27阴性样本,检测机型aceanovocyte(a为cd3vsssc图,用于圈出t淋巴细胞,b为hla-b27vscount图,读取cd3+群,显示为cd3+hla-b27+荧光强度峰)。
具体实施方式
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例的技术方案进行清楚、完整的描述。显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于所描述的本发明的实施例,本领域普通技术人员在无需创造性劳动的前提下所获得的所有其他实施例,都属于本发明的保护范围。
除非另作定义,本公开所使用的技术术语或者科学术语应当为本发明所属领域内有一般技能的人士所理解的通常意义,本公开所使用的试剂均为市场上可以购买获得的。
实施例1
试剂盒包含
(1)单克隆抗体原材料hla-b27fitc/cd3percp(含purifiedhla-b7):
1)hla-b27fitc,cloneabc.m3使用浓度0.01~1.00μg/test;
2)purifiedhla-b7,clonebb7.1使用浓度0.1~10.0μg/test;
3)cd3percp,clonesk7使用浓度0.0125~0.125μg/test;
(2)免洗红细胞裂解液原材料:
1)甲醛浓度2.5%~25%;
2)二乙二醇浓度10%~35%
3)柠檬酸钠浓度2%~5%
4)肝素钠浓度5ku~20ku
(3)标准荧光微球
fitc8000~12000mesf1ml(微球数量在20000个)。
实施例1的试剂盒与人hla-b27核酸检测试剂盒同时检测269例临床样本(其中159例hla-b27阳性,110例hla-b27阴性),本方法的操作步骤为取20μlhla-b27fitc/cd3percp(含purifiedhla-b7)试剂和50μl外周血室温避光15分钟,加入450μl稀释至1×的免洗的红细胞裂解液室温避光孵育15分钟,即可上机检测,检测结果如表1所示。
表1实施例1检测结果
检测结果表明,本发明的实施例1检测灵敏度为158/159=99.37%,特异性108/110=98.18%,总体符合率(158+108)/269=98.88%。
实施例2
试剂盒包含
(1)单克隆抗体原材料hla-b27fitc/cd3percp(含purifiedhla-b7):
1)hla-b27fitc,cloneabc.m3使用浓度0.01~1.00μg/test;
2)purifiedhla-b7,clonebb7.1使用浓度0.1~10.0μg/test;
3)cd3percp,clonesk7使用浓度0.0125~0.125μg/test;
(2)免洗红细胞裂解液原材料:
1)甲醛浓度2.5%~25%;
2)二乙二醇浓度10%~35%
3)柠檬酸钠浓度2%~5%
4)肝素钠浓度5ku~20ku
(3)标准荧光微球
fitc8000~12000mesf1ml(微球数量在20000个)。
检测的流式细胞仪包括
aceanovocyte
bdfacscalibur
bcdxflex
ubdiagcyto
实施例2与人hla-b27核酸检测试剂盒同时检测498例临床样本(其中269例hla-b27阳性,229例hla-b27阴性),本方法的操作步骤为取20μlhla-b27fitc/cd3percp(含purifiedhla-b7)试剂和50μl外周血室温避光15分钟,加入450μl稀释至1×的免洗的红细胞裂解液室温避光孵育15分钟,即可上机检测,其中使用校准微球上各台流式细胞仪,各流式细胞仪调整荧光通道的电压/增益值将微球的荧光信号调整至如表2所示对应值。其中检测机型为aceanovocyte时hla-b27阳性样本如图1所示,hla-b27阴性样本如图2所示。其中,图1a为cd3vsssc图,用于圈出t淋巴细胞,图1b为hla-b27vscount图,读取cd3+群,显示为cd3+hla-b27+荧光强度峰;图2a为cd3vsssc图,用于圈出t淋巴细胞,图2b为hla-b27vscount图,读取cd3+群,显示为cd3+hla-b27+荧光强度峰。
表2各流式细胞仪的标准荧光微球信号值
检测结果显示如表3-5所示,从269例阳性样本和229例阴性样本的判断结果看,表3两台仪器的一致性为100%,表4两台仪器的一致性为99.80%,表5两台仪器的一致性为99.80%。
表3ubdiagcyto和aceanovocyte检测结果
表4ubdiagcyto和bdfacscalibur检测结果
表5ubdiagcyto和bcdxflex检测结果
因此,本发明拓展了检测使用的流式细胞仪,提高了现有医院/检验服务平台的资源利用率,降低该检验项目的检测成本。
以上实施例的说明只是用于帮助理解本发明方法及其核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!