一种sBCMA磁微粒化学发光免疫检测试剂盒及其制备方法和应用与流程
本发明属于化学发光免疫分析技术领域,涉及一种sbcma磁微粒化学发光免疫检测试剂盒及其制备方法和应用。
背景技术:
多发性骨髓瘤(multiplemyeloma,mm)是一种以血液和尿液含有高浓度单克隆抗体为主要特征的克隆性浆细胞异常增殖的恶性肿瘤,占全部恶性肿瘤的1%,其发病率位居血液系统恶性肿瘤第2位,多发于老年人。目前,临床上缺乏有效的标志物对多发性骨髓瘤进行诊断和预后监测,对于疑似mm的患者,需要进行凝血功能、血清蛋白电泳(包括m蛋白含量)、尿免疫固定电泳、骨髓活检、血液血清游离轻链(sflc)测定等大量检验以达到诊断目的,预后监测同样需要进行大量的检测。
b细胞成熟抗原(bcellmaturationantigen,bcma),又称为肿瘤坏死因子受体超家族成员17(tnfrs17),是一种iii型跨膜蛋白,仅表达在成熟b细胞表面。bcma的表达与许多癌症,自身免疫性疾病和感染性疾病相关。具有增加的bcma表达的癌症包括一些血液癌症,例如多发性骨髓瘤,霍奇金淋巴瘤和非霍奇金淋巴瘤,各种白血病和胶质母细胞瘤等。bcma是用于治疗mm的合适的靶抗原。
bcma胞外部分可被γ-分泌酶切割形成可溶性bcma(sbcma)。研究表明,测定血液sbcma水平可为mm患者提供重要的诊断和预后监测信息。诊断方面,活跃期mm患者的血清sbcma浓度高于早期mm患者,且均明显高于健康人。预后监测方面,mm病人接受治疗后,外周血中的sbcma比m蛋白降低速度更快,且其浓度不受肾功能的影响,较sflc检测更可靠,能更好的预测治疗响应状态。
磁微粒化学发光免疫检测技术是利用具有超顺磁性、粒径均一的固体粒子作为固相载体包被抗体或抗原,同时将具有高灵敏度的化学发光技术与之相结合,用于测定各种蛋白、激素、小分子药物等的免疫检测技术,是在放射免疫检测技术(irma)和酶联免疫吸附检测技术(elisa)的基础上发展而来的免疫分析技术,具有灵敏度高等优点。
目前,国内外检测sbcma的方法主要是酶联免疫吸附测定法,该方法线性范围窄,稳定性较差,操作繁琐,检测时间长,自动化程度低,易受人为操作影响,制约了sbcma检测的应用。
因此,本领域急需开发一种能够快速高效诊断多发性骨髓瘤,且检测结果准确可靠的sbcma检测试剂盒,以满足市场需求。
技术实现要素:
鉴于现有技术中存在的问题,本发明提供一种sbcma磁微粒化学发光免疫检测试剂盒及其制备方法和应用,所述免疫检测试剂盒制备方法简单,检测待测样品时实验操作也较为简便,检测效率高,所得检测结果准确可靠。
为达此目的,本发明采用以下技术方案:
第一方面,本发明提供一种sbcma磁微粒化学发光免疫检测试剂盒,包括:偶联链霉亲和素的磁微粒、生物素标记的sbcma抗体、化学发光标记物标记的sbcma抗体、sbcma蛋白校准品、清洗液和激发液。
本发明提供的sbcma检测试剂盒,在检测待测样品中的sbcma蛋白时,sbcma蛋白、生物素标记的sbcma抗体和化学发光标记物标记的sbcma抗体能够形成“三明治夹心”结构,同时链霉亲和素和生物素结合,利用磁微粒作为载体,使得本发明提供的检测试剂盒具有反应快速、干扰因素较少和检测结果准确可靠等优点,同时,链霉亲和素和生物素的放大效应使得所述试剂盒具有较宽的线性范围。
作为本发明一种优选的技术方案,所述生物素标记的sbcma抗体选自sbcma蛋白的单克隆抗体和/或多克隆抗体。
优选地,所述化学发光标记物标记的sbcma抗体选自sbcma蛋白的单克隆抗体和/或多克隆抗体。
优选地,所述化学发光标记物为吖啶酯。
本发明中,使用吖啶酯作为化学发光标记物具有背景发光低、信噪比高、发光反应干扰因素少,光释放快速集中、发光效率高、发光强度大等优点,且吖啶酯易于与蛋白质联结且联结后光子产率不减少,同时吖啶酯稳定,在2-8℃下可保存数月之久。
作为本发明一种优选的技术方案,所述磁微粒为四氧化三铁微粒。
优选地,所述磁微粒的表面覆盖有亲水性聚合物涂层和羧基官能团。
优选地,所述磁微粒的粒径为0.5~3μm,例如可以是0.5μm、0.8μm、1μm、1.2μm、1.5μm、1.8μm、2μm、2.2μm、2.4μm、2.5μm、2.8μm或3μm等。
作为本发明一种优选的技术方案,所述激发液包括激发液1和激发液2,所述激发液1包含硝酸和过氧化氢,所述激发液2包含氢氧化钠和表面活性剂。
优选地,所述激发液1为含有硝酸和过氧化氢的水溶液。
优选地,所述硝酸的摩尔浓度为0.05~1m,例如可以是0.05m、0.1m、0.2m、0.25m、0.3m、0.5m、0.6m、0.7m、0.8m、0.9m或1m等。
优选地,所述过氧化氢的质量浓度为0.2~3%,例如可以是0.2%、0.5%、0.6%、0.8%、1%、1.2%、1.5%、1.8%、2%、2.2%、2.4%、2.5%、2.8%或3%等。
优选地,所述激发液2为含有氢氧化钠和表面活性剂的水溶液。
优选地,所述氢氧化钠的摩尔浓度为0.1~1m,例如可以是0.1m、0.2m、0.25m、0.3m、0.5m、0.6m、0.7m、0.8m、0.9m或1m等。
优选地,所述表面活性剂的质量浓度为0.5~4%,例如可以是0.5%、0.6%、0.8%、1%、1.2%、1.5%、1.8%、2%、2.5%、2.8%、3%、3.5%、3.8%或4%等。
优选地,所述表明活性剂为tritonx-100。
优选地,所述sbcma蛋白校准品的浓度为0~1000ng/ml,例如可以是0ng/ml、50ng/ml、100ng/ml、200ng/ml、300ng/ml、500ng/ml、600ng/ml、800ng/ml或1000ng/ml等。
优选地,所述sbcma磁微粒化学发光免疫检测试剂盒中包含6~10种(例如可以是6种、7种、8种、9种或10种等)不同浓度的sbcma蛋白校准品。
作为本发明一种优选的技术方案,所述sbcma磁微粒化学发光免疫检测试剂盒还包括清洗液。
优选地,所述清洗液为tris缓冲液。
优选地,所述清洗液的ph为7.3-7.5,例如可以是7.3、7.32、7.35、7.4、7.42、7.45或7.5等,优选为7.4。
优选地,所述清洗液中含有无机盐、表面活性剂或抑菌剂中的任意一种或两种以上的组合。
第二方面,本发明还提供一种如第一方面所述的sbcma磁微粒化学发光免疫检测试剂盒的制备方法,所述制备方法包括如下步骤:
(1)将磁微粒活化后加入链霉亲和素反应,制备偶联有链霉亲和素的磁微粒;
(2)制备生物素标记的sbcma抗体和化学发光标记物标记的sbcma抗体,而后配制激发液、清洗液和sbcma蛋白校准品,得到所述sbcma磁微粒化学发光免疫检测试剂盒。
本发明提供的制备方法步骤简单,对温度等条件的要求较为温和、不苛刻,便于易于制备,适合工业化生产。
作为本发明一种优选的技术方案,步骤(1)所述活化使用的活化剂为edc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)。
优选地,所述活化的时间为20~40min,例如可以是20min、22min、25min、28min、30min、32min、35min、38min或40min等。
优选地,步骤(1)所述加入链霉亲和素反应的时间为1~3h,例如可以是1h、1.2h、1.4h、1.5h、1.8h、2h、2.2h、2.5h、2.8h或3h等。
优选地,步骤(1)所述加入链霉亲和素反应的温度为23~28℃,例如可以是23℃、23.5℃、24℃、25℃、25.5℃、26℃、26.5℃、27℃、27.5℃或28℃等。
优选地,步骤(1)所述加入链霉亲和素反应后还包括加入封闭液封闭的操作。
优选地,步骤(2)所述制备生物素标记的sbcma抗体的方法为:将sbcma抗体与生物素混合,而后加入碳酸盐缓冲液反应1~2h(例如可以是1h、1.2h、1.4h、1.6h、1.8h或2h等)得到所述生物素标记的sbcma抗体。
优选地,所述sbcma抗体和生物素的分子数比为1:(10~20),例如可以是1:10、1:12、1:14、1:15、1:16、1:17、1:18或1:20等。
优选地,制备得到所述生物素标记的sbcma抗体后还包括透析的操作。
优选地,步骤(2)所述制备化学发光标记物标记的sbcma抗体的方法为:将sbcma抗体与化学发光标记物混合,而后加入碳酸盐缓冲液反应1~2h(例如可以是1h、1.2h、1.4h、1.6h、1.8h或2h等)得到所述化学发光标记物标记的sbcma抗体。
优选地,制备得到所述化学发光标记物标记的sbcma抗体后还包括透析的操作。
作为本发明一种优选的技术方案,所述制备方法包括如下步骤:
(1)先用偶联缓冲液清洗并重悬磁珠后,使用edc活化20~40min,而后加入链霉亲和素23~28℃下震荡反应1~3h,制备得到偶联有链霉亲和素的磁微粒,再加入封闭液进行封闭;
(2)将sbcma抗体与生物素混合,而后加入碳酸盐缓冲液反应1~2h,在2~8℃下透析后得到所述生物素标记的sbcma抗体,
(3)将sbcma抗体与化学发光标记物混合,而后加入碳酸盐缓冲液反应1~2h,在2~8℃下透析后得到所述化学发光标记物标记的sbcma抗体;
(4)配制激发液、清洗液和sbcma蛋白校准品,得到所述sbcma磁微粒化学发光免疫检测试剂盒。
第三方面,本发明提供一种如第一方面所述的sbcma磁微粒化学发光免疫检测试剂盒在检测sbcma中的应用。
本发明所述的数值范围不仅包括上述例举的点值,还包括没有列举出的上述数值范围之间的任意的点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
与现有技术相比,本发明至少具有以下有益效果:
(1)本发明提供的sbcma磁微粒化学发光免疫检测试剂盒采用磁微粒作为载体,提供了近似于均相的反应体系,选用吖啶酯为标记物,具有反应快速、干扰因素较少、检测结果准确、使用方法简单、检验效率高等优点;
(2)本发明提供的免疫检测试剂盒利用链霉亲和素和生物素放大效应,使得sbcma磁微粒化学发光免疫检测试剂盒能够在较宽的线性范围内测定sbcma浓度,线性更宽、稳定性更好,使用时样本无需稀释,可自动化检测,在临床检验和用药指导等方面有广阔的应用前景,填补了相关领域的空白。
附图说明
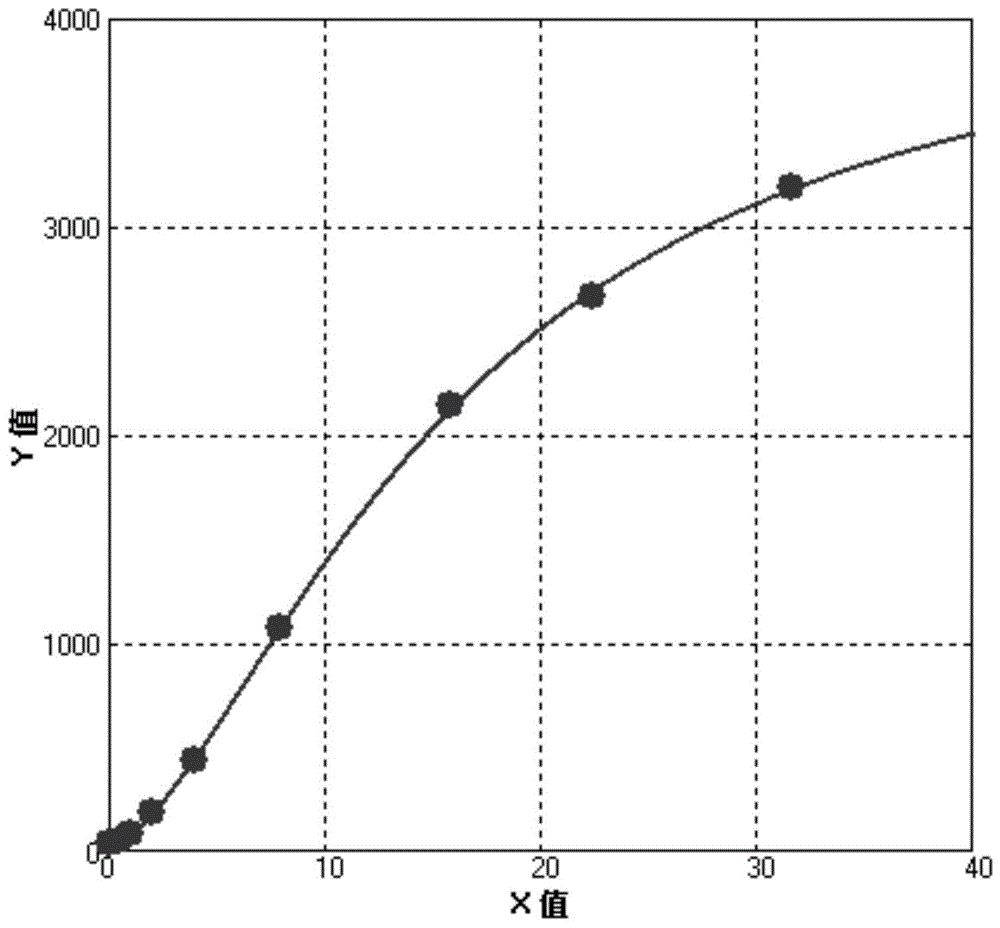
图1为实施例3中通过sbcma蛋白校准品得到的校准曲线。
图2为实施例4中sbcma磁微粒化学发光免疫检测试剂盒和humanbcma/tnfrsf17duosetelisakit对sbcma含量检测结果的相关性分析曲线图。
具体实施方式
下面结合附图并通过具体实施方式来进一步说明本发明的技术方案,但下述的实例仅仅是本发明的简易例子,并不代表或限制本发明的权利保护范围,本发明的保护范围以权利要求书为准。
以下实施例中,所用封闭液为含有质量分数为1~5%bsa、0.5~1‰蔗糖、1~2‰tween-20和0.5~2‰proclin300的ph为7.4的磷酸盐缓冲液。
以下实施例中所述室温为25℃。
以下实施例中,所用校准品稀释液为含有质量分数为0.9%nacl、10~20%bsa、0.5%酪蛋白、0.05~0.2%tween-20和0.1~0.2%proclin300的tris缓冲液。
实施例1
本实施例提供一种sbcma磁微粒化学发光免疫检测试剂盒,具体包含以下部分:偶联有链霉亲和素的磁微粒、生物素标记的sbcma抗体、吖啶酯标记的sbcma抗体、sbcma蛋白校准品、激发液和清洗液。
所述试剂盒的具体制备步骤如下:
(1)制备偶联有链霉亲和素的磁微粒
取10mg磁微粒于反应管中,磁分离1min去上清,用1ml偶联缓冲液(0.1mmes溶液,ph5.0)重悬,然后加入100μl浓度为10mg/ml的edc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐),室温震荡活化30min;
加入1000μg链霉亲和素,室温震荡反应2h,磁分离1min去上清,并用清洗液洗涤3次,然后加入1ml封闭液(含质量分数为2%bsa、0.1%proclin300、ph为7.4的磷酸盐缓冲液),室温震荡封闭1h,磁分离1min去上清,用清洗液洗涤磁微粒3次,得到偶联有链霉亲和素的磁微粒;
然后加入含0.9%nacl、1%bsa、0.5‰蔗糖、1‰tween-20、1‰proclin300的ph为7.4的磷酸盐缓冲液重悬,使磁微粒的浓度为1mg/ml,4℃保存待用。
(2)制备生物素标记的sbcma抗体
取1mg待标记的sbcma单克隆抗体(购自genetex公司)加入到反应管中,然后按照抗体分子和生物素分子数比为1:10的比例加入生物素溶液,最后加入50mm、ph9.0的碳酸盐缓冲液,充分混匀,室温反应1.5h得到生物素标记的sbcma抗体;
将标记后的抗体移入透析袋,以20mm的磷酸盐缓冲液为透析液,4℃条件下透析,每隔3h换一次透析液,更换5次以上,以去除未标记的生物素;
从透析袋中取出标记抗体,并加入等体积的甘油,轻轻吹打混匀,保存到-20℃待用。
(3)制备吖啶酯标记的sbcma抗体
取200μg待标记的sbcma单克隆抗体(r&dsystems公司)至反应管中,并加入0.5μl浓度为2mg/ml的吖啶酯溶液,然后加入50mm、ph9.0的碳酸盐缓冲液,充分混匀,室温避光反应2h得到吖啶酯标记的sbcma抗体;
将标记后的抗体移入透析袋,以20mm的磷酸盐缓冲液为透析液,4℃条件下透析,每隔4h换一次透析液,更换10次以上,以去除游离的吖啶酯;
从透析袋中将标记后抗体吸出,并加入等体积的甘油,轻轻吹打混匀,保存到-20℃待用。
(4)制备sbcma蛋白校准品
用校准品稀释液(含有0.9%氯化钠、10%bsa、0.5%酪蛋白、0.05%tween-20及0.1%proclin300的tris缓冲液)将sbcma蛋白(购自novoprotein公司)稀释成1000ng/ml、500ng/ml、250ng/ml、50ng/ml、25ng/ml、10ng/ml、2ng/ml和0.2ng/ml八个浓度的校准品,同时将不添加sbcma蛋白的校准品稀释液作为0ng/ml的校准品。
(5)制备激发液和清洗液
激发液包含激发液1和激发液2两种组分,激发液1为硝酸和过氧化氢水溶液,其中硝酸的摩尔浓度为0.05m,过氧化氢的质量分数为0.2%;激发液2为氢氧化钠和tritonx-100水溶液,其中氢氧化钠的摩尔浓度为0.1m,tritonx-100的体积分数为1%;
清洗液为含有质量分数为0.9%氯化钠、0.5‰表面活性剂tween-20及0.1%抑菌剂proclin300、ph为7.4的tris缓冲液,最终得到sbcma磁微粒化学发光免疫检测试剂盒。
实施例2
本实施例提供一种sbcma磁微粒化学发光免疫检测试剂盒,具体包含以下部分:偶联有链霉亲和素的磁微粒、生物素标记的sbcma抗体、吖啶酯标记的sbcma抗体、sbcma蛋白校准品、激发液和清洗液。
所述试剂盒的具体制备步骤如下:
(1)制备偶联有链霉亲和素的磁微粒
取10mg磁微粒于反应管中,磁分离1min去上清,用1ml偶联缓冲液重悬,然后加入100μl浓度为10mg/ml的edc,室温震荡活化30min;
加入2000μg链霉亲和素,室温震荡反应2h,磁分离1min去上清,并用清洗液洗涤3次,然后加入1ml封闭液(含质量分数为10%bsa、0.2%proclin300、ph为7.4的磷酸盐缓冲液),室温震荡封闭1h,磁分离1min去上清,用清洗液洗涤磁微粒3次,得到偶联有链霉亲和素的磁微粒;
然后加入封闭液(含0.9%nacl、5%bsa、1‰蔗糖、2‰tween-20、2‰proclin300的ph为7.4的磷酸盐缓冲液)重悬,使磁微粒的浓度为4mg/ml,4℃保存待用。
(2)制备生物素标记的sbcma抗体
取1mg待标记的sbcma单克隆抗体加入到反应管中,然后按照抗体分子和生物素分子数比为1:20的比例加入生物素溶液,最后加入50mm、ph9.0的碳酸盐缓冲液,充分混匀,室温反应2h得到生物素标记的sbcma抗体;
将标记后的抗体移入透析袋,以20mm的磷酸盐缓冲液为透析液,4℃条件下透析,每隔4h换一次透析液,更换5次以上,以去除未标记的生物素;
从透析袋中取出标记抗体,并加入等体积的甘油,轻轻吹打混匀,保存到-20℃待用。
(3)制备吖啶酯标记的sbcma抗体
取200μg待标记的sbcma单克隆抗体至反应管中,并加入0.5μl浓度为2mg/ml的吖啶酯溶液,然后加入50mm、ph9.0的碳酸盐缓冲液,充分混匀,室温避光反应2h得到吖啶酯标记的sbcma抗体;
将标记后的抗体移入透析袋,以20mm的磷酸盐缓冲液为透析液,4℃条件下透析,每隔4h换一次透析液,更换10次以上,以去除游离的吖啶酯;
从透析袋中将标记后抗体吸出,并加入等体积的甘油,轻轻吹打混匀,保存到-20℃待用。
(4)制备sbcma蛋白校准品
用校准品稀释液(含有%氯化钠、20%bsa、0.5%酪蛋白、0.2%tween-20及0.2%proclin300的tris缓冲液)将sbcma蛋白(购自novoprotein公司)稀释成1000ng/ml、500ng/ml、250ng/ml、50ng/ml、25ng/ml、10ng/ml、2ng/ml和0.2ng/ml八个浓度的校准品,同时将不添加sbcma蛋白的校准品稀释液作为0ng/ml的校准品。
(5)制备激发液和清洗液
激发液包含激发液1和激发液2两种组分,激发液1为硝酸和过氧化氢水溶液,其中硝酸的摩尔浓度为1m,过氧化氢的质量分数为3%;激发液2为氢氧化钠和tritonx-100水溶液,其中氢氧化钠的摩尔浓度为1m,tritonx-100的体积分数为4%;
清洗液为含有质量分数为0.9%氯化钠、2‰表面活性剂tween-20及0.2%抑菌剂proclin300、ph为7.5的tris缓冲液,最终得到sbcma磁微粒化学发光免疫检测试剂盒。
实施例3
本实施例中利用实施例1提供的sbcma磁微粒化学发光免疫检测试剂盒中的sbcma蛋白校准品得到所述试剂盒的校准曲线。
取50μl生物素标记的sbcma抗体、20μlsbcma蛋白校准品及100μl吖啶酯标记的sbcma抗体混匀后在37℃条件下孵育10min,然后加入20μl偶联有链霉亲和素磁微粒,37℃条件下孵育5min,磁分离后用清洗液洗涤3次,然后依次加入激发液1和激发液2,使用berthold公司的lumat3lb9508管式发光检测仪测定信号值(rlu),并拟合出试剂盒校准曲线;
所述试剂盒中共有九种不同浓度的sbcma蛋白校准品,最终所得到的校准曲线如图1所示,采用logistic(四参数)法拟合曲线,其中,y值代表信号值的平方根值,x值代表sbcma校准品浓度值的平方根值。
实施例4
本实施例利用实施例1提供的sbcma磁微粒化学发光免疫检测试剂盒对40份人血清样本(19例男性,21例女性,年龄在50-80岁之间)中的sbcma进行检测,具体操作如下:
取50μl生物素标记的sbcma抗体、20μl人血清样本(样本不需要处理,直接可以测试)及100μl吖啶酯标记的sbcma抗体混匀后在37℃条件下孵育10min,然后加入20μl偶联有链霉亲和素磁微粒,37℃条件下孵育5min,磁分离后用清洗液洗涤3次,然后依次加入激发液1和激发液2,测定信号值(rlu),通过试剂盒校准曲线计算出被测样本的sbcma浓度。
使用实施例1提供的检测试剂盒和r&dsystems公司的humanbcma/tnfrsf17duosetelisakit对40份人血清样本同时进行检测,并比较测试结果,具体数据如表1所示:
表1
由于不同免疫分析所选的抗体对和方法学等因素的不同,可能会导致检测时受到病人体内干扰物的干扰程度不同,因此无法直接从检测结果的数值来判断两种试剂盒的检测结果是否准确。
因此,对humanbcma/tnfrsf17duosetelisakit的检测结果和实施例1提供的试剂盒的检测结果进行相关性分析,构建回归方程,所得曲线如图2所示,所得方程为y=0.7965x-3.7048,r2=0.9531,由此可知,本发明提供的sbcma检测试剂盒的检测结果与市售的elisa试剂盒检测结果相近,检测结果准确可靠。
综上所述,本发明提供的sbcma磁微粒化学发光免疫检测试剂盒利用链霉亲和素和生物素放大效应,采用磁微粒作为载体,吖啶酯作为化学发光标记物,使得sbcma磁微粒化学发光免疫检测试剂盒能够在较宽的线性范围内测定sbcma浓度,线性更宽、稳定性更好,结果准确可靠,在临床检验和用药指导等方面有广阔的应用前景,填补了相关领域的空白。
申请人声明,本发明通过上述实施例来说明本发明的详细结构特征,但本发明并不局限于上述详细结构特征,即不意味着本发明必须依赖上述详细结构特征才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明所选用部件的等效替换以及辅助部件的增加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种使用磁微粒化学发光定量检测抗SS-B抗体IgG的试剂盒及其制备方法和检测方法
- 一种使用磁微粒化学发光定量检测抗核小体抗体IgG的试剂盒及其制备方法和检测方法
- 一种使用磁微粒化学发光定量检测抗nRNP/Sm抗体IgG的试剂盒及其制备方法和检测方法
- 一种甲状腺球蛋白的磁微粒分离化学发光免疫检测方法
- 一种免疫磁微粒化学发光法HCMVpp65抗原检测试剂盒的制作方法
- 纳米磁微粒化学发光法检测血清总IgE的试剂盒及方法
- 一种使用磁微粒化学发光定量检测抗Scl-70抗体IgG的试剂盒及其制备方法和检测方法
- 基于磁微粒化学发光的多目标物定量检测的微流控芯片的制作方法
- 用于全血样品检测的磁微粒直接化学发光微流控芯片的制作方法
- 定量检测全血中脑钠肽的磁微粒化学发光微流控芯片的制作方法