用于检测新型冠状病毒SARS-CoV-2的试纸条、传感器及其制备与应用的制作方法
本发明涉及核酸检测技术领域,特别是涉及一种用于检测新型冠状病毒sars-cov-2的试纸条、传感器及其制备与应用。
背景技术:
新型冠状病毒,国际病毒分类委员会冠状病毒研究小组(csg)正式命名为“sars-cov-2”,其结构简单、成分简单,属于β属冠状病毒,是一种蛋白包裹的单链正链rna病毒,颗粒呈圆形或椭圆形,常为多形性,直径大约在60~140nm,寄生和感染包括人在内的高等动物。其基因特征与蝙蝠sars样冠状病毒(bat-sl-covzc45)同源性达85%以上。这种病毒体外分离培养时,96小时左右即可在人呼吸道上皮细胞内发现。
新型冠状病毒sars-cov-2传染性强、危害大,早发现、早诊断、早治疗、早隔离是防控治疗的最有效手段。现在,采用实时荧光rt-pcr检测临床诊断病例或疑似病例的呼吸道标本或血液标本是全球普遍确认的标准方法,即核酸检测,若新型冠状病毒核酸呈阳性者,则可判断该患者为确诊病例。采用实时荧光rt-pcr仪器检测核酸包括核酸提取和检测两个步骤,但该方法存在操作繁琐、检测时间长等问题,且需要集中送检。
因此,若能开发一种具有快速诊断、现场筛查能力的新型冠状病毒检测方法,用来作为社区基础医疗卫生机构防控的重要措施,将作为与核酸检测方法互补的有益手段,有助于更快速、精准地对感染疫病社区进行全面筛查,满足大规模人群筛查需要。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供用于检测新型冠状病毒sars-cov-2的试纸条、传感器及其制备与应用,用于解决现有的核酸检测方法操作繁琐、检测速度长、需要集中送检等问题。
为实现上述目的及其他相关目的,本发明第一方面提供一种用于检测新型冠状病毒sars-cov-2的比色法试纸条,所述比色法试纸条包括底板和沿层析方向依次设置在底板上的样品垫、结合垫、检测垫和吸收垫,所述检测垫上设有检测线和控制线,所述结合垫上喷涂有分别由检测探针detprobec1和检测探针detprobec2修饰的mos2@au纳米球,所述纳米球能结合新型冠状病毒;所述检测垫检测线处先后喷涂有链霉亲和素和探针t-dna,所述检测垫控制线处先后喷涂有链霉亲和素和探针c-dna。进一步,所述检测探针detprobec1和检测探针detprobec2均由polya方式修饰,所述探针t-dna和探针c-dna均由生物素修饰;所述检测探针detprobec1和探针c-dna的碱基序列,除采用polya和生物素修饰部分外,其余碱基序列互补;所述检测探针detprobec2和探针t-dna的碱基序列,除采用polya和生物素修饰部分外,其余碱基序列完全相同。
可选地,所述检测探针detprobec1的碱基序列为:
5’-aaaaa-gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc-3’。
可选地,所述检测探针detprobec2的碱基序列为:
5’-aaaaa-gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc-3’。
可选地,所述探针t-dna的碱基序列为:
5’-biotin-gctggatgtgtcatatgactcagacaatccgatgtccgacaatcgggagacatcagc-3’。
可选地,所述探针c-dna的碱基序列为:
5’-biotin-gctggatgtgtcaatgtagcggtgcccctaaggaatattgtcgtaagcgacatccagc-3’。
本发明第二方面提供一种如第一方面所述的用于检测新型冠状病毒sars-cov-2的比色法试纸条的制备方法,包括如下步骤:
(1)mos2@aunp-detprobec2复合物的制备:
①在mos2量子点溶液中加入聚乙烯吡咯烷酮,搅拌反应,再加入氯金酸溶液,继续搅拌反应,然后离心取上清液,超声清洗获得mos2量子点为核,金为壳的mos2@au纳米球溶液;
②用d-pbs缓冲液将检测探针detprobec1配制成detprobec1溶液,将detprobec1溶液、三(2-羧乙基)膦盐酸盐溶液加入到mos2@au纳米球溶液中,搅拌反应,然后加入三磷酸腺嘌呤脱氧核苷酸溶液,继续搅拌反应,反应结束后将其冷藏,待其稳定后离心,取沉淀用d-pbsb溶液清洗后获得mos2@aunp-detprobec1复合物;
(2)mos2@aunp-detprobec2复合物的制备:按照步骤(1)的方法,将步骤②中的检测探针detprobec1替换为检测探针detprobec2,即可获得mos2@aunp-detprobec1复合物;
(3)将mos2@aunp-detprobec1复合物和mos2@aunp-detprobec2复合物喷涂在结合垫上;
(4)将t-dna溶液与链霉亲和素溶液混匀后于室温下培养,然后用超滤离心管离心,取内管中溶液固定在检测垫检测线处;将c-dna溶液与链霉亲和素溶液混匀后于室温下培养,然后用超滤离心管离心,取内管中溶液固定在检测垫控制线处;
(5)将样品垫、结合垫、检测垫和吸收垫顺次搭接在底板上,获得比色法试纸条。
可选地,步骤①中,所述mos2量子点(mos2qds)溶液的制备方法为:用乙醇/水混合溶液将mos2晶体粉末制备为mos2分散液,经超声得到黑绿色悬浊液,然后离心,取上清液真空干燥,将干燥后的产物溶于水中,再离心取中间层溶液,过滤纯化后即得到mos2量子点溶液。
优选地,所述乙醇/水混合溶液为体积分数为30%-50%乙醇/水混合溶液,更优选为体积分数为45%的乙醇/水混合溶液。
优选地,超声功率为150-250w,更优选为250w;超声时间为16-48h,更优选为24h。
优选地,真空干燥温度为60-90℃,更优选为70℃。
可选地,所述步骤①中,mos2量子点溶液的浓度为0.5-5mg/ml,优选为1mg/ml;每毫升mos2量子点溶液中需加入聚乙烯吡咯烷酮的量为0.005-0.05g,优选为0.01g。
可选地,所述步骤①中,mos2量子点溶液与聚乙烯吡咯烷酮的反应时间为0.5-1.5,优选为1h。
可选地,所述步骤①中,氯金酸溶液的浓度为20-50mm,优选为25mm;mos2量子点溶液与氯金酸溶液的体积比为(50-120):1,优选为100:1。
可选地,所述步骤①中,氯金酸溶液加入后反应时间为5-20min,优选为10min。
可选地,所述步骤②中,detprobec1溶液浓度为5-20μm,优选为10μm;三(2-羧乙基)膦盐酸盐溶液浓度为0.5-2mm,优选为1mm;三磷酸腺嘌呤脱氧核苷酸(datp)溶液浓度为10-20μm,优选为15μm。
可选地,所述步骤②中,detprobec1溶液、三(2-羧乙基)膦盐酸盐溶液、mos2@au纳米球溶液、三磷酸腺嘌呤脱氧核苷酸(datp)溶液的体积比为2:1:30:2。
可选地,所述步骤②中,冷藏温度为4℃;冷藏时间为2-5h,优选为4h。
可选地,所述步骤②中,所述d-pbsb溶液为5%bsa的d-pbs缓冲液。
可选地,所述步骤(3)中,mos2@aunp-detprobec1复合物和mos2@aunp-detprobec2复合物分别分散在分散液中后再喷涂在结合垫上,所述分散液包括10%蔗糖、0.25%tween-20、5%bsa和20mmna3po4·12h2o;优选地,mos2@aunp-detprobec1复合物溶液和mos2@aunp-detprobec2复合物溶液的浓度均为25-60μm,更优选为50μm;优选地,mos2@aunp-detprobec1复合物溶液和mos2@aunp-detprobec2复合物溶液的用量为0.5-2ml,更优选为1ml。
可选地,所述步骤(4)中,t-dna溶液和c-dna溶液的浓度为5-15μm,优选为10μm;链霉亲和素溶液的浓度为1.5-3mg/ml,优选为2mg/ml;t-dna溶液与链霉亲和素溶液、c-dna溶液与链霉亲和素溶液的体积比均为(5-20):1,优选为10:1。
可选地,所述步骤(4)中,培育时间为0.5-1.5h,优选为1h。
本发明第三方面提供一种用于检测新型冠状病毒sars-cov-2的比色法试纸条传感器,含有如第一方面所述的比色法试纸条。
本发明第四方面提供一种如第一方面所述的比色法试纸条、如第三方面所述的比色法试纸条传感器在检测新型冠状病毒sars-cov-2中的应用。
本发明第五方面提供一种用于检测新型冠状病毒sars-cov-2的荧光法试纸条,所述荧光法试纸条包括底板和沿层析方向依次设置在底板上的样品垫、结合垫、检测垫和吸收垫,所述检测垫上设有检测线和控制线,所述结合垫上喷涂有两种能与新型冠状病毒结合的纳米材料,第一种纳米材料为mos2qds-detprobef1,由检测探针detprobef1和mos2量子点(mos2qds)反应制得,第二种纳米材料为mos2nss-bsa,由mos2纳米片(mos2nss)与牛血清蛋白(bsa)偶联形成;
所述检测垫检测线处喷涂有链霉亲和素和检测探针detprobef2;所述检测垫控制线处喷涂有由第一种纳米材料mos2qds-detprobef1与牛血清蛋白(bsa)偶联形成的detprobef1-mos2qds-bsa。
可选地,所述检测探针detprobef1由羧基方式修饰,其碱基序列为:
5’-carbox-gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc-3’。
可选地,所述检测探针detprobef2探针由生物素修饰,其碱基序列为:
5’-biotin-gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc-3’。
本发明第六方面提供一种如第五方面所述的用于检测新型冠状病毒sars-cov-2的荧光法试纸条的制备方法,包括如下步骤:
(1)mos2qds-detprobef1-bsa的制备:
①在mos2量子点溶液中加入半胱氨酸,搅拌均匀后进行加热反应,反应结束后冷却至室温,将1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟基琥珀酰亚胺(nhs)加入mos2量子点溶液中,搅拌反应,然后将活化的mos2量子点溶液加入detprobef1溶液中,并用d-pbs缓冲液调整溶液浓度,将复合物在室温下放置待其稳定,用超滤离心管离心,取内管中溶液,即得mos2qds-detprobef1复合物溶液;
②将mos2qds-detprobef1复合物溶液、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟基琥珀酰亚胺(nhs)加入水中,避光搅拌反应,再加入bsa,继续避光搅拌反应,然后离心取沉淀,即得mos2qds-detprobef1-bsa;
(2)mos2nss-bsa的制备:按照步骤(1)的方法,将步骤①中的mos2量子点溶液替换为mos2纳米片(mos2nss)溶液,即可获得mos2nss-bsa;
(3)将mos2qds-detprobef1和mos2nss-bsa喷涂在结合垫上;
(4)将detprobef2溶液和链霉亲和素溶液混匀后于室温下培养,然后用超滤离心管离心,取内管中溶液固定在检测垫检测线处;将mos2qds-detprobef1-bsa喷涂在检测垫控制线处;
(5)将样品垫、结合垫、检测垫和吸收垫顺次搭接在底板上,获得荧光法试纸条。
可选地,所述步骤①中,所述mos2量子点(mos2qds)溶液的制备方法为:用乙醇/水混合溶液将mos2晶体粉末制备为mos2分散液,经超声得到黑绿色悬浊液,然后离心,取上清液真空干燥,将干燥后的产物溶于水中,再离心取中间层溶液,过滤纯化后即得到mos2量子点溶液。
可选地,所述步骤①中,加热反应需在特氟龙容器中进行。
可选地,所述步骤①中,加热反应的温度为180-300℃,优选为200℃;加热反应的时间为20-40min,优选为30min。
可选地,所述步骤①中,mos2量子点溶液的浓度为0.5-5mg/ml,优选为1mg/ml;每毫升mos2量子点溶液中需加入的半胱氨酸为0.5-5g,优选为1g。其中,半胱氨酸为l-半胱氨酸。
可选地,所述步骤①中,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟基琥珀酰亚胺(nhs)与mos2量子点溶液的用量比为2.4:3.6:1(w/w/v)。
可选地,所述步骤①中,mos2qds溶液与detprobef1溶液的体积比为(5-20):1,优选为10:1。
可选地,所述步骤①中,复合物在室温下放置时间为2-5h,优选为4h。
可选地,所述步骤②中,mos2qds-detprobef1复合物、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、n-羟基琥珀酰亚胺(nhs)、牛血清蛋白的用量比优选为50:7:4:10(v/v/v/v)。
可选地,所述步骤②中,避光反应时间为10-40min,优选为30min。
可选地,所述步骤(2)中,所述mos2纳米片(mos2nss)的制备方法为:用乙醇/水混合溶液将mos2晶体粉末制备为mos2分散液,经超声得到黑绿色悬浊液,然后离心,取上清液真空干燥,将干燥后的产物溶于水中,再离心取上清液,过滤纯化后即得到mos2纳米片溶液。
可选地,步骤(3)中,mos2qds-detprobef1和mos2nss-bsa分别用d-pbs缓冲液配制成溶液后再喷涂在结合垫上;优选地,mos2qds-detprobef1溶液和mos2nss-bsa溶液的浓度均为25-60μm,更优选为50μm;优选地,mos2qds-detprobef1溶液和mos2nss-bsa溶液的用量为0.5-2ml,更优选为1ml。
可选地,步骤(4)中,detprobef2溶液的浓度为5-15μm,优选为10μm;链霉亲和素溶液的浓度为1.5-3mg/ml,优选为2mg/ml。
可选地,步骤(4)中,detprobef2溶液与链霉亲和素溶液的体积比为(5-20):1,优选为10:1。
本发明第七方面提供一种用于检测新型冠状病毒sars-cov-2的荧光法试纸条传感器,含有如第五方面所述的荧光法试纸条。
本发明第八方面提供一种如第五方面所述的荧光法试纸条、如第七方面所述的荧光法试纸条传感器在检测新型冠状病毒sars-cov-2中的应用。
如上所述,本发明的用于检测新型冠状病毒sars-cov-2的试纸条、传感器及其制备与应用,具有以下有益效果:
本发明先运用超声液相法,采用乙醇/水混合溶剂制备出纳米尺寸的二硫化钼(mos2)纳米结构,包括二硫化钼量子点(mos2qds)和二硫化钼纳米片(mos2nss);然后以上述二硫化钼量子点为晶种,采用种子生长法合成分散性良好的具有各向异性结构的以二硫化钼量子点为核,金(au)为壳的mos2@au核壳结构纳米颗粒。
接着,本发明通过筛选,获得对新型冠状病毒n蛋白具有高亲和力的两种核酸适配体,运用核酸适配体分别功能化二硫化钼量子点为核,金为壳的mos2@au纳米球,以及二硫化钼量子点,建立基于核酸适配体功能化纳米材料的新型冠状病毒试纸条比色法和荧光法检测传感器,运用纳米材料放大检测信号,实现对新型冠状病毒的简便、快速检测。
本发明可直接通过目视试纸条方法,定性判断检测结果。同时,也可以通过使用仪器读取试纸条光学信息,实现定量检测。
综上所述,本发明建立了比色法和荧光法两种检测体系,两种检测模式互补,可作为现有的实时荧光rt-pcr检测方法的有益补充,完成新型冠状病毒的快速检测,本发明的试纸条及传感器操作简便、成本低廉,有助于更快速、精准地对感染疫病社区进行全面筛查,满足大规模人群筛查需要。
附图说明
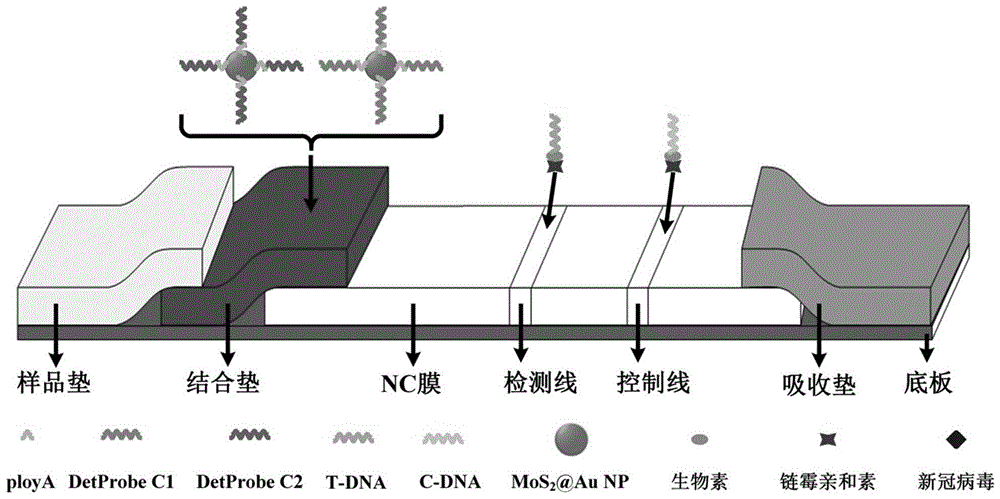
图1显示为本发明实施例2中比色法试纸条的组成示意图。
图2显示为本发明实施例2中比色法试纸条的检测线及控制线阳性反应原理图。
图3显示为本发明实施例2中比色法试纸条的检测线及控制线阴性反应原理图。
图4显示为本发明实施例3中荧光法试纸条的组成示意图。
图5显示为本发明实施例3中荧光法试纸条的检测线及控制线阳性反应原理图。
图6显示为本发明实施例3中荧光法试纸条的检测线及控制线阴性反应原理图。
图7显示为本发明实施例4中比色法试纸条检测等比例稀释的阳性血清结果相关性分析结果图。
图8显示为本发明实施例4中比色法试纸条检测等比例稀释的阳性血清照片。
图9显示为本发明实施例4中荧光法试纸条检测等比例稀释的阳性血清结果相关性分析结果图。
图10显示为本发明实施例4中荧光法试纸条检测等比例稀释的阳性血清照片。
图11显示为本发明实施例5中比色法试纸条检测结果特异性对比图。
图12显示为本发明实施例5中荧光法试纸条检测结果特异性对比图。
具体实施方式
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
本发明提供了两种用于检测新型冠状病毒(sars-cov-2,简称为新冠病毒)的试纸条,一种为比色法试纸条,另一种为荧光法试纸条;进一步地,可采用这两种试纸条分别制作成比色法试纸条传感器和荧光法试纸条传感器。除此之外,本发明中的比色法试纸条和荧光法试纸条也可以制备成用于检测新型冠状病毒的试剂盒或其他结构形式的检测试剂及相关的产品。
需要注意的是,本发明中的新型冠状病毒(简称为新冠病毒)是指国际病毒分类委员会冠状病毒研究小组命名为sars-cov-2的病毒。
如图1所示,本发明提供了一种用于检测新型冠状病毒的比色法试纸条,包括底板和沿层析方向依次设置在底板上的样品垫、结合垫、检测垫和吸收垫,检测垫上依次设置有检测线和控制线。结合垫上喷涂有两种能结合新型冠状病毒的mos2@au纳米球,两种mos2@au纳米球分别由检测探针detprobec1和检测探针detprobec2修饰。检测垫检测线处先后喷涂有链霉亲和素(streptavidin)和探针t-dna,检测垫控制线处先后喷涂有链霉亲和素(streptavidin)和探针c-dna。
具体的,检测探针detprobec1由polya方式(在5’端修饰上连续5个腺嘌呤脱氧核苷酸序列)修饰,其碱基序列为:
5’-aaaaa-gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc-3’。
检测探针detprobec2由polya方式(在5’端修饰上连续5个腺嘌呤脱氧核苷酸序列)修饰,其碱基序列为:
5’-aaaaa-gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc-3’。
探针t-dna由生物素修饰,其碱基序列为:
5’-biotin-gctggatgtgtcatatgactcagacaatccgatgtccgacaatcgggagacatcagc-3’。
探针c-dna由生物素修饰,其碱基序列为:
5’-biotin-gctggatgtgtcaatgtagcggtgcccctaaggaatattgtcgtaagcgacatccagc-3’。
其中,检测探针detprobec1和探针c-dna的碱基序列,除采用polya和生物素修饰部分外,其余碱基序列互补;检测探针detprobec2和探针t-dna的碱基序列,除采用polya和生物素修饰部分外,其余碱基序列完全相同。
除此之外,检测探针detprobec1、检测探针detprobec2、t-dna和c-dna还可以采用巯基、au-se方式修饰。
如图4所示,本发明提供了一种用于检测新型冠状病毒的荧光法试纸条,包括底板和沿层析方向依次设置在底板上的样品垫、结合垫、检测垫和吸收垫,检测垫上依次设置有检测线和控制线。结合垫上喷涂有能结合新型冠状病毒的两种纳米材料,第一种纳米材料为mos2qds-detprobef1,由检测探针detprobef1通过羧基修饰于二硫化钼量子点而得,第二种纳米材料为mos2nss-bsa,由二硫化钼纳米片(mos2nss)与牛血清蛋白(bsa)偶联形成。检测垫检测线处先后喷涂有链霉亲和素(streptavidin)和检测探针detprobef2;检测垫控制线处喷涂有由第一种纳米材料mos2qds-detprobef1与bsa偶联形成的detprobef1-mos2qds-bsa。
具体的,检测探针detprobef1由羧基方式修饰,其碱基序列为:
5’-carbox-gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc-3’。
检测探针detprobef2探针由生物素修饰,其碱基序列为:
5’-biotin-gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc-3’。
除此之外,检测探针detprobef1和检测探针detprobef2还可以采用巯基、au-se方式修饰。
本发明对两种试纸条及其制成的传感器的外观和尺寸没有特殊要求,采用本领域常规试纸条的尺寸即可,在本发明具体实施过程中,试纸条的宽度优选为3~5mm。在本发明中,底板为具有粘性的衬板,样品垫、结合垫、检测垫和吸收垫依次搭接在底板上;本发明中各部分搭接的长度优选为1.8~2.5mm;本发明各部分搭接设置的目的为在待测液从一个材料过渡到另一个材料时能够保证流动的一致性。
本发明的试纸条包括底板、样品垫、结合垫、检测垫和吸收垫,本发明对底板、样品垫、结合垫、检测垫和吸收垫的材料没有特殊要求,采用本领域常规的材料即可。在本发明具体实施过程中,底板的材料为塑料,样品垫的材料为纤维素,结合垫的材料为玻璃纤维,检测垫为硝酸纤维素膜(nc膜),吸收垫的材料为纤维素;检测垫上检测限和控制线的位置和间距根据本领域常规的要求设计即可。
本发明的试纸条传感器在使用的过程中,是将含有待检样品溶液滴加到样品垫上,随即触发生化反应。
以下实施例中,样品为血清。
以下实施例中,测试结果通过有色反应或者颜色转变而能够对使用者可见,一般为红色或蓝色。
本发明实施例中的试纸条的具体制备和实施过程如下:
实施例1
二硫化钼纳米材料[二硫化钼量子点(mos2qds)、二硫化钼纳米片(mos2nss)]的制备
(1)、首先,用电子天平称量300mg的mos2晶体粉末,并将其加到250ml烧杯中。接着,配置100ml45%体积分数的乙醇/水混合溶液,并加到上述烧杯中形成mos2分散液。然后将密封的烧杯放到超声波清洗机里,在53khz频率,250w功率下超声24h。超声完成后会得到黑绿色的悬浊液,为了移除未剥离完全的大的mos2颗粒,将超声所得的悬浊液在6000rpm转速下离心20分钟,取离心后的上清液并重复该离心过程两次。为了去除离心后所得溶液里的乙醇,将该溶液放到70℃真空干燥箱里干燥,得到干燥后的产物。
(2)、将步骤(1)干燥后的产物溶于超纯水中,在6000rpm转速下离心20分钟,取离心后的上清液并重复该离心过程一次。最后,用0.22μm微孔滤膜过滤器进一步纯化最后离心得到的上清液,即可获得尺寸为在15nm左右,厚度为2~3nm的二硫化钼纳米片(mos2nss)。
(3)将步骤(1)干燥后的产物溶于超纯水中,在6000rpm转速下离心20分钟,取离心后的中间层溶液并重复该离心过程一次。最后,用0.22μm微孔滤膜过滤器进一步纯化最后离心得到的中间层液体,即可获得尺寸为在15nm左右,厚度为3~4nm的二硫化钼量子点(mos2qds)。
(4)将得到的mos2纳米片(mos2nss)和mos2量子点(mos2qds)溶液置于4℃冰箱中,备用。
实施例2
一、比色法试纸条的制备
1、以二硫化钼量子点为核,金为壳的mos2@au纳米球的制备
取5ml预先准备好的mos2量子点溶液装入离心管中,添加0.05g聚乙烯吡咯烷酮(pvp),在室温下搅拌1小时。然后,取50μl,25mm氯金酸溶液添加至离心管连续搅拌,反应10min。收集在离心管中混合溶液,以8000rpm转速离心,取离心后上清液溶液,超声清洗3次,溶液黄绿色变为红色,置于4℃冰箱中备用。
2、mos2@aunp-detprobec1的制备
将检测探针detprobec1在12000rpm下离心2分钟后,使用d-pbs缓冲液(137mmnacl,2.7mmkcl,1.5mmkh2po4,8mmna2hpo4,1mmcacl2,0.5mmmgcl2,ph7.4)配制成浓度为10μm的溶液待用。取80μl检测探针detprobec1溶液,40μl浓度为1mm的三(2-羧乙基)膦盐酸盐(tcep)溶液加入到1.2mlmos2@au核壳结构的纳米球溶液,在室温下搅拌1小时,随后加入80μl浓度为15μm的三磷酸腺嘌呤脱氧核苷酸(datp)溶液,继续搅拌反应。上述反应30分钟后,将复合物在4℃条件下放置4小时待其稳定。反应结束后,将复合物以12,000rpm的转速离心15分钟,用5%d-pbsb(d-pbs缓冲液,5%bsa)清洗三次,将获得的mos2@aunp-detprobec1复合物沉淀重新分散在1.2ml的分散液(10%蔗糖,0.25%tween-20,5%bsa,20mmna3po4·12h2o)中,4℃条件下储存待用。
3、mos2@aunp-detprobec2的制备
该纳米材料的制备,类似mos2@aunp-detprobec1的制备过程。在反应步骤中,将检测探针detprobec1替换为检测探针detprobec2即可。
4、比色法试纸条结合垫的制备
取1ml,50μmmos2@aunp-detprobec1溶液和1ml,50μmmos2@aunp-detprobec2溶液混合后,使用划线喷金仪喷涂在结合垫上。
5、比色法试纸条检测垫检测线的制备
将200μl的探针t-dna溶液(10μm)与20μl链霉亲和素溶液(2mg/ml)混合均匀,并在室温下培养1小时。反应完毕后,使用超滤离心管离心,去除外管中的滤液,保留内管中溶液备用。使用划线喷金仪将该溶液固定在检测垫上的检测线处。随后将检测垫在37℃下干燥过夜,并在4℃下储存备用。
6、比色法试纸条检测垫控制线的制备
将200μl的c-dna溶液(10μm)与20μl链霉亲和素溶液(2mg/ml)混合均匀,并在室温下培养1小时。反应完毕后,使用超滤离心管离心,去除外管中的滤液,保留内管中溶液备用。使用划线喷金仪将该溶液固定在检测垫上的控制线处。随后将检测垫在37℃下干燥过夜,并在4℃下储存备用。
二、使用比色法试纸条检测样品
将样品分别滴加在比色法试纸条的样品垫上,等待30分钟,观察检测垫检测线和控制线处的反应变化。
对于对比色法试纸条,可直接使用目视方法进行定性观察;使用层析试纸图像质控分析仪,可检测、计算检测线(t线)和控制线(c线)吸收光强度的比值,进行定量分析,检测新冠病毒的浓度。
三、比色法试纸条的工作原理
样品滴加在样品垫上后,通过毛细管作用向吸收垫方向迁移。通过结合垫时,如图2所示,若样品中存在新冠病毒,mos2@aunp-detprobec1和mos2@aunp-detprobec2将分别结合新冠病毒,形成mos2@aunp-detprobec1/sars-cov-2/mos2@aunp-detprobec2的聚集体,引起纳米颗粒聚集并形成三维网格。当其通过检测线时,由于探针t-dna与新冠病毒具有亲和力,该三维网格外围尚有空余蛋白位点的新冠病毒将被探针t-dna捕获,从而导致大量聚集体在检测线停止迁移。至此,检测线上产生可见的红色带。剩余液体继续迁移,尚未发生反应的mos2@aunp-detprobec1流经控制线处。由于探针c-dna和检测探针detprobec1互补形成双链,mos2@aunp-detprobec1被探针c-dna捕获,在控制线上形成红色带。
如图3所示,若样品中不存在新冠病毒情况时,检测线上的探针t-dna不能捕获mos2@aunp-detprobec1和mos2@aunp-detprobec2纳米球。混合物流过检测线时,纳米球与探针t-dna之间没有发生互相作用。混合物继续流向控制线。由于混合物中存在mos2@aunp-detprobec1纳米球,控制线上的探针c-dna将其捕获。因此,该种情况发生时,仅在控制线处显示红色带。
实施例3
一、荧光法试纸条的制备
1、mos2qds-detprobef1的制备
将1gl-半胱氨酸加入mos2量子点(mos2qds)溶液中(1mg/ml),于室温下搅拌30分钟。混合溶液转移至500ml特氟龙容器,加热至200℃,持续30分钟。加热完毕,冷却至室温备用。将2.4mgedc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)和3.6mgnhs(n-羟基琥珀酰亚胺)加入1mlmos2qds溶液中,在室温下搅拌30分钟。用d-pbs缓冲液将检测探针detprobef1配置成detprobef1溶液,然后,将活化后的mos2qds溶液加入100μl检测探针detprobef1溶液中,并用d-pbs缓冲液将溶液浓度调整至20μm,搅拌10min,静置备用。将复合物在25℃条件下放置4小时待其稳定。为将未反应的edc、nhs和检测探针detprobef1去除,将反应完毕后的复合物,使用超滤离心管离心,去除外管中的滤液,保留内管中溶液备用。
2、mos2qds-detprobef1-bsa的制备
将100μlmos2qds-detprobef1溶液加入400μl超纯水中,再加入14μl1mg/ml的edc和8μl1mg/ml的nhs,在室温下避光搅拌30分钟。加入20μl10%的bsa,在室温下避光搅拌2小时。混合物在4℃,12,000rpm下离心30分钟,弃上清液,加入200μld-pbs缓冲液,备用。
3、mos2nss-bsa的制备
mos2nss-bsa的制备方法与mos2qds-detprobef1-bsa的制备方法类似。在操作过程中,将mos2qds-detprobef1替换为mos2nss即可。
4、荧光法试纸条结合垫的制备
取1ml,50μmmos2nss-bsa溶液,使用划线喷金仪喷涂在试纸条荧光法传感器结合垫上,再将1ml,50μmmos2qds-detprobef1溶液喷涂在该结合垫上。
5、荧光法试纸条检测垫检测线的制备
将200μl的detprobef2溶液(10μm)与20μl链霉亲和素溶液(2mg/ml)混合均匀并室温下培养1小时。反应完毕后,使用超滤离心管离心,去除外管中的滤液,保留内管中溶液备用。使用划线喷金仪将该溶液固定在检测垫上的检测线处。随后将检测垫在37℃下干燥过夜,并在4℃下储存备用。
6、荧光法试纸条检测垫控制线的制备
使用划线喷金仪,将mos2qds-detprobef1-bsa喷涂在检测垫上的控制线处。随后将检测垫在37℃下干燥过夜,并在4℃下储存备用。
二、使用荧光法试纸条检测样品
将样品分别滴加在荧光法试纸条的样品垫上,等待30分钟,观察试纸条检测垫上检测线和控制线处的反应变化。
对于荧光法试纸条,使用激发光为320nm左右光源,照射试纸条可进行目视观察,进行定性分析;采用层析试纸图像质控分析仪,可检测、计算检测线(t线)和控制线(c线)荧光强度的比值,进行定量分析,检测新冠病毒的浓度。
三、荧光法试纸条的工作原理
样品滴加在样品垫上,通过毛细管作用向吸收垫方向迁移。样品进入结合垫后,如图5所示看,若混合物中存在新冠病毒,mos2qds-detprobef1将通过检测探针detprobef1捕获新冠病毒。由于检测探针detprobef1与新冠病毒间的高特异性结合以及毛细管作用效果强于二硫化钼量子点与二硫化钼纳米片之间微弱的范德华力,结合了新冠病毒的二硫化钼量子点mos2qds-detprobef1将离开二硫化钼纳米片mos2nss-bsa,向检测线方向迁移。由于检测线处的检测探针detprobef2能捕获新冠病毒的其余蛋白位点,二硫化钼量子点mos2qds-detprobef1迁移至检测线时,二硫化钼量子点复合物将在检测线处被捕获。在激发光照射下,由于检测线和控制线位置均有二硫化钼量子点的存在。因此,这两条线处均有荧光。
如图6所示,当样品中没有新冠病毒时,由于范德华力的作用,位于结合垫上的二硫化钼量子点mos2qds-detprobef1将继续与二硫化钼纳米片mos2nss-bsa结合。处于结合垫上的二硫化钼量子点的自发荧光会继续被猝灭。在这种情况下,仅在控制线处存在二硫化钼量子点。因此,在激发光照射下,检测线处不会观察到荧光。控制线位置的荧光强度保持不变。
实施例4
试纸条检测结果与新型冠状病毒浓度的关系
1、取5ml含有新型冠状病毒的血清样品,按照2倍、4倍、8倍、16倍、32倍和64倍比例用pbs进行稀释,用比色法试纸条进行测试,结果如图7和图8所示。检测结果线性相关性分析结果显示,相关系数r2为0.968。上述结果显示,针对不同浓度的血清,比色法试纸条检测结果与新型冠状病毒浓度具有良好的一致性,比色法试纸条检测垫检测线处颜色深度与新型冠状病毒浓度成正比例关系。
2、取5ml含有新型冠状病毒的血清样品,按照2倍、4倍、8倍、16倍、32倍和64倍比例用pbs进行稀释,用荧光法试纸条进行测试,结果如图9和图10所示。检测结果线性相关性分析结果显示,相关系数r2为0.985。上述结果显示,针对不同浓度的血清,荧光法试纸条检测结果与新型冠状病毒浓度具有良好的一致性,荧光法试纸条检测线处荧光亮度与控制线处荧光亮度的比值,和新型冠状病毒浓度成正比例关系。
实施例5
试纸条特异性试验
在对试纸条的特异性测试方面,用pbs配置浓度为20ng/ml的乙肝表面抗体(抗-hbs)和人血小板衍生生长因子bb(pdgf-bb)的血清,以及浓度为4000cell/l的大肠杆菌o157:h7(e.colio157:h7)溶液。分别取1ml溶液,各自加入4ml健康体检者血清样品,搅拌5分钟,静置10分钟,混合均匀。
1、取5ml含有新型冠状病毒的血清,以及5ml浓度为20ng/ml的抗-hbs、pdgf-bb溶液,浓度为4000cell/l的e.colio157:h7溶液,用比色法试纸条进行特异性分析。检测结果如图11所示。仅在含有新型冠状病毒血清滴在试纸条比色法传感器上,吸收光强度比值会有较大变化。说明比色法试纸条特异性好,检测结果不受其他物质的干扰。
2、取5ml含有新型冠状病毒的血清,以及5ml浓度为20ng/ml的抗-hbs、pdgf-bb溶液,浓度为4000cell/l的e.colio157:h7溶液,用荧光法试纸条进行特异性分析。检测结果如图12所示。仅在含有新型冠状病毒血清滴在荧光法试纸条上,荧光强度比值会有较大变化。说明试纸条特异性好,检测结果不受其他物质的干扰。
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
sequencelisting
<110>中国科学院重庆绿色智能技术研究院,重庆医科大学
<120>用于检测新型冠状病毒sars-cov-2的试纸条、传感器及其制备与应用
<130>2020
<160>6
<170>patentinversion3.5
<210>1
<211>63
<212>dna
<213>artificial
<220>
<223>detprobec1
<400>1
aaaaagctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatcc60
agc63
<210>2
<211>63
<212>dna
<213>artificial
<220>
<223>detprobec2
<400>2
aaaaagctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatcc60
agc63
<210>3
<211>57
<212>dna
<213>artificial
<220>
<223>t-dna
<400>3
gctggatgtgtcatatgactcagacaatccgatgtccgacaatcgggagacatcagc57
<210>4
<211>58
<212>dna
<213>artificial
<220>
<223>c-dna
<400>4
gctggatgtgtcaatgtagcggtgcccctaaggaatattgtcgtaagcgacatccagc58
<210>5
<211>58
<212>dna
<213>artificial
<220>
<223>detprobef1
<400>5
gctggatgtcgcttacgacaatattccttaggggcaccgctacattgacacatccagc58
<210>6
<211>58
<212>dna
<213>artificial
<220>
<223>detprobef2
<400>6
gctggatgtcaccggattgtcggacatcggattgtctgagtcatatgacacatccagc58
- 还没有人留言评论。精彩留言会获得点赞!