一种直接质谱鉴定含氨基代谢物同分异构体的方法及其应用与流程
本发明属于氨基代谢物同分异构体鉴定领域,具体涉及一种直接质谱鉴定含氨基代谢物同分异构体的方法及其应用。
背景技术:
含氨基代谢物是指含有氨基的小分子代谢物,包括氨基酸、多肽、神经递质及多胺等,涉及到生命活动中多种代谢途径。在代谢组学的研究中,对复杂生物样品中的含氨基代谢物进行定性定量分析具有重要的意义[1,2]。由于含氨基代谢物包括氨基、甲基、羧基等官能团,这类物质存在同分异构体的现象,增加了在复杂生物样品中检测的难度。
目前,同分异构体的检测方法包括色谱法、光谱法和质谱法[3]。色谱法前处理复杂、操作繁琐,而光谱法难以实现在复杂样品中进行同分异构体的鉴别。常规的单级质谱不能区分异构体,而二级质谱碎片对于结构稳定、碎片离子相同的同分异构体无法鉴定。离子淌度质谱能根据化合物空间结构上的差异,通过独有的离子淌度功能区分同分异构体,但是离子淌度质谱仪器昂贵,目前还没有普及使用[4,5]。
物质衍生化后由于衍生化基团的加入能丰富同分异构体二级碎片离子,通过对比离子的特征碎片,为区分同分异构体提供了一种检测鉴定方法[6,7]。
参考文献:
1.johnson,d.w.freeaminoacidquantificationbylc-ms/msusingderivatizationgeneratedisotope-labelledstandards.jchromatogrb.2011,879,1345–1352.
2.li,s.w.;balazsk.;lieveb.;filipc.;fredericl.;frank.v.quantitativemetaboliteprofilingofanaminogroupcontainingpharmaceuticalinhumanplasmaviaprecolumnderivatizationandhigh-performanceliquidchromatography-inductivelycoupledplasmamassspectrometry.anal.chem.2017,89(3),1907-1915.
3.zhanga.h.;sunh.;wangp.;hany.;wangx.j.modernanalyticaltechniquesinmetabolomicsanalysis.analyst,2012,137(2),293-300.
4.doddsj.n;bakere.s.ionmobilityspectrometry:fundamentalconcepts,instrumentation,applications,andtheroadahead.j.am.soc.mass.spectr.2019,30(11),2185-2195.
5.picachej.a.;roseb.s.;balinskia.;leaptrotk.l.;sherrods.d.;mayj.c.;mcleanj.a.collisioncrosssectioncompendiumtoannotateandpredictmulti-omiccompoundidentities.chem.sci.2019,10(4),983-993.
6.huangt.;armbrusterm.r.;coultonj.b.;edwardsj.l.chemicaltagginginmassspectrometryforsystemsbiology.anal.chem.2019,91(1),109-125.
7.el-maghrabeym.h.;kishikawan.;kurodan.currenttrendsinisotope-codedderivatizationliquidchromatographic-massspectrometricanalyseswithspecialemphasisontheirbiomedicalapplication.biomed.chromatogr.2020,34(3),e4756.
技术实现要素:
针对上述现有技术存在的不足之处,本发明目的在于提供一种直接质谱鉴定含氨基代谢物同分异构体的方法及其应用。为了达成上述目的,本发明的解决方案是:
一种直接质谱鉴定含氨基代谢物同分异构体的方法,其特征在于具体包含以下步骤:
(1)氨基代谢物衍生化反应:将氨基代谢物配制为氨基代谢物标准溶液,然后加入衍生试剂溶液进行衍生化反应,将所得混合物浓缩后往残留液中加酸调节ph值到2~3,除盐处理后即可制得氨基代谢物衍生化产物;所述衍生试剂的表达式为dipp-r-nhs,其中,dipp代表n-二异丙基磷酸基,nhs代表n-羟基琥珀酰亚胺酯,r代表为含同位素标记或不含同位素的l-构型或d-构型的氨基酸,所述氨基酸选自丙氨酸、亮氨酸、异亮氨酸、缬氨酸或苯丙氨酸中的一种;
(2)氨基代谢物衍生化产物检测:将步骤(1)中制得的氨基代谢物衍生化产物加溶剂制成重悬浮液,然后将所得重悬浮液稀释后即可进行质谱进样检测;
质谱分析条件:正离子模式,离子源为esi;喷雾温度为280-380℃;喷雾电压为2.8-4.5kv;鞘气和辅助气体流量分别为60和10单位;轨道阱入口温度为280-380℃;毛细管温度为280-380℃;s-lensrf为30-50%;样品分析质量扫描范围为m/z80-1500;质谱仪操作依据数据模式自动进行ms和ms/ms扫描,通过hcd碎片化分离得到10-50个丰度最高的前体离子进行分析鉴定。
优选地,步骤(1)中所述的氨基代谢物选自亮氨酸和异亮氨酸、丙氨酸和β-丙氨酸、天冬氨酸和亚氨基二乙酸组成的含氨基代谢物的同分异构体中的一组;所述的氨基代谢物标准溶液由10-100mm碳酸氢钠溶液(其他碱性缓冲溶液也可,优选50mm碳酸氢钠溶液)制成,溶液ph值为8-10。
优选地,步骤(1)中所述的衍生化反应条件为冰浴反应10min以上,然后常温反应10min以上。
优选地,步骤(1)中所述的调节ph值的酸为甲酸、乙酸或盐酸溶液。
优选地,步骤(2)中所述的重悬浮液为乙腈或甲醇溶液。
所述的直接质谱鉴定含氨基代谢物同分异构体方法在细胞氨基代谢物同分异构体的鉴定中的应用。
所述的直接质谱鉴定含氨基代谢物同分异构体方法在动物组织氨基代谢物同分异构体的鉴定中的应用。
所述的直接质谱鉴定含氨基代谢物同分异构体方法在动物血清氨基代谢物同分异构体的鉴定中的应用。
所述的直接质谱鉴定含氨基代谢物同分异构体方法在植物组织氨基代谢物同分异构体的鉴定中的应用。
本发明的具体原理如下:
本发明所提供的直接质谱鉴定含氨基代谢物同分异构体方法是通过衍生化试剂分别与互为同分异构体的氨基代谢物进行衍生化反应,然后通过分析所产生的二级质谱图中特征碎片来区分鉴定同分异构体,选择合适的衍生化试剂可以丰富二级质谱图的碎片峰,同时形成特征碎片峰,具体的例子在实施例部分会再详细说明。
本发明的优点:
(1)本发明所提供的直接质谱鉴定含氨基代谢物同分异构体方法是一种识别氨基代谢物同分异构体的全新方法,成功建立起通过衍生试剂dipp-r-nhs对氨基代谢物同分异构体进行高效标记并通过二级质谱进行鉴定的方法。
(2)本发明所提供的直接质谱鉴定含氨基代谢物同分异构体方法具有操作简单、精确度高及重复性好的优点。
(3)本发明所提供的直接质谱鉴定含氨基代谢物同分异构体方法可用于细胞、组织、血清及其他动植物体液或组织萃取物中氨基代谢物同分异构体的鉴定,结果表明:本发明所提供的定量方法均具有高灵敏度和高准确性。
附图说明
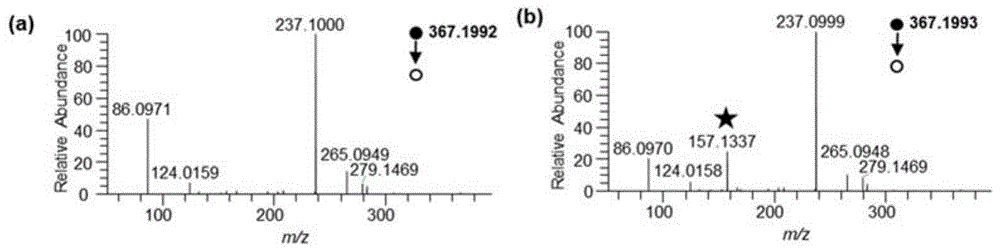
图1n-二异丙基磷酸-l-丙氨酸-亮氨酸(a)和n-二异丙基磷酸-l-丙氨酸-异亮氨酸(b)二级质谱碎片图;
图2n-二异丙基磷酸-l-丙氨酸-丙氨酸(a)和n-二异丙基磷酸-l-丙氨酸-β-丙氨酸(b)的二级质谱碎片图;
图3n-二异丙基磷酸-l-丙氨酸-天冬氨酸(a)和n-二异丙基磷酸-l-丙氨酸-亚氨基二乙酸(b)的二级质谱碎片图;
图4细胞中含氨基代谢物同分异构体的鉴定(a)n-二异丙基磷酸-l-丙氨酸-亮氨酸;(b)n-二异丙基磷酸-l-丙氨酸-异亮氨酸;(c)n-二异丙基磷酸-l-丙氨酸-丙氨酸;(d)n-二异丙基磷酸-l-丙氨酸-β-丙氨酸的二级质谱碎片图;
图5动物组织中含氨基代谢物同分异构体的鉴定(a)n-二异丙基磷酸-l-丙氨酸-亮氨酸;(b)n-二异丙基磷酸-l-丙氨酸-异亮氨酸;(c)n-二异丙基磷酸-l-丙氨酸-丙氨酸;(d)n-二异丙基磷酸-l-丙氨酸-β-丙氨酸;(e)n-二异丙基磷酸-l-丙氨酸-二甲胺;(f)n-二异丙基磷酸-l-丙氨酸-乙胺的二级质谱碎片图;
图6血清中含氨基代谢物同分异构体的鉴定(a)n-二异丙基磷酸-l-丙氨酸-亮氨酸;(b)n-二异丙基磷酸-l-丙氨酸-异亮氨酸;(c)n-二异丙基磷酸-l-丙氨酸-丙氨酸;(d)n-二异丙基磷酸-l-丙氨酸-β-丙氨酸;(e)n-二异丙基磷酸-l-丙氨酸-天冬氨酸;(f)n-二异丙基磷酸-l-丙氨酸-亚氨基二乙酸的二级质谱碎片图;
图7铁观音茶叶中含氨基代谢物同分异构体的鉴定(a)n-二异丙基磷酸-l-丙氨酸-亮氨酸;(b)n-二异丙基磷酸-l-丙氨酸-异亮氨酸;(c)n-二异丙基磷酸-l-丙氨酸-丙氨酸;(d)n-二异丙基磷酸-l-丙氨酸-β-丙氨酸的二级质谱碎片图。
具体实施方式
下面进一步结合实施例以详细说明本发明。同样应理解,以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,示例中具体的质量、反应时间和温度、工艺参数等也仅是合适范围中的一个示例,本领域的技术人员根据本发明的上述内容做出的一些非本质的改进和调整均属于本发明的保护范围。实施例中未注明具体技术或条件者,均为按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市场购买的常规产品。
本发明所有实施例均是借助esi离子源和q-exactiveorbitrap质谱进行样品的质谱测试和分析。
实施例1
氨基酸同分异构体鉴定的检测方法步骤如下:
(1)衍生化反应:分别配制100μl10mm亮氨酸、异亮氨酸、丙氨酸、β-丙氨酸、天冬氨酸和亚氨基二乙酸标准品的50mm碳酸氢钠溶液,ph值约为8,在冰浴条件下分别各加入40μl50mmdipp-l-ala-nhs乙腈溶液,每一份溶液涡旋混匀,在冰浴反应10min以上,然后常温反应10min以上;将所得混合物真空离心蒸发浓缩器除去乙腈;往残留液加入10%甲酸溶液调节ph到2~3;然后用反相的
(2)衍生产物直接质谱分析条件:正离子模式,离子源为esi;喷雾温度为280-380℃;喷雾电压为2.8-4.5kv;鞘气和辅助气体流量分别为60和10单位;轨道阱入口温度为280-380℃;毛细管温度为280-380℃;s-lensrf为30-50%;样品分析质量扫描范围为m/z80-1500。ms/ms谱图在分辨率为17500的orbitrap质量分析仪上获得。质谱仪操作依据数据模式自动进行ms和ms/ms扫描,通过hcd碎片化分离得到10个最激烈的前体离子。
(3)数据处理:采用thermoxcaliburqualbrowser处理raw格式质谱数据,并导出质谱图谱。
(4)亮氨酸和异亮氨酸同分异构体的判断:通过dipp-l-ala-nhs衍生化后,得到n-二异丙基磷酸-l-丙氨酸-亮氨酸(dipp-l-ala-leu)和n-二异丙基磷酸-l-丙氨酸-异亮氨酸(dipp-l-ala-ile)的二级质谱碎片图如图1所示:质子化后的母离子[m+h]+分别为m/z367.1992和367.1993,理论质量为367.1992,误差小于1ppm。dipp-l-ala-leu的主要碎片有m/z279.1469(理论质量为279.1468)、m/z265.0949(理论质量为265.0948)、m/z237.1000(理论质量为237.0999)、m/z124.0159(理论质量为124.0158)、m/z86.0971(理论质量为86.0964)。dipp-l-ala-ile的主要碎片有m/z279.1469、m/z265.0948、m/z237.0999、m/z157.1337(理论质量为157.1335)、m/z124.0158、m/z86.0970。这两种氨基酸衍生化产物的二级质谱(ms2)碎片离子相对信号强度见表1,结果发现:亮氨酸衍生物产物也有m/z157.1336,相对其他碎片离子其信号较弱,是最高碎片m/z279.1469信号强度的2.12%;而异亮氨酸衍生化后产生的离子碎片m/z157相对信号强度是亮氨酸衍生化后的11倍,其它碎片离子相对信号强度差异不明显。亮氨酸和异亮氨酸通过dipp-l-ala-nhs标记产物的ms2碎片离子都存在m/z157的碎片离子,这说明亮氨酸和异亮氨酸衍生化产物遵循一个共同的解离途径;但是碎片m/z157相对信号强度差距明显,这一个区别正是区分氨基酸异构体的关键。因此,碎片m/z157.1335的是衍生化后异亮氨酸区分亮氨酸的特征碎片离子峰。
丙氨酸和β-丙氨酸同分异构体的判断:通过dipp-l-ala-nhs衍生化后,得到dipp-l-ala-ala和dipp-l-ala-β-ala的二级质谱碎片图如图2所示:发现两个二级谱图差异明显,dipp-l-ala-ala的碎片离子m/z195.0529(理论质量195.0529)信号强度明显高于dipp-l-ala-β-ala中m/z195.0533,因此,碎片m/z195.0529为区别丙氨酸和β-丙氨酸的特征碎片离子峰。
天冬氨酸和亚氨基二乙酸同分异构体的判断:天冬氨酸和亚氨基二乙酸通过dipp-l-ala-nhs衍生化后,得到n-二异丙基磷酸-l-丙氨酸-天冬氨酸(dipp-l-ala-asp)和n-二异丙基磷酸-l-丙氨酸-亚氨基二乙酸(dipp-l-ala-ida)的二级质谱碎片图如图3所示:发现两个二级谱图差异显著:dipp-l-ala-asp的碎片主要离子按照强度由高到低依次为m/z221.0322(理论质量221.0322)、m/z239.0427(理论质量221.0322)、m/z267.0377(理论质量267.0377)、m/z88.0399(理论质量88.0393)、m/z285.0483(理论质量285.0482)、m/z134.0449(理论质量134.0448)。dipp-l-ala-ida的碎片主要离子按照强度由高到低依次为m/z88.0399、m/z134.0449、m/z267.0376、m/z239.042、m/z124.0160、m/z285.0481、m/z134.0449,其中,离子m/z221.0322在dipp-l-ala-asp碎片中强度最高,而在dipp-l-ala-ida碎片中没有,因此碎片离子m/z221.0322是鉴定asp和ida衍生化后的特征碎片离子峰。
表1氨基酸衍生化后的同分异构体ms2主要碎片及特征碎片离子信号强度
*加粗部分为对比的特征碎片离子峰
实施例2、细胞中含氨基代谢物同分异构体的鉴定步骤如下:
步骤(1)细胞代谢物萃取:将培养好的hepg2细胞从培养箱中拿出后,吸走培养基;用2ml37℃pbs洗细胞除去残余培养基然后吸走pbs,重复该步2次;然后将细胞刮到15ml离心管中,再用1ml-20℃甲醇清洗培养板,将清洗后的甲醇也放入15ml离心管中;将离心管放入液氮冷冻30s。从液氮中取出离心管,冰上解冻2min,涡旋15s,超声30s,冰上孵育10min;涡旋15s,3000g离心5min,收集上清液。往沉淀中加入500μl甲醇,重复以上萃取步骤,收集上清液;再往沉淀中加入500μl超纯水,按照上述步骤,收集上清液;合并三次所得的上清液,15000g离心15min,收集上清液,30℃旋转蒸发至100到200μl,冷冻干燥制得细胞代谢物;
步骤(2)细胞代谢物衍生化反应:往步骤(1)制得的细胞代谢物中加入100μl50mmnahco3溶液溶解,充分溶解后,15000g离心15min,取90μl上清液;加入20μl50mmdipp-l-ala-nhs进行衍生化反应,冰上反应30min,常温反应30min;真空离心蒸发浓缩器除去乙腈;残留液加入适量的10%乙酸溶液调节ph到2~3;用反相的
步骤(3)衍生产物直接质谱分析:正离子模式,离子源为esi;喷雾温度为300℃;喷雾电压为3.5kv;鞘气和辅助气体流量分别为60和10单位;orbitrap入口温度为320℃;毛细管温度为360℃;s-lensrf为35%;样品分析质量扫描范围为m/z80-1500。ms/ms谱图在分辨率为17500的orbitrap质量分析仪上获得。质谱仪操作依据数据模式自动进行ms和ms/ms扫描,通过hcd碎片化分离得到10个最激烈的前体离子。
步骤(4)数据处理:采用thermoxcaliburqualbrowser处理raw格式质谱数据,并导出质谱图谱。
步骤(5)寻找细胞氨基代谢物同分异构体:细胞中氨基代谢物的二级质谱碎片图如图4所示:发现离子m/z367.1991的二级碎片与实施例1中标准品亮氨酸衍生产物的离子碎片相同,m/z367.1994的二级碎片与实施例1中标准品异亮氨酸的离子碎片相同,确定细胞中存在亮氨酸和异亮氨酸,特征碎片离子为m/z157.1336;发现离子m/z325.1525的二级碎片与标准品丙氨酸衍生产物的离子碎片相同,m/z325.1524的二级碎片与标准品β-丙氨酸衍生产物的离子碎片相同,确定细胞中存在丙氨酸和β-丙氨酸,特征碎片离子为m/z195.0529。
实施例3、动物组织中含氨基代谢物同分异构体的鉴定步骤如下:
步骤(1)组织代谢物萃取:将甲醇/氯仿/水以2:2:3比例配成萃取剂。称取10mg小鼠肝脏组织样品,在4℃下,4ml/g甲醇和2ml/g水的混合溶液中匀浆。匀浆液移入小玻璃瓶中,加入4ml/g氯仿和4ml/g水涡漩60s。在冰上静置15min后,在4℃下以10000rpm离心10min,取上清液移入玻璃瓶中,得到的液体在冷冻干燥除去甲醇和水,得到组织代谢物粉末存于-80度冰箱保存。
步骤(2)组织代谢物衍生化反应:10mg组织提取的代谢物粉末加入100μl50mmnahco3溶液溶解,充分溶解后,15000g离心15min,取90μl上清液;加入40μl50mmdipp-l-ala-nhs进行衍生化反应,后续反应条件与实施例2中的步骤(2)相同。
步骤(3)衍生产物直接质谱分析:与实施例2中的步骤(3)相同。
步骤(4)数据处理:与实施例2中的步骤(4)相同。
步骤(5)寻找动物组织中氨基代谢物同分异构体:动物组织中氨基代谢物的二级质谱碎片图如图5所示:发现离子m/z367.1993的二级碎片与标准品亮氨酸衍生产物的离子碎片相同,m/z367.1990的二级碎片与标准品异亮氨酸的离子碎片相同,确定组织中存在同分异构体亮氨酸和异亮氨酸,特征碎片离子为m/z157.1338;发现离子m/z325.1523的二级碎片与标准品丙氨酸衍生产物的离子碎片相同,m/z325.1524的二级碎片与标准品β-丙氨酸衍生产物的离子碎片相同,确定组织中存在同分异构体丙氨酸和β-丙氨酸,特征碎片离子为m/z195.0531。
另外,组织中发现m/z281.1619的二级碎片离子按信号强度从高到低排列依次为m/z117.1024、m/z197.0684、m/z239.1152;m/z281.1620的二级碎片离子按信号强度从高到低排列依次为m/z197.0684、m/z117.1024、m/z142.0263、m/z239.1153。推测m/z281.1619和m/z281.1620可能是二甲胺或者乙胺衍生产物质子化离子(理论质量281.1625),通过标准品验证,二甲胺衍生产物的二级碎片离子与组织中m/z281.1619二级碎片一致,乙胺衍生产物的二级碎片离子与组织中m/z281.1620二级碎片一致;乙胺衍生产物碎片中存在m/z142.0263,而二甲胺衍生产物碎片中不存在,离子m/z142.0263可以作为衍生化后乙胺区别二甲胺的特征离子碎片,确定组织中存在同分异构体二甲胺和乙胺。
实施例4、动物血清中含氨基代谢物同分异构体的鉴定步骤如下:
步骤(1)血清代谢物提取:小鼠血清采集后在冰上静置30min;800g离心10min,取100μl上清液;加入与400μl甲醇,涡旋,20000g离心15min,收集上清,将上清液离心干燥。
步骤(2)血清代谢物衍生化反应:100μl血清提取的代谢物粉末加入100μl50mmnahco3溶液溶解,充分溶解后,15000g离心15min,取90μl上清液;加入40μl50mmdipp-l-ala-nhs进行衍生化反应,后续反应条件与实施例一步骤2相同。
步骤(3)衍生产物直接质谱分析:与实施例2中的步骤(3)相同。
步骤(4)数据处理:与实施例2中的步骤(4)相同。
步骤(5)寻找血清代谢物中氨基代谢物同分异构体:动物血清中含氨基代谢物的二级质谱碎片图如图6所示:发现离子m/z367.1991的二级碎片与标准品亮氨酸衍生产物的离子碎片相同,m/z367.1995的二级碎片与标准品异亮氨酸的离子碎片相同,确定血清中存在同分异构体亮氨酸和异亮氨酸,特征碎片离子为m/z157.1334;发现离子m/z325.1522的二级碎片与标准品丙氨酸衍生产物的离子碎片相同,m/z325.1525的二级碎片与标准品β-丙氨酸衍生产物的离子碎片相同,确定血清中存在同分异构体丙氨酸和β-丙氨酸,特征碎片离子为m/z195.0528;离子m/z369.1420的二级碎片与标准品天冬氨酸衍生产物的离子碎片相同,m/z369.1424的二级碎片与标准品亚氨基二乙酸衍生产物的离子碎片相同,确定血清中存在同分异构体天冬氨酸和亚氨基二乙酸,特征碎片离子为m/z221.0321。
实施例5、植物组织液或组织代谢物中氨基代谢物同分异构体的鉴定步骤如下:
步骤(1)植物组织代谢物提取:铁观音茶叶样品磨成粉末,过150目筛后,称量茶叶粉末20mg,加入500μl超纯水冲泡,并置于80(±2)℃水浴30min;冷却至室温后,加入500μl甲醇,涡旋混匀;15000g离心15min,取500μl上清液离心干燥制得茶叶粉末提取物;
步骤(2)铁观音茶叶成分衍生化反应:往步骤(1)中制得的茶叶粉末提取物中加入100μl50mmnahco3溶液溶解,充分溶解后,15000g离心15min,取90μl上清液;加入40μl50mmdipp-l-ala-nhs进行衍生化反应,后续反应条件与实施例一步骤(2)相同。
步骤(3)衍生产物直接质谱分析:与实施例2中的步骤(3)相同。
步骤(4)数据处理:与实施例2中的步骤(4)相同。
步骤(5)寻找茶叶中氨基代谢物同分异构体:植物组织中含氨基代谢物的二级质谱碎片图如图7所示:发现离子m/z367.1993的二级碎片与实施例1中标准品亮氨酸衍生产物的离子碎片相同,m/z367.1989的二级碎片与实施例1中标准品异亮氨酸的离子碎片相同,确定茶叶中存在亮氨酸和异亮氨酸,特征碎片离子为m/z157.1335;发现离子m/z325.1521的二级碎片与标准品丙氨酸衍生产物的离子碎片相同,m/z325.1523的二级碎片与标准品β-丙氨酸衍生产物的离子碎片相同,确定茶叶中存在丙氨酸和β-丙氨酸,特征碎片离子为m/z195.0528。
- 还没有人留言评论。精彩留言会获得点赞!