检测抗链球菌溶血素O的试剂及其制备方法与流程
本发明涉及生物
技术领域:
,尤其涉及检测抗链球菌溶血素o的试剂及其制备方法。
背景技术:
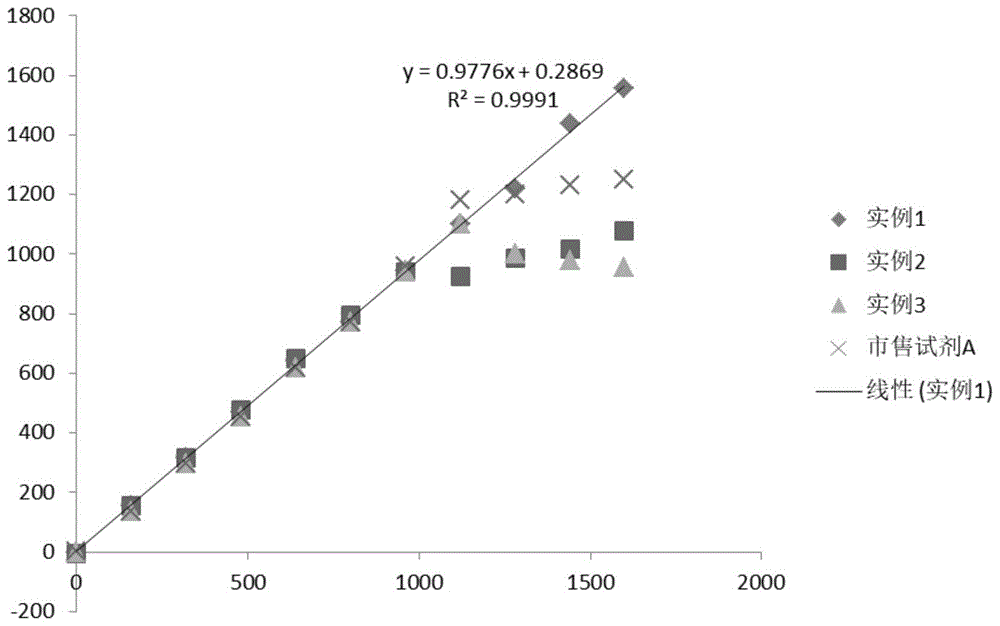
:链球菌溶血素“o”(简称aso)是溶血性链球菌在人体内的代谢产物之一,它是一种含有-sh基且具有溶血性质的蛋白质,可以溶解机体的红细胞,在空气中易于被氧化,氧化后可暂时失去溶血能力,被还原剂还原后可重新恢复溶血能力。人体被链球菌感染后,链球菌溶血素o可刺激机体免疫系统产生相应的抗体,从而使血液中的抗链球菌溶血素o浓度升高,一般来说,85-90%的受到溶血素链球菌感染的患者在感染后15-20天到病愈后的数月或一年血清中都会存在抗链球菌溶血素o,若患者血清中检测出抗链球菌溶血素o,则表明该患者近期感染过溶血性链球菌,因此抗链球菌溶血素o在临床诊断方面具有重要的意义,通过检测血清中抗链球菌溶血素o可用于辅助诊断肾小球肾炎、风湿热、猩红热、扁桃体炎、咽炎、风湿性心脏病、等链球菌性变态反应疾病。抗链球菌溶血素o的临床检测方法有溶血抑制法、胶乳凝集法、酶联免疫法、胶乳颗粒增强免疫比浊法。其中溶血抑制法操作繁琐、测定结果易受影响,重复性差。酶联免疫法测定过程操作复杂,对测试人员有较高专业要求,且只能定性或半定量检测,不能满足临床需要。而胶乳凝集法只可定性检测。胶乳颗粒增强免疫比浊法(petia)是近年来出现的一种应用较为广泛的检测方法,petia法包括散射比浊检测法和透射比浊检测法,两者检测原理十分相似,都是基于抗原抗体的特异性反应。在高分子胶乳胶乳颗粒表面交联抗体(抗原),当交联了胶乳颗粒的抗体(抗原)与抗原(抗体)结合后会会迅速聚集在一起形成浊度,从而改变反应体系的透光性或散光性。反应体系的透光性或散光性的改变与被测样本中的抗原(抗体)浓度有相关性,因此检测透光性或散光性的变化可反应被测样本中的抗原(抗体)浓度。该方法省时省力、可直接在生化分析仪上操作,方便快捷,测定结果准确度高、可定量检测,测值影响因素较少,因此近年来被广泛应用。市面上现有的抗链球菌溶血素o检测试剂盒多用胶乳颗粒增强免疫比浊法,但在实际应用中发现,市售试剂在检测中的线性与精密度不可得兼,无法满足临床检测需求。技术实现要素:有鉴于此,本发明要解决的技术问题在于提供检测抗链球菌溶血素o的试剂及其制备方法,从而使检测的线性与精密度都得到保证。本发明提供的抗链球菌溶血素o的检测试剂,包括试剂r1和试剂r2:所述试剂r1包括:80~120mmol/l磷酸盐缓冲液、genape11g/l~10g/l、吐温-201g/l~10g/l、edta2~4g/l、nan30.5~2g/l、nacl4~6g/l和牛血清白蛋白0.5~2g/l;所述试剂r2由如下原料制得:80nm胶乳颗粒、300nm胶乳颗粒、edc、链球菌溶血素o、mes缓冲液、tris缓冲液、bsa和保存液;所述保存液包括:30mmtaps、1%bsa、6%蔗糖、1g/l叠氮钠和0.9%氯化钠。本发明试剂r1中,采用双表面活性剂系统,从而在检测中起到了良好的抗干扰的作用,特别是能够抗乳糜干扰。在研究中发现采用的这两种表面活性剂中任一者都不可省略或替代,且比例也不能随意调整,上述任何一种改变都会导致检测效果的下降。试剂r2中,采用两种粒径的胶乳颗粒,粒径选择合理,且与缓冲液配合得当,提高了测定结果的低值精密度、线性和抗干扰性能。本发明中,所述试剂r1由100mmol/l磷酸盐缓冲液、genape15g/l~7.5g/l、吐温-202.5g/l~5g/l、edta3g/l、nan31g/l、nacl5g/l和牛血清白蛋白1g/l组成;其中genape1与吐温-20的质量比为1:1。本发明中,所述试剂r1由100mmol/l磷酸盐缓冲液、genape15g/l、吐温-205g/l、edta3g/l、nan31g/l、nacl5g/l和牛血清白蛋白1g/l组成;所述试剂r1的制备方法包括:依次添加各组分,然后调节ph值至6.0。所述r1的制备在室温下进行。所述室温为18~30℃。所述试剂r2的制备方法包括:将链球菌溶血素o以tris缓冲液稀释,获得抗原稀释液;将80nm胶乳颗粒以mes缓冲液稀释,加入edc活化后,与抗原稀释液混合反应,然后加入bsa封闭,离心收集沉淀以保存液悬浮,获得a液;将300nm胶乳颗粒以mes缓冲液稀释,加入edc活化后,与抗原稀释液混合反应过夜,然后加入bsa封闭,离心收集沉淀以保存液悬浮,获得b液;将所述a液与所述b液混合,制得试剂r2。所述tris缓冲液的浓度为50mmol/l;所述抗原稀释液中,链球菌溶血素o的浓度为0.3mg/ml。所述mes缓冲液的浓度为10mmol/l;制备所述a液的步骤中,所述80nm胶乳颗粒以mes缓冲液稀释至浓度为3.625g/l;制备所述b液的步骤中,所述300nm胶乳颗粒以mes缓冲液稀释至浓度为2.175g/l。所述加入edc为加入含有edc的mes缓冲液,其中,edc浓度为1.4mg/ml,mes的浓度为10mmol/l;所述制备a液的步骤中加入edc至浓度为0.15mg/ml;所述制备b液的步骤中加入edc至浓度为0.05mg/ml;所述活化的条件为室温振荡20min。所述室温为18~30℃。所述制备a液的步骤中与抗原稀释液混合至抗原的浓度为0.1mg/ml;所述制备b液的步骤中与抗原稀释液混合至抗原的浓度为0.15mg/ml;所述与抗原稀释液混合反应的条件为室温反应8~12h。所述室温为18~30℃。所述制备a液的步骤中加入bsa至其浓度为1.2mg/ml;所述制备b液的步骤中加入bsa至其浓度为1.2mg/ml,所述封闭的反应条件为室温反应20~40min。所述室温为18~30℃。所述a液与所述b液混合的体积比为1:1。所述试剂r2中,乳胶颗粒浓度为2.9g/l,其中80nm胶乳颗粒的质量占总胶乳颗粒质量的37.5%~62.5%。一些实施例中,80nm胶乳颗粒的质量占总胶乳颗粒质量的62.5%。本发明所述试剂适用于胶乳颗粒增强免疫比浊法检测,检测使用全自动生化分析仪。检测方法为终点法,检测波长540nm,测定温度为37℃。本发明提供的检测试剂中包括试剂r1和试剂r2,其中试剂r1采用双表面活性剂系统,试剂r2采用两种粒径的乳胶颗粒。该检测试剂适用于抗链球菌溶血素o的胶乳颗粒增强免疫比浊法检测。相对于市售的只含有单粒径胶乳颗粒的市售试剂a本发明在线性、低值精密度、抗干扰方面具有明显优势。实验表明,该试剂的线性检测中r2值可达0.9991,同时精密度也非常高,cv值低于2%。附图说明图1示各试剂盒的线性考察结果,其横坐标为理论浓度,纵坐标为实测浓度。具体实施方式本发明提供了检测抗链球菌溶血素o的试剂及其制备方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本
发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。本发明采用的试材皆为普通市售品,皆可于市场购得。下面结合实施例,进一步阐述本发明:实施例1抗链球菌溶血素o双粒径胶乳增强免疫比浊法检测试剂盒及其制备:试剂r1组成如下:以上各组分在室温条件下依次加入完成配制,并调节ph至6.0,4℃密封存储,备用。试剂r2制备如下:(1)链球菌溶血素o蛋白洗涤纯化:取购买的链球菌溶血素o蛋白溶液置于透析袋中,将透析袋置于生理盐水溶液中,透析过夜后备用。(2)胶乳颗粒的活化:分别将相同体积的粒径分别为80nm、300nm的胶乳颗粒用10mmph=5.0mes缓冲液稀释,将大小两种不同粒径的胶乳颗粒稀释液称作a液、b液。准确称量edc并用10mmph=5.0mes缓冲液稀释至浓度为1.4mg/ml。在a液、b液中分别添加edc使得a液中edc浓度为0.15mg/ml,b液中edc浓度为0.05mg/ml。将加入了edc的a液、b液在室温条件下放在摇床上震荡20min。(3)抗原稀释液的配制:将纯化洗涤后的链球菌溶血素o加入50mmph=8.0tris缓冲液中配制为抗原稀释液,抗原稀释液中链球菌溶血素o的浓度为0.3mg/ml。(4)包被有链球菌溶血素o的不同粒径的胶乳颗粒的制备:将配制好的链球菌溶血素o稀释液分别添加进已活化的胶乳颗粒a、b液中,使得a、b液中抗原浓度分别为:0.1mg/ml和0.15mg/ml,将a、b液在室温条件下置于混匀仪上反应过夜。反应过夜后在a、b液中添加10%bsa,使a、b液中bsa浓度达到1.2mg/ml,进行封闭处理30min。将封闭后的a、b也在15000rpm转速下离心5min,去除上清液,加入一定体积的保存液,保存液配方为:30mmtapsph8.0+1%bsa+6%蔗糖+1g/l叠氮钠+0.9%氯化钠,然后进行超声分散。(5)r2制备:将以上制备的不同粒径的包被了链球菌溶血素o的胶乳颗粒溶液按一定体积比例混合,并按胶乳浓度加入对应体积的保存液(同步骤4中的保存液配方相同),使r2中双粒径胶乳浓度为2.9g/l,其中小粒径胶乳颗粒质量占总胶乳颗粒质量比为62.5%。两种溶液按比例混匀后即为制备的r2试剂。实施例2抗链球菌溶血素o双粒径胶乳增强免疫比浊法检测试剂盒及其制备:试剂r1组成:同实施例1试剂r2制备如下:(1)链球菌溶血素o蛋白洗涤纯化:同实施例1(2)胶乳颗粒的活化:同实施例1(3)抗原稀释液的配制:同实施例1(4)包被有链球菌溶血素o的不同粒径的胶乳颗粒的制备:同实施例1(5)r2制备:将以上制备的不同粒径的包被了链球菌溶血素o的胶乳颗粒溶液按一定体积比例混合,并按胶乳浓度加入对应体积的保存液(同步骤4中的保存液配方相同),使r2中双粒径胶乳浓度为2.9g/l,使其中小粒径胶乳颗粒质量占总胶乳颗粒质量比为37.5%。两种溶液按比例混匀后即为制备的r2试剂。实施例3抗链球菌溶血素o双粒径胶乳增强免疫比浊法检测试剂盒及其制备:试剂r1组成:同实施例1。试剂r2制备如下:(1)链球菌溶血素o蛋白洗涤纯化:同实施例1。(2)胶乳颗粒的活化:同实施例1。(3)抗原稀释液的配制:将纯化洗涤后的链球菌溶血素o加入50mmph=8.8tris缓冲液中配制为抗原稀释液,抗原稀释液中链球菌溶血素o的浓度为0.3mg/ml。(4)包被有链球菌溶血素o的不同粒径的胶乳颗粒的制备:同实施例1。(5)r2制备:同实施例1实施例4抗链球菌溶血素o双粒径胶乳增强免疫比浊法检测试剂盒及其制备:试剂r1组成如下:以上各组分在室温条件下依次加入完成配制,并调节ph至6.0,4℃密封存储,备用。试剂r2制备如下:(1)链球菌溶血素o蛋白洗涤纯化:同实施例1(2)胶乳颗粒的活化:同实施例1(3)抗原稀释液的配制:同实施例1(4)包被有链球菌溶血素o的不同粒径的胶乳颗粒的制备:同实施例1(5)r2制备:同实施例1抗链球菌溶血素o的检测使用全自动生化分析仪按照下表检测参数进行检测:表1.本发明所述试剂盒在全自动生化分析仪上的检测参数(1)精密度检测分别采用两个样品,各取样10次测定本发明所述试剂的精密度。表2.本发明所述试剂盒的精密度考察(样品1)序号实施例1实施例2实施例3市售试剂a1196.65197.96190.51196.902196.46203.86192.14192.493196.47209.59184.93195.004196.06192.20185.81191.995196.56203.54189.00184.316196.35205.85191.65195.847196.83193.94195.38199.188199.20209.37199.87183.339198.52190.69181.56195.6710198.73197.99188.34186.57ave197.18200.50189.92192.13sd1.166.925.295.54cv0.59%3.45%2.79%2.89%表3.本发明所述试剂盒的精密度考察(样品2)序号实施例1实施例2实施例3市售试剂a148.3247.1049.1346.35246.3845.2745.5246.77347.5046.2147.0647.86447.8549.5645.8348.94548.4247.7648.4945.24649.3346.9946.6949.63747.4045.0046.0648.82848.9749.5849.5448.39948.9349.4949.8749.311048.9847.9447.4748.29ave48.2147.4947.5747.96sd0.921.701.601.41cv1.92%3.58%3.36%2.95%(2)线性检测,以实施例1~3制备的检测试剂为受试对象,进行线性检测。同时,以市售试剂为对照。结果如图1,结果表明,各受试对象中,实施例1制备的检测试剂具有最佳的检测线性,r2值可达0.9991。(3)抗干扰检测表4.本发明所述试剂盒的抗干扰性能考察综上,通过对比本发明试剂盒实施例1、实施例2、实施例3、实施例4和市售试剂盒a在精密度、线性、抗干扰性能方面的对比,结果显示:相对于市售的只含有单粒径胶乳颗粒的市售试剂a本发明在线性、低值精密度、抗干扰方面具有明显优势。其中,实施例1制备的检测试剂的效果更优。以上仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1