粪便形态学质控品及其制备方法与流程
本发明涉及医学检验,具体涉及粪便形态学质控品及其制备方法。
背景技术:
1、粪便有形成份检查是临床检验常规项目,是粪便常规检验不可缺少的组成部分,其中红细胞、白细胞、脂肪球、真菌及寄生虫卵等有形成分的识别对疾病的鉴别诊断、疗效观察、预后判断及科研与临床教学有重要价值。粪便形态学质控品在自动粪便处理分析系统中检测时,能准确的监控自动粪便处理分析系统的状态。虽然粪便有形成分检查已经在临床应用多年,但市面上并没有找到粪便有形成分的质控品。
技术实现思路
1、本发明的目的在于提供粪便形态学质控品及其制备方法,能够解决现有的自动粪便处理分析系统没有形态学质控品的问题;从而达到了能准确的监控自动粪便处理分析系统状态的目的。
2、本发明通过下述技术方案实现:
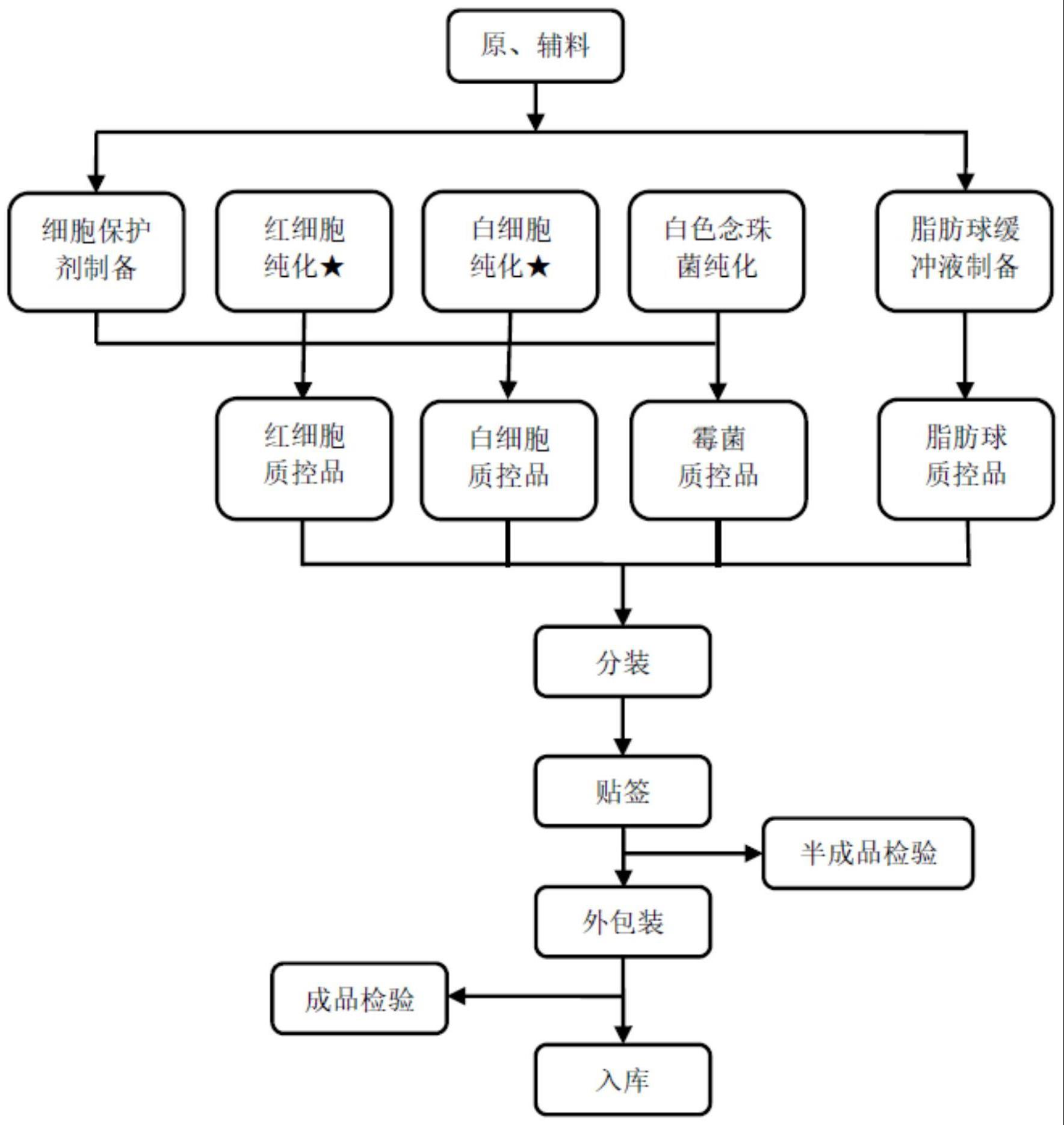
3、粪便形态学质控品的制备方法,所述粪便形态学质控品包括红细胞质控品、白细胞质控品、霉菌质控品和脂肪球质控品;
4、所述红细胞质控品的制备过程为:将向抗凝全血依次进行离心、重悬后摇床混匀、正立静置、重悬混匀检测,当氯化钠镜检溶液高倍视野中红细胞数量为20~30个/视野,获得红细胞质控品;
5、所述白细胞质控品的制备过程为:将抗凝全血进行离心、裂解、离心、重悬后摇床混匀、重悬混匀检测;当氯化钠镜检溶液高倍视野中白细胞数量为20~30个/视野,获得白细胞质控品;
6、所述霉菌质控品的制备过程为:将霉菌培养基溶液依次进行高温蒸汽灭菌、培养基培养、离心、重悬混匀检测,当氯化钠镜检溶液高倍视野中霉菌数量为20~30个/视野,获得霉菌质控品;
7、所述脂肪球质控品的制备过程为:将菜籽油和脂肪球缓冲液混匀获得脂肪球质控品。
8、通过本发明所述制备方法分别成功制备红细胞质控品、白细胞质控品、霉菌质控品和脂肪球质控品,通过对粪便形态学质控品(红细胞质控品、白细胞质控品、霉菌质控品和脂肪球质控品)的检测能准确的监控自动粪便处理分析系统的状态,确保了自动粪便分析系统在对粪便有形成分检测时的准确性。
9、进一步地,红细胞质控品的制备过程包括以下步骤:
10、s1a、将抗凝全血加入5~10倍全血体积的0.85%氯化钠溶液稀释混匀,离心5-8min,去掉上清,保留红细胞沉淀;
11、s2a、将红细胞沉淀用5~10倍全血体积的0.85%氯化钠溶液稀释混匀、离心去掉上清,保留红细胞沉淀,重复5~10次,对红细胞沉淀进行纯化处理;
12、s3a、将纯化好的红细胞沉淀用细胞保护剂溶液重悬,摇床混匀过夜;
13、s4a、固定好的红细胞于2℃~8℃环境正立静置48~72小时,待红细胞沉降完全后去除上层浮末和上清,保留固定好的红细胞沉淀;
14、s5a、将红细胞沉淀用3~6倍体积的细胞保护剂溶液重悬混匀,取混匀后的红细胞加入氯化钠溶液混匀,转移至粪便采集管中放置于自动粪便处理分析系统中进行检测;根据高倍视野中红细胞数量调整氯化钠溶液稀释红细胞的稀释倍数,以确保稀释后的溶液镜检高倍视野中红细胞数量为20~30个/视野;当稀释后的溶液镜检高倍视野中红细胞数量为20~30个/视野,获得红细胞质控品。
15、本发明的高倍视野为显微镜400倍放大后视野。
16、本发明的红细胞质控品与血液中正常红细胞形态一致,使用含1%~4%甲醛,0.14%磷酸氢二钠,0.024%磷酸二氢钾,0.8%氯化钠,0.02%氯化钾,ph为7.4的溶液,该溶液为等渗溶液,固定过程中不会应为细胞膜内外渗透压不同导致红细胞涨破或缩小,使红细胞固定前后形态一致。
17、进一步地,白细胞质控品的制备过程包括以下步骤:
18、s1b、将抗凝全血离心去上清;
19、s2b、加入5~10倍细胞沉淀体积tris-nh4cl溶液混匀,裂解5~8min后,300rpm离心2min,重复本步骤,直到红细胞裂解完全;
20、s3b、离心后的细胞沉淀用生理盐水重悬、离心去上清;
21、s4b、加入细胞保护剂重悬摇床混匀过夜;
22、s5b、取混匀后的白细胞加入氯化钠溶液混匀,转移至粪便采集管中放置于自动粪便处理分析系统中进行检测;根据高倍视野中白细胞数量调整氯化钠溶液稀释白细胞的稀释倍数,以确保稀释后的溶液镜检高倍视野中白细胞数量为20~30个/视野;当稀释后的溶液镜检高倍视野中白细胞数量为20~30个/视野,获得白细胞质控品。
23、本发明的白细胞质控品通过控制裂解时间,使全血中的红细胞充分裂解,而白细胞保持其原有的形态不变。
24、所述细胞保护剂溶液包括以下重量百分比组分:
25、1%~4%甲醛,0.14%磷酸氢二钠,0.024%磷酸二氢钾,0.8%氯化钠,0.02%氯化钾,ph为7.4。
26、进一步地,霉菌质控品的制备过程包括以下步骤:
27、s1c、将配制好的霉菌培养基溶液进行121℃高温蒸汽灭菌20-30min;
28、s2c、将霉菌菌种液接入灭菌后的培养基中,混匀后置于恒温摇床中28℃培养48小时;
29、s3c、将培养好的菌液离心后弃去上清,收集沉淀;
30、s4c、将过夜后的霉菌沉淀,用细胞保护剂溶液重悬后摇床混匀过夜;
31、s5c、取混匀后的霉菌菌液加入氯化钠溶液混匀,转移至粪便采集管中放置于自动粪便处理分析系统中进行检测;根据高倍视野中霉菌数量调整氯化钠溶液稀释霉菌的稀释倍数,以确保稀释后的溶液镜检高倍视野中霉菌数量为20~30个/视野;当稀释后的溶液镜检高倍视野中霉菌数量为20~30个/视野,获得霉菌质控品。
32、本发明的霉菌质控品通过控制霉菌培养时间,使霉菌处于对数生长期,此时固定的霉菌质控品形态较好,既有分裂后单个的霉菌,也有正在出芽的霉菌。
33、进一步地,白细胞质控品和红细胞质控品制备时离心条件为8℃,300~500rpm,5-8min。
34、进一步地,霉菌质控品制备时离心条件为8℃,3000~5000rpm,5-8min。
35、进一步地,白细胞质控品制备时裂解采用tris-nh4cl溶液,ph为7.2~8.0。
36、进一步地,脂肪球缓冲液为磷酸盐,并且不含有与脂肪反应的成分。
37、所述脂肪球缓冲液包括以下重量百分比组分:0.12%磷酸氢二钠,0.05%磷酸二氢钠,0.8%氯化钠,0.02%叠氮化钠,ph为7.4。
38、进一步地,红细胞质控品、白细胞质控品、霉菌质控品中使用的细胞保护剂为等渗液体,首次细胞保护剂重悬后需重悬摇床混匀过夜,摇床混匀过夜时间不得少于16小时。
39、如上述制备方法所制备的粪便形态学质控品。
40、本发明与现有技术相比,具有如下的优点和有益效果:
41、本发明通过对粪便形态学质控品(红细胞质控品、白细胞质控品、霉菌质控品和脂肪球质控品)的检测能准确的监控自动粪便处理分析系统的状态,确保了自动粪便分析系统在对粪便有形成分检测时的准确性,能够解决现有的自动粪便处理分析系统没有形态学质控品的问题;从而达到了能准确的监控自动粪便处理分析系统状态的目的。
- 还没有人留言评论。精彩留言会获得点赞!