一种基于UPLC-MS/MS检测人血浆中阿司匹林和水杨酸浓度的方法及其应用与流程
本发明属于药品测试,具体涉及一种基于uplc-ms/ms检测人血浆中阿司匹林和水杨酸浓度的方法及其应用以及一种bufferin的仿制药研发中用于制备标准曲线样品和质控样品及其它未做特殊说明的方法学验证样品的健康人空白血浆采集方法和一种bufferin的仿制药研发中受试者含药血浆采集方法。
背景技术:
1、铝镁匹林片(ⅱ)为抗血栓药,是复方制剂,成分包括阿司匹林、重质碳酸镁和甘羟铝。小剂量的阿司匹林能抑制血栓素a2的形成,从而不可逆地抑制正常血小板聚集过程,防止血栓形成,与制酸药甘羟铝和重质碳酸镁合用能保护胃肠粘膜。适用于需使用阿司匹林抑制血小板粘附和聚集,但患者不能耐受阿司匹林的胃肠道反应时:不稳定心绞痛、急性心肌梗塞、局部缺血性脑血管障碍等。
2、铝镁匹林片(ⅱ)最早于2001年在日本由lion公司研发上市,商品名为bufferin。根据nmpa发布的关于仿制药生物等效性试验工作开展的相关要求以及《药物注册管理办法》,研制该药品需进行临床生物等效性试验。因此,亟需一种快速、准确的定量分析方法用于检测临床试验受试者服用铝镁匹林片(ⅱ)后血浆中目标待测物阿司匹林和水杨酸的浓度,助力我国仿制药研发生产。
3、目前文献报道多为服用铝镁匹林片(ⅱ)后仅检测血浆中水杨酸的浓度,阿司匹林作为主成分具有药物活性,因此也有文献报道检测血浆中目标待测物阿司匹林和水杨酸,多采用液质联用色谱法进行检测。这些方法存在前处理使用血浆量大、待测物阿司匹林不稳定、两种待测物分别测定使得检测效率低下、定量灵敏度较低等问题。
4、cn112540138a公开了一种血浆中丹酚酸b、阿司匹林、水杨酸的联合定量测定方法,通过采用uplc-ms/ms分析测定待测血浆中丹酚酸b、阿司匹林、水杨酸,助力阿司匹林与含有丹酚酸b成分的中药制剂联合研发,但该测定方法存在以下缺陷:阿司匹林又名乙酰水杨酸,因结构中含有酰胺键极易被水解为水杨酸,极不稳定,该方法为常规血样检测方法,并未加入稳定剂或提供低温环境以达到稳定阿司匹林的目的,未见待测物相互干扰试验结果;该方法使用乙酸乙酯作为提取溶剂,极性适中,提取物质较多,干扰较大;该方法丹酚酸b、阿司匹林、水杨酸的线性范围均为5-6000ng/ml,并未按照药物在人体内吸收代谢程度分别规定合适的线性范围,会导致阿司匹林实际血药浓度集中在标准曲线的一端或大量样品中水杨酸血药浓度超出标准曲线范围,均不利于实际生物样品中阿司匹林和水杨酸的准确检测;该方法检测样品为含药beagle犬血浆,未见明确可用于人血浆样品检测的描述。
技术实现思路
1、基于上述问题,本发明提供一种基于uplc-ms/ms检测人血浆中阿司匹林和水杨酸浓度的方法,该方法血浆用量仅为100μl,并解决了血浆中待测物阿司匹林不稳定问题。本发明的检测方法,样品仅需一次前处理即可同时测得两个待测物的血药浓度,前处理方法简单、快速、便捷,检测方法选择性好、灵敏度和准确度高,可实现高通量检测,适用于临床样品中阿司匹林和水杨酸的浓度测定。
2、一种基于uplc-ms/ms检测人血浆中阿司匹林和水杨酸浓度的方法,包括如下步骤:
3、s1,绘制标准曲线:
4、s01,配制阿司匹林及水杨酸的储备液和标准曲线工作溶液;
5、s02,配制阿司匹林-氘4及水杨酸-氘4的内标储备液和内标工作液;
6、s03,配制标准曲线血浆样品;
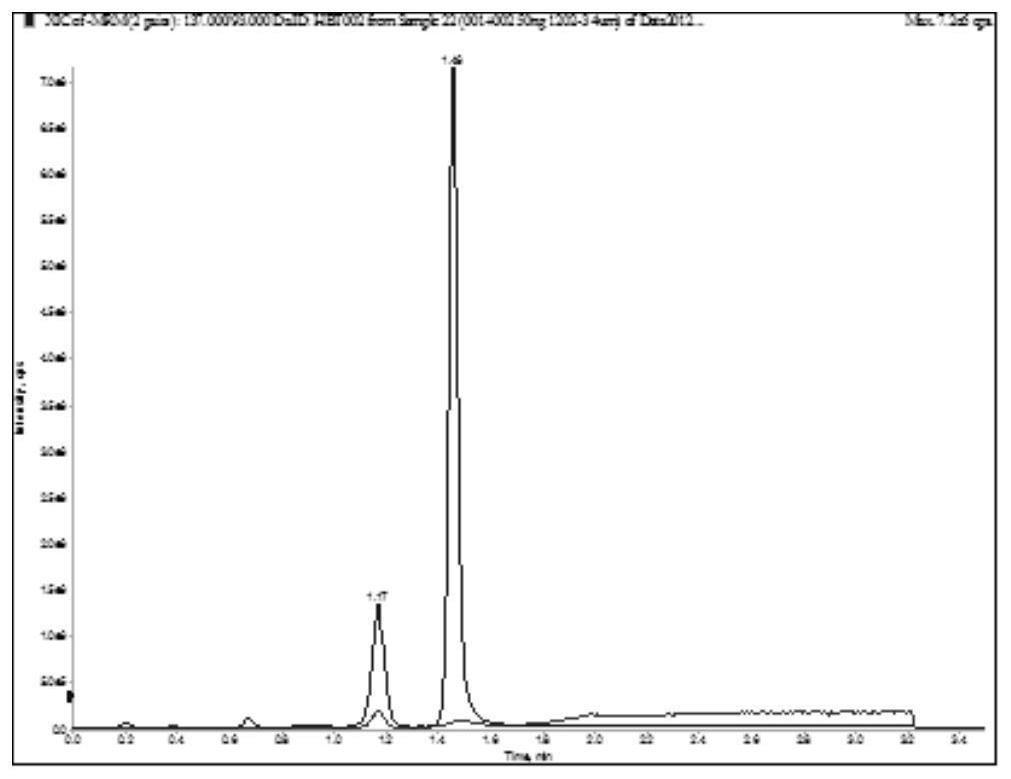
7、s04,分别取s03制备的标准曲线样品经液液萃取后,进样uplc-ms/ms进行分析,记录标准曲线样品中阿司匹林、水杨酸、内标阿司匹林-氘4、内标水杨酸-氘4的色谱图、色谱峰面积;然后分别以标准曲线样品溶液中阿司匹林、水杨酸浓度为横坐标,阿司匹林与内标阿司匹林-氘4、水杨酸与内标水杨酸-氘4的色谱峰面积比为纵坐标,采用最小二乘法进行回归运算,分别绘制得到阿司匹林、水杨酸标准曲线方程;
8、s2,取待测含药血浆样品经液液萃取后,进样uplc-ms/ms进行分析,记录待测含药血浆样品中阿司匹林、水杨酸、内标阿司匹林-氘4、内标水杨酸-氘4的色谱图、色谱峰面积;接着分别将待测含药血浆样品中阿司匹林与内标阿司匹林-氘4、水杨酸与内标水杨酸-氘4的色谱峰面积比分别带入绘制的阿司匹林、水杨酸的标准曲线方程,计算得到待测血浆样品中阿司匹林、水杨酸的浓度;其中待测含药血浆样品通过以下方式制取:采用含k2edta抗凝剂和氟化钠添加剂的真空采血管采集受试者服药后不同采血时间点的上肢静脉全血,全血离心后,在血浆中加入适量乙酸水溶液。全血样品及离心后的血浆样品需在冰浴条件下暂存,直至放入超低温冰箱。
9、本发明人血浆中待测物为阿司匹林和水杨酸,其内标分别为阿司匹林-氘4和水杨酸-氘4;
10、包括如下步骤:
11、采用uplc-ms/ms检测经过前处理的血浆样品中阿司匹林和水杨酸的浓度,通过超高效液相色谱将阿司匹林和水杨酸与血浆样品中的基质成分分离,选用稳定同位素作为内标,采用内标法定量。以阿司匹林峰面积与其内标阿司匹林-氘4峰面积之比为纵坐标,以标准曲线样品中阿司匹林的浓度为横坐标,绘制标准曲线,计算血浆中阿司匹林的浓度;以水杨酸峰面积与其内标水杨酸-氘4峰面积之比为纵坐标,以标准曲线样品中水杨酸的浓度为横坐标,绘制标准曲线,计算血浆中水杨酸的浓度。
12、进一步地,所述超高效液相串联质谱的液相色谱条件为:
13、所述高效液相色谱条件包括:
14、色谱柱:shim-pack gist-hp c18,3μm,2.1×100mm;
15、流速:0.35-0.45ml/min;
16、流动相:水相为含0.16%乙酸0.04%甲酸和0.1mmol/l甲酸铵的水溶液;有机相为含0.016%乙酸0.004%甲酸和0.01mmol/l甲酸铵的90%乙腈水溶液;
17、柱温:25-35℃
18、采用流动相a和流动相b不同体积混合,进行梯度洗脱,所述流动相a为含甲酸、乙酸和甲酸铵的水溶液,流动相b为含甲酸、乙酸和甲酸铵的乙腈水溶液;
19、进样量:10μl;
20、所述梯度洗脱过程如下:在0.00-0.50分钟中,流动相a和流动相b的体积比为60:40;在0.50-1.80分钟内,流动相a和流动相b的体积比由60:40匀速渐变至0:100;在1.80-2.80分钟内,流动相a和流动相b的体积比保持为0:100;在2.80-2.81分钟内,流动相a和流动相b的体积比由0:100匀速渐变至60:40;在2.81-3.80分钟内,流动相a和流动相b的体积比保持为60:40,每个样品采集时间为3.80分钟。
21、洗针液:含0.5%甲酸的80%甲醇水溶液。
22、进一步地,所述超高效液相串联质谱的质谱条件为:
23、在电喷雾电离检测模式下,采用多反应监测模式,负离子模式扫描;阿司匹林的离子对为:m/z 179.0→137.0,阿司匹林-氘4内标的离子对为:m/z 182.9→141.1,水杨酸的离子对为:m/z 137.0→65.1,水杨酸-氘4内标的离子对为:m/z 141.0→69.0,扫描时间为100ms,毛细管电压为-4500v;离子源温度为400℃;雾化气(gas 1)为40psi;涡轮气(gas2)为40psi;气帘气(cur)为30psi。
24、进一步地,所述血浆样品中的抗凝剂和添加剂为:
25、采用含k2edta抗凝剂和氟化钠添加剂的真空采血管,全血离心后,取适量血浆加入19.42%乙酸水溶液(加入体积为血浆体积的1%)。全血样品及离心后的血浆样品需在冰浴条件下暂存,直至放入超低温冰箱。
26、进一步地,所述血浆样品前处理的步骤按照以下方法进行:
27、取血浆样品100μl于96孔圆孔板中,向其中加入20μl氘代内标工作液和20μl25%盐酸水溶液,1600rpm左右转速振摇1min后,向其中加入700μl甲基叔丁基醚,封膜后在1500rpm左右转速振摇30min,在4℃、2120g离心10min,取上层有机溶液500μl,置30℃下用氮气吹干,向其中加入350μl含5%乙酸的25%乙腈水溶液,1500rpm左右转速振摇10min,在4℃、2120g离心10min,取上清液,待进样分析。整个前处理过程除涡旋混匀、氮吹、离心、移液、封膜外均需在冰浴中操作。
28、进一步地,所述内标工作液按照以下方法制备:
29、取适量的阿司匹林-氘4对照品于透明聚丙烯瓶中,根据校正因子折算其质量后,在室温白光条件下完全溶解于适量体积的1%乙酸乙腈溶液中,制得浓度为1.00mg/ml的阿司匹林-氘4储备液。取适量的水杨酸-氘4对照品于透明玻璃瓶中,根据校正因子折算其质量后,在室温白光条件下完全溶解于适量体积的1%乙酸乙腈溶液中,制得浓度为1.00mg/ml的水杨酸-氘4储备液。取阿司匹林-氘4储备液30μl加入到970μl含4%乙酸的50%乙腈水溶液中,混合均匀,配制成30μg/ml的阿司匹林-氘4氘代内标溶液,取30μg/ml的阿司匹林-氘4氘代内标溶液100μl、水杨酸-氘4储备液30μl加入到870μl含4%乙酸的50%乙腈水溶液中,混合均匀后取800μl加入到3200μl含4%乙酸的50%乙腈水溶液中,配制成含0.6μg/ml的阿司匹林-氘4及6μg/ml的水杨酸-氘4氘代内标工作液,存于-20℃冰箱储存备用。
30、进一步地,所述标准曲线样品和质控样品按照以下方法制备:
31、使用含4%乙酸的50%乙腈水溶液稀释阿司匹林和水杨酸储备液,配制多个浓度的标准曲线工作液和质控工作液。取10μl标准曲线工作液或质控工作液,加入190μl空白血浆基质混合,再加入0.192%乙酸水溶液适量(加入体积为标准曲线工作液或质控工作液和空白血浆总样品体积的1%),制成阿司匹林/水杨酸浓度为1.00/60.00ng/ml,2.50/150.00ng/ml,20.00/500.00ng/ml,120.00/1000.00ng/ml,500.00/2500.00ng/ml,1200.00/5000.00ng/ml,1900.00/7500.00ng/ml,2400.00/9000.00ng/ml的标准曲线血浆样品和浓度为1.00/60.00ng/ml,3.00/180.00ng/ml,50.00/700.00ng/ml,800.00/3500.00ng/ml,1800.00/7000.00ng/ml的质控血浆样品,用阿司匹林和内标阿司匹林-氘4、水杨酸和内标水杨酸-氘4的峰面积比和标准曲线样品的相应浓度来建立标准曲线,得到相应的线性回归方程。
32、进一步地,所述标准曲线线性回归方程如下:
33、测得的阿司匹林在人血浆中的标准曲线回归方程为:y=0.008124x+0.000123,线性拟合度r2为0.9989;水杨酸在人血浆中的标准曲线回归方程为:y=0.000702x+0.001860,线性拟合度r2为0.9996。所述标准系列的阿司匹林和水杨酸工作溶液的浓度范围分别为20ng/ml~48000ng/ml和1200ng/ml~180000ng/ml;线性范围分别为1.00ng/ml~2400.00ng/ml和60.00ng/ml~9000.00ng/ml,该方法阿司匹林和水杨酸的血药浓度的最低定量下限为1.00ng/ml和60.00ng/ml。
34、本发明还提供一种bufferin的仿制药研发中用于制备标准曲线样品和质控样品及其它未做特殊说明的方法学验证样品的健康人空白血浆采集方法。
35、一种bufferin的仿制药研发中用于制备标准曲线样品和质控样品及其它未做特殊说明的方法学验证样品的健康人空白血浆采集方法,所述采集方法通过以下方式获取:符合伦理要求的健康人在采集空白全血的前2天不得食用富含水杨酸的食物,禁止吸烟,采集空白全血置于含k2edta、氟化钠的采血管中,轻柔颠倒多次混匀后离心,离心条件为2℃~8℃(4℃),以1700g的离心力离心10min,离心之后取上层空白血浆(含k2edta、氟化钠),即得。
36、进一步地,富含水杨酸的食物为食用茶、咖啡、含咖啡饮料、含醇类饮料、杏仁果、苹果、杏果、蓝莓、黑莓、小红莓、薄荷、樱桃、葡萄、桃、橘子、橙、胡柚、柠檬、梅、番茄、黄瓜、火锅、西柚、葡萄柚、芒果、葡萄汁、中药材。
37、本发明还提供一种bufferin的仿制药研发中受试者含药血浆采集方法。
38、一种bufferin的仿制药研发中受试者含药血浆采集方法,其特征在于,所述采集方法通过以下方式获取:采用含k2edta抗凝剂和氟化钠添加剂的真空采血管采集受试者服药后不同采血时间点的上肢静脉全血,全血离心后,在血浆中加入适量乙酸水溶液。全血样品及离心后的血浆样品需在冰浴条件下暂存,直至放入超低温冰箱。
39、采用本发明提供的检测方法可以同时测定人血浆中两种待测物阿司匹林和水杨酸,方法快速、简便、准确度好、灵敏度高。本发明阿司匹林和水杨酸的定量下限分别可以达到1.00ng/ml和60.00ng/ml,定量范围分别可以达到1.00ng/ml~2400.00ng/ml和60.00ng/ml~9000.00ng/ml,检测范围宽,且灵敏度高,符合受试者服用铝镁匹林片(ii)后血药浓度检测范围需求。
40、采用含k2edta抗凝剂和氟化钠添加剂的真空采血管,全血离心后,取适量血浆加入19.42%乙酸水溶液(加入体积为血浆体积的1%),离心前采集的全血和分离后放入超低温冰箱前的血浆均在冰浴中暂存。上述操作均能有效提高样品中阿司匹林的稳定性,样品在室温白光放置5小时、白光冰浴放置27小时、-20℃和-80℃放置40天或冻融循环5次均能保持稳定。
41、阿司匹林又名乙酰水杨酸,因结构中含有酰胺键极易被水解为水杨酸,极不稳定,阿司匹林会发生源内裂解为水杨酸,本发明提供的检测方法,尤其是液相色谱条件可以有效避免上述裂解行为对水杨酸定量产生的干扰。
42、因此,本方法的选择性、精密度、准确度、线性和稳定性等均符合生物样品的分析要求,灵敏度高,可以用于临床铝镁匹林片(ⅱ)的治疗药物监测。
- 还没有人留言评论。精彩留言会获得点赞!