一种高效液相-质谱法检测全血中吲达帕胺的方法与流程
本发明涉及药物生物检测,尤其涉及一种高效液相-质谱法检测全血中吲达帕胺的方法。
背景技术:
1、吲达帕胺(indapamide),是一种带有吲哚环的磺胺衍生物,具有利尿和钙拮抗作用,是新型的抗高血压药物,对血管平滑肌的选择性比较高,可以降低血管外周阻力;还可以通过抑制肾皮质稀释段对钠的重吸收,增加尿钠和尿氯的排出量,发挥抗高血压作用。服用2.5mg剂量后,药物达到峰值血药浓度的时间为1至2小时。吲达帕胺在体内广泛分布,与红细胞结合率高达80%,与血浆蛋白结合率大于75%,因此临床中经常从全血中提取吲达帕胺用于药代动力学考察。
2、近年来曾有研究者采用lc-ms/ms的高通量检测方法从200μl全血样品提取待测物吲达帕胺。具体操作为:于200μl全血样品中加入20μl内标(吲达帕胺-d3),200μl 0.2m硫酸锌水溶液,涡旋混匀30s后加入4ml乙醚,涡旋混匀3min。然后样品在2080g下离心3min,并在-70℃条件下冷冻10min。分离有机层并在氮气流下吹干。然后加入2ml甲醇和7.5mm乙酸铵水溶液(70:30)复溶,涡旋混合30s,取20μl进样考察。
3、lc-ms/ms的高通量检测方法,缩短了样本检测的时长,提高了检测的灵敏度。但是该方法对血液需求量比较大,每次处理都需要200μl血液样品,这就要求临床采血时需要增加采血量,对受试者的身体来说也增加了伤害;该方法萃取剂使用量较大,需要加入4ml乙醚萃取,试剂使用成本较高;该方法前处理时间也较长,步骤复杂,过长的处理时间不利于样品大批量检测,增加了检测时间成本;该方法进样量比较大,需要20μl复溶液进样考察,大的进样量会增加仪器被污染的几率。
技术实现思路
1、为了解决现有技术中存在的问题,本发明提供一种灵敏度高、检测时间短的全血中吲达帕胺的检测分析方法;
2、为实现上述目的,本发明采用如下技术方案:一种高效液相-质谱法检测全血中吲达帕胺的方法,具体包括以下步骤:
3、s1.全血样品预处理:
4、将全血样品在室温黄光下融化,涡旋混匀后吸取一定量样品于连排管中,加入内标工作液、细胞皱缩剂、ph调节剂,涡旋混匀;加入萃取剂,涡旋后,在4℃条件下离心,取上清液至进样套管中,氮气吹干;向进样套管中加入复溶液进行复溶、涡旋,即得待测样品溶液。
5、s2.标准曲线样品配制:
6、称取一定量的吲达帕胺对照品于棕色玻璃瓶中,加入甲醇溶解,制成标准对照品储备液,于-15℃至-30℃的冷冻冰箱中保存,备用。
7、将标准对照品储备液用稀释液进行稀释,配制成一系列浓度的标准曲线工作液。
8、取标准曲线工作液,加入空白全血,混合均匀,制得具有浓度梯度的吲达帕胺标准曲线溶液。
9、s3.lc-ms/ms测定:
10、分别取样品溶液和吲达帕胺标准曲线溶液,采用液相色谱-串联质谱法进行定性或定量检测。
11、其中,s1和s2步骤无先后顺序。
12、优选地,所述s1样品预处理过程中,用到的全血量为50μl。
13、优选地,s1步骤中,所述细胞皱缩剂选用0.2m硫酸锌溶液。
14、优选地,s1步骤中,所述ph调节剂选用饱和碳酸氢钠溶液。
15、本发明中,采用0.2m硫酸锌高渗溶液作为细胞皱缩剂,可以使全血中红细胞皱缩,裂解,使吲达帕胺从红细胞中全部被释放出来,从而保证检测的准确性。由于吲达帕胺是一种碱性化合物,在血液样品中加入弱碱性ph调节剂,本发明选用饱和碳酸氢钠,不但可以稀释血液,克服血液粘滞性,还可以增加化合物离子化强度,提高提取回收率。
16、优选地,步骤s1中,所述内标工作液为溶有内标的50%甲醇水溶液,所述内标为吲达帕胺-d3。
17、优选地,所述内标工作液中吲达帕胺-d3的浓度为150ng/ml。
18、优选地,步骤s1中,所述萃取剂选用乙酸乙酯,乙酸乙酯的用量为500μl。
19、优选地,步骤s1中,所述复溶液为75%甲醇水溶液。
20、优选地,s1具体步骤为:将全血样品在室温黄光下融化后,涡旋混匀1min;吸取50.0μl样品于连排管中,加入20μl内标工作液、50μl细胞皱缩剂、50μlph调节剂,涡旋1min;再加入500μl乙酸乙酯进行液液萃取,涡旋5min,于4℃条件下,3700rpm离心5min,取上清液至进样套管中,氮气吹干;然后加入150μl75%甲醇水溶液复溶,涡旋2min,即得待测的样品溶液。
21、优选地,步骤s2中,所述稀释液为50%甲醇水溶液。
22、优选地,步骤s2中,所述标准对照品储备液的浓度为4mg/ml。
23、优选地,步骤s2中,所述吲达帕胺标准曲线溶液的浓度范围为2-220ng/ml。
24、优选地,步骤s3中,所述液相色谱的分析条件为:
25、色谱柱:c18柱;柱温:35-45℃;流速:0.2-0.7ml/min;进样量:3-8μl;流动相a为含0.02-0.08%甲酸的3-15mmol甲酸铵水溶液,流动相b为甲醇,进行梯度洗脱。
26、更优选地,步骤s3中,所述液相色谱的分析条件为:
27、色谱柱:shimadzu shim-pack giss-hp 3μm c18 2.1×50mm;柱温:40℃;流速:0.5ml/min;进样量:5μl;流动相a为含0.05%甲酸的10mm甲酸铵水溶液,流动相b为甲醇,进行梯度洗脱。
28、优选地,步骤s3中,所述梯度洗脱的条件为:
29、0-0.5min,90%流动相a,10%流动相b;0.5-1.5min,流动相a从90%降至10%,流动相b从10%升至90%;1.5-3min,10%流动相a,90%流动相b;3min-3.1min,流动相a从10%升至90%,流动相b从90%降至10%;3.1-4min,90%流动相a,10%流动相b。
30、优选地,步骤s3中,所述质谱条件为:
31、采用正离子电喷雾离子化多反应检测模式,离子源电压:5000v,离子源温度:500℃,气帘气:20psi,碰撞气:8psi,雾化气:50psi,辅助气:
32、50psi。
33、优选地,步骤s3中,所述多反应离子检测的参数设置为:
34、待测物吲达帕胺的参数设置:q1 mass:366,q3 mass:132,dwell:
35、200ms,ce:15v,dp:70v;内标吲达帕胺-d3的参数设置:q1 mass:
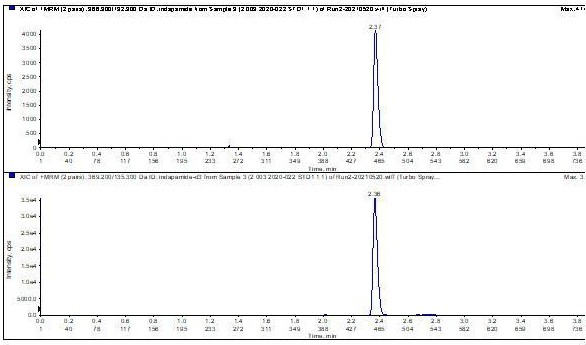
36、369,q3 mass:135,dwell:100ms,ce:10v,dp:70v。其中,待测物吲达帕胺和内标吲达帕胺-d3的子离子扫描图见图1和图2。
37、与现有技术相比,本发明的有益效果为:
38、1.本发明的检测方法中全血使用量为50μl,全血使用量较低,减少了受试者各个时间点的采血量,有利于临床试验的顺利进行;
39、2.本发明的检测方法中萃取剂的使用量为500μl,萃取剂的使用量较现有技术明显减少,有利于降低检测成本。
40、3.本发明的检测方法中加入细胞皱缩剂可以使全血中红细胞皱缩,裂解,从而使吲达帕胺从红细胞中全部被释放出来;ph调节剂的加入不但可以稀释血液,克服血液粘滞性,还可以增加化合物离子化强度;细胞皱缩剂和ph调节剂的加入,有利于提高吲达帕胺提取回收率。
41、4.本发明的检测方法中色谱分离运行时间短,进样量小,有利于提高检测通量,提高检测效率。
42、5.本发明可以实现对于全血中的吲达帕胺准确定性、定量检测,检测结果准确度高、精密度高、耗时短,可以有效应用于药代动力学和生物等效性研究。
- 还没有人留言评论。精彩留言会获得点赞!