用于形成设置有包括牺牲盐的正电极的锂离子电池单元的方法与流程
本发明涉及锂离子可再充电电池的总体领域。
更确切地说,本发明涉及一种用于形成电池单元的方法,所述电池单元包括正电极材料,所述正电极材料包括至少一种牺牲盐。
背景技术:
通常,锂离子电池包括一个或多个阴极、一个或多个阳极、电解质以及用于防止电极之间的任何直接接触的由多孔聚合物或任何其他合适的材料组成的隔板。
锂离子电池已经在众多移动应用中得以广泛使用。这种趋势尤其可以通过比常规镍镉(ni-cd)和镍金属氢化物(ni-mh)蓄电池的体积和质能密度大得多的体积和质能密度、不存在记忆效应、相对于其他蓄电池的低自放电以及与这种技术相关联的千瓦时成本的降低来解释。
尽管如此,对这种技术的改进对于获得如经常需要高能量密度、高功率密度以及长寿命的电动车辆和混合动力车辆等新市场来说仍是必要的。
一旦锂离子电池单元被活化,即,当单元已经被组装并且单元已经浸有电解质时,在对所述单元进行充电的第一循环期间涉及热力反应,并且发生电极之间的第一锂离子交换。由这些反应产生的产物积累在电极的表面上从而形成所谓的“固体电解质中间相(solidelectrolyteinterphase,sei)”层。此层对于锂离子电池的适当操作来说是必要元件,因为所述层不仅非常好地传导锂离子,而且其还具有阻止对溶剂的催化分解的优点。
然而,已知的是,在形成此层时,电池损失其正电极的电势容量的5%与20%之间,由此限制了所述电池的能量密度,在形成此层期间,负电极不可逆地消耗锂。
已经设想了多种用于解决此问题的方式。
因此,已经将金属锂添加到负电极中以补偿在第一充电循环期间的不可逆锂消耗,如文件jp2012/009209中所描述的。然而,使用金属状态下的锂引起了许多问题,因为锂与水分以及电极油墨应用中常用的极性溶剂(通常是水或n-甲基吡咯烷酮(nmp))发生剧烈反应。
还可以将牺牲盐添加到正电极中,如文件fr2961634中所描述的。此专利中公开了一种具体的草酸锂盐,但是其被认为是不适合的,因为其氧化电势太高。
此外,已经将诸如如由奥尔巴克(aurbach)等人在“ontheuseofvinylenecarbonate(vc)asanadditivetoelectrolytesolutionsforli-ionbatteries(论将碳酸亚乙烯酯(vc)用作锂离子电池的电解质溶液的添加剂)”(《电化学杂志(electrochemicaacta)》第47期(2002年),1423-1439页)中设想的碳酸亚乙烯酯,或者如由左(zuo)等人在“electrochemicalreductionof1,3-propanesultoneongraphiteelectrodesanditsapplicationinli-ionbatteries(石墨电极上的1,3-丙烷磺酸内酯的电化学还原及其在锂离子电池中的应用)”(《电化学与固态快报(electrochemicaandsolid-stateletters)》第9(4)期,a196-a199页(2006年))中设想的碳酸丙烷磺酸内酯等添加剂添加到电解质中以提高sei的质量,这因而对单元的使用寿命有影响。
然而,使用添加剂的主要缺点与用于形成sei层的正电极的锂的消耗相关联。这对单元的初始容量有影响,而且对所述单元的寿命周期的总时长有影响。
技术实现要素:
本发明旨在提出用于解决与由于锂离子电池的第一形成周期而引起的不可逆容量相关的问题的解决方案,从而允许增加所述电池的耐久性。
根据本发明,一种用于形成锂离子电池单元的方法包括以下连续步骤,所述锂离子电池单元包括具有从20%到35%的孔隙率水平的正电极材料并且包括至少一种牺牲盐、负电极材料、隔板以及电解质:
(a)将所述单元加热到在从30℃到45℃的范围内的温度t1;
(b)将所述单元充电至小于或等于4.8v、优选地从4.6v到4.8v、更优选地从4.7v到4.8v的电势。
根据本发明的方法大大减少了锂离子电池单元的正电极的容量在第一充电循环期间的损失,由此引起所述电池的寿命增加。
附图说明
在审查详细说明和附图之后,本发明的其他优点和特征将变得更清楚,在附图中:
-图1是曲线图,示出了三个锂离子电池单元的作为时间的函数的电势变化;
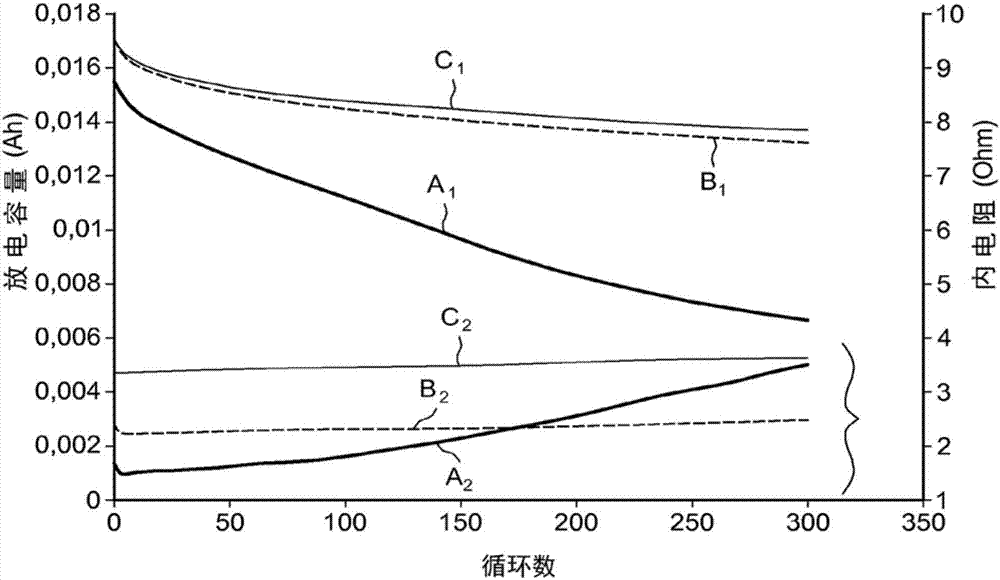
-图2是曲线图,示出了三个锂离子电池单元的作为循环数量的函数的放电容量变化和内电阻变化;
-图3是曲线图,示出了具有特定孔隙率水平的三个锂离子电池单元的作为循环数量的函数的放电容量变化和电阻变化。
具体实施方式
在本发明的说明书中,术语“基于”是“主要包括”的同义词。
另外,应当指出,本说明书中使用的表述“从…到…”将被理解为包括所提及的限制中的每一个。
如以上解释的,根据本发明的形成方法涉及锂离子电池单元,所述锂离子电池单元包括具有在从20%到35%的范围内的孔隙率水平的正电极材料,并且包括至少一种牺牲盐、负电极材料、隔板以及电解质。
电极的真实密度(dr)是根据电极沉积物的质量和厚度来计算的。可以根据每个部件的密度来计算理论(压实)沉积密度(dth)。因此,被定义为电极中的空置空间的比例的孔隙率水平(tp,被表示为百分比)由以下等式(i)给出:
tp=(1–dr/dth)*100(i)。
牺牲盐是能够在将经组装电池单元充电至例如在从2v到5v的范围内的电势的第一循环期间氧化的化合物。氧化时,牺牲盐产生渗入电解质中的离子(当牺牲盐是li+阳离子盐时,产生的是li+离子)。于是,所述盐被称为具有预锂化性质。所述离子至少部分地补偿在负电极上形成sei层期间损失的容量。
此外,被氧化的盐在电极内产生多孔性,必须精细地控制这种情况以防止锂离子蓄电池的性能损失。事实上,过高孔隙率限制了粒子之间的电子接触并且增大了电化学单元的电阻。
根据本发明的具体实施例,牺牲盐选自以下各项:li2c2o4、lin3、li2c3o5、li2c4o6、li2c3o3、li2c4o4、li2c5o5、li2c6o6、li2n4o2、以及[li2n2c2o2]n、并且优选地li2c2o4,n为从1到100、优选地从1到50、更优选地从1到10。
草酸锂是具有545mah/g的容量、在空气中稳定、可以结合到正电极配方中的盐。在4.5v与5.5v之间(相对于li+/li),草酸锂氧化,从而释放出二氧化碳和两个锂离子。所释放的锂离子能够补偿锂离子电池单元的不可逆第一充电容量,由此增大其初始容量。二氧化碳在形成结束时排出,并且因此其质量(草酸盐水平的函数)对电池的质量没有贡献。
根据本发明的另一个特征,正电极材料包括相对于正电极的总重量从3wt%到10wt%、优选地从3%到7%、更优选地从4%到6%的牺牲盐。
有利地,正电极的孔隙率水平为从25%到35%。
优选地,正电极材料包括选自以下各项的活性材料:
-橄榄石结构磷酸盐livtapo4,其中,0≤v≤1,并且ta选自fe、ni、co、mn及其混合物;
-式li1+u(madb)1-uo2的材料,其中,0.01≤u≤0.33,m选自ni、mn、co及其混合物,d表示选自na、zn、cd、mg、ti、ca、zr、sr、ba、al以及k的一种或多种掺杂金属,0≤b≤0.05并且a+b=1;以及
-选自limn2o4和lini0.5mn1.5o4的尖晶石结构材料,
更优选地所述橄榄石结构磷酸盐、甚至更优选地lifepo4。
草酸锂的氧化电势太高而不能与如基于linixmnycozo2(nmc)(其中,x+y+z=1)的电极、基于lini0.8co0.15al0.05o2(nca)的电极、或基于licoo2(lco)的电极等结构在超过4.5v时不稳定的一些正电极一起使用。
然而,在尖晶石型材料(limn2o4或lini0.5mn1.5o4)、或锂化磷酸li(fe,mn,ni)po4、或(li1+xmo2)型材料的情况下,可以设想5v的电势,因为或者这些材料的活性范围与草酸盐的活化电势一致,或者所述活性范围完全不相关。例如,在lifepo4型材料的情况下,氧化还原活性在3.4v与3.5v之间,并且所述材料在超过所述电势时不会氧化。通过添加草酸盐,其可以在5v下氧化,而不会有干扰活性材料的结构的任何风险。
然而,已知的是,锂离子电池的标准电解质(基于碳酸盐)在超过4v时开始氧化,这种现象在超过5v时变得突出。因此,希望尽可能降低最大充电电势以避免这些寄生反应。
优选地,正电极材料包括一种或多种粘合剂。
优选地,所述一种或多种粘合剂是有机聚合物、优选地聚丁二烯-苯乙烯胶乳、聚酯、聚醚、甲基丙烯酸酯聚合物衍生物、丙烯腈聚合物衍生物、羧甲基纤维素及其衍生物、聚醋酸乙烯酯或聚丙烯酸乙酸酯、聚偏二氟乙烯、及其混合物。
根据依据本发明的方法的变体,负电极材料基于石墨。石墨碳可以选自合成石墨碳以及始于净化和/或后处理之后的天然前体的天然石墨碳。可以使用其他基于碳的活性材料,诸如热解炭、无定形碳、活性炭、焦炭、煤焦油沥青以及石墨烯。石墨与这些材料中的一种或多种的混合物是可能的。当芯包括高容量石墨并且壳体包括保护芯免于与重复的锂离子嵌入/脱嵌效应相关的芯退化的基于碳的材料时,可以使用具有芯-壳结构的材料。
有利地,负电极材料基于选自以下复合材料的复合材料:硅/石墨、锡/石墨、氧化锡/石墨(诸如,sno2/石墨)、及其混合物、优选地硅/石墨复合材料。
优选地,硅/石墨复合材料包括相对于复合材料的总重量从0wt%到30wt%、更优选地从0%到15%、甚至更优选地从5%到10%的硅。
优选地,隔板位于电极之间并且充当电绝缘体的角色。可以将多种材料用作隔板。隔板通常由多孔聚合物、优选地聚乙烯和/或聚丙烯组成。
有利地,所使用的隔板是
优选地,所述电解质是液体电解质。
根据本发明的另一个特征,所述电解质包括一种或多种锂盐。
有利地,所述一种或多种锂盐选自以下各项:二[三氟甲基磺酰]亚胺锂(lin(cf3so2)2)、三氟甲磺酸锂(licf3so3)、二(草酸)硼酸锂(libob)、二(全氟乙基磺酰)亚胺锂(lin(cf3cf2so2)2)、liclo4、liasf6、lipf6、libf4、lii、lich3so3、lib(c2o4)2、lirfsosrf、lin(rfso2)2、lic(rfso2)3,rf是选自氟原子的基团以及包括一到八个碳原子的全氟烃基团。
优选地,电解质包括溶剂(所述溶剂包括碳酸乙烯酯)和选自以下各项的至少一种溶剂的混合物:碳酸甲乙酯、碳酸二甲酯、碳酸二乙酯、及其混合物。
根据本发明的具体实施例,电解质包括锂盐lipf6为1m、按体积计比例为1/1/1的碳酸乙烯酯、碳酸二甲酯和碳酸甲乙酯的混合物。
如上文所提及的,根据本发明的形成方法的步骤(a)由将单元加热到从30℃到45℃的温度t1组成。
优选地,温度t1处于从35℃到45℃的范围内,并且更优选地,温度t1为40℃。
如以上解释的,根据本发明的形成方法的步骤(b)由将单元充电至小于或等于4.8v、优选地从4.6v到4.8v、更优选地从4.7v到4.8v的电势组成。更优选地,对单元的充电进行到高达从4.75v到4.8v的电势。
根据本发明的具体实施例,根据本发明的形成方法包括以下连续步骤,所述形成方法被应用于包括具有在从20%到35%(优选地35%)的范围内的孔隙率水平的正电极材料的电池单元,所述材料包括式lifepo4的活性材料以及相对于正电极的总重量5wt%的草酸锂、负电极材料、隔板、以及电解质:
(a)将单元加热到40℃的温度t1;
(b)将单元充电至高达从4.7v到4.8v、优选地4.8v的电势。
示例
1.制备包括包含草酸锂的正电极的锂离子电池单元
1.1制备正电极
使用式lifepo4的活性材料。通过混合85wt%的活性材料、5wt%的super
通过在铝箔上沉积20μm厚度的混合物来制作电极。通过在80℃下进行压延来干燥和压缩电极。
1.2制备负电极
制备了基于硅/石墨复合材料(日立化成(hitachichemical))的负电极。通过混合94wt%的活性材料、2wt%的羧甲基纤维素(cmc)、以及4wt%的
通过在铜箔上沉积10μm厚度的混合物来制作电极。通过在80℃下进行压延来干燥和压缩电极。
1.3隔板
使用
1.4电解质
所使用的电解质由溶解在按体积计比例为1/1/1的碳酸乙烯酯、碳酸二甲酯以及碳酸甲乙酯的混合物中的1m锂盐lipf6组成。
1.5电化学单元
通过堆叠面积为10cm2的正电极和如上所述的负电极来组装锂离子电池,如上所述的隔板被定位在电极之间,并且然后使单元浸有如上所述的电解质。
2.锂离子电池单元的电化学性能
2.1评估锂离子电池单元的作为时间的函数的电势变化
方法
将分别被称为方法a、方法b和方法c的三种具体形成方法应用于如以上制备的锂离子电池单元。
将方法a应用于被称为单元a的锂离子单元。将方法b应用于被称为单元b的单元,并且将方法c应用于被称为单元c的单元。
对比方法a包括:将单元a加热到22℃的步骤,然后是将单元a充电至高达4.8v电势的步骤。
根据本发明的方法b包括:将单元b加热到40℃的步骤,然后是将单元b充电至高达4.8v电势的步骤。
对比方法c包括:将单元c加热到50℃的步骤,然后是将单元c充电至高达4.8v电势的步骤。
结果
在图1中,曲线a、b和c分别对应于单元a、b和c的电势变化。
图1清楚地示出了单元b和c显示出不同于单元a的电化学行为的电化学行为。
当电势接近3.2v到3.3v时,这3条曲线具有对应于式lifepo4的活性材料的氧化还原活性的平稳状态。
当电势接近4.8v时,曲线a具有对应于草酸锂的氧化还原活性的平稳状态。然而,当电势为约4.5v时,曲线b和c具有也对应于草酸锂的氧化还原活性的平稳状态。
因此,图1示出了温度从22℃升高到40℃至50℃允许草酸锂在较低电势下活化,从而使得有可能将充电结束电势降低到4.8v。
这表示相当大的优势,因为常规锂离子电池电解质(即,基于碳酸盐溶剂)在电势超过5v时不稳定。
2.2评估锂离子电池单元的作为循环数量的函数的放电容量和内电阻变化
方法
所述方法与段落2.1中给出的方法完全相同。
结果
在图2中,曲线a1对应于单元a的放电容量变化,并且曲线a2对应于单元a的内电阻变化。曲线b1对应于单元b的放电容量变化,并且曲线b2对应于单元b的内电阻变化。曲线c1对应于单元c的放电容量变化,并且曲线c2对应于单元c的内电阻变化。
图2示出了在300个循环之后观察到低放电容量(曲线a1)并且单元a的内电阻随着循环数量而显著增大(曲线a2)。
然而,根据曲线b1和c1,观察到了单元b和c的良好放电容量。单元c具有比单元b的内电阻(曲线b2)高的内电阻(曲线c2)。事实上,过高的温度和4.8v的电势由于电解质在牺牲盐——草酸锂——的活化时退化而产生较高内电阻。
因此,清楚地示出了将单元加热到在从30℃到45℃的范围内的约40℃的温度对于同时获得低的稳定内电阻、良好的放电容量以及良好的循环行为是理想。
2.3评估具有特定孔隙率水平的锂离子电池单元的作为循环数量的函数的放电容量和内电阻变化
方法
将根据本发明的形成方法b应用于各自包括正电极的被称为单元d、单元e和单元f的三个锂离子电池单元,正电极中的每一个都具有通过三个不同压延水平来获得的三个不同的孔隙率水平,分别为47%、35%和42%。
因此,将对比形成方法d应用于单元d;将根据本发明的形成方法e应用于单元e;并且将对比形成方法f应用于单元f。
结果
在图3中,曲线d1对应于单元d的放电容量变化,并且曲线d2对应于单元d的电阻变化。曲线e1对应于单元e的放电容量变化,并且曲线e2对应于单元e的电阻变化。曲线f1对应于单元f的放电容量变化,并且曲线f2对应于单元f的电阻变化。
图3示出了单元d具有高内电阻(曲线d2)、低放电容量以及差循环行为(曲线d1)。
单元e具有低电阻(曲线e2)和良好的放电容量(曲线e1)。
单元f具有相对较高的内电阻(曲线f2)和良好的放电容量(f1)。
因此,示出了正电极中的35%孔隙率水平使得有可能同时获得低的稳定内电阻、良好的放电容量以及良好的循环行为。
超过35%的孔隙率水平时,正电极的导电率受到限制,并且电池的电阻显著增大。事实上,电池性能大幅降低。
- 还没有人留言评论。精彩留言会获得点赞!